生產(chǎn)具有一致質(zhì)量的重組腺相關病毒 (rAAV) 的上����、下游工藝的優(yōu)化取決于快速表征關鍵質(zhì)量屬性 (CQA) 的能力。在 rAAV 生產(chǎn)的背景下�,病毒滴度、衣殼含量和聚體被確定為潛在的 CQA����,影響 rAAV 介導的基因治療產(chǎn)品的效力、純度和安全性�。盡管快速、高通量的方法開始被開發(fā)和商業(yè)化���,檢測這些屬性的分析方法通常會因工藝開發(fā)的周轉時間長或產(chǎn)量低而受到影響�����。這些方法尚未在學術或工業(yè)實踐中得到很好的確立�����,支持性數(shù)據(jù)也很少���。在這里��,我們回顧了已建立和即將推出的 rAAV 質(zhì)量屬性定量檢測分析方法��。在評估每種方法時��,我們強調(diào) rAAV 快速在線表征的進展�����。此外���,我們發(fā)現(xiàn)從傳統(tǒng)方法過渡到新方法的一個關鍵挑戰(zhàn)是后者缺乏學術和工業(yè)經(jīng)驗。這篇文獻綜述可作為選擇針對質(zhì)量屬性的分析方法的指南����,以在rAAV 介導的基因療法的工藝開發(fā)過程中進行快速、高通量的過程表征���。
重組腺相關病毒 (rAAV) 被廣泛用作體內(nèi)基因治療的載體���,主要是因為它們對人類無致病性、低免疫原性和長期基因表達�����。美國食品藥品監(jiān)督管理局 (FDA) 已經(jīng)批準了兩種基于 rAAV 的基因療法���,用于治療罕見的單基因疾?。杭顾栊约∥s癥 (Zolgensma) 和 Leber 先天性黑蒙 (Luxturna)����。此外,基于 rAAV 的基因療法目前正在 200 多項臨床試驗中進行研究��,用于治療從腫瘤到神經(jīng)系統(tǒng)疾病的一系列疾病����。隨著rAAV 的臨床潛力得到認可,在不影響效力�����、純度和安全性的情況下規(guī)模放大其生物生產(chǎn)過程的挑戰(zhàn)變得越來越受重視。
生物藥生產(chǎn)平臺的開發(fā)需要識別產(chǎn)品的關鍵質(zhì)量屬性 (CQA) 并表征 CQA 與工藝參數(shù)之間的功能關系�。CQA 被定義為“一種物理、化學�、生物或微生物特性或特點,其應處于適當?shù)南薅?�、范圍或分布?nèi)�����,以確保所需的產(chǎn)品質(zhì)量”�����,CQA 是一種屬性 - 廣泛對應于產(chǎn)品的特性�����、效力�、純度或安全性 - 如果超出其目標范圍,將對產(chǎn)品質(zhì)量和功效產(chǎn)生嚴重影響�。工藝參數(shù)變化對這些 CQA 的影響的表征,例如通過使用實驗設計����,提高了對工藝的理解�,使其得以優(yōu)化�,并最終通過設計確保產(chǎn)品質(zhì)量(表 1)�。對于生物藥,如 rAAV�,藥物底物的屬性(例如,一致性)和雜質(zhì)知識 - 無論是與產(chǎn)品相關的(例如�����,非活性產(chǎn)品異構體和聚體)還是與工藝相關的(例如�,宿主細胞蛋白或 DNA) - 幫助在開發(fā)早期識別CQA。盡管與工藝相關的屬性并不是 rAAV 生產(chǎn)所獨有的����,但與 rAAV 產(chǎn)品或產(chǎn)品相關雜質(zhì)有關的 CQA 才剛剛開始被明確識別。在這篇綜述中�,我們重點關注 rAAV 生產(chǎn)的生產(chǎn)力、病毒滴度���、具有完整基因組的衣殼的比例(含量比)以及聚集衣殼的數(shù)量��,基于它們對產(chǎn)品安全性和功效的影響而可作為潛在的CQA�。
表1. 與工藝開發(fā)相關的重要術語的定義
rAAV的質(zhì)量屬性通常使用耗時的質(zhì)量控制檢測進行分析,以對最終產(chǎn)品進行批次放行測試�,確保它們符合安全使用的監(jiān)管規(guī)范。然而����,此類產(chǎn)品開發(fā)時間短,需要具有快速周轉和高通量的經(jīng)濟分析方法����。例如,用于早期篩選 rAAV 生產(chǎn)平臺的部分因子設計(三個級別的五個工藝參數(shù))需要對實驗進行快速�、高度并行的分析。這種通量不可避免地會導致大多數(shù)已建立的質(zhì)量控制分析的分析能力出現(xiàn)瓶頸����。或者��,快速���、高通量的分析方法可以迅速產(chǎn)生可操作的結果��,促進對過程的理解并加快開發(fā)決策�。然而���,有限的樣品數(shù)量和基質(zhì)效應(例如�����,緩沖液特性�����、殘留 DNA 或蛋白質(zhì)以及離子強度)對工藝開發(fā)中的此類方法提出了挑戰(zhàn)�。通常�����,實驗室規(guī)模的生產(chǎn)僅可獲得幾毫升 (mL) 的純化 rAAV - 相當于1012-1014 載體基因組 (vg) - 因此分析所需的樣本量可能會導致產(chǎn)品的顯著損失�����。同時���,樣品中的病毒濃度涵蓋多個數(shù)量級����,從粗培養(yǎng)收獲液的 1010 - 1011 vg/mL 到純化產(chǎn)物中的 1013 - 1014 vg/mL����,并且樣品基質(zhì)變化很大�,在最初的下游步驟中����,殘留的副產(chǎn)物、宿主細胞蛋白和 DNA的質(zhì)量濃度比 rAAV 高 10 - 100 倍��。這種過量的殘留副產(chǎn)物限制了特異性不足的方法的適用性���,除非進行了大量的樣品純化工作��。
在本文中,我們首先介紹基因組和衣殼滴度��、含量比率和聚體含量這三個質(zhì)量屬性��,用于表征 rAAV 中產(chǎn)生的主要衣殼類型(圖 1)��。為了將這些質(zhì)量屬性確定為 CQA��,我們將概述它們在常見生產(chǎn)過程中的可變性以及它們對 rAAV 產(chǎn)品安全性和有效性的一般影響��。然后,我們在工藝開發(fā)的背景下討論它們作為 CQA 的優(yōu)點和缺點��。最后��,我們將介紹當前最先進的��、用于表征 rAAVCQA的分析方法��,并為進一步的方法開發(fā)提出建議��。
rAAV的產(chǎn)品相關CQA
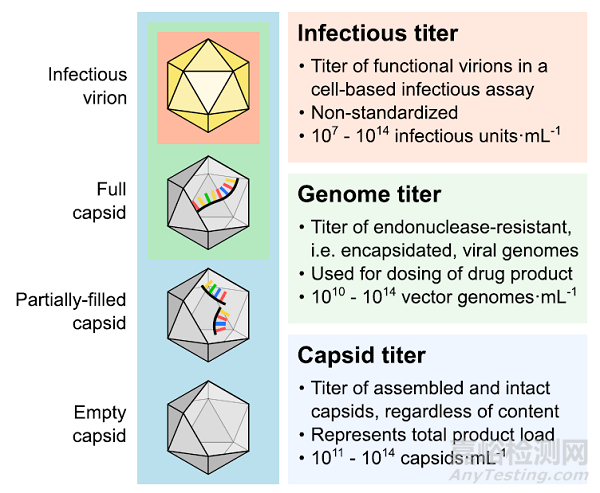
作為第一個潛在的 CQA��,病毒滴度或濃度是指感染性��、基因組或衣殼滴度(圖 2)��。在這里��,我們將關注基因組和衣殼滴度��,因為從工藝開發(fā)的角度來看��,它們實際上是可測量的��?�;蚪M滴度代表包含載體基因組(即病毒體)的衣殼��,估計樣品的效力��,被主要用于 rAAV 臨床給藥劑量的確定��。相反��,衣殼滴度代表所有衣殼,與包含的基因組無關��?�?傄職さ亩繉τ谙掠位厥栈蚣兓に嚨牟僮骱蛢?yōu)化至關重要��,這些工藝取決于產(chǎn)品的上樣而不是其效力��,例如��,制備型層析柱的上樣��,或柱餾分的合并。此外��,衣殼往往會聚集,這取決于它們的總濃度和環(huán)境條件��,例如溫度��、離子強度和 pH 值��。因此��,根據(jù)所考慮的工藝單元��,基因組和衣殼滴度都可以指示產(chǎn)品的效力��、安全性和功效��。相比之下��,感染性滴度(一種體外生物活性的量度)需要 1-3 天才能量化��,并表現(xiàn)出多個數(shù)量級的可變性��;因此��,及時表征產(chǎn)品效力是不切實際的��。其定量方法基于端點稀釋測定、感染中心測定和轉基因表達測定��,這些方法將不在本文中進行討論��。
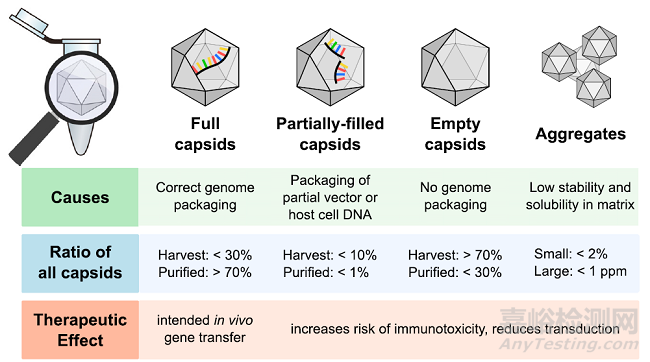
含量比��,作為第二個潛在的 CQA��,是指病毒衣殼缺失或具有部分基因組的比例��,分別稱為空衣殼或部分包裹衣殼��,代表rAAV 生產(chǎn)中最常見的產(chǎn)品相關雜質(zhì)(圖 1)��。不同的因素��,例如載體基因組的長度和類型(即單鏈或自互補)��,會導致沒有預期載體基因組的衣殼總比例的差異性��。此外��,生產(chǎn)平臺的選擇和質(zhì)粒的大小會影響非轉基因序列的反向包裹��,導致不同程度地產(chǎn)生部分包裹 DNA 雜質(zhì)的不希望的衣殼亞群��。空衣殼��,以及帶有非轉基因序列的衣殼��,可以引發(fā)不必要的免疫反應并競爭載體結合位點��,增加免疫毒性的風險并降低完整衣殼的轉導率��,這是產(chǎn)品功效所必需的��。完整衣殼與所有衣殼的比率��,稱為含量比��,在收獲時的生產(chǎn)培養(yǎng)物中可以從 <1% 到 30% 不等��,并且在不同批次的生產(chǎn)運行之間不一致(圖 1)��。含量比影響工藝效率和產(chǎn)品純度��,最近已將含量比添加到基于病毒的基因療法的監(jiān)管產(chǎn)品規(guī)范中��,并且是工藝開發(fā)中的一個重要質(zhì)量屬性。與空衣殼不同��,部分包裹的衣殼和帶有宿主細胞/質(zhì)粒 DNA 的完整衣殼可能具有額外的基因毒性作用,具體取決于包裹的基因組的類型��。除了空的和部分包裹的衣殼外��,其它雜質(zhì)也可能導致免疫或基因毒性作用��,例如殘留的輔助病毒(來自上游轉導步驟)��、殘留的蛋白質(zhì)(來自宿主細胞或細胞培養(yǎng)基)��,或核酸(宿主細胞 DNA/RNA)��。
作為第三個潛在 CQA 的衣殼聚體代表了另一種與產(chǎn)品相關的雜質(zhì)��,對載體產(chǎn)品的安全性和長期穩(wěn)定性產(chǎn)生不利影響��,因為即使是痕量水平(例如��,<1%)也為進一步聚集提供了成核位點��。rAAV 制劑中存在小的低聚物(d < 100 nm)和大的��、亞可見聚集體(d > 100 nm)��,并且樣品基質(zhì)中的高濃度衣殼��、殘留核酸或低離子強度被證明有助于rAAV2 的聚集。因此��,聚集可能發(fā)生在下游工藝中存在這些條件的多個節(jié)點��,例如��,在濃縮步驟期間或作為緩沖液置換的結果��。為確保產(chǎn)品安全��,需要盡量減少聚集程度并確定影響該產(chǎn)品屬性的工藝條件��。
圖 1. rAAV 生產(chǎn)過程中產(chǎn)生的主要衣殼類型概述:所有衣殼的比例結果包括在收獲時rAAV 生產(chǎn)培養(yǎng)液(“收獲液”)��,例如��,在任何純化之前的細胞裂解液中��,以及在產(chǎn)品中純化后(“純化液”)中��,即在從細胞裂解液中純化完整衣殼之后��,但在將完整衣殼與空衣殼幾乎完全分離的任何精純步驟之前��。數(shù)據(jù)基于報告的大規(guī)模 rAAV 生產(chǎn)的文獻��。根據(jù)大?�。ǘ嗑垠w��,d < 100 nm)或大(d > 100 nm)來識別聚體��,其含量與商業(yè)純化的 rAAV 產(chǎn)品相同��。
圖 2. rAAV 樣品的傳染性��、基因組和衣殼滴度之間的差異:生產(chǎn)過程中滴度的常見范圍以其常用單位給出��,基于報告的大規(guī)模 rAAV生產(chǎn)的文獻��。
分析方法在質(zhì)量屬性表征中的表現(xiàn)
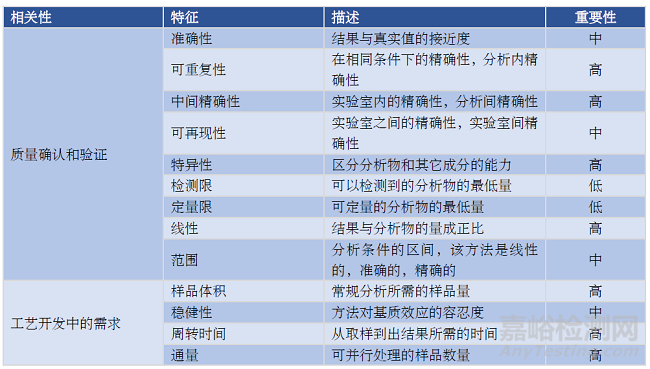
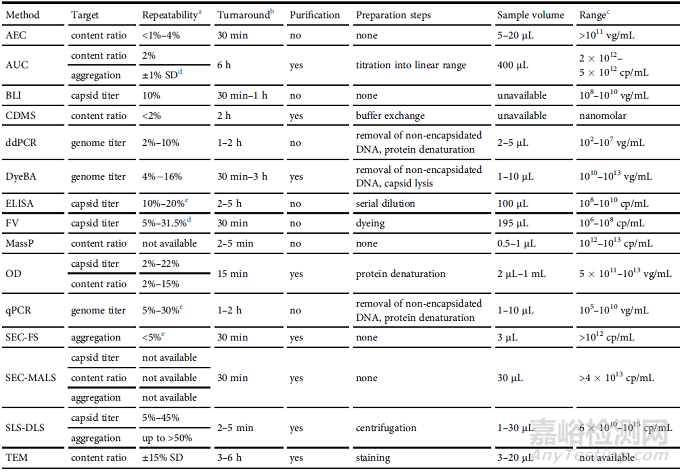
分析方法必須具備一系列特性��,以證明其適用于其預期目的(即方法確認和驗證)��,以及滿足工藝開發(fā)中的特定需求(表 3)��。對于后者��,這些特性還可能包括適用于近線(at-line)或入線(in-line)應用��。與需要將樣品從采樣點移至實驗室環(huán)境的離線(off-line)分析相比��,能夠近線或入線應用的方法有助于使用靠近采樣點(近線)或直接集成到工藝本身(入線)。工藝開發(fā)中使用的方法不要求基于分析程序驗證監(jiān)管指南中定義的特征對分析方法進行確認和驗證��。盡管如此��,這些特征中的大多數(shù)��,例如準確度��、精確度和特異性��,仍然適用��,因為通常在開發(fā)的早期階段使用這些特征來對檢測進行確認��。對于后期開發(fā)階段以及認證生產(chǎn)所使用的分析��,需要基于監(jiān)管指南進行全面分析驗證��,而不僅是質(zhì)量確認��。表 4 總結了本綜述中討論的分析方法的上述特征��,表 5 列出了關鍵結論��。
表3. 與方法確認、驗證和工藝開發(fā)需求相關的分析方法的特征
表4. 本文討論的分析方法的最重要性能標準的數(shù)據(jù)
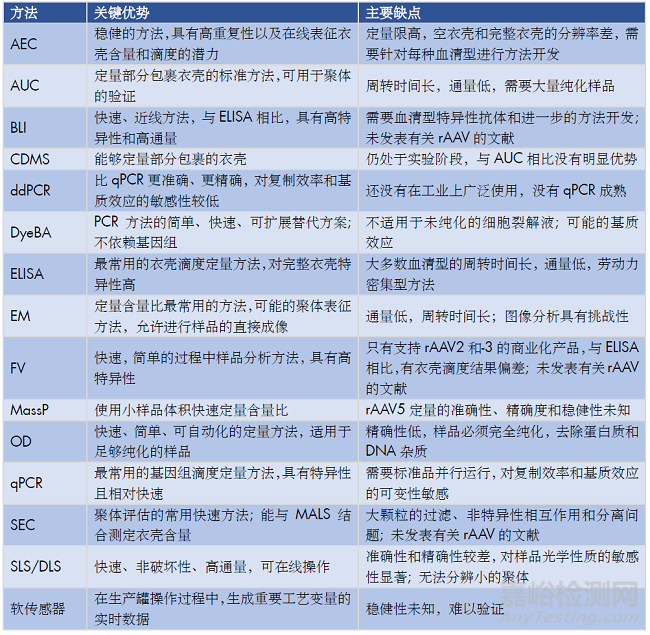
表5. 每種分析方法的主要優(yōu)點和缺點
原文:A.L.Gimpel, G.Katsikis, S.Sha, et al., Analytical methods for process and product characterization of recombinant adeno-associated virus-based gene therapies. Molecular Therapy: Methods & Clinical Developmen, 2021, 20.
參考資料
【1】《基因治療研發(fā)和生產(chǎn)外包服務市場研究報告》��,弗若斯特沙利文咨詢公司��,2021年5月
【2】《基因治療的研究進展》��,中國細胞生物學學報��,2020年4月
【3】《2022基因治療行業(yè)研究報告》��,動脈網(wǎng)��、蛋殼研究院��,2022年6月