生物制藥行業(yè)如火如荼的發(fā)展�,對(duì)相關(guān)配套技術(shù)也提出了更高的要求。且一款生物制品從臨床前研究到上市�,正常需要8~12年時(shí)間,期間需要大量的研發(fā)投入�。而激烈的市場(chǎng)角逐,以及相關(guān)的生物仿制藥和后續(xù)藥物的開(kāi)發(fā)�,迫使該行業(yè)降低成本并保持靈活性以應(yīng)對(duì)市場(chǎng)的變化。
這也因此加速了在生物制品的研發(fā)生產(chǎn)中�,一次性系統(tǒng)取代不銹鋼系統(tǒng)的趨勢(shì)。使用一次性系統(tǒng)可以通過(guò)降低資本成本�,提高工廠靈活性,減少啟動(dòng)時(shí)間和成本以及消除非增值工藝步驟和交叉污染風(fēng)險(xiǎn)來(lái)顯著影響制造工藝效率�。此外,它還顯著降低了工藝液體浪費(fèi)�、人工成本以及現(xiàn)場(chǎng)質(zhì)量和驗(yàn)證要求。
如今�,一次性工藝正逐漸取代不銹鋼系統(tǒng),涵蓋了整個(gè)生物制藥工藝過(guò)程的各個(gè)單元操作�,從上游細(xì)胞培養(yǎng)到下游純化,直至最終灌裝�。但在實(shí)際應(yīng)用中�,如果制藥商們無(wú)法以安全穩(wěn)妥的方式將各個(gè)組件以完全封閉的形式連接成一個(gè)完整的無(wú)菌系統(tǒng)�,那么一次性技術(shù)的優(yōu)勢(shì)將無(wú)法得到充分發(fā)揮,過(guò)程中的風(fēng)險(xiǎn)也將增加�。
總的來(lái)說(shuō),在生物工藝的流體系統(tǒng)中�,通常意義上的快速插拔式連接(如魯爾接頭)屬于開(kāi)放式連接�;而一次性無(wú)菌連接領(lǐng)域的傳統(tǒng)解決方案,即無(wú)菌軟管接管機(jī)/封管機(jī)是否可以確保完整的封閉式連接也存在爭(zhēng)議�。
包括魯爾接頭在內(nèi)的快速插拔連接方案通常能和相應(yīng)管道配套使用,但這種接頭屬于開(kāi)放式連接�,對(duì)操作環(huán)境的要求很高,使用過(guò)程需配備層流罩(即需在層流保護(hù)下使用)或在Class A環(huán)境下使用�。當(dāng)脫離無(wú)菌環(huán)境,開(kāi)放式連接依然可能帶來(lái)外部污染�。
此外,封管機(jī)和接管機(jī)也是軟管無(wú)菌連接的傳統(tǒng)解決方案�。由于需要用到加熱刀片,封管機(jī)和接管機(jī)仍然有可能將外部的污染物帶入管路中�,而且操作過(guò)程相對(duì)繁瑣,增加了時(shí)間成本�。同時(shí),這兩種機(jī)器也需適配特定型號(hào)的熱塑管�,增加庫(kù)存壓力和耗材成本,也增加了未知的風(fēng)險(xiǎn)�。
基于此�,傳統(tǒng)的一次性無(wú)菌連接需要解決一些連接技術(shù)上的挑戰(zhàn)�,才能實(shí)現(xiàn)完整的全封閉系統(tǒng):
傳統(tǒng)的無(wú)菌連接方案對(duì)環(huán)境要求很高,而且依然存在外源性的污染風(fēng)險(xiǎn)(比如接管機(jī)的刀片等)�。如何能在在有菌環(huán)境中仍然實(shí)現(xiàn)可靠、易操作的無(wú)菌連接和斷開(kāi)�?
無(wú)菌連接和斷開(kāi)的傳統(tǒng)解決方案需要不同的輔助設(shè)備和步驟。是否有能簡(jiǎn)化無(wú)菌連接和無(wú)菌斷開(kāi)的操作流程�,將兩種功能進(jìn)行集成,從而節(jié)省時(shí)間和空間�、降低風(fēng)險(xiǎn)?
除了上述基于降低污染風(fēng)險(xiǎn)的考慮�,一次性系統(tǒng)的推進(jìn)還需要考慮以下因素:
體積限制了一次性設(shè)備在大規(guī)模生產(chǎn)上的運(yùn)用,包括大流量的下游應(yīng)用和小流量的的小管路連接方案�,比如針對(duì)細(xì)胞與基因治療(CGT)領(lǐng)域的一次性連接。隨著對(duì)更高產(chǎn)量生物制品和CGT應(yīng)用的需求增加�,一次性部件制造商已經(jīng)在朝這個(gè)方向研發(fā)新的解決方案。比如�,CPC的AseptiQuik L 可以做到1英寸到1.5英寸的大流量,而MicroCNX® 系列則可以連接小至1/16英寸(1.6mm)的管路�。
一次性部件的完整性以及溶出物、析出物相關(guān)風(fēng)險(xiǎn)也需要企業(yè)針對(duì)自己的產(chǎn)品工藝進(jìn)行評(píng)估�。目前形成趨勢(shì)的解決方案便是由部件制造商來(lái)對(duì)一次性部件進(jìn)行預(yù)驗(yàn)證。
一次性設(shè)備的對(duì)接�、溶液轉(zhuǎn)移等步驟的自動(dòng)化改良將是大勢(shì)所趨,以減少隱形的人工成本和人工干預(yù)風(fēng)險(xiǎn),保證產(chǎn)品的一致性和有效性等�,同時(shí)減輕監(jiān)管負(fù)擔(dān)。
新一代的無(wú)菌連接技術(shù)
可見(jiàn)�,傳統(tǒng)的連接技術(shù)在有效形成封閉系統(tǒng)和靈活使用等方面均有可提升的空間。CPC 的一次性無(wú)菌連接系列產(chǎn)品便是為幫助制藥商快速輕松�、安全地傳輸生物介質(zhì)而研發(fā)。
AseptiQuik® G DC 連接器是 CPC AseptiQuik® G 系列不分公母無(wú)菌連接器的最新成員�,在無(wú)菌連接的基礎(chǔ)上增加了無(wú)菌斷開(kāi)功能。
為了進(jìn)一步簡(jiǎn)化生物制藥�,CPC實(shí)現(xiàn)了只需用一個(gè)產(chǎn)品便可以進(jìn)行無(wú)菌連接和斷開(kāi),無(wú)需使用額外的卡箍�、夾具或接管機(jī)/封管機(jī)等任何輔助設(shè)備即可實(shí)現(xiàn)無(wú)菌連接和斷開(kāi)。
AseptiQuik® G DC 連接器軟管倒鉤端接尺寸包括 1/4英寸�、3/8英寸 和 1/2英寸�。其薄膜拉片可以確保同時(shí)安全去除兩個(gè)膜片,內(nèi)置自動(dòng)截止閥�,能在各種極端條件下實(shí)現(xiàn)可靠性能。
MicroCNX®是首款針對(duì)小規(guī)模封閉式無(wú)菌工藝的一次性連接器�,為生物制藥和再生醫(yī)學(xué)領(lǐng)域的研發(fā)制造商提供一種簡(jiǎn)單、高效的小規(guī)模管路連接方案�。
專為廣泛使用小管徑的應(yīng)用而設(shè)計(jì),包括1/16英寸(1.6mm)�、3/32英寸(2.4mm)和1/8英寸(3.2mm),適用但不限于采樣�、培育擴(kuò)增和早期細(xì)胞培養(yǎng)等工藝。
保證各連接流動(dòng)路徑一致�,幫助制造商提高效率�,減少創(chuàng)建封閉系統(tǒng)的時(shí)間和總成本�,提供可靠的結(jié)果。
CPC的創(chuàng)新技術(shù)可以幫助制藥商在有菌環(huán)境中仍然快速地進(jìn)行管路的無(wú)菌連接和斷開(kāi)�,形成真正的封閉式系統(tǒng)。直觀的“翻轉(zhuǎn)—咔嗒—拉拔”三步操作設(shè)計(jì)�,可以確保用戶方便傳輸介質(zhì),降低因操作失誤所導(dǎo)致的風(fēng)險(xiǎn)�。
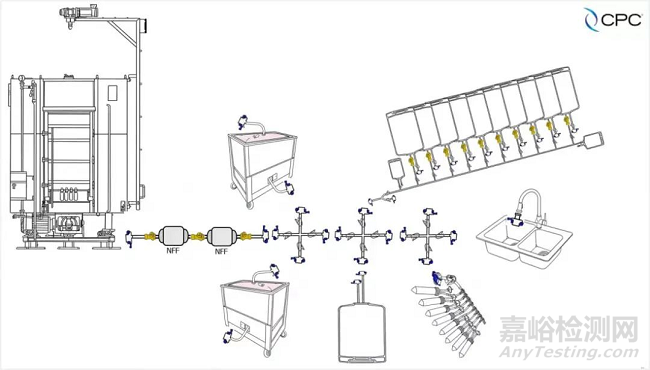
上游細(xì)胞培養(yǎng)中的無(wú)菌連接方案
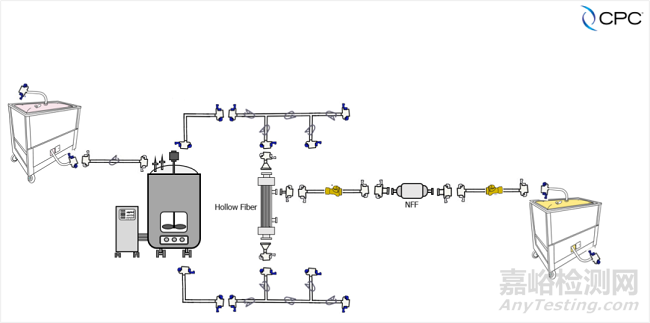
下游純化過(guò)濾中的無(wú)菌連接方案
結(jié)語(yǔ)
對(duì)于無(wú)菌工藝而言,連接和斷開(kāi)管路進(jìn)行流體輸送而不增加污染風(fēng)險(xiǎn)是其關(guān)鍵�。無(wú)菌連接技術(shù)可以將不同的子系統(tǒng)或工藝組合起來(lái)形成真正的封閉系統(tǒng),從而提高了從上游發(fā)酵至下游灌裝過(guò)程中的安全性�、靈活性和效率。由于連接件是保持工藝無(wú)菌性的決定性因素之一�,制藥商需要仔細(xì)選擇合適的連接方案和產(chǎn)品。同時(shí)�,制藥商應(yīng)按照市場(chǎng)需求,持續(xù)開(kāi)發(fā)產(chǎn)品�,以滿足制藥商對(duì)無(wú)菌處理的需求。
參考來(lái)源:
[1]Jayaraman P, Lim R, Ng J, Vemuri MC. Acceleration of Translational Mesenchymal Stromal Cell Therapy Through Consistent Quality GMP Manufacturing. Front Cell Dev Biol. 2021 Apr 13;9:648472. doi: 10.3389/fcell.2021.648472. PMID: 33928083; PMCID: PMC8076909.
[2]https://doi.org/10.1016/j.fbp.2013.12.002
[3]https://doi.org/10.1016/j.tibtech.2012.10.004
[4]洪小栩.藥品生產(chǎn)用一次性使用系統(tǒng)風(fēng)險(xiǎn)管控的思考[J].中國(guó)食品藥品監(jiān)管,2022(02):51-59.
[5]黃景德,劉薇,黃義.一次性使用系統(tǒng)可靠性試驗(yàn)方案設(shè)計(jì)與分析[J].大連交通大學(xué)學(xué)報(bào),2014,35(S1):131-134.