面對(duì)生產(chǎn)低風(fēng)險(xiǎn)醫(yī)療器械的制造商普遍關(guān)心的問(wèn)題��,MDSAP認(rèn)證是可以豁免的么��?新版MDSAP審計(jì)方法為大家?guī)?lái)了答案����。
2022年MDSAP AUDIT APPROACH 迎來(lái)了更新版本,其中一個(gè)顯著變化是,新增了附錄6�,澄清了MDSAP五國(guó)的監(jiān)管機(jī)構(gòu)允許的豁免政策。
"審核組織不得將任何過(guò)程��、產(chǎn)品或服務(wù)排除在審核范圍或證書范圍之外��,除非認(rèn)可的監(jiān)管機(jī)構(gòu)所管理的法規(guī)允許排除"��。這一要求被用來(lái)證明參加MDSAP的組織必須接受認(rèn)證范圍的審核�,包括所有醫(yī)療器械分銷的司法管轄區(qū),以及在這些司法管轄區(qū)分銷的所有醫(yī)療設(shè)備����。
有資格被排除在MDSAP計(jì)劃之外的活動(dòng)/過(guò)程����、產(chǎn)品或設(shè)備首次在MDSAP AUDIT APPROACH中以附件的方式列出。
請(qǐng)注意:
● 一個(gè)設(shè)備只有在符合所有適用于審計(jì)的管轄區(qū)的相應(yīng)排除標(biāo)準(zhǔn)時(shí)����,才能被排除在MDSAP的審計(jì)范圍之外。
● 一個(gè)轄區(qū)只有在沒(méi)有任何醫(yī)療設(shè)備在該轄區(qū)銷售的情況下才可以被排除����,或者在該轄區(qū)銷售的所有醫(yī)療設(shè)備都可以被排除。
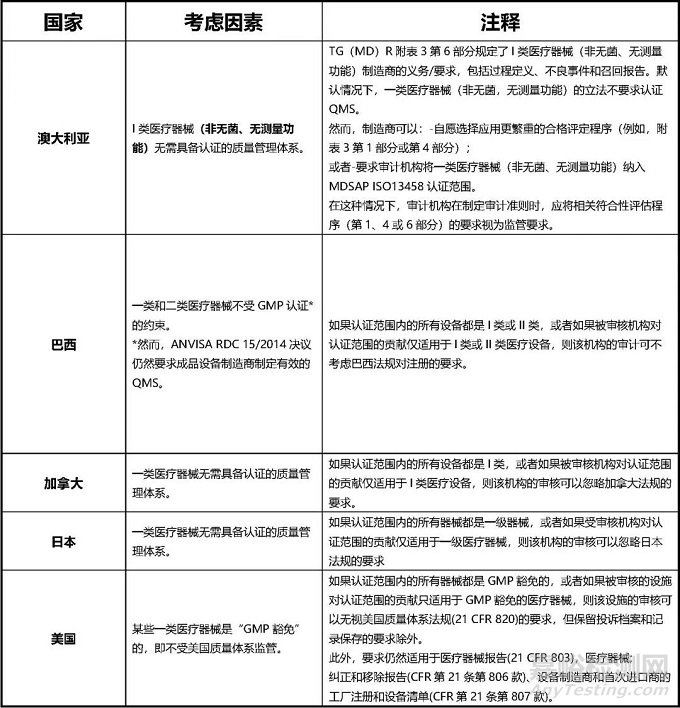
從上我們可以看到,并非所有的一類醫(yī)療器械制造商可以豁免在質(zhì)量體系認(rèn)證之外����,比如澳大利亞對(duì)一類滅菌和一類帶測(cè)量功能的設(shè)備是不能豁免的;巴西雖然對(duì)一類醫(yī)療器械制造商豁免體系認(rèn)證����,但仍要求成品制造商制定有效的質(zhì)量管理體系。
美國(guó)的要求中明確指明了僅GMP豁免的一類器械才可以����。
從如下FDA官網(wǎng)中我們可以查詢510(k)豁免清單和GMP的要求:
Medical Device Exemptions 510(k) and GMP Requirements (fda.gov)
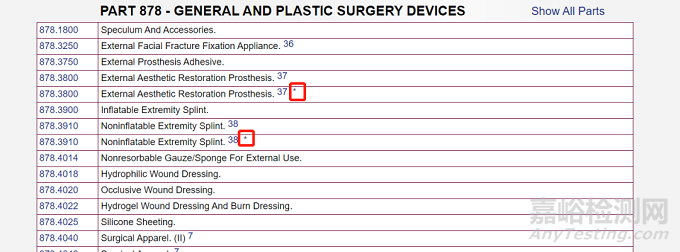
在網(wǎng)頁(yè)上我們可以看到重要提醒:只有帶星號(hào)(*)的I類器械也被豁免于GMP法規(guī)。
而從下面的截圖我們可以看到只有極少數(shù)產(chǎn)品標(biāo)注了*號(hào)��。這就是說(shuō)美國(guó)可以豁免GMP的器械其實(shí)是很少的����。