FDA的醫(yī)療器械開發(fā)工具(MDDT)計劃旨在通過提供一種更高效�、更可預(yù)測的方法來收集必要的信息,以支持監(jiān)管提交和相關(guān)決策�����,從而促進(jìn)醫(yī)療器械的開發(fā)和及時評估�,并促進(jìn)創(chuàng)新。
醫(yī)療器械贊助商可以選擇在醫(yī)療器械的開發(fā)和評估中使用這些MDDT工具�����。這些工具包括:生物標(biāo)記測試�����、臨床醫(yī)生報告的結(jié)果測量�、患者報告的結(jié)果測量等工具,或者動物或計算模型等非臨床評估模型�����,以及傳感器或可穿戴設(shè)備等數(shù)字健康技術(shù)���,使用它們有助于FDA了解醫(yī)療設(shè)備在安全性�、有效性和其他性能方面的工作原理�。
MDDT計劃是自愿參加的,參加MDDT計劃將有助于提高器械開發(fā)和監(jiān)管審查的可預(yù)測性和效率�����。在決定是否對工具進(jìn)行認(rèn)證時�,F(xiàn)DA會評估該工具和可用的支持證據(jù),以確定其是否可用于在特定的使用環(huán)境下產(chǎn)生科學(xué)上合理的測量結(jié)果�����。醫(yī)療器械贊助商可以使用合格的工具���,并確保它們將被FDA接受���,而無需在相同的使用環(huán)境下再次確認(rèn)工具的適用性和實(shí)用性。
為什么FDA制定MDDT認(rèn)證計劃�?
在制定MDDT認(rèn)證計劃之前,F(xiàn)DA對每個醫(yī)療器械申請的工具進(jìn)行了逐案評估���。
FDA創(chuàng)建自愿MDDT計劃的目的是:
• 通過關(guān)注評估新技術(shù)所需的科學(xué)來推進(jìn)創(chuàng)新���。
• 提高醫(yī)療器械申辦者的可預(yù)測性���,明確FDA接受MDDT的評估,以證明醫(yī)療器械在合格的使用范圍內(nèi)使用時的安全性���、有效性或性能���。
• 通過促進(jìn)在多個醫(yī)療器械提交和制造商之間使用經(jīng)過驗證和合格的工具,提高效率和透明度�。
• 鼓勵在開發(fā)工具和支持證據(jù)方面的合作,以集中資源并推動合格工具的使用和接受�。
目前批準(zhǔn)的合格的醫(yī)療器械開發(fā)工具(MDDTs)有哪些?
FDA已經(jīng)批準(zhǔn)了用于心血管�、神經(jīng)病學(xué)、眼科�、整形外科、自動胰島素給藥和成像設(shè)備的MDDTs�,以及用于植入式醫(yī)療器械和網(wǎng)絡(luò)安全的橫切工具。
近日新增了一個工具--Chemical RISk (CHRIS) Calculator�。
Chemical RISk (CHRIS) Calculator的特點(diǎn)
• 是一種非臨床評估模型(NAM),可被醫(yī)療器械公司和贊助研究人員用于進(jìn)行篩選級別的風(fēng)險評估�����,以幫助對含有顏色添加劑(CAs)的聚合醫(yī)療器械組件進(jìn)行生物相容性評估。
• 計算聚合醫(yī)療器械組件中包含的CA的安全值保守余量���,以幫助確定是否需要根據(jù)用戶提供的輸入對CA和/或相關(guān)雜質(zhì)進(jìn)一步評估一個或多個生物相容性端點(diǎn)���。與其他MDDT一樣�,所有評估都依賴于在其使用環(huán)境中使用的工具。
• 可協(xié)助器械制造商提供即時反饋���,說明器械中是否存在CA或與CA相關(guān)的其他添加劑和雜質(zhì)���,需要額外的論證和/或測試,以證明可接受的生物風(fēng)險�����。
通過FDA認(rèn)證的MDDTs見如下截圖���,每個批準(zhǔn)的MDDT的證據(jù)和認(rèn)證依據(jù)摘要(SEBQ)會公布在FDA官網(wǎng)�。該總結(jié)包括:
• 工具的簡要描述
• 限定的使用上下文
• 支持資格證明的證據(jù)概述
• 使用該工具的優(yōu)點(diǎn)和缺點(diǎn)的簡要評估
• 關(guān)于如何聯(lián)系工具開發(fā)人員以訪問工具的信息
醫(yī)療器械申辦者提交依賴于合格MDDT的上市申請時�����,可在cover letter或3514表格(F或J部分)中包含MDDT提交編號。每個合格工具的MDDT提交號可以在SEBQ中找到�����。
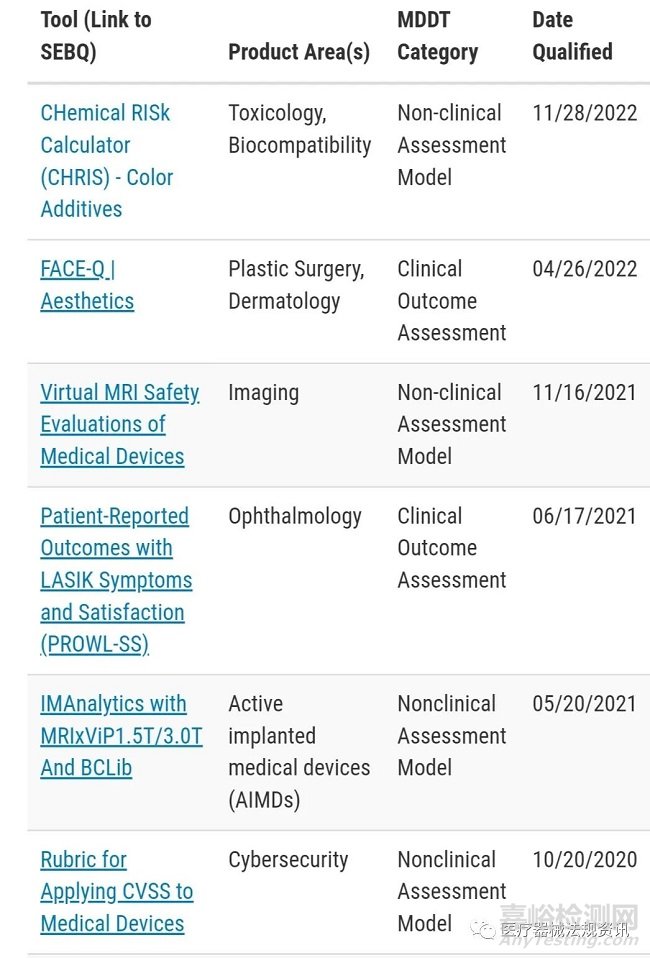
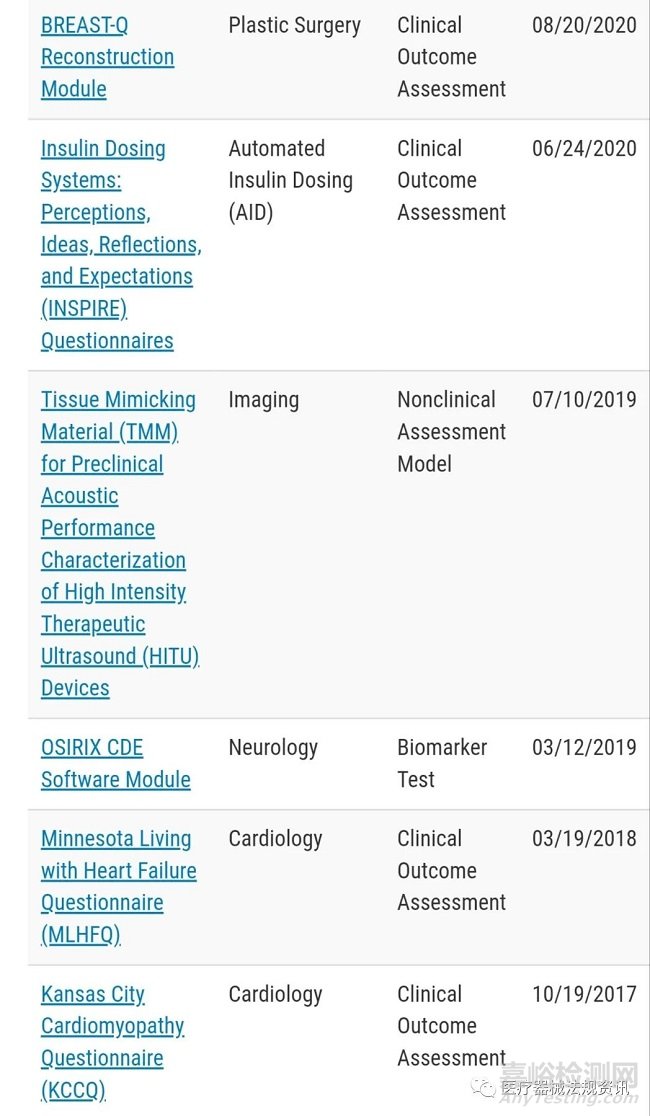
MDDT類別有哪些�?
FDA將MDDTs分為三類,主要通過工具測量相關(guān)參數(shù)的方式來區(qū)分:
1�����、臨床結(jié)果評估(COA)可以通過臨床醫(yī)生���、患者�����、非臨床醫(yī)生觀察者報告或者通過基于性能的評估來進(jìn)行�����。它可用于告知患者資格或臨床研究終點(diǎn)�。有關(guān)COAs的詳細(xì)信息�����,請參見醫(yī)療器械決策中的臨床結(jié)果評估(COAs)。
2���、生物標(biāo)記測試(BT)是一種用于檢測或測量生物標(biāo)記的測試或儀器���。生物標(biāo)記測試可用于評估風(fēng)險,或識別安全性問題�,或預(yù)測患者的治療結(jié)果���。
3�、非臨床評估模型(NAM)是一種測量或預(yù)測器械功能或體內(nèi)器械性能的非臨床測試模型或方法�����。它可以是計算機(jī)模型或動物模型���,用于:
• 測量或預(yù)測感興趣的參數(shù)
• 減少或取代動物試驗
• 減少測試持續(xù)時間或樣本量���。
關(guān)于MDDT類別的更多信息,請見最終指南Qualification of Medical Device Development Tools���。



