今日頭條
賽生GD2單抗獲批用于神經(jīng)母細(xì)胞瘤�。賽生藥業(yè)與Y-mAbs Therapeutics合作開發(fā)的那西妥單抗(naxitamab-gqgk,Danyelza)獲國家藥監(jiān)局批準(zhǔn)上市�����,用于治療復(fù)發(fā)性或難治性高危神經(jīng)母細(xì)胞瘤患者��。那昔妥單抗是一款GD2單抗�,通過與腫瘤細(xì)胞表面的GD2結(jié)合,能夠引起抗體介導(dǎo)的細(xì)胞毒性反應(yīng)并激活補(bǔ)體系統(tǒng)����,從而達(dá)到殺傷腫瘤的效果。2020年11月��,F(xiàn)DA已加速批準(zhǔn)那昔妥單抗上市�。
國內(nèi)藥訊
1.暉致HIV三合一復(fù)方國內(nèi)獲批上市。暉致醫(yī)藥申報(bào)的5.1類新藥依非米替片(I)獲國家藥監(jiān)局批準(zhǔn)上市�,用于治療成人和體重至少35kg兒童患者中的1型人免疫缺陷病毒(HIV-1)感染。這是Mylan公司開發(fā)的一款三聯(lián)組合療法,每片含有依非韋倫400mg�����、拉米夫定300mg及富馬酸替諾福韋二吡呋酯300mg��,已在海外獲批上市��,商品名為Symfi Lo�����,用于治療成人和兒童HIV-1感染者�����。
2.綠葉抗抑郁癥1類新藥Ⅲ期臨床積極��。綠葉制藥將在BESETO會(huì)議上公布鹽酸托魯?shù)匚睦ㄐ辆忈屍?/span>(LY03005)用于治療抑郁癥的Ⅲ期臨床研究結(jié)果����。與安慰劑相比���,LY03005組第八周時(shí)患者的蒙哥馬利-艾斯伯格抑郁量表(MADRS)�����、17項(xiàng)漢密爾頓抑郁量表(HAM-D17)和漢密爾頓焦慮量表(HAM-A)的評分較基線的變化均具顯著性改善����。藥物的耐受性良好,不引發(fā)嗜睡����,不影響性功能、體重和脂代謝����。
3.和譽(yù)FGFR抑制劑尿路上皮癌II期臨床積極。和譽(yù)醫(yī)藥泛FGFR抑制劑Fexagratinib治療尿路上皮癌中國患者的II期臨床結(jié)果積極����。大部分伴有FGFR3變異的轉(zhuǎn)移性尿路上皮癌患者出現(xiàn)腫瘤縮小,約30.7% (4/13)的患者達(dá)到獨(dú)立評審委員會(huì)確認(rèn)的部分緩解��;在伴有FGFR3突變的癌患者中觀察到更好的緩解率(44%���,4/9)��。藥物總體耐受性良好����,在美國,F(xiàn)exagratinib已獲得FDA授予的針對胃癌治療的孤兒藥認(rèn)定�。
4.加科思KRAS抑制劑擬納入突破性治療品種。加科思1類新藥JAB-21822獲CDE擬納入突破性治療品種�,擬用于治療既往至少一種系統(tǒng)治療(至多不超過三線治療)的攜帶KRAS p. G12C突變的局部晚期或轉(zhuǎn)移性非小細(xì)胞肺癌患者。JAB-21822是一種KRAS p. G12C共價(jià)抑制劑���,加科思正在中國�、美國及歐洲同步臨床開發(fā)��。在Ⅰ期臨床中����,JAB-21822達(dá)到客觀緩解率為56.3%,疾病控制率為90.6%����。
5.石藥新冠口服3CL蛋白酶抑制劑獲批臨床�。石藥集團(tuán)宣布抗新冠病毒口服小分子3CL蛋白酶抑制劑SYH2055獲國家藥監(jiān)局批準(zhǔn),將在中國開展臨床試驗(yàn)�����。SYH2055是一款擁有全球自主知識(shí)產(chǎn)權(quán)的口服小分子1類新藥,旨在通過作用于新冠病毒主蛋白酶抑制病毒前體蛋白的切割���,進(jìn)而阻斷病毒復(fù)制并發(fā)揮抗新冠病毒的作用����。該產(chǎn)品有望克服奈瑪特韋必須與利托那韋聯(lián)用的缺陷��,覆蓋更多患者群體��。
國際藥訊
1.全球首款逆轉(zhuǎn)擴(kuò)瞳眼科新藥報(bào)NDA�。Ocuphire公司已向FDA提交其含有0.75%的酚妥拉明滴眼液Nyxol的新藥申請 (NDA),用于逆轉(zhuǎn)由腎上腺素能激動(dòng)劑(例如去氧腎上腺素)或副交感神經(jīng)阻滯劑(例如托吡卡胺)或其組合引起的擴(kuò)瞳��。Nyxol可通過特異性阻斷僅在虹膜擴(kuò)張肌上表達(dá)的α1受體來調(diào)節(jié)瞳孔大小����。來自MIRA-2和MIRA-3研究結(jié)果顯示,與安慰劑相比�,Nyxol在90分鐘內(nèi)使患者瞳孔直徑恢復(fù)至基線水平(≤0.2mm)的比例更高(49%vs6%,58%vs7%)�。
2.第一三共HER2-ADC臨床最新數(shù)據(jù)積極。阿斯利康與第一三共開發(fā)的HER2-ADC新藥Enhertu(trastuzumab deruxtecan)在既往接受曲妥珠單抗和紫杉烷治療的HER2陽性不可切除/轉(zhuǎn)移性乳腺癌的Ⅲ期臨床(DESTINY-Breast03)結(jié)果積極����。與活性對照組相比���,Enhertu降低36%的死亡風(fēng)險(xiǎn)(HR:0.64,CI:0.47-0.87���,p=0.0037)���;第2年時(shí),兩組預(yù)估生存率分別為77.4%與69.9%���。詳細(xì)數(shù)據(jù)公布在SABCS2022大會(huì)上�����,并同時(shí)發(fā)布于《柳葉刀》上����。
3.抑郁癥速效鼻噴劑獲FDA快速通道認(rèn)定��。Vistagen公司靶向鼻化學(xué)感覺受體細(xì)胞的神經(jīng)活性類固醇噴霧劑PH10獲FDA授予快速通道資格�,用于鼻內(nèi)給藥治療重度抑郁癥(MDD)。在為期8周的IIa期臨床中����,6.4μg PH10每日兩次鼻內(nèi)給藥在一周內(nèi)就能使患者漢密爾頓抑郁量表(HAM-D-17)評分顯著改善;而且PH10起效快速�、副作用極小。
4.TL1A單抗炎癥性腸?��、蚱谂R床數(shù)據(jù)積極��。Prometheus Biosciences公司潛在“first-in-class”抗TL1A單抗PRA023�,在治療潰瘍性結(jié)腸炎(UC)和克羅恩病(CD)的兩項(xiàng)Ⅱ期臨床結(jié)果積極�。在治療中重度UC的試驗(yàn)中,PRA023治療組12周時(shí)達(dá)到臨床緩解的患者比例為26.5%(對照組為1.5%����,p<0.0001))。在治療中重度活動(dòng)性CD的試驗(yàn)中���,PRA023組中26.0%獲得內(nèi)鏡緩解�,與歷史安慰劑組緩解率(12%)相比具統(tǒng)計(jì)學(xué)意義(p=0.002)����。藥物總體耐受性良好。
5.eIF2B激動(dòng)劑漸凍人癥早期臨床積極�。Denali公司eIF2B激動(dòng)劑DNL343治療肌萎縮側(cè)索硬化(ALS)的Ⅰb期臨床結(jié)果積極。DNL343旨在通過抑制ISR通路�,預(yù)防或減緩與應(yīng)激顆粒形成和TDP-43聚集相關(guān)的疾病進(jìn)展��。中期結(jié)果顯示���,DNL343在血漿中呈劑量依賴性增加;腦脊液中藥物與血漿中未結(jié)合藥物的平均比例在1.02-1.23之間��,表明DNL343能穿過BBB進(jìn)入到中樞神經(jīng)系統(tǒng)中��;ISR通路生物標(biāo)志物(ATF4和CHAC1)的衰減��,顯示DNL343對該通路的強(qiáng)烈抑制作用�����。此外��,患者的耐受性良好���。
6.改良型細(xì)胞療法低劑量早期臨床積極�。Achilles公司在ESMO IO2022大會(huì)上公布新抗原反應(yīng)性T細(xì)胞(cNeT)治療晚期不可切除或轉(zhuǎn)移性非小細(xì)胞肺癌(NSCLC)和黑色素瘤的兩項(xiàng)Ⅰ/Ⅱa期臨床(CHIRON和THETIS)的中期更新數(shù)據(jù)�。在NSCLC患者中,使用小劑量的cNeT��、低劑量的淋巴細(xì)胞清除及IL-2治療后實(shí)現(xiàn)部分緩解和疾病穩(wěn)定�����;12周時(shí)達(dá)到71%的臨床緩解率����。在黑色素瘤患者組中,有50%的黑色素瘤患者(3/6)病情穩(wěn)定�。cNeT治療的安全性良好。
醫(yī)藥熱點(diǎn)
1.最大程度保障就醫(yī)安全有序����。12月7日,國務(wù)院聯(lián)防聯(lián)控機(jī)制綜合組印發(fā)《關(guān)于進(jìn)一步優(yōu)化就醫(yī)流程做好當(dāng)前醫(yī)療服務(wù)工作的通知》明確���,醫(yī)療機(jī)構(gòu)要繼續(xù)做好門診預(yù)檢分診工作�,通過多種方式查看就診患者48小時(shí)核酸檢測結(jié)果�。門診區(qū)域要?jiǎng)澐殖龊怂彡栃院完幮栽\療區(qū),分別接診相應(yīng)患者�。對于急診就診患者不得以沒有48小時(shí)核酸結(jié)果為由影響救治;對出現(xiàn)發(fā)熱��、呼吸道癥狀等患者�,引導(dǎo)至發(fā)熱門診就診,進(jìn)行抗原或者核酸檢測并開展相應(yīng)診療服務(wù)�����。《通知》強(qiáng)調(diào)�,未經(jīng)衛(wèi)生健康部門同意,不得擅自關(guān)閉發(fā)熱門診���。
2.浙江加強(qiáng)“西學(xué)中”培訓(xùn)管理�����。浙江省出臺(tái)《浙江省非中醫(yī)類別醫(yī)師學(xué)習(xí)中醫(yī)培訓(xùn)管理辦法(試行)》��,建立“理論培訓(xùn)學(xué)分制���、臨床實(shí)踐基地化、管理考核統(tǒng)一化”的西學(xué)中人員培養(yǎng)機(jī)制���,第一階段為線上理論培訓(xùn)���,第二階段為線下集中培訓(xùn)和臨床實(shí)踐培訓(xùn),各階段的培訓(xùn)時(shí)間一般為1年��。《管理辦法》明確�����,執(zhí)業(yè)醫(yī)師在取得“西學(xué)中”培訓(xùn)合格證后�,均可開展與專業(yè)相關(guān)的中醫(yī)診療活動(dòng)。
3.甘肅將“兩慢病”納入門診慢特病保障��。甘肅省醫(yī)保局印發(fā)通知�����,自2023年1月1日起��,將高血壓���、糖尿病“兩慢病”納入門診慢特病補(bǔ)助范圍,進(jìn)一步減輕省直醫(yī)保參?����;颊哚t(yī)療費(fèi)用負(fù)擔(dān)�����。參保人員自認(rèn)定之日起享受待遇,限額在一年內(nèi)有效�,高血壓年度內(nèi)最高支付限額為1500元,糖尿病年度內(nèi)最高支付限額為2000元���,報(bào)銷比例按90%計(jì)算�;每年7月1日之后認(rèn)定的年度限額減半�,不與高血壓(并發(fā)癥)、糖尿?。úl(fā)癥)重復(fù)享受待遇。
評審動(dòng)態(tài)
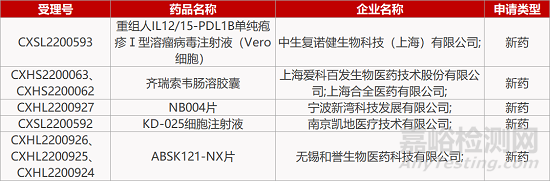
1. CDE新藥受理情況(12月08日)
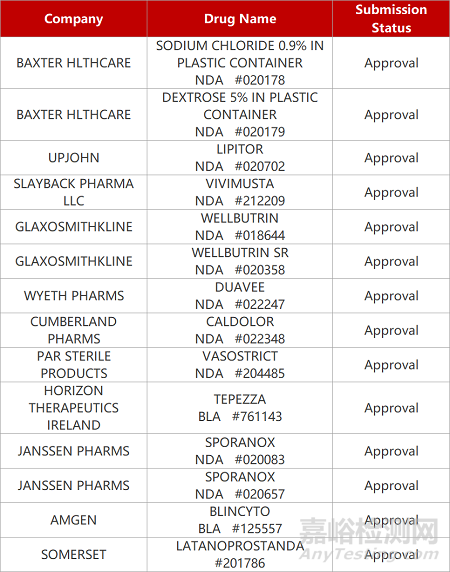
2. FDA新藥獲批情況(北美12月07日)