今日頭條
通化東寶雙靶點(diǎn)痛風(fēng)新藥獲批臨床����。通化東寶全資子公司東寶紫星1類化藥THDBH151片獲國家藥監(jiān)局臨床默示許可,擬用于痛風(fēng)的治療����。THDBH151是一款雙靶點(diǎn)抑制劑,能夠抑制黃嘌呤氧化酶(XO)���,從源頭上減少尿酸產(chǎn)生�;也能夠抑制腎小管URAT1轉(zhuǎn)運(yùn)體對尿酸重吸收���,加快尿酸排出����。此外���,THDBH151還能夠通過平衡好XO/Urat1在降尿酸中的作用����,在提高藥效的同時(shí)降低副作用。
國內(nèi)藥訊
1.再鼎引進(jìn)ADC啟動國際Ⅲ期臨床���。再鼎醫(yī)藥從Seagen公司引進(jìn)的“first-in-class”抗體偶聯(lián)藥物tisotumab vedotin(Tivdak)登記啟動一項(xiàng)國際(含中國)Ⅲ期臨床���,旨在復(fù)發(fā)性或轉(zhuǎn)移性宮頸癌患者中比較tisotumab vedotin與化療方案的臨床療效改善。該項(xiàng)試驗(yàn)計(jì)劃國際入組482人���,中國入組74人�。試驗(yàn)的中國部分將由中國醫(yī)學(xué)科學(xué)院腫瘤醫(yī)院主任醫(yī)師吳令英博士擔(dān)任主要研究者�,主要終點(diǎn)指標(biāo)為治療第21周的總生存期(OS)。
2.華夏英泰STAR-T獲FDA孤兒藥資格���。華夏英泰基于其創(chuàng)新STAR-T平臺開發(fā)的YTS104細(xì)胞注射液獲FDA授予孤兒藥資格����,用于治療復(fù)發(fā)/難治急性髓系白血病(R/R AML)�。該產(chǎn)品通過慢病毒基因轉(zhuǎn)導(dǎo),將特定STAR基因?qū)胱泽wT細(xì)胞內(nèi)并經(jīng)體外細(xì)胞擴(kuò)增制備�。YTS104采用兩個(gè)自主篩選的不同表位的納米抗體���,分別連接在STAR結(jié)構(gòu)的α鏈及β鏈上,預(yù)期具有更好的抗原識別和殺傷作用����。
3.中生制藥HER2靶向ADC獲批臨床�。中國生物制藥1類生物制品注射用TQB2102獲國家藥監(jiān)局臨床試驗(yàn)?zāi)驹S可,擬用于晚期惡性腫瘤的治療�。TQB2102是一種靶向HER2兩個(gè)非重疊表位ECD2及ECD4的抗體偶聯(lián)藥物(ADC)。與單抗及單抗ADC相比���,TQB2102對腫瘤細(xì)胞具有更強(qiáng)的結(jié)合���、內(nèi)化效率和殺傷作用,對HER2中低表達(dá)的腫瘤具有優(yōu)勢����。同時(shí),雙表位的特異性和ADC的作用機(jī)制能夠有效解決單抗的耐藥性�。
4.華昊中天【優(yōu)替德隆膠囊】在美獲批臨床。北京華昊中天開發(fā)的優(yōu)替德隆膠囊(UTD2)獲FDA臨床許可�。優(yōu)替德隆是一種埃博霉素類似物,其抗腫瘤機(jī)制與紫杉醇相似����,具備多藥耐藥和廣譜抗腫瘤活性����。華昊中天還計(jì)劃近期提交其優(yōu)替德隆注射液(UTD1)在美國開展注冊性臨床試驗(yàn)的申請����,尋求直接開展UTD1治療晚期乳腺癌的Ⅲ期臨床,以及治療晚期非小細(xì)胞肺癌的Ⅱ/Ⅲ期臨床�。
5.先聲PDL1/IL-15雙抗國內(nèi)獲批臨床。先聲藥業(yè)PD-L1/IL15v雙功能融合蛋白注射用SIM0237獲國家藥監(jiān)局臨床試驗(yàn)許可�,擬用于治療局部晚期不可切除或轉(zhuǎn)移性實(shí)體瘤。SIM0237通過結(jié)合PD-L1阻斷PD-1/PD-L1免疫抑制通路����,同時(shí)將IL-15直接遞送至腫瘤微環(huán)境,激活CD8+T細(xì)胞和NK細(xì)胞���,從而起到解除免疫抑制和激活免疫系統(tǒng)的雙重協(xié)同作用�。今年10月�,F(xiàn)DA已批準(zhǔn)該新藥在美國開展臨床研究。
6.百奧賽圖PD1/CD40雙抗國內(nèi)報(bào)IND���。百奧賽圖旗下祐和醫(yī)藥1類生物制品PD-1/CD40雙抗YH008的臨床試驗(yàn)申請獲NMPA受理���。YH008具有PD-1依賴的CD40激動活性�,同時(shí)又具有兩個(gè)靶點(diǎn)的免疫協(xié)同作用����,擬開發(fā)用于實(shí)體瘤和血液瘤的治療。今年12月19日����,YH008已獲FDA批準(zhǔn)開展I期臨床����,評估單藥治療PD-(L)1耐藥的晚期實(shí)體瘤和血液瘤患者的安全性和初步療效。
7.君實(shí)PD-1抑制劑海外授權(quán)�。君實(shí)生物宣布與Hikma MENA FZE公司就其PD-1藥物特瑞普利單抗達(dá)成獨(dú)家合作和許可協(xié)議。根據(jù)協(xié)議�,Hikma公司將獲得在約旦、沙特阿拉伯�、阿聯(lián)酋、卡塔爾����、摩洛哥、埃及等中東和北非地區(qū)共20個(gè)國家開發(fā)和商業(yè)化特瑞普利單抗����;君實(shí)生物將獲得合計(jì)最高達(dá)1,200萬美元的付款�,以及銷售凈額近20%的階梯分成���。此外�,君實(shí)還授予Hikma三項(xiàng)在研藥物在Hikma區(qū)域內(nèi)的優(yōu)先談判權(quán)���。
國際藥訊
1.新型基因療法兒科罕見病臨床積極����。美國加州大學(xué)舊金山分校研究人員開發(fā)的創(chuàng)新基因療法治療Artemis缺陷型重癥聯(lián)合免疫缺陷(Artemis-SCID)患兒的I/II期臨床結(jié)果積極�。將健康A(chǔ)rtemis基因拷貝添加到從患兒體內(nèi)收集的骨髓干細(xì)胞中,然后將經(jīng)過校正后的骨髓干細(xì)胞輸注回患兒身體���。所有患兒到12周時(shí)都長出自己的T細(xì)胞和B細(xì)胞����;有4例到12個(gè)月時(shí)實(shí)現(xiàn)完全的T細(xì)胞免疫重建�;有4例到24個(gè)月時(shí)也實(shí)現(xiàn)完全的B細(xì)胞免疫。
2.雅培微型植入止痛醫(yī)療器械獲批上市�。雅培基于其專有的BurstDR鎮(zhèn)痛技術(shù)開發(fā)的脊髓神經(jīng)刺激(SCS)系統(tǒng)Eterna獲FDA批準(zhǔn)上市,用于慢性疼痛的治療。BurstDR鎮(zhèn)痛技術(shù)能在疼痛信號從脊髓傳輸?shù)酱竽X的過程中�,通過發(fā)送溫和的周期性脈沖來改變疼痛信號。Eterna是目前市場上最小的可植入����、可充電脊髓刺激器,它一年只需要充電5次���,避免患者每天或每周充電的需求���。
3.日本批準(zhǔn)Aβ淀粉蛋白血檢試劑盒。Sysmex公司與衛(wèi)材開發(fā)的血液檢測試劑盒獲日本監(jiān)管機(jī)構(gòu)批準(zhǔn)�,用于測量血液中存在的兩種β-淀粉樣蛋白(Aβ)之間的比例����,以識別具有阿爾茨海默病標(biāo)志性癥狀的潛在患者。這種簡單的血檢方法可用于多次以跟蹤單個(gè)患者的進(jìn)展����。此前,分析這些蛋白質(zhì)需要進(jìn)行痛苦且更具侵入性的腰椎穿刺或昂貴的PET掃描����。
4.禮來與ProQR擴(kuò)大RNA編輯合作。禮來宣布擴(kuò)大與ProQR Therapeutics的合作協(xié)議,將利用后者Axiomer® RNA編輯平臺來獲得中樞神經(jīng)系統(tǒng)和外周神經(jīng)系統(tǒng)的其他靶點(diǎn)候選療法����。禮來將支付7500萬美元的預(yù)付款和股權(quán)投資,以及5000萬美元的進(jìn)一步擴(kuò)大合作關(guān)系的選擇權(quán)����。ProQR公司Axiomer®RNA編輯平臺能夠以高度靶向性和特異性的方式編輯RNA序列中的單個(gè)核苷酸,該技術(shù)平臺利用內(nèi)源性的腺苷脫氨酶ADAR特定編輯RNA序列中的單個(gè)核苷酸�。
5.Vistagen收購一家神經(jīng)疾病藥物公司。Vistagen公司宣布收購專注于神經(jīng)系統(tǒng)疾病的藥物研發(fā)公司Pherin Pharmaceuticals����,并獲得該公司全部研發(fā)管線。Pherin的主要候選產(chǎn)品包括臨床后期擬用于治療社交焦慮障礙(ASD)的神經(jīng)類固醇鼻噴劑PH94B���、擬用于治療重度抑郁癥(MDD)的神經(jīng)活性類固醇噴霧劑PH10���,以及用于治療重癥抑郁的口服NMDA受體抑制劑AV-101。通過收購�,Vistagen還將獲得3款臨床前階段的候選產(chǎn)品(PH15、PH80及PH284)����。
醫(yī)藥熱點(diǎn)
1.2023年度衛(wèi)生專業(yè)技術(shù)資格考試時(shí)間公布。12月26日,國家衛(wèi)健委人才交流服務(wù)中心發(fā)布《關(guān)于2023年度衛(wèi)生專業(yè)技術(shù)資格考試有關(guān)問題的通知》����,明確2023年度衛(wèi)生專業(yè)技術(shù)資格考試時(shí)間為4月15、16�、22、23日����。參加新冠疫情防控的一線醫(yī)務(wù)人員,晉升高一級職稱可提前一年申報(bào)參加考試����;對做出突出貢獻(xiàn),獲得省部級以上表彰獎勵的���,晉升高一級職稱可直接申報(bào)參加考試�。
2.上海探索派出麻醉醫(yī)生支援“120”院前急救����。上海市衛(wèi)健委日前透露�,針對近一周全上海120呼入量環(huán)比上升33.5%的嚴(yán)峻問題,上海15家三級醫(yī)院的45名麻醉醫(yī)師����、7個(gè)中心城區(qū)逾190名醫(yī)生已支援上海市急救中心����;各郊區(qū)衛(wèi)健委組織區(qū)屬醫(yī)院56名醫(yī)師支援郊區(qū)急救中心���。上海創(chuàng)新探索由麻醉醫(yī)生跟隨“120”救護(hù)車出診救治���,將有利于對危重病人作出準(zhǔn)確的評估以及及時(shí)處理,與國際院前急救體系接軌�。
3.遵義醫(yī)科大學(xué)成立全科醫(yī)學(xué)院。12月21日���,遵義醫(yī)科大學(xué)全科醫(yī)學(xué)院正式成立�,為貴州省首個(gè)全科醫(yī)學(xué)院���。遵義醫(yī)科大學(xué)創(chuàng)建于1947年����,是抗日戰(zhàn)爭勝利后中國共產(chǎn)黨創(chuàng)辦的第一所醫(yī)學(xué)本科院校�,曾用關(guān)東醫(yī)學(xué)院、大連大學(xué)醫(yī)學(xué)院�、大連醫(yī)學(xué)院等名稱�。全科醫(yī)學(xué)院的成立���,是該學(xué)校南遷貴州遵義后發(fā)展史上的重要里程碑����,整合學(xué)校優(yōu)質(zhì)醫(yī)療資源和教育資源�,將進(jìn)一步推動省級全科醫(yī)學(xué)的人才隊(duì)伍建設(shè)。
評審動態(tài)
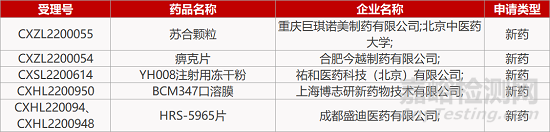
1. CDE新藥受理情況(12月26日)
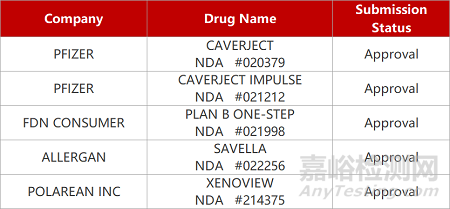
2. FDA新藥獲批情況(北美12月23日)