今日頭條
海思科EGFR靶向PROTAC報(bào)IND。海思科自主研發(fā)的1類化藥HSK40118片的臨床試驗(yàn)申請(qǐng)獲CDE受理�。HSK40118是一款EGFR-PROTAC小分子抗腫瘤藥物����,是該公司Protac研發(fā)平臺(tái)篩選出的第二款新藥,由靶向EGFR蛋白的小分子抑制劑、E3泛素連接酶的招募配體和連接這兩個(gè)部分的linker組成的三聯(lián)體���。該新藥擬開發(fā)用于治療EGFR突變的晚期非小細(xì)胞肺癌。
國內(nèi)藥訊
1.首個(gè)國產(chǎn)ECMO醫(yī)療器械獲批上市����。1月4日����,國家藥監(jiān)局應(yīng)急批準(zhǔn)深圳漢諾醫(yī)療科技開發(fā)的體外心肺支持輔助設(shè)備����、一次性使用膜式氧合器套包注冊(cè)申請(qǐng),二者配合使用����,用于急性呼吸衰竭或急性心肺功能衰竭�、其他治療方法難以控制并有可預(yù)見的病情持續(xù)惡化或死亡風(fēng)險(xiǎn)的成人患者���。這也是我國首個(gè)體外膜肺氧合治療(ECMO)設(shè)備和耗材套包����,具有自主知識(shí)產(chǎn)權(quán),性能指標(biāo)基本達(dá)到國際同類產(chǎn)品水平����。
2.捷思英達(dá)啟動(dòng)ERK抑制劑聯(lián)合用藥臨床。捷思英達(dá)宣布ERK抑制劑JSI-1187的臨床開發(fā)在美國已進(jìn)展至Ⅰ期劑量遞增階段���,聯(lián)合BRAF抑制劑達(dá)拉非尼開展針對(duì)已確診攜帶BRAF V600E/K突變的局部晚期或轉(zhuǎn)移性實(shí)體瘤患者的擴(kuò)展研究。ERK信號(hào)的重新激活是患者產(chǎn)生獲得性耐藥的關(guān)鍵�。ERK/BRAF抑制劑聯(lián)合治療有可能提供一種有針對(duì)性的方法,來延遲或克服患者的耐藥性���。
3.渤健引進(jìn)帕金森病新藥啟動(dòng)臨床。渤健從Denali Therapeutics引進(jìn)的小分子LRRK2抑制劑BIIB122(DNL151)登記啟動(dòng)一項(xiàng)國際(含中國)Ⅱb期臨床�,評(píng)估減緩30至80歲早期金森病受試者疾病惡化的有效性與安全性。計(jì)劃在國際入組640人���,在中國入組9人���。該項(xiàng)研究的中國部分由北京醫(yī)院主任醫(yī)師陳海波醫(yī)生擔(dān)任主要研究者。BIIB122旨在抑制LRRK2活性以恢復(fù)溶酶體的功能����,該新藥在海外已處于Ⅲ期臨床開發(fā)。
4.華藥康明溶瘤痘苗病毒獲FDA臨床批件���。華藥康明自主研發(fā)的溶瘤痘苗病毒產(chǎn)品KM1獲FDA批準(zhǔn)����,將在美國開展用于晚期惡性實(shí)體瘤治療的臨床研究。KM1是華藥康明申報(bào)的首款溶瘤病毒產(chǎn)品����,去年9月已獲得國家藥監(jiān)局臨床默示許可���,目前已啟動(dòng)國內(nèi)針對(duì)晚期實(shí)體瘤的Ⅰ期臨床試驗(yàn)準(zhǔn)備工作���。華藥康明另一主打產(chǎn)品溶瘤腺病毒KMAd1預(yù)計(jì)2023年第二季度申報(bào)IND����。
5.映恩生物DITAC授權(quán)Adcendo公司����。映恩生物宣布與Adcendo ApS公司簽訂技術(shù)許可協(xié)議����,將其獨(dú)創(chuàng)的DITAC平臺(tái)的技術(shù)授權(quán)給Adcendo公司�,用于治療間葉組織腫瘤的uPARAP ADC項(xiàng)目?��;贒ITAC設(shè)計(jì)的ADC產(chǎn)品���,可有效和持續(xù)地遞送毒素至腫瘤內(nèi)���,通過旁觀者效應(yīng)殺傷腫瘤抗原低表達(dá)甚至陰性表達(dá)的癌細(xì)胞����。根據(jù)協(xié)議���,映恩生物將獲得合作項(xiàng)目的首付款����、里程碑后期付款以及相應(yīng)的分層特許權(quán)使用費(fèi)���。
6.藥明生物4款抗體藥物授權(quán)GSK�。藥明生物宣布與葛蘭素史克達(dá)成許可協(xié)議,授予后者1款處于臨床前階段的TAA/CD3雙抗和至多3款處于早期發(fā)現(xiàn)階段的T細(xì)胞重定向雙抗(TCE)抗體的全球獨(dú)家研究���、開發(fā)���、生產(chǎn)和商業(yè)化權(quán)利�。根據(jù)協(xié)議���,藥明生物將獲得4000萬美元的首付款�,最高達(dá)14.6億美元的里程碑潛在付款,以及產(chǎn)品的銷售提成�。
國際藥訊
1.FIC端粒酶抑制劑血癌Ⅲ期臨床積極����。Geron公司潛在“first-in-class”端粒酶抑制劑imetelstat在治療復(fù)發(fā)/難治性低風(fēng)險(xiǎn)骨髓增生異常綜合征(MDS)的Ⅲ期臨床達(dá)到主要終點(diǎn)和關(guān)鍵次要終點(diǎn)。與安慰組相比�,imetelstat顯著提高不需要輸血的患者比例。第8周和24周時(shí)�,兩組維持不依賴輸血的患者比例分別為39.8%vs15.0%�,以及28.0%vs3.3%���。該公司計(jì)劃在今年向FDA和歐盟監(jiān)管機(jī)構(gòu)遞交上市申請(qǐng)�。
2.TL1A單抗治療BID的Ⅱb期臨床積極�。Roivant公司與輝瑞合作開發(fā)的TL1A單抗RVT-3101在治療潰瘍性結(jié)腸炎(IBD)的Ⅱb期臨床(TUSCANY-2)獲積極中期結(jié)果。數(shù)據(jù)顯示����,與安慰劑組相比���,RVT-3101組患者的臨床緩解率更高(32%vs12%�,p=0.01)����,內(nèi)鏡改善率更高(40%vs19%,p=0.01)���;在經(jīng)過生物標(biāo)志物篩選的患者隊(duì)列中�,接受預(yù)期Ⅲ期推薦劑量RVT-3101治療的患者的臨床緩解率為40%(vs10%,p=0.02)����,內(nèi)鏡改善率為56%(vs10%,p=0.0005)����。
3.BLyS/APRIL抑制劑IgA腎?��、騜期臨床成功�。Vera公司開發(fā)的BLyS/APRIL雙重抑制劑阿塞西普(Atacicept)在治療免疫球蛋白A腎病(IgAN)的Ⅱb期臨床(ORIGIN)達(dá)到主要終點(diǎn)���。Atacicept治療組患者第24周時(shí)通過UPCR評(píng)估的蛋白尿變化與基線相比平均降低31%(p=0.037)���,其中150mg劑量組的蛋白尿水平與基線相比減少33%(p=00.047)����。第36周時(shí)���,與安慰劑相比����,阿塞西普組患者的蛋白尿的進(jìn)一步減少,腎小球?yàn)V過率穩(wěn)定����,致病性Gd-IgA1持續(xù)降低。藥物的總體耐受性良好���。
4.FDA批準(zhǔn)DNA口腔矯治器用于OSA����。Vivos Therapeutics公司專有的DNA口腔矯治器(日間-夜間裝置)獲得FDA 510(k)批準(zhǔn),用于治療輕中度阻塞性睡眠呼吸暫停(OSA)����。DNA裝置主要通過打開氣道,讓患者從口呼吸轉(zhuǎn)為鼻呼吸���,解決許多人打鼾和/或OSA的根本原因�。在一項(xiàng)關(guān)于患者對(duì)DNA治療的滿意度的研究中����,97%的患者達(dá)到了預(yù)期效果�,愿意向朋友推薦這種治療���。
5.Belharra公司與羅氏達(dá)成合作協(xié)議�。Belharra公司宣布完成5000萬美元的A輪融資,并與羅氏旗下基因泰克公司達(dá)成長期研發(fā)合作���,利用基于光親和力(photoaffinity)的化學(xué)蛋白組學(xué)平臺(tái)����,合作開發(fā)非共價(jià)����、小分子候選藥物����。Belharra新一代化學(xué)蛋白組學(xué)平臺(tái)讓篩選過程可以在完整細(xì)胞環(huán)境中進(jìn)行����,不需要依靠獨(dú)特的氨基酸進(jìn)行標(biāo)記���,能夠探索整個(gè)蛋白組�。根據(jù)協(xié)議����,Belharra將獲得8000萬美元的預(yù)付款和高達(dá)20億美元的里程碑付款�。
6.GAA酶替代療法成功治療龐貝病胎兒����。加州大學(xué)舊金山分校�、杜克大學(xué)和渥太華大學(xué)聯(lián)合團(tuán)隊(duì)利用GAA酶替代療法(ERT)成功地治療了尚在子宮內(nèi)的患有龐貝病的胎兒���。研究團(tuán)隊(duì)在這名叫艾拉·巴希爾(Ayla Bashir)的小女孩的母親懷孕24周時(shí),開始通過臍靜脈注射GAA酶來進(jìn)行治療�。目前,這名小女孩已1歲半����,并達(dá)到發(fā)育里程碑,她的的心臟和肌肉功能正常�,且能走路,肌損傷和糖原積累的生物標(biāo)志物正常����。研究成果發(fā)表在《新英格蘭醫(yī)學(xué)期刊》(NEJM)上���。
醫(yī)藥熱點(diǎn)
1.中疾控:XBB近期引發(fā)大流行可能性極低�。針對(duì)“XBB.1.5毒株是否會(huì)攻擊人的腸道���?是否會(huì)引發(fā)二次感染”熱點(diǎn)問題,中國疾控中心微信公眾號(hào)于1月4日發(fā)布了該中心病毒病預(yù)防控制所專家的釋疑文章�。專家表示,無證據(jù)提示XBB.1.5比其他毒株更容易導(dǎo)致嚴(yán)重的腹瀉或胃腸道其他臨床表現(xiàn)���,我國3個(gè)月內(nèi)由XBB系列變異株引發(fā)大規(guī)模流行的可能性極低����。
2.新型抗腫瘤藥物應(yīng)用原則發(fā)布���。近日�,國家衛(wèi)健委發(fā)布《新型抗腫瘤藥物臨床應(yīng)用指導(dǎo)原則(2022年版)》。新版指導(dǎo)原則增加了多種新型抗腫瘤藥物���。其中����,呼吸系統(tǒng)腫瘤用藥由原來的26種增加到32種,消化系統(tǒng)腫瘤用藥由原來的22種增加到28種�,血液腫瘤用藥由原來的21種增加到29種,泌尿系統(tǒng)腫瘤用藥由11種增加到17種等���。該指導(dǎo)原則還增加了不同器官重啟免疫治療注意事項(xiàng)���。
3.鄭正春任湖北省腫瘤醫(yī)院黨委書記。1月5日上午����,湖北省腫瘤醫(yī)院召開全院干部大會(huì),宣布湖北省衛(wèi)健委關(guān)于省腫瘤醫(yī)院黨委書記任免決定���,任命鄭正春同志為湖北省腫瘤醫(yī)院黨委書記����、黨委委員。鄭正春表態(tài)����,將以奮斗者的姿態(tài)投入省腫瘤醫(yī)院的發(fā)展���,與院長魏少忠同志一起團(tuán)結(jié)帶領(lǐng)全院干部職工銳意進(jìn)取、開拓創(chuàng)新���、腳踏實(shí)地����、埋頭苦干���,努力以高質(zhì)量黨建引領(lǐng)醫(yī)院的高質(zhì)量發(fā)展����。
評(píng)審動(dòng)態(tài)
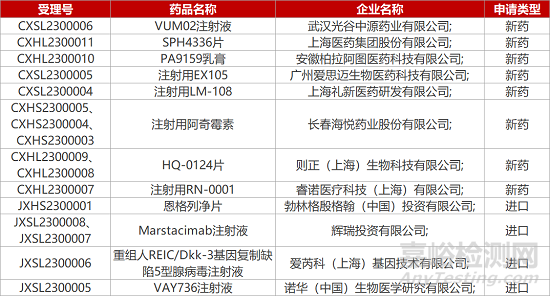
1. CDE新藥受理情況(01月05日)
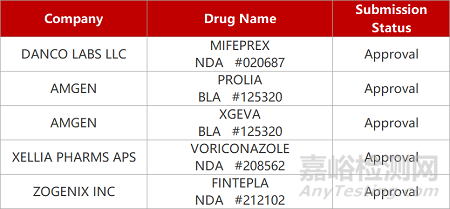
2. FDA新藥獲批情況(北美01月4日)