注冊(cè)基本原則:
基于軟件安全性級(jí)別提交注冊(cè)申報(bào)資料
詳盡程度取決于安全性級(jí)別和復(fù)雜程度
獨(dú)立軟件和軟件組件申報(bào)原則總體相同
安全性級(jí)別
YY/T 0664《醫(yī)療器械軟件 軟件生存周期過(guò)程》進(jìn)行分級(jí)���,軟件安全性級(jí)別基于軟件損害嚴(yán)重度分為:
A級(jí):不可能對(duì)健康有傷害和損壞;
B級(jí):可能有不嚴(yán)重的傷害�����;
C級(jí):可能死亡或嚴(yán)重傷害���。
判定原則
時(shí)機(jī):采取風(fēng)險(xiǎn)控制措施之前
方法:基于定義�����、風(fēng)險(xiǎn)管理
要素:預(yù)期用途���、使用場(chǎng)景、核心功能
一�、劃分獨(dú)立軟件的注冊(cè)單元
醫(yī)療器械產(chǎn)品注冊(cè)單元應(yīng)以產(chǎn)品技術(shù)結(jié)構(gòu)、性能指標(biāo)和預(yù)期用途為劃分依據(jù)�����,產(chǎn)品技術(shù)結(jié)構(gòu)�����、性能指標(biāo)或預(yù)期用途不同���,原則上應(yīng)劃分為不同的注冊(cè)單元���。
1. 技術(shù)結(jié)構(gòu)
產(chǎn)品的基本原理不同,應(yīng)劃分為不同的注冊(cè)單元���。
例如:
利用電化學(xué)法為基本原理的血糖儀與利用光化學(xué)法為基本原理的血糖儀應(yīng)劃分為不同的注冊(cè)單元�����。
2. 性能指標(biāo)
性能指標(biāo)有較大差異的�����,應(yīng)考慮劃分為不同的單元�����。
3. 預(yù)期用途
產(chǎn)品預(yù)期用途不同�����,應(yīng)劃分為不同的注冊(cè)單元�����。
二�、醫(yī)療器械軟件標(biāo)準(zhǔn)基礎(chǔ)
GB/T 25000.51-2016《系統(tǒng)與軟件工程 系統(tǒng)與軟件質(zhì)量要求和評(píng)價(jià) 第51部分:就緒可用軟件產(chǎn)品的質(zhì)量要求和測(cè)試細(xì)則》
YY 0775-2010《遠(yuǎn)距離放射治療計(jì)劃系統(tǒng)高能X(γ)射束劑量計(jì)算準(zhǔn)確性要求和試驗(yàn)方法》
YY 0637-2013《醫(yī)用電氣設(shè)備 放射治療計(jì)劃系統(tǒng)的安全要求》
YY/T 0664-2017《醫(yī)療器械軟件 軟件生存周期過(guò)程》
三、編制獨(dú)立軟件的產(chǎn)品技術(shù)要求和測(cè)試文檔
應(yīng)當(dāng)滿足《醫(yī)療器械軟件注冊(cè)技術(shù)審查指導(dǎo)原則》附錄Ⅰ中獨(dú)立軟件模板所列舉的條款的要求���,由于獨(dú)立軟件其本質(zhì)上是計(jì)算機(jī)程序���,無(wú)實(shí)體既看不見(jiàn)也摸不著,因此在編制產(chǎn)品技術(shù)要求時(shí)�,對(duì)于沒(méi)有測(cè)試工具或測(cè)試軟件的功能性檢查,應(yīng)采用黑盒測(cè)試法�,選取較為直觀的測(cè)試用例和測(cè)試方法,編制成測(cè)試文檔集�����,以供檢測(cè)機(jī)構(gòu)參照進(jìn)行產(chǎn)品檢測(cè)�����,同時(shí)應(yīng)確保提供的測(cè)試方法和測(cè)試用例以及輸出的測(cè)試結(jié)果的再現(xiàn)性�����、重復(fù)性和穩(wěn)定性,測(cè)試文檔集的編制可參考GB25000.51-2016 第六章的要求進(jìn)行編制���。
四、醫(yī)療器械軟件注冊(cè)適用范圍
適用對(duì)象
第二�����、三類醫(yī)療器械
醫(yī)療器械軟件�����,包括獨(dú)立軟件���、軟件組件
獨(dú)立軟件:作為醫(yī)療器械或其附件的軟件�。
1)具有一個(gè)或多個(gè)醫(yī)療用途
2)無(wú)需醫(yī)療器械硬件即可完成預(yù)期用途
3)運(yùn)行于通用計(jì)算平臺(tái)
軟件組件:作為醫(yī)療器械或其部件���、附件組成的軟件�����。
控制(驅(qū)動(dòng))醫(yī)療器具有一個(gè)或多個(gè)醫(yī)療用途
械硬件或運(yùn)行于專用(醫(yī)用)計(jì)算平臺(tái)�。
五���、獨(dú)立軟件的臨床評(píng)價(jià)對(duì)于豁免目錄外的產(chǎn)品�,選擇使用
同品種醫(yī)療器械臨床經(jīng)驗(yàn)數(shù)據(jù)作為臨床評(píng)價(jià)路徑時(shí),應(yīng)確保選取的對(duì)比產(chǎn)品與申報(bào)產(chǎn)品的實(shí)質(zhì)性等同和對(duì)比產(chǎn)品的臨床經(jīng)驗(yàn)數(shù)據(jù)充分且充足���,如數(shù)據(jù)不充足應(yīng)進(jìn)行臨床試驗(yàn)�,在臨床試驗(yàn)時(shí)應(yīng)注意選定合適的金標(biāo)準(zhǔn)進(jìn)行參照���,比如診斷類軟件應(yīng)選取公認(rèn)的診斷準(zhǔn)確率較高的方法學(xué)或產(chǎn)品進(jìn)行參照�,而治療類也應(yīng)當(dāng)選取臨床公認(rèn)的治療效果較好的方法或產(chǎn)品進(jìn)行參照�����,以確保臨床評(píng)價(jià)充分且充足�����。
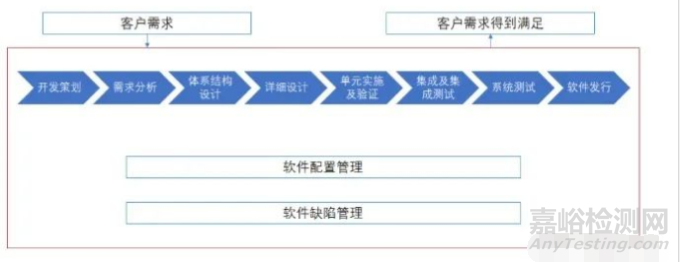
六�����、軟件生命周期