隨著防疫措施的優(yōu)化��,國內(nèi)新冠感染人數(shù)急劇攀升�����,廣大的人口基數(shù)下對(duì)應(yīng)著巨大的重癥風(fēng)險(xiǎn)人群用藥需求�����,雖然NMPA已批準(zhǔn)法匹拉韋��、奈瑪特韋���、莫諾拉韋及阿茲夫定四款小分子抗病毒藥物,但該類藥物仍一藥難求���,人民群眾迫切需要更多安全有效的抗病毒藥物供應(yīng)�����。令人欣喜的是��,監(jiān)管機(jī)構(gòu)��、醫(yī)藥企業(yè)等各方都在努力推進(jìn)新冠小分子藥的上市和供應(yīng)�����,先聲藥業(yè)的SIM0417最快將于2月獲批��,VV116安慰劑對(duì)照III期也已啟動(dòng)���,眾生藥業(yè)���、廣生堂��、前沿生物等一眾國產(chǎn)新冠小分子玩家也已推進(jìn)到臨床III期���,相信不需要等太久��,中國人民就能迎來小分子抗新冠病毒藥物的上市潮�����,為重癥風(fēng)險(xiǎn)人群構(gòu)筑堅(jiān)實(shí)屏障���。
1、3CLp和RdRp是當(dāng)前新冠小分子藥物開發(fā)主流靶點(diǎn)
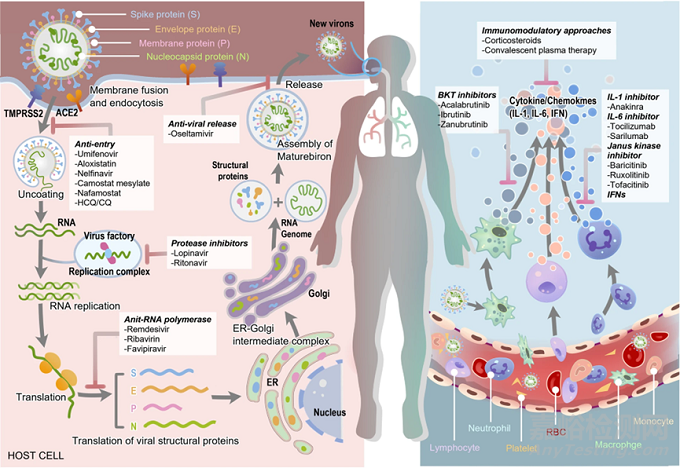
新冠病毒為β屬單鏈RNA病毒���,有包膜��,顆粒呈圓形或橢圓形�����。其基因組可分為六個(gè)部分�����,分別編碼包膜蛋白(E)�����、刺突蛋白(S)���、膜(M)蛋白���、核衣殼蛋白(N)和復(fù)制酶多聚蛋白pp1a和pp1ab,pp1a和pp1ab合成后被切割成16種參與病毒復(fù)制組裝的非結(jié)構(gòu)蛋白��。
新冠病毒的感染過程與一般病毒一致���,首先通過與細(xì)胞表面ACE2受體結(jié)合融合后進(jìn)入細(xì)胞���,釋放編碼RNA�����,復(fù)制翻譯后再組裝為新的病毒顆粒��,這一系列過程中參與的蛋白質(zhì)包括新冠病毒的S蛋白�����、人體細(xì)胞的ACE2受體��、催化RNA合成的RNA依賴性RNA聚合酶(RdRp)���、切割前體蛋白的3-胰凝乳蛋白酶樣蛋白酶(3CLp)以及其他的非結(jié)構(gòu)蛋白如NSP13��、NSP14���、NSP16等�����,阻斷其中任意蛋白均可起到抑制病毒復(fù)制的作用�����。
除了阻止病毒復(fù)制對(duì)人體組織的直接破壞以外���,緩解炎癥細(xì)胞浸潤和細(xì)胞因子風(fēng)暴也是十分重要的對(duì)癥治療���,尤其是對(duì)重癥患者來說。因此�����,各種細(xì)胞因子信號(hào)通路蛋白也是重要的新冠肺炎治療靶點(diǎn)�����,包括BTK�����、JAK��、IL-1�����、IL-6等,通過阻斷相關(guān)炎癥信號(hào)通路��,可以減輕炎癥和器官衰竭水平���,挽救重癥患者生命���。
新冠病毒感染潛在治療靶點(diǎn)[1]
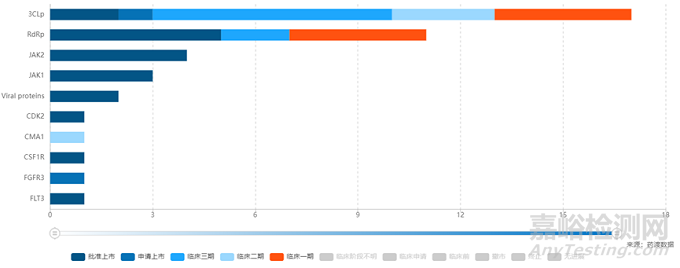
從臨床試驗(yàn)來看,目前新冠小分子開發(fā)熱點(diǎn)主要集中在3CLp和RdRp��,二者均是新冠病毒復(fù)制必須的關(guān)鍵蛋白酶��,且結(jié)構(gòu)和功能較為保守�����,對(duì)應(yīng)抑制劑物具有效果好��、廣譜���、安全性好的優(yōu)點(diǎn)。其中3CLp靶點(diǎn)已有2款藥物獲批���,1款申請上市中��,RdRp靶點(diǎn)則有高達(dá)5款藥物獲批���,此外還有超過20款針對(duì)3CLp和RdRp的藥物處于臨床試驗(yàn)中[2]��。
新冠病毒肺炎靶點(diǎn)情況[2]
2��、全球已有10款小分子藥物獲批���,輝瑞的Paxlovid最為暢銷
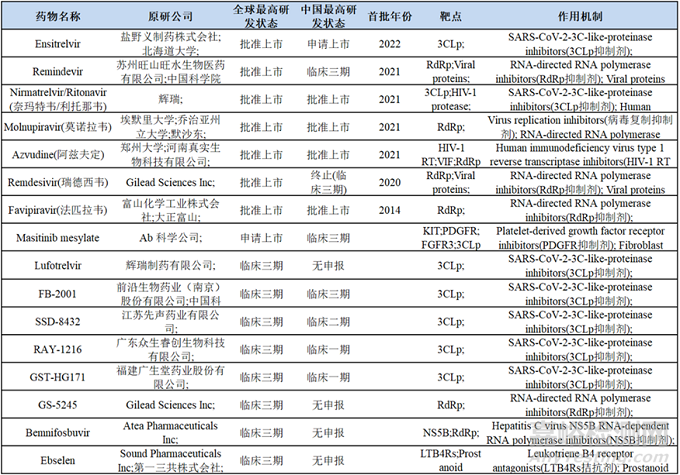
據(jù)不完全統(tǒng)計(jì),截至目前全球范圍內(nèi)已經(jīng)有10款新冠小分子藥物獲得各國監(jiān)管機(jī)構(gòu)批準(zhǔn)���,除上面提到的7款RdRp/3CLp抑制劑外�����,還包括用于FDA批準(zhǔn)的用于重癥患者的JAK抑制劑巴瑞替尼(Baricitinib)���、印度藥監(jiān)局批準(zhǔn)的2-去氧-d-葡萄糖以及獲巴拉圭EUA許可的普克魯胺[3]。
NMPA目前僅批準(zhǔn)了海正藥業(yè)的法匹拉韋���、輝瑞的奈瑪特韋/利托那韋(Paxlovid)���、默沙東的莫諾拉韋(Molnupiravir)以及真實(shí)生物的阿茲夫定用于新冠病毒感染患者的治療�����,鹽野義的Ensitrelvir已遞交NDA��,此外還有先聲藥業(yè)�����、前沿生物��、眾生藥業(yè)�����、廣生堂等國內(nèi)藥企也已推進(jìn)到III期臨床�����,靶點(diǎn)均為3CLp��,而根據(jù)先聲藥業(yè)公告��,其III期臨床已完成,最快可于今年2月上市。
新冠小分子藥物研發(fā)情況[2]
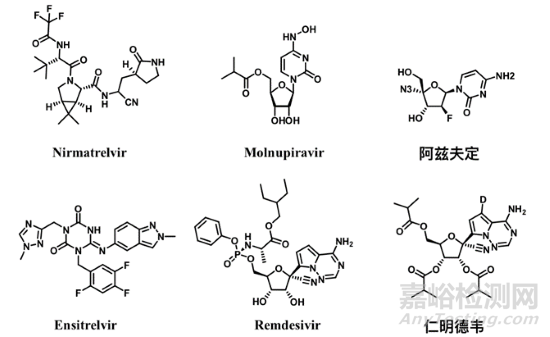
3��、部分新冠小分子藥化學(xué)結(jié)構(gòu)
奈瑪特韋/利托那韋(Paxlovid)
由輝瑞研發(fā)���,于2021年12月22日獲得FDA批準(zhǔn)��,2022年2月12日獲NMPA批準(zhǔn)�����,用于發(fā)病5天內(nèi)的輕型和普通型且伴有進(jìn)展為重癥高風(fēng)險(xiǎn)因素的成人新冠肺炎患者���。Paxlovid為3CLp抑制劑奈瑪特韋和HIV-1蛋白酶抑制劑利托那韋的復(fù)方制劑,利托那韋主要用于抑制肝藥酶CYP3A4對(duì)奈瑪特韋的代謝��,提升血藥濃度增強(qiáng)藥效��,但這同時(shí)也增加了使用其他藥物(如洛伐他丁�����、夫西地酸等)的風(fēng)險(xiǎn)���,患者用藥時(shí)需嚴(yán)格遵循醫(yī)囑�����。
根據(jù)輝瑞發(fā)表在NEJM上的數(shù)據(jù)[5]��,在有癥狀�����、未接種疫苗���、未住院�����、有進(jìn)展為重癥風(fēng)險(xiǎn)的患者群體中�����,Paxlovid給藥組697例患者僅有5例發(fā)生住院���,0例死亡,而安慰劑對(duì)照組682名患者共44例發(fā)生住院���,其中9例死亡�����,給藥組重癥發(fā)生率較對(duì)照組低5.81%(P<0.001)��,證實(shí)Paxlovid可將有進(jìn)展為重癥風(fēng)險(xiǎn)的患者的死亡或住院風(fēng)險(xiǎn)降低89%且不良反應(yīng)事件與安慰劑相似�����。而對(duì)無重癥風(fēng)險(xiǎn)因素的成人患者或接種過疫苗的重癥風(fēng)險(xiǎn)患者��,Paxlovid可將重癥風(fēng)險(xiǎn)減低51%��,但并未表現(xiàn)出統(tǒng)計(jì)學(xué)意義[6]���,意味著該藥對(duì)無重癥風(fēng)險(xiǎn)的患者基本無效。但這并不妨礙Paxlovid成為最暢銷的新冠治療藥物���,根據(jù)輝瑞財(cái)報(bào)數(shù)據(jù)��,Paxlovid在2022年一至三季度銷售額分別為15億�����、81億��、75億美元���,預(yù)計(jì)全年銷售額可達(dá)220億美元���,而左手疫苗右手口服藥的組合也預(yù)計(jì)將為輝瑞創(chuàng)造近540億美元的年?duì)I收。
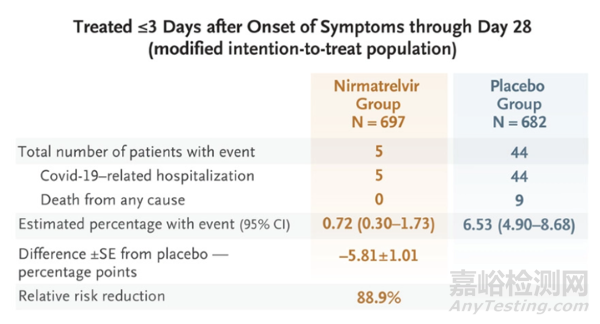
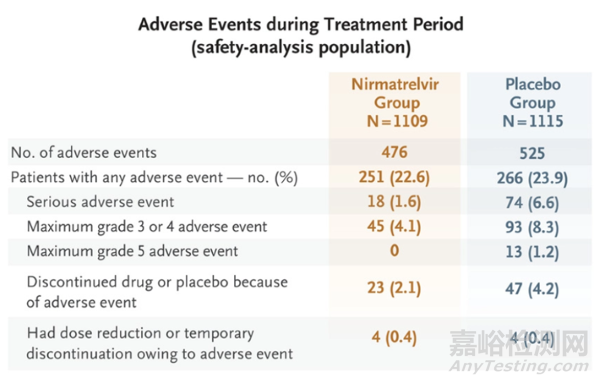
輝瑞EPIC-HR臨床試驗(yàn)數(shù)據(jù)[5]
莫諾拉韋(Molnupiravir)
由默沙東和Ridgeback Biotherapeutics開發(fā)���,是全球首個(gè)獲批的口服抗新冠病毒藥物���,于2021年11月4日獲英國藥品和保健產(chǎn)品監(jiān)管局批準(zhǔn)、2021年12月23日獲FDA批準(zhǔn)��、2022年12月30日獲NMPA批準(zhǔn)�����,用于輕度和中度伴有進(jìn)展為高風(fēng)險(xiǎn)因素的成人新冠患者���。該藥為核苷類似物�����,可抑制RdRp�����,通過誘導(dǎo)病毒RNA發(fā)生突變來阻斷病毒復(fù)制和傳播�����。
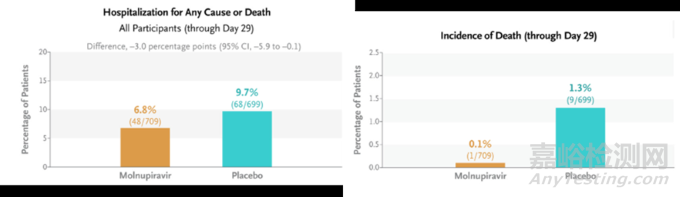
根據(jù)默沙東發(fā)表在NEJM上的數(shù)據(jù)[7]���,在有癥狀、未接種疫苗���、未住院��、有至少一個(gè)重癥風(fēng)險(xiǎn)因素的患者群體中�����,Molnupiravir給藥組709例患者有48例住院其中1例死亡�����,安慰劑對(duì)照組699例患者有68例住院其中9例死亡���,Molnupiravir組住院或死亡發(fā)生率較對(duì)照組低3.0%(P=0.001)�����,說明Molnupiravir可將患者的住院風(fēng)險(xiǎn)降低31%��,死亡風(fēng)險(xiǎn)降低92%�����。此外�����,給藥組的不良反應(yīng)事件也與安慰劑組相似�����,但其誘導(dǎo)RNA突變的抗病毒機(jī)制存在潛在致畸風(fēng)險(xiǎn)�����,所以該藥被FDA添加了黑框警告��。
默沙東MOVe-OUT臨床試驗(yàn)數(shù)據(jù)[7]

Molnupiravir黑框警告
雖然不是頭對(duì)頭試驗(yàn)���,但Paxlovid對(duì)Molnupiravir的療效優(yōu)勢還是十分明顯(重癥風(fēng)險(xiǎn)降低89% vs 31%)���,因而在Paxlovid上市后,Molnupiravir的市場也是受到明顯擠壓�����,根據(jù)默沙東財(cái)報(bào)��,Molnupiravir在2022年一至三季度銷售收入分別為32億��、12億���、4億美元,全年預(yù)計(jì)僅52-54億美元��。
阿茲夫定(Azvudine)
由鄭州大學(xué)和真實(shí)生物合作開發(fā)��,于2021年7月獲NMPA批準(zhǔn)用于成年HIV-1感染患者��,2022年7月獲NMPA批準(zhǔn)用于普通型新型冠狀病毒肺炎成年患者��。該藥為核苷類似物�����,是一種VIF抑制劑、HIV-1 RT抑制劑和RdRp抑制劑��。
根據(jù)真實(shí)生物招股書[8]��,阿茲夫定于2022年3月完成III期臨床試驗(yàn)��,共招募348名患者���,該試驗(yàn)的主要療效指標(biāo)為治療第7天和第14天的病毒載量變化���。次要療效指標(biāo)包括新型冠狀病毒核酸轉(zhuǎn)陰率、新型冠狀病毒核酸轉(zhuǎn)陰時(shí)間��、肺部影像改善���、體溫正?��;⒑粑荔w征及癥狀改善以及其他癥狀改善��。結(jié)果顯示給藥組病毒載量下降快于對(duì)照組��,且有顯著性差異,但呼吸道體征�����、癥狀改善���、肺部影像等次要療效指標(biāo)均無顯著性差異���。
阿茲夫定中國III期臨床數(shù)據(jù)[8]
此外,阿茲夫定作為核苷類似物的RdRp抑制劑��,與Molnupiravir一樣具有遺傳和生殖毒性的安全性風(fēng)險(xiǎn)��,使用時(shí)需謹(jǐn)慎衡量風(fēng)險(xiǎn)和臨床獲益���。
恩賽特韋(Ensitrelvir)
由日本鹽野義制藥株式會(huì)社和北海道大學(xué)合作研發(fā)的3CLp抑制劑,于2022年11月22日獲得PMDA批準(zhǔn)用于治療新冠病毒感染��。作用機(jī)制與Paxlovid相同���,抑制3CLp后使新冠病毒無法復(fù)制增殖��,但該分子藥動(dòng)學(xué)數(shù)據(jù)更佳�����,清除率低�����,無需聯(lián)用肝藥酶抑制劑來提升藥效,故理論上來講安全性將優(yōu)于Paxlovid���。
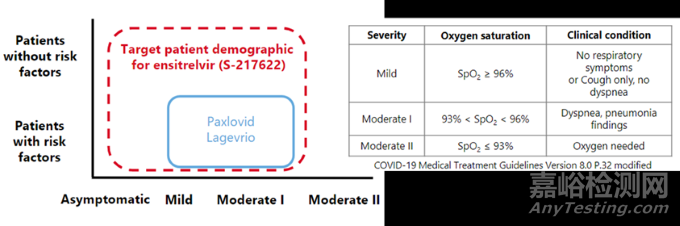
Ensitrelvir的目標(biāo)患者群體[9]
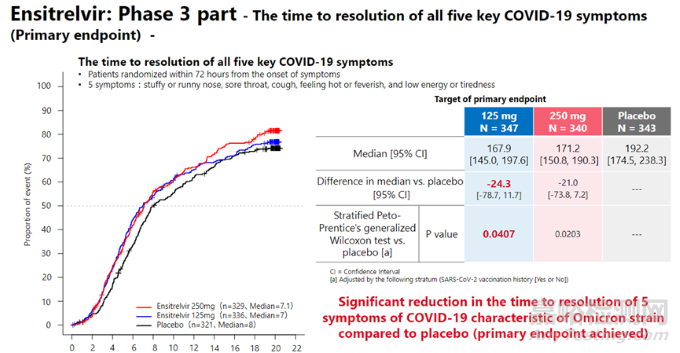
根據(jù)鹽野義公布的數(shù)據(jù)[9],其III期臨床試驗(yàn)共招募1821名輕/中度癥狀患者�����,90%以上患者接種過疫苗��,有重癥風(fēng)險(xiǎn)因素和無重癥風(fēng)險(xiǎn)因素的患者均囊括在內(nèi)�����,試驗(yàn)發(fā)現(xiàn)Ensitrelvir給藥組五種Omicron感染癥狀(鼻塞或流鼻涕��、喉嚨痛���、咳嗽�����、發(fā)熱或發(fā)燒�����、精力不足或疲倦)的緩解中位時(shí)間相比安慰劑組可縮短24小時(shí)(167.9 vs 192.2��,p=0.04)��。病毒RNA載量也較安慰劑組顯著減少���,三次給藥后即降低至給藥前的1/300���,而安慰劑只降低至給藥前的1/10。臨床試驗(yàn)中未發(fā)現(xiàn)嚴(yán)重不良事件及副作用��。
Ensitrelvir癥狀緩解效果[9]
仁明德韋(VV116�����,Remindevir)
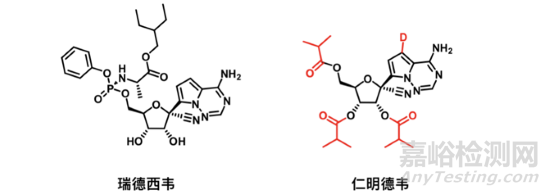
由上海藥物研究所��、武漢病毒研究所以及旺山旺水生物醫(yī)藥公司合作開發(fā)的一款RdRp核苷類小分子抑制劑��,于2021年12月31日在烏茲別克斯坦獲批�����,成為全球第三款獲批用于口服治療新冠的小分子藥物��。仁明德韋在瑞德西韋結(jié)構(gòu)基礎(chǔ)上改造而來���,提高了口服生物利用度和組織滲透性�����,在體內(nèi)外都表現(xiàn)出顯著的抗新冠病毒作用��。
Remindevir及Remdesivir結(jié)構(gòu)
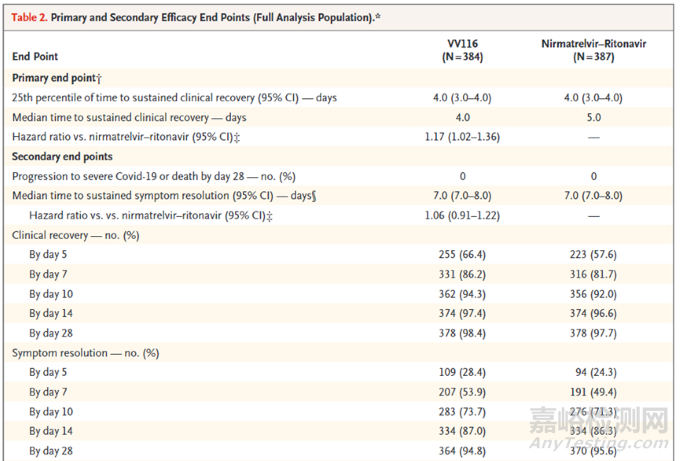
根據(jù)君實(shí)發(fā)表在NEJM上的數(shù)據(jù)[10]���,在和Paxlovid的頭對(duì)頭III期臨床研究中,共入組了822名有癥狀且有重癥風(fēng)險(xiǎn)因素的輕至中度患者��,75%已接種至少2劑疫苗�����。試驗(yàn)發(fā)現(xiàn)VV116組和Paxlovid組持續(xù)臨床恢復(fù)的中位時(shí)間分別為4天和5天���,兩組均未出現(xiàn)重癥或死亡���,第7天���、第28天的癥狀緩解率也基本一致,表明了VV116較Paxlovid的非劣性以及在加速輕中癥患者恢復(fù)上的有效性��。此外��,VV116的任何不良事件和嚴(yán)重不良事件的發(fā)生率均低于Paxlovid���。
仁明德韋III期臨床數(shù)據(jù)[10]
但與此同時(shí)���,文章的作者也指出了該臨床試驗(yàn)的不足之處,由于未來得及制備Paxlovid安慰劑��,該臨床試驗(yàn)僅為觀察者單盲���,也沒有空白對(duì)照��,暫時(shí)無法證明VV116在降低重癥風(fēng)險(xiǎn)方面的作用��。不過��,君實(shí)已于2022年10月啟動(dòng)JT001-015研究[11]�����,一項(xiàng)在輕中度伴或不伴有高危風(fēng)險(xiǎn)COVID-19受試者中評(píng)價(jià)VV116有效性和安全性的多中心���、雙盲、隨機(jī)�����、安慰劑對(duì)照�����、III 期臨床試驗(yàn)��,期待能夠讀出優(yōu)秀數(shù)據(jù)��,加快VV116上市步伐���。
先諾欣(SIM0417)
由先聲藥業(yè)宣布��、上海藥物所��、武漢病毒所合作開發(fā)��,是一款3CLp抑制劑��,2022 年3月30日首次在國內(nèi)獲批臨床���,目前���,該項(xiàng)目已啟動(dòng)7項(xiàng)NCT臨床試驗(yàn),針對(duì)輕中癥成年患者的隨機(jī)��、雙盲��、安慰劑對(duì)照II/III期臨床研究全部1208 例患者也已入組完成[2]��,是國內(nèi)進(jìn)度最快的3CLp抑制劑��,據(jù)江蘇省藥監(jiān)局預(yù)計(jì)��, SIM0417最快可于今年2月獲批上市��。
RAY1216
由眾生藥業(yè)開發(fā)��,同樣為3CLp抑制劑,該藥用于治療輕型和普通型患者的隨機(jī)���、雙盲��、安慰劑對(duì)照 III 期臨床研究已入組完成,共1360例��。
HY3000
由中科院微生物研究所和深圳翰宇藥業(yè)合作開發(fā)��,是一種膜融合抑制劑多肽��,作用于新冠病毒刺突蛋白的HR1區(qū)域�����,通過與HR1區(qū)域結(jié)合�����,阻止病毒六螺旋束結(jié)構(gòu)形成���,阻斷病毒侵染細(xì)胞的路徑�����。該項(xiàng)目開發(fā)劑型為鼻噴劑��,經(jīng)鼻給藥���,能夠在病毒入侵人體的首要路徑上建立抗病毒防線���,起到阻斷新冠病毒感染的作用,目前正處于臨床II期試驗(yàn)中���。
總結(jié)
小分子治療藥物生產(chǎn)成本更低���,給藥和運(yùn)輸也更為便捷,在應(yīng)對(duì)變異毒株方面也更具優(yōu)勢��,是抗擊新冠疫情最重要的武器之一�����。雖然國內(nèi)已有Paxlovid�����、Molnupiravir和阿茲夫定獲批���,但對(duì)正在經(jīng)歷奧密克戎疫情的中國來說�����,新冠小分子抗病毒藥物供應(yīng)明顯不足��,特效藥仍一藥難求���。令人欣喜的是,各方都在努力推進(jìn)新冠小分子藥的供應(yīng)���,相信中國人民不需要等太久�����,就能迎來新冠小分子藥物的上市潮���,為臨床治療提供更多選擇。
參考:
[1] Therapeutic targets and interventional strategies in COVID-19: mechanisms and clinical studies. Sig Transduct Target Ther 6, 317 (2021).
[2] https://data.pharmacodia.com/drug#/main/drugInfo
[3] Lei, S., Chen, X., Wu, J. et al. Small molecules in the treatment of COVID-19. Sig Transduct Target Ther 7, 387 (2022)
[4] Lei Z, Zhipeng Z, Jun Z et al. Recent advances in small-molecular therapeutics for COVID-19, Precision Clinical Medicine, Volume 5, Issue 4, December 2022, pbac024
[5] Hammond J, Leister-Tebbe H, Gardner A et al. Oral Nirmatrelvir for High-Risk, Nonhospitalized Adults with Covid-19. N Engl J Med. 2022 Apr 14;386(15):1397-1408.
[6] https://www.pfizer.com/news/press-release/press-release-detail/pfizer-reports-additional-data-paxlovidtm-supporting
[7] Jayk Bernal A, Gomes da Silva MM, Musungaie DB et al. Molnupiravir for Oral Treatment of Covid-19 in Nonhospitalized Patients. N Engl J Med. 2022 Feb 10;386(6):509-520.
[8]真實(shí)生物科技有限公司招股書
[9] https://www.shionogi.com/global/en/investors/ir-library/presentation-materials.html
[10] Cao Z, Gao W, Bao H et al. VV116 versus Nirmatrelvir-Ritonavir for Oral Treatment of Covid-19. N Engl J Med. 2022 Dec 28.
[11] http://file.finance.sina.com.cn › hkdata98 › news