首先我們先來確定一下什么是設備����?什么又是設施?
設備——主要指藥品生產(chǎn)過程中所使用的的混合�、制粒、干燥����、滅菌、包裝等生產(chǎn)工藝設備和生產(chǎn)輔助設備����。
設施——主要指藥品生產(chǎn)所需的建筑物以及與工藝配套的凈化空調(diào)系統(tǒng)、純化水系統(tǒng)��、壓縮空氣系統(tǒng)��、真空系統(tǒng)��、蒸汽系統(tǒng)等公用工程設施�。
概括的了解了設備和設施的基本定義,下面我們從幾個方面來對設備設施驗證與確認做一個簡單的概論��。
一、設備設施驗證與確認定義及基本原則
首先我們需要先明確設備設施驗證與確認都有哪些需要進行的活動:
1�、設計確認(DQ)——對新建或新引入的設施�、設備的設計方案進行的一系列審核活動,目的是確保設計符合用戶所提出的各方面需求����,即證明設施、設備的設計符合GMP和設施����、設備產(chǎn)品標準、URS����,并有相關文件記錄證明。
2��、安裝確認(IQ)——設施����、設備安裝后進行各種系統(tǒng)檢查,證明設施����、設備的建造和安裝符合設計標準及需求。
3、運行確認(OQ)——為確認設施����、設備或與其相關的系統(tǒng)達到設定要求而進行的各種運行試驗,證明設施�、設備的運行符合設計標準。
4����、性能確認(PQ)——設施、設備在規(guī)定的操作方法和工藝條件下逆序證明有效的運行��,并生產(chǎn)出符合質(zhì)量標準的產(chǎn)品��。
接下來進行驗證范圍及驗證深度的確定:
我們需要對設施設備進行一個初始的系統(tǒng)影響性的風險評估��,確定其屬于哪種類型的系統(tǒng)——直接影響系統(tǒng)����、間接影響系統(tǒng)or無影響系統(tǒng)。通常情況下直接影響系統(tǒng)需要進行設備設施驗證/確認或清潔驗證��;間接影響和無影響系統(tǒng)無需進行驗證/確認�。確定好需要進行驗證或確認的設施設備需要進一步的執(zhí)行部件關鍵性的風險評估,以確認有哪些關鍵部件�,以及確定最終的驗證深度�。
最后來討論一下設施設備驗證與確認過程中一些基本的原則:
1��、設備PQ可以和工藝驗證或清潔驗證合并進行(工藝驗證或清潔驗證涵蓋了PQ的全部內(nèi)容)�;若設備用于多個品種時,可評估選擇最差品種進行性能確認�;若設備所用品種增加時�,需評估對設備運行確認和性能確認的影響。
2�、PQ與OQ合并的條件:
(1)相對簡單的設施或設備;
(2)并不是所有的檢驗設備都要做PQ��,例如某些計量設備�;
(3)OQ和PQ不易做嚴格劃分的或者沒有PQ(如軟件系統(tǒng)驗證等);
(4)OQ和PQ項目較少����,經(jīng)過審核和評估允許進行合并。
3����、確認/驗證過效期的設施設備不得使用。
4��、驗證應按照預先確定和批準的方案實施�,驗證方案應明確實施驗證的職責�,并經(jīng)過審核��、批準�,驗證工作完成后,應出具驗證報告�,驗證結(jié)果和結(jié)論應有記錄并存檔。
5��、設備設施的初次驗證完成后����,應通過再驗證對設備設施的驗證狀態(tài)進行維護。
二�、設備設施驗證與確認分類
(一)首次驗證
1、新建設施����、新購設備的第一次驗證;
2�、需驗證的設施設備必須在首次驗證合格后才能投入生產(chǎn)使用;
3��、首次驗證應包含DQ����、IQ�、OQ����、PQ等完整的4個階段。
(二)再確認
1��、變更性再確認——設備發(fā)生關鍵部件更換�、改造、長時間停用后重新啟用�、位移等����,經(jīng)評估需進行再確認的。
2�、周期性再確認——從設備性能異常的發(fā)生頻率、設備性能異常對產(chǎn)品質(zhì)量及生產(chǎn)連續(xù)性影響的嚴重程度��、設備性能異常的可測定性三個角度設置相應的問題�,并對問題進行回答,來評估設施設備再確認周期��。
3����、臨時性確認——設備對關鍵部件進行故障維修或維護更換時,可通過確認該部件受影響的性能指標滿足用戶需求后�,允許該設備投入使用時,執(zhí)行此流程�。
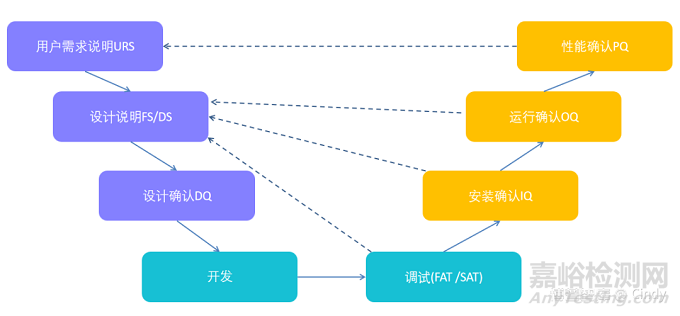
三、設備設施驗證與確認工作執(zhí)行流程
基本流程圖:
(一)設計階段
旨在審查設計的合理性����,所選用設施、設備的性能及設定的技術參數(shù)是否適合使用方的產(chǎn)品����、生產(chǎn)工藝、維修保養(yǎng)����、清洗和消毒等方面的要求,是否符合GMP����,以及是否滿足設施、設備的產(chǎn)品標準��,以確認設計的設備�、系統(tǒng)符合URS中定義的預期用途。
設計階段包括用戶需求說明(URS)�、風險評估(RA)�、設計確認(DQ):
URS——在設備��、設施概念設計階段開始編制����,并在詳細設計開始之前確定下來�。一旦開始驗證,URS的修訂需按照變更流程執(zhí)行��。
RA——設計階段的質(zhì)量風險評估是一個反復的過程��,與系統(tǒng)的設計開發(fā)相關聯(lián)�?���?稍谙到y(tǒng)概念提出階段時起草,在涉及文檔批準時結(jié)束����。
DQ——符合設備�、系統(tǒng)的URS�,對設備�、系統(tǒng)的設計文件依次進行完整性和準確性的檢查,以確保系統(tǒng)的設計能滿足需求��。
執(zhí)行設計確認活動前需確認系統(tǒng)的URS已生效����、供應商提供了所有設計文檔(FDS�、系統(tǒng)儀表清單�、系統(tǒng)說明書、P&ID圖、報警清單����、參數(shù)清單�、I/O清單����、標識與標簽清單����、電子元件清單�、材料表、電纜清單��、設計資格證明等)�。
設計確認活動一般涉及系統(tǒng)主要性能指標確認(如:生產(chǎn)能力�、產(chǎn)品規(guī)格、主要技術指標��、噪音等)����、主要工藝功能�、可清洗和消毒(滅菌)性、關鍵部分材質(zhì)��、電氣系統(tǒng)和控制功能、與設備及相關公用工程的接口關系��、結(jié)構(gòu)和外觀�、儀表計量方式等�。
(二)調(diào)試階段
設備、系統(tǒng)在投入使用前一般要經(jīng)過驗收測試����,本階段不屬于GMP管理范疇,按照使用方和供應商的需求開展,若調(diào)試階段的測試內(nèi)容用于驗證��,則調(diào)試階段需按照GMP的要求進行管理��。
調(diào)試階段包括工廠驗收測試(FAT)和現(xiàn)場驗收測試(SAT)�。
FAT——設備依據(jù)設計完成建造后 ,在發(fā)貨前需在客戶見證下由供應商在制造場地對待交付的設備進行工廠驗收測試����,旨在保證設備已經(jīng)嚴格按照要求完成了組裝調(diào)試。測試方案由供應商負責編寫��,并完成測試�,F(xiàn)AT的報告需由用戶審核�、批準�。當測試內(nèi)容不受運輸或安裝影響時����,且在執(zhí)行中按照GMP的驗證管理要求開展FAT�,則后續(xù)的驗證中可不重復進行�,將FAT相關的測試附在驗證文件中即可�。
SAT——當設備到達使用現(xiàn)場后����,為保證系統(tǒng)在使用場所能達到用戶需求����,同時提高驗證成功的可能性,在驗證開展前�,需開展現(xiàn)場驗收測試。該測試由供應商在移交系統(tǒng)前進行����,測試方案由供應商編寫����,使用方審核����、批準��,使用方應復核測試結(jié)果�,并審核��、批準測試報告����。當測試內(nèi)容在執(zhí)行中按照GMP的驗證管理要求開展SAT����,則在后續(xù)的驗證中可不重復進行�,將SAT相關的測試附在驗證文件中即可����。
(三)安裝確認
旨在證明設施��、設備的安裝符合安裝規(guī)范的技術要求��,且其安裝環(huán)境�、結(jié)構(gòu)、配置��、規(guī)格型號、電氣特性等都將被確認����。是在設備����、設施安裝后進行的各種系統(tǒng)檢查及技術資料文件化的工作��。
在執(zhí)行安裝確認活動前需要確認DQ已完成并符合預期目標,如果存在未關閉偏差�,偏差不影響IQ的進行����;FAT/SAT(如有)報告已完成審批,如果存在遺留尾項��,遺留尾項不影響IQ運行�;方案執(zhí)行前完成相關人員培訓����。并準備好安裝確認所需資料�,如:裝箱單����、合格證����、使用說明書和主要配套件說明書��、與藥品直接接觸零部件清單和材質(zhì)證明�、如安裝圖紙、電氣原理及接線圖����,潤滑位置圖表��、備件明細表����、易損件目錄�、檢測報告(如潤滑油證明、壓力容器質(zhì)量報告��、壓力容器設計和制造資格證書等)、出廠合格證����、儀器儀表名稱����、規(guī)格型號�、安裝位置、編號�、生產(chǎn)廠家、相關公用介質(zhì)(工藝氣體��、工藝用水����、蒸汽����、冷媒等)確認文件及記錄、如設計圖��、施工圖、竣工圖��、驗收文件�、關鍵儀表或強制檢定儀表已完成校準證明等。
安裝確認活動一般涉及安裝地點的環(huán)境、安裝位置和空間��、配套工藝管道、電氣控制系統(tǒng)連接��、主要機械零件的結(jié)構(gòu)以及配件的完整性等是否符合法規(guī)及使用需求��。
(四)運行確認
旨在通過對設施設備各功能的測試,以及空載和滿載運行����,確認設施設備運行�、操作和控制性能符合相應生產(chǎn)工藝條件和生產(chǎn)能力要求��。
執(zhí)行運行確認活動前需確認IQ已完成并符合預期目標����,如果存在未關閉偏差,偏差不影響OQ的進行����;設備操作SOP或崗位操作SOP有草稿版�,在OQ階段審核SOP的準確性和適用性����,在性能確認前完成審批�;方案執(zhí)行前完成相關人員的培訓����。
運行確認活動一般涉及設備初步檢查����,如開停機��、安全��、連鎖檢查等完成設備啟動的檢查��。
運行操作檢查����,如開機后的運轉(zhuǎn)檢查,急停檢查��,功能測試(包含挑戰(zhàn)性測試����。測試中��,應包含運行設備的上下限,必要時選擇“最差條件”)��;以及涉及標準和URS制定的其他測試項目(URS中必須達到的設備參數(shù)需要在運行確認中確認達到要求)�。
(五)性能確認
旨在證明設施設備的運行達到預期使用目的而進行的系統(tǒng)性試驗,通過觀察��、記錄��、取樣檢測等手段����,搜集及分析數(shù)據(jù),考察設施設備運行的可靠性��,主要參數(shù)的穩(wěn)定性和結(jié)果的重現(xiàn)性�。
執(zhí)行性能確認前需確認OQ已經(jīng)完成并符合預期目標,如果存在未關閉的偏差��,偏差不影響PQ的進行��;設備操作SOP或崗位操作SOP��,設備維護保養(yǎng)操作SOP已批準�;方案執(zhí)行前相關人員的培訓。
性能確認用替代物(使用替代物時需注意替代物的性質(zhì)應與生產(chǎn)物料相似或相同)或?qū)嶋H生產(chǎn)原料按生產(chǎn)工藝測試設備運行的質(zhì)量和設備功能的適應性、連續(xù)性和可靠性�,應至少進行3次重復測試��,必要時應進行挑戰(zhàn)試驗��。
性能確認一般涉及在負載運行條件下對藥品生產(chǎn)要求的適用性生產(chǎn)能力��、藥品生產(chǎn)質(zhì)量相關指標�、運行結(jié)果的重復性、控制精度準確性����、安全性能、負載運行的可靠性試驗等����。
以上關于設施設備驗證與確認的一些淺顯的概括,僅供參考����。