FDA器械與輻射健康中心(CDRH)發(fā)布2022年年度報告��,以突出該中心截至2022年12月31日的成就�,其中包括:應(yīng)對突發(fā)傳染病大流行、醫(yī)療器械用戶費用修正案(Medical Device User Fee Amendment MDUFA)��、器械創(chuàng)新(DEVICE INNOVATION)��、OTC助聽器最終規(guī)則和器械安全(Device Safety)�。1
截至到2022年12月31日��,CDRH已將 135 臺設(shè)備納入了“突破性設(shè)備計劃”(自2015年計劃成立以來�,總共 752 個設(shè)備被納入“突破性設(shè)備計劃”),并授予19個“突破性設(shè)備”的市場授權(quán)����。
什么是“突破性設(shè)備計劃”�?
突破性設(shè)備計劃(Breakthrough Devices Program) 是美國食品藥品監(jiān)督管理局(FDA)于2015年4月啟動的一種加快醫(yī)療器械開發(fā)和審查過程的“綠色通道”��,讓患者能盡快獲得有效診斷或可治療危及生命疾病的醫(yī)療器械����。
被FDA納入“突破性設(shè)備計劃”有什么好處?
FDA將被授予“突破性醫(yī)療器械”稱號的產(chǎn)品提供有關(guān)設(shè)備開發(fā)�、臨床試驗方案的優(yōu)先權(quán)審查、FDA審核團隊支持以及產(chǎn)品商業(yè)化決策的交流服務(wù)��。此舉可以大大推動創(chuàng)新醫(yī)療器械的上市過程��。
FDA是否會公布設(shè)備何時被授予突破性設(shè)備稱號�?
在獲得上市許可證之前,除非申辦者決定向公眾提供該信息����,否則FDA不能公開披露申辦者是否已提交器械突破性器械請求。此外�,F(xiàn)DA計劃在官網(wǎng)上定期更新獲得突破性設(shè)備稱號的設(shè)備列表,一旦設(shè)備獲得營銷授權(quán)�,就會將設(shè)備添加到列表中。
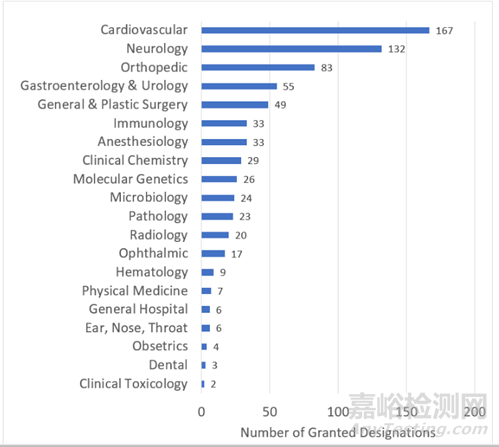
圖 獲得突破性設(shè)備的類別
FDA目前公布了哪些獲得營銷授權(quán)的突破性產(chǎn)品����?
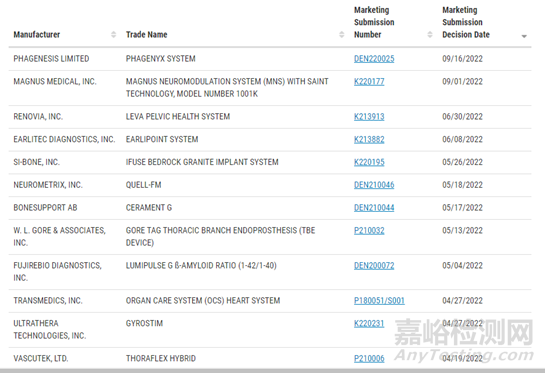
下表為截至到2022年9月30日��,已獲得上市許可的CDRH和CBER突破性設(shè)備列表�。(此表為截至發(fā)文時間����,F(xiàn)DA官網(wǎng)所公布的突破性設(shè)備列表,文末已附突破性設(shè)備列表原文鏈接)
產(chǎn)品1:Phagenyx System
制造商:Phagenesis Limited
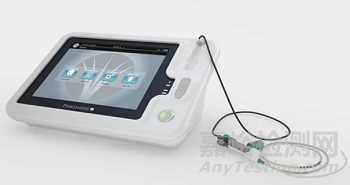
產(chǎn)品介紹:
Phagenyx System是一種先進的治療系統(tǒng)�,通過咽部電刺激(PES)對吞咽協(xié)調(diào)的神經(jīng)組分進行刺激,來治療由神經(jīng)系統(tǒng)的破壞而產(chǎn)生的神經(jīng)源性吞咽困難��。該系統(tǒng)適用于治療常常會遇到吞咽難題的中風(fēng)病人��、老年病人以及那些在加護病房內(nèi)需要依靠機械通氣設(shè)備的病人��。
產(chǎn)品2:MAGNUS NEUROMODULATION SYSTEM (MNS) WITH SAINT TECHNOLOGY, MODEL NUMBER 1001K
制造商:MAGNUS MEDICAL, INC.
產(chǎn)品介紹:
SAINT神經(jīng)調(diào)節(jié)系統(tǒng)可以用于治療重度抑郁癥��。SAINT具有作用快速�、非侵入性等特點。它結(jié)合了先進的成像技術(shù)����、個性化瞄準(zhǔn)和新穎的神經(jīng)刺激模式��,通過使用突破性算法,SAINT可以對腦神經(jīng)進行結(jié)構(gòu)定位和功能性層面的MRI成像��,從而確定重度抑郁癥患者接收神經(jīng)刺激的最佳靶點����。
產(chǎn)品3:Leva Pelvic Health system
制造商:RENOVIA, INC.
產(chǎn)品介紹:
leva骨盆健康系統(tǒng)是一種非侵入性數(shù)字療法,旨在康復(fù)和訓(xùn)練弱骨盆底肌肉�。它允許患者通過專用的移動應(yīng)用程序無線實時性能數(shù)據(jù)來監(jiān)控他們在盆底肌肉訓(xùn)練期間的進展。
產(chǎn)品4:EARLIPOINT SYSTEM
制造商:EARLITEC DIAGNOSTICS, INC.
產(chǎn)品介紹:
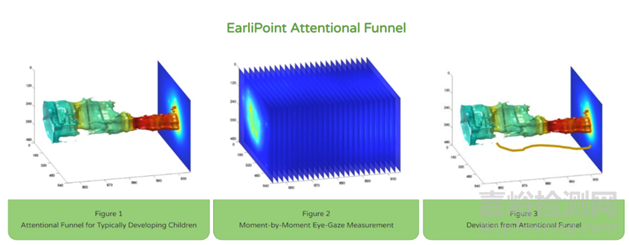
EARLIPOINT SYSTEM是一種幫助臨床醫(yī)生診斷和評估兒童自閉癥譜系障礙(ASD)的客觀測量工具�。 EarliPoint評估可以幫助早期識別ASD,并提供與社會殘疾水平����、語言和非語言能力相關(guān)的服務(wù)EarliPoint嚴(yán)重指數(shù)。
產(chǎn)品5:IFUSE BEDROCK GRANITE IMPLANT SYSTEM
制造商:SI-BONE, INC.
產(chǎn)品介紹:
IFUSE BEDROCK GRANITE IMPLANT SYSTEM旨在提供骶髂融合術(shù)和骶骨固定��,作為節(jié)段性脊柱融合的基礎(chǔ)要素�。
產(chǎn)品6:QUELL-FM
制造商:NEUROMETRIX, INC.
產(chǎn)品介紹:
Quell-FM裝置是一種經(jīng)皮神經(jīng)電刺激器,用于治療纖維肌痛癥狀��。Quell產(chǎn)品是一種完全自動化的可穿戴神經(jīng)刺激技術(shù)����,可與智能手機或Apple Watch無線協(xié)作。
產(chǎn)品7:CERAMENT G
制造商:BONESUPPORT AB
產(chǎn)品介紹:
Cerament G是全身性抗生素治療和清創(chuàng)手術(shù)的輔助手段�,可作為骨髓炎手術(shù)治療的一部分,旨在促進骨愈合并降低再感染和截肢的風(fēng)險。
產(chǎn)品8:GORE TAG THORACIC BRANCH ENDOPROSTHESIS (TBE DEVICE)
制造商:W. L. GORE & ASSOCIATES, INC.
產(chǎn)品介紹:
GORE TAG胸支內(nèi)假體旨在修復(fù)位于胸部最大動脈(降主動脈)的損傷��。胸支內(nèi)假體由三根鎳鈦諾骨架(支架移植物)支撐的植入式織物管組成�。每個支架移植物都有一個基于導(dǎo)管的輸送系統(tǒng)。
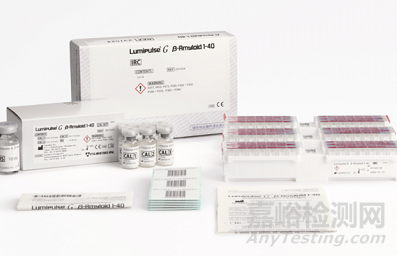
產(chǎn)品9:LUMIPULSE G ß-AMYLOID RATIO (1-42/1-40)
制造商:FUJIREBIO DIAGNOSTICS, INC.
產(chǎn)品介紹:
Lumipulse G β-淀粉樣蛋白比值 (1-42/1-40) 測試適用于 55 歲及以上�、患有認(rèn)知障礙的成年患者。Lumipulse測試旨在測量人腦脊液(CSF)中發(fā)現(xiàn)的β-淀粉樣蛋白1-42和β-淀粉樣蛋白1-40(可以積聚并形成斑塊的特定蛋白質(zhì))濃度的比例����,這可以幫助醫(yī)生確定患者是否有阿爾茨海默病的標(biāo)志即淀粉樣斑塊。
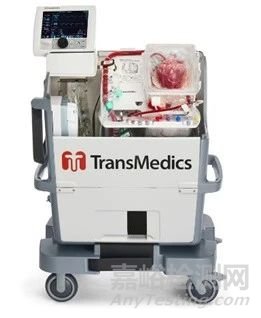
產(chǎn)品10:ORGAN CARE SYSTEM (OCS) HEART SYSTEM
制造商:TRANSMEDICS, INC.
產(chǎn)品介紹:
TransMedics器官護理系統(tǒng)(OCS)心臟系統(tǒng)旨在移植前保存供體心臟����。該系統(tǒng)包括一個便攜式外殼,可以保溫供體心臟�,為其提供氧氣和營養(yǎng),以及提供心臟保存解決方案�。
產(chǎn)品11:GYROSTIM
制造商:ULTRATHERA TECHNOLOGIES, INC.
產(chǎn)品介紹:
GyroStim是一款計算機控制的自動化多軸旋轉(zhuǎn)椅,它能夠通過預(yù)先編程的動作使患者在空中移動身體����,從而對感覺運動系統(tǒng)造成刺激。GyroStim已被FDA批準(zhǔn)為用于治療平衡障礙和前庭功能障礙的突破性醫(yī)療設(shè)備�。
產(chǎn)品12:THORAFLEX HYBRID
制造商:VASCUTEK, LTD.
產(chǎn)品介紹:
Thoraflex Hybrid是一種一次性醫(yī)療設(shè)備,結(jié)合了Gelweave聚酯移植物和鎳鈦自膨脹支架移植物�,適用于主動脈弓和降主動脈受損或病變血管的開放式手術(shù)修復(fù)或置換�。
產(chǎn)品13:AGILI-C
制造商:CARTIHEAL, LTD.
產(chǎn)品介紹:
Agili-C是一種植入物����,旨在治療膝關(guān)節(jié)骨骼周圍軟骨中發(fā)生的缺陷或病變�。植入物是多孔的,生物相容的和可吸收的雙相支架�,由相互連接的天然無機碳酸鈣組成。
怎么才能被納入突破性項目計劃��?
申請上市前批準(zhǔn)(PMA)����、上市前通告 (510(k)) 或 De Novo指定的器械產(chǎn)品,需同時符合以下兩個條件:一是該器械可治療或診斷危害生命的疾病��。二是該器械應(yīng)滿足以下至少一項:a.代表突破性技術(shù)b.無已批上市替代產(chǎn)品c.與現(xiàn)有或已批準(zhǔn)的替代產(chǎn)品相比具有顯著優(yōu)勢d.器械可及性符合患者最大利益��。
圖 符合突破性器械項目的條件
除此之外��,F(xiàn)DA認(rèn)為一些不符合“突破性設(shè)備計劃“��,但在治療或診斷不太嚴(yán)重疾病方面具有顯著安全優(yōu)勢的醫(yī)療器械也能夠提供公共衛(wèi)生利益��。因此����,F(xiàn)DA建立了醫(yī)療器械安全技術(shù)計劃(Safer Technologies Program����,STeP)以鼓勵醫(yī)療器械廠商開發(fā)創(chuàng)新的��、比現(xiàn)有產(chǎn)品更安全的替代品設(shè)備����。根據(jù)FDA2022年年報指出,2022年收到了30多項納入該計劃的請求����,并通過了14項目批準(zhǔn)。
FDA網(wǎng)頁原文及產(chǎn)品介紹原文:
[1] CDRH2022年年報
https://www.fda.gov/about-fda/cdrh-reports/cdrh-2022-annual-report
[2] 產(chǎn)品1 Phagenyx System詳細(xì)介紹原文
https://www.fdanews.com/articles/209517-fda-authorizes-phagenesis-phagenyx-system
[3]產(chǎn)品2 Magnus Medical Receives FDA Clearance for the SAINT Neuromodulation System for Non-Invasive, Individualized and Precise Treatment of Severe Depression. 詳細(xì)介紹原文
https://www.magnusmed.com/press-releases/magnus-medical-receives-fda-clearance-for-the-saint-neuromodulation-system/
[4] 產(chǎn)品3 Leva Pelvic Health system詳細(xì)介紹原文
https://www.urologytimes.com/view/fda-grants-clearance-to-leva-pelvic-health-system-for-chronic-fecal-incontinence
[5] 產(chǎn)品4 EARLIPOINT SYSTEM 詳細(xì)介紹原文
https://www.earlitecdx.com/solutions/
[6] 產(chǎn)品5 IFUSE BEDROCK GRANITE IMPLANT SYSTEM詳細(xì)介紹原文
https://www.nsmedicaldevices.com/news/si-bone-secures-fda-approval-for-ifuse-bedrock-granite-implant-system/
[7] 產(chǎn)品6 QUELL-FM詳細(xì)介紹原文
https://www.myhealthyapple.com/nuerometrix-clears-denovo-on-its-quell-fm-wearable-that-works-with-apple-watch/
[8] 產(chǎn)品7 CERAMENT G 詳細(xì)介紹原文
https://www.ceramentgusa.com/#join
[9] 產(chǎn)品8 GORE TAG THORACIC BRANCH ENDOPROSTHESIS (TBE DEVICE) 詳細(xì)介紹原文
https://www.fda.gov/medical-devices/recently-approved-devices/gore-tag-thoracic-branch-endoprosthesis-p210032
[10] 產(chǎn)品9 LUMIPULSE G ß-AMYLOID RATIO (1-42/1-40) 詳細(xì)介紹原文
https://www.fda.gov/news-events/press-announcements/fda-permits-marketing-new-test-improve-diagnosis-alzheimers-disease
[11] 產(chǎn)品10 ORGAN CARE SYSTEM (OCS) HEART SYSTEM詳細(xì)介紹原文
https://www.fda.gov/medical-devices/recently-approved-devices/organ-care-system-ocs-heart-system-p180051
[12] 產(chǎn)品11 GYROSTIM詳細(xì)介紹原文
https://www.gyrostim.com/gyrostim-about
[13] 產(chǎn)品12 THORAFLEX HYBRID詳細(xì)介紹原文
https://www.fda.gov/medical-devices/recently-approved-devices/agili-c-p210034
[14] 產(chǎn)品13 AGILI-C詳細(xì)介紹原文
https://www.fda.gov/medical-devices/recently-approved-devices/agili-c-p210034
[15] 突破性器械項目的原則和優(yōu)勢����,F(xiàn)DA原文
https://www.fda.gov/media/108135/download