無(wú)菌隔離器在制藥行業(yè)的使用愈加廣泛�����,但已有的研究更多地聚焦于設(shè)計(jì)布局�����、物料狀態(tài)等方面���,對(duì)人員操作因素的影響方面關(guān)注較少。以本公司凍干制劑生產(chǎn)車(chē)間為例�����,設(shè)計(jì)了一系列合理的無(wú)菌隔離器內(nèi)干預(yù)操作�,并在操作人員實(shí)行干預(yù)操作的基礎(chǔ)上進(jìn)行氣流流型測(cè)試和無(wú)菌工藝驗(yàn)證。根據(jù)驗(yàn)證結(jié)果�����,判定操作人員在日常生產(chǎn)中的操作具有規(guī)范性���,可為其他車(chē)間的無(wú)菌隔離器操作人員的培訓(xùn)和考察提供參考�。
隔離技術(shù)最早起源于第二次世界大戰(zhàn)時(shí)使用的手套箱技術(shù),用于處理放射性物質(zhì)以保護(hù)操作人員安全 [1]���。自 20 世紀(jì) 80 年代以來(lái)���,隔離技術(shù)的應(yīng)用日益廣泛。最初�����,供實(shí)驗(yàn)室使用的無(wú)菌檢查隔離器在歐洲發(fā)展起來(lái)���,該設(shè)備通過(guò)提供可靠的環(huán)境保障來(lái)有效防止微生物對(duì)待測(cè)試物品的污染,可減少假陽(yáng)性的產(chǎn)生 �;隨后�����,無(wú)菌隔離系統(tǒng)開(kāi)始廣泛應(yīng)用于食品工業(yè)���、制藥工業(yè)等領(lǐng)域�����。目前�����,國(guó)際上常用的隔離系統(tǒng)主要有限制進(jìn)出屏障系統(tǒng) (restricted access barrier system���,RABS) 和無(wú)菌隔離器 (isolator) 等 [2-3]���。
相較而言,無(wú)菌隔離器的優(yōu)勢(shì)明顯���,因其采用完全密閉的系統(tǒng)將生產(chǎn)空間與周?chē)h(huán)境和操作人員完全隔離�,可保護(hù)產(chǎn)品免遭環(huán)境污染 ( 包括來(lái)自操作人員在過(guò)濾和密封時(shí)帶來(lái)的污染 )�����。據(jù) 2015 年的統(tǒng)計(jì)數(shù)據(jù)�,30%的原料藥都具有強(qiáng)烈的毒性 [2],無(wú)菌隔離器的應(yīng)用可保護(hù)操作人員免受生產(chǎn)過(guò)程中有毒�����、有害物質(zhì)帶來(lái)的傷害���。此外�,無(wú)菌隔離器配備的單獨(dú)高效過(guò)濾器���、空氣處理系統(tǒng)和無(wú)菌隔離器集成氣化過(guò)氧化氫滅菌系統(tǒng),可自動(dòng)控制無(wú)菌隔離器中的生產(chǎn)環(huán)境條件�。通過(guò)陰性分?jǐn)?shù)法或過(guò)度殺滅法證實(shí)滅菌隔離器可以使微生物數(shù)降至 10–6 [4-6]�,而在傳統(tǒng)潔凈室內(nèi),微生物數(shù)只能控制在 10–3 的水平 [7]。
《中華人民共和國(guó)藥典》2020 年版 (ChP 2020)四部通則 9206 無(wú)菌檢查用隔離系統(tǒng)驗(yàn)證指導(dǎo)原則中對(duì)無(wú)菌檢查法等做出了相關(guān)要求���,并制定了配套的無(wú)菌檢查用隔離系統(tǒng)驗(yàn)證和應(yīng)用指導(dǎo)原則�����,對(duì)無(wú)菌隔離器的相關(guān)驗(yàn)證進(jìn)行了規(guī)范�����。相關(guān)指導(dǎo)原則的出臺(tái)引起了大量驗(yàn)證技術(shù)研究 [8-9]。在對(duì)無(wú)菌產(chǎn)品的質(zhì)量研究中�����,已經(jīng)確認(rèn)包括生產(chǎn)區(qū)的設(shè)計(jì)及其設(shè)備布局、生產(chǎn)時(shí)的環(huán)境狀況�、所有與生產(chǎn)相關(guān)的設(shè)備及物料的污染狀況�、人員操作和衛(wèi)生狀況等�,每個(gè)環(huán)節(jié)都對(duì)最終產(chǎn)品的質(zhì)量有舉足輕重的意義。而已有的研究更多地聚焦于設(shè)計(jì)布局�����、物料狀態(tài)等方面,對(duì)人員操作因素的影響方面關(guān)注較少���。
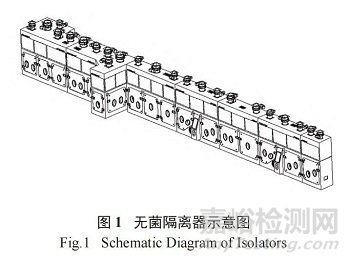
因此�����,以本公司凍干制劑生產(chǎn)車(chē)間為例 ( 圖 1為車(chē)間使用的無(wú)菌隔離器示意圖 ),本研究詳細(xì)論述無(wú)菌隔離器內(nèi)人員操作的規(guī)范性對(duì)產(chǎn)品質(zhì)量的重要影響�,為其他車(chē)間合理使用無(wú)菌隔離器、規(guī)范人員操作動(dòng)作等提供參考�����。
一�、無(wú)菌隔離器內(nèi)的操作設(shè)計(jì)及驗(yàn)證
凍干制劑呈粉狀,容易通過(guò)呼吸進(jìn)入人體�����,從而對(duì)人體造成危害�����。此外,在產(chǎn)品灌裝過(guò)程中,任何不當(dāng)操作都有可能導(dǎo)致產(chǎn)品污染���。因此本車(chē)間對(duì)操作人員的動(dòng)作進(jìn)行嚴(yán)格規(guī)范 :(1) 無(wú)菌隔離器中所有動(dòng)作都不能幅度過(guò)大或動(dòng)作過(guò)快 �;(2) 手套不能接觸任何與工藝操作無(wú)關(guān)的表面�����。上述要求內(nèi)容均在車(chē)間相關(guān)標(biāo)準(zhǔn)操作規(guī)程中明確���,在此基礎(chǔ)上�����,為驗(yàn)證操作人員操作是否符合規(guī)范和文件要求�����,本車(chē)間按照相關(guān)法規(guī)���,在確保無(wú)菌隔離器內(nèi)清潔合格、排除前批操作對(duì)驗(yàn)證結(jié)果影響的前提下�,定期進(jìn)行無(wú)菌工藝模擬和氣流流型測(cè)試�����。
1、無(wú)菌隔離器內(nèi)的操作設(shè)計(jì)
要保證操作人員在無(wú)菌隔離器內(nèi)的操作規(guī)范性�,需先對(duì)操作人員在無(wú)菌隔離器內(nèi)的操作內(nèi)容進(jìn)行嚴(yán)格設(shè)計(jì)。設(shè)計(jì)內(nèi)容應(yīng)包含操作人員在無(wú)菌隔離器內(nèi)日常生產(chǎn)時(shí)的操作�����,以及無(wú)菌隔離器內(nèi)設(shè)備出現(xiàn)異常時(shí)的操作�����,并確保所有干預(yù)操作均是實(shí)際生產(chǎn)中可能出現(xiàn)的�����,不進(jìn)行不合理干預(yù) [10]�。
每批生產(chǎn)均會(huì)發(fā)生的、正常的���、有計(jì)劃的生產(chǎn)工藝本身固有的干預(yù)操作匯總見(jiàn)表 1�,包括無(wú)菌隔離器內(nèi)的環(huán)境監(jiān)測(cè)�����、過(guò)渡部位對(duì)接�����、在線稱(chēng)重�、取樣等。糾正性干預(yù)操作 ( 即在生產(chǎn)過(guò)程中進(jìn)行糾正或調(diào)整的操作 ) 匯總見(jiàn)表 2�����,包括無(wú)菌隔離器使用過(guò)程中可能發(fā)生的情況�����,如倒瓶�、炸瓶、碎瓶�、傳感器異常和針頭調(diào)節(jié)等。
2�����、無(wú)菌隔離器內(nèi)操作規(guī)范性的驗(yàn)證
氣流流型測(cè)試
氣流流型測(cè)試是指通過(guò)將無(wú)菌隔離器內(nèi)的氣流可視化�,來(lái)驗(yàn)證設(shè)備運(yùn)行和人員操作是否會(huì)對(duì)流型產(chǎn)生影響 [11]。具體測(cè)試方法為有資質(zhì)的驗(yàn)證人員使用煙霧發(fā)生器進(jìn)行測(cè)試�。在確保無(wú)菌隔離器處于關(guān)閉狀態(tài)后���,驗(yàn)證人員將設(shè)置好的煙霧發(fā)生器連接發(fā)煙管、調(diào)整方向�,對(duì)準(zhǔn)工作區(qū)域上方�、均流膜下方 30 cm 處���,啟動(dòng)煙霧發(fā)生器���,使煙霧進(jìn)入氣流并隨氣流流動(dòng)�。
傳統(tǒng)的潔凈室設(shè)計(jì)通常在關(guān)鍵區(qū)域采用單向流的方式�����,并且在靠近打開(kāi)的無(wú)菌產(chǎn)品和容器的地方通常要求塵埃粒子符合 A 級(jí)潔凈度級(jí)別���,以減少產(chǎn)品和人員污染。本車(chē)間根據(jù)《醫(yī)藥工業(yè)潔凈廠房設(shè)計(jì)規(guī)范》和《藥品生產(chǎn)質(zhì)量管理規(guī)范 (2010 年修訂 )》附錄 1 無(wú)菌藥品的要求 [12-13]�,A 級(jí)潔凈區(qū)采用單向流���。然而���,能否控制潔凈區(qū)內(nèi)的空氣潔凈度�����,氣流的影響較大。無(wú)菌隔離器內(nèi)為 A 級(jí)環(huán)境,能否在日常生產(chǎn)中一直維持其內(nèi)部的單向流對(duì)環(huán)境潔凈度���、產(chǎn)品質(zhì)量有重要影響。該測(cè)試會(huì)使用攝像設(shè)備全程記錄生產(chǎn)過(guò)程中的煙霧流動(dòng)方向�����。測(cè)試過(guò)程中,無(wú)菌隔離器內(nèi)設(shè)備處于正常生產(chǎn)狀態(tài)�����,人員在各個(gè)崗位進(jìn)行模擬干預(yù)操作���,模擬操作方法見(jiàn)表 1�、表 2。通過(guò)是否引起紊流或空氣停滯等異常狀態(tài)來(lái)驗(yàn)證人員在無(wú)菌隔離器內(nèi)的操作是否規(guī)范�����。
無(wú)菌工藝模擬 (aseptic process simulation,APS)
APS 是指使用大豆胰蛋白胨液體培養(yǎng)基來(lái)代替藥品進(jìn)行生產(chǎn) [14]�����。因?yàn)樵诖蠖鄶?shù)情況下�,微生物在培養(yǎng)基中的生長(zhǎng)繁殖要遠(yuǎn)比在實(shí)際產(chǎn)品中容易�,所以使用培養(yǎng)基進(jìn)行生產(chǎn),其無(wú)菌風(fēng)險(xiǎn)遠(yuǎn)大于正常生產(chǎn)�,不僅可用于評(píng)價(jià)生產(chǎn)工藝對(duì)產(chǎn)品無(wú)菌保證的有效性和穩(wěn)定性���,還可用于驗(yàn)證人員的無(wú)菌操作能力�。國(guó)家藥品監(jiān)督管理局藥品審評(píng)中心在對(duì)企業(yè)的APS 檢查中也提出 [10]�����,相關(guān)企業(yè)在人員的培訓(xùn)與操作方面問(wèn)題較大���。因此�,非常有必要對(duì)人員在無(wú)菌隔離器內(nèi)的操作進(jìn)行驗(yàn)證�。為保證該驗(yàn)證的普遍適用性���,本研究對(duì)驗(yàn)證中的人員在無(wú)菌隔離器內(nèi)的操作行動(dòng)進(jìn)行規(guī)范。在APS 驗(yàn)證中�,人員需在無(wú)菌隔離器內(nèi)進(jìn)行“1.1”項(xiàng)下所述的干預(yù)操作,包含生產(chǎn)過(guò)程中可能涉及的所有操作�,具體操作內(nèi)容如表 1、表 2 所示�。
在整個(gè) APS 驗(yàn)證過(guò)程中���,按 GMP 要求采用最差的灌裝條件,并且對(duì)無(wú)菌工藝模擬生產(chǎn)的培養(yǎng)基產(chǎn)品進(jìn)行促生長(zhǎng)試驗(yàn)�����,保證操作人員的任何不規(guī)范操作均會(huì)反映在培養(yǎng)基產(chǎn)品上���。同時(shí)���,對(duì)無(wú)菌隔離器內(nèi) A 級(jí)環(huán)境和無(wú)菌隔離器所在的 C 級(jí)背景環(huán)境按正常生產(chǎn)頻率進(jìn)行動(dòng)態(tài)環(huán)境監(jiān)測(cè)�,監(jiān)測(cè)項(xiàng)目為沉降菌���、浮游菌���、懸浮粒子和表面微生物。此外�,及時(shí)記錄潔凈區(qū)之間的壓差、溫度和濕度���,通過(guò)環(huán)境監(jiān)測(cè)結(jié)果和培養(yǎng)基產(chǎn)品的培養(yǎng)結(jié)果來(lái)驗(yàn)證人員在無(wú)菌隔離器內(nèi)的操作是否規(guī)范。
二�、無(wú)菌隔離器內(nèi)操作的驗(yàn)證結(jié)果
1���、 氣流流型測(cè)試
在無(wú)菌隔離器內(nèi)的設(shè)備處于正常生產(chǎn)狀態(tài)且人員在各個(gè)崗位上進(jìn)行模擬干預(yù)操作的條件下�,由相關(guān)驗(yàn)證人員完成氣流流型測(cè)試���。驗(yàn)證人員應(yīng)根據(jù)實(shí)際情況�����,選擇無(wú)菌隔離器內(nèi)的流型測(cè)試點(diǎn)�����,確保人員在無(wú)菌隔離器內(nèi)的模擬干預(yù)操作均在煙霧氣流下方。氣流流型測(cè)試動(dòng)作節(jié)選如圖 2 所示�����,人員在無(wú)菌隔離器內(nèi)進(jìn)行操作時(shí)���,無(wú)菌隔離器內(nèi)的單向流沒(méi)有發(fā)生改變�,未產(chǎn)生紊流現(xiàn)象,且與靜態(tài)測(cè)試相比�����,氣流流型相同���,則說(shuō)明人員在無(wú)菌隔離器內(nèi)的操作規(guī)范�����,不會(huì)對(duì)無(wú)菌隔離器內(nèi)的環(huán)境產(chǎn)生影響�,進(jìn)而影響產(chǎn)品質(zhì)量。
2���、APS 驗(yàn)證
生產(chǎn)前無(wú)菌隔離器的準(zhǔn)備
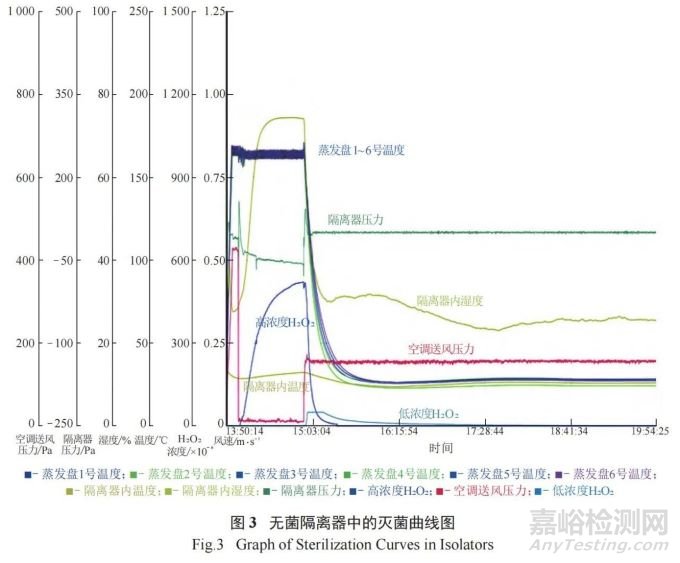
無(wú)菌隔離器在生產(chǎn)前會(huì)進(jìn)行清潔�����、消毒���、滅菌,以保證設(shè)備運(yùn)行前無(wú)微生物污染���,不會(huì)對(duì)驗(yàn)證結(jié)果產(chǎn)生影響�。
對(duì)無(wú)菌隔離器內(nèi)的固定設(shè)備和手套等采用異丙醇進(jìn)行噴霧和擦拭�,以對(duì)其表面進(jìn)行清潔和消毒。無(wú)菌隔離器內(nèi)的灌裝壓塞機(jī)需進(jìn)行泄漏檢測(cè)���,檢測(cè)合格后�����,進(jìn)行在線高溫濕熱滅菌 (121 ℃�����,30 min)�����。隨后���,將設(shè)備運(yùn)行過(guò)程中所需的輔助器具 ( 如不銹鋼條和培養(yǎng)皿等物品 ) 經(jīng)預(yù)處理后放置于無(wú)菌隔離器中。按無(wú)菌隔離器驗(yàn)證的裝載示意圖定點(diǎn)放置后���,對(duì)無(wú)菌隔離器進(jìn)行泄漏測(cè)試,測(cè)試合格后���,采用經(jīng)第三方機(jī)構(gòu)通過(guò)對(duì)無(wú)菌隔離器內(nèi)的過(guò)氧化氫濃度以及生物指示劑的挑戰(zhàn)驗(yàn)證得出的滅菌運(yùn)行參數(shù)( 預(yù)處理 10 min、充氣 15 min�����、保壓 40 min、通風(fēng)120 min) 進(jìn)行滅菌�����,通風(fēng)至過(guò)氧化氫濃度降至 10–6以下���,然后對(duì)過(guò)氧化氫滅菌曲線與崗位標(biāo)準(zhǔn)操作規(guī)程模板曲線進(jìn)行審核�����,確保滅菌效果達(dá)到要求�。過(guò)氧化氫滅菌曲線見(jiàn)如圖 3�����。
APS
APS 過(guò)程在 C 級(jí)潔凈區(qū)背景下的無(wú)菌隔離器 A級(jí)潔凈區(qū)環(huán)境中進(jìn)行�����。操作人員按表 1 和表 2 所示模擬方法進(jìn)行干預(yù)操作�����,并記錄每項(xiàng)干預(yù)操作的次數(shù)和時(shí)間。整個(gè)過(guò)程通過(guò)攝像設(shè)備記錄�����,動(dòng)作節(jié)選如圖4所示�����,操作人員通過(guò)手套箱操作時(shí)�,動(dòng)作干凈、移動(dòng)緩慢且穩(wěn)健�����。
APS 過(guò)程的環(huán)境監(jiān)測(cè)
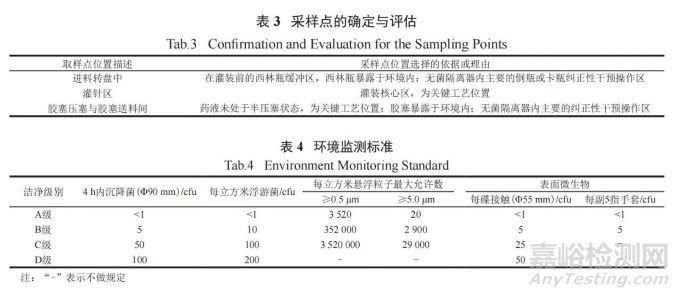
在 APS 全程中進(jìn)行沉降菌�����、浮游菌�����、懸浮粒子和表面微生物的監(jiān)測(cè)�。沉降菌、浮游菌和懸浮粒子的采樣點(diǎn)確定與評(píng)估見(jiàn)表 3,監(jiān)測(cè)標(biāo)準(zhǔn)嚴(yán)格遵守GMP 規(guī)定 ( 見(jiàn)表 4)���。
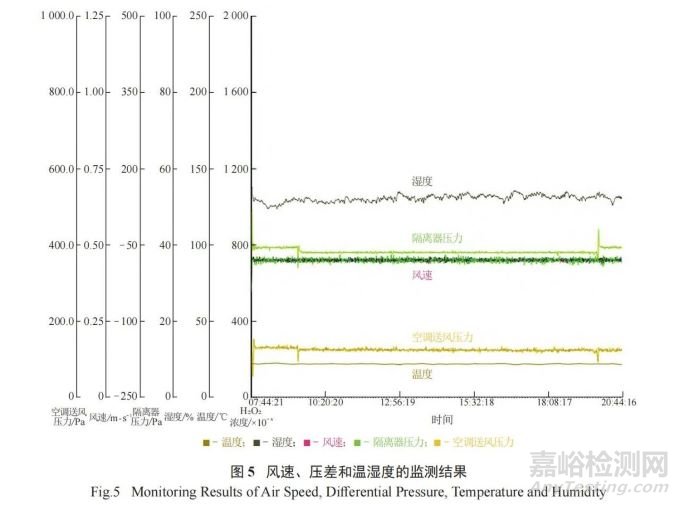
表面微生物的監(jiān)測(cè)除設(shè)備表面、無(wú)菌隔離器手套表面外�,還包括人員監(jiān)測(cè) ( 如人員穿戴的潔凈服表面和人員佩戴的手套表面等 ),進(jìn)一步對(duì)人員在無(wú)菌隔離器內(nèi)的操作規(guī)范性進(jìn)行限制���。監(jiān)測(cè)結(jié)果表明�,整個(gè)模擬過(guò)程中微生物的污染水平未超過(guò)法規(guī)規(guī)定的限度�����,證明人員在無(wú)菌隔離器內(nèi)的操作不會(huì)對(duì)環(huán)境造成影響���。除此之外�����,整個(gè)APS過(guò)程中�,風(fēng)速���、壓差和溫濕度等監(jiān)測(cè)結(jié)果均符合相關(guān)法規(guī)要求�����,監(jiān)測(cè)記錄曲線見(jiàn)圖 5�����。
APS 的培養(yǎng)基產(chǎn)品檢查
在 APS 結(jié)束后���,由車(chē)間燈檢崗位人員對(duì)所有產(chǎn)品進(jìn)行初步燈檢�。燈檢后�����,將待培養(yǎng)品充分振搖 ( 確保接觸西林瓶?jī)?nèi)表面 )�,然后倒立置于 20 ~25 ℃培養(yǎng)室內(nèi)培養(yǎng),培養(yǎng)時(shí)間不得少于 7 d �;隨后將灌裝品翻轉(zhuǎn),正位放置于 30 ~ 35 ℃培養(yǎng)室內(nèi)培養(yǎng)�,培養(yǎng)時(shí)間不得少于 7 d,進(jìn)行培養(yǎng)觀察���,并由具有資質(zhì)的質(zhì)量管理部人員按 ChP 2020 的要求對(duì)培養(yǎng)基產(chǎn)品進(jìn)行澄清度檢查�����。培養(yǎng) 14 d 后的培養(yǎng)基溶液在澄明度檢測(cè)儀下仍為澄清溶液�,無(wú)異物、渾濁�����,確認(rèn)無(wú)微生物生長(zhǎng)�����。按 GMP 附錄無(wú)菌藥品要求�����,APS 樣品的培養(yǎng)結(jié)果應(yīng)為零污染,因此可根據(jù)零污染的培養(yǎng)結(jié)果�,確認(rèn)人員在無(wú)菌隔離器內(nèi)操作的規(guī)范性。
三���、總結(jié)與展望
與 RABS 技術(shù)相比,無(wú)菌隔離器的優(yōu)勢(shì)明顯�����。從隔離系統(tǒng)設(shè)計(jì)本身分析,RABS 的回風(fēng)系統(tǒng)會(huì)產(chǎn)生回風(fēng)不均勻的問(wèn)題���,導(dǎo)致外圍環(huán)境空氣質(zhì)量下降 [15]�����,且人員操作的污染風(fēng)險(xiǎn)相對(duì)較高�����。無(wú)菌隔離器的背景環(huán)境要求在 D 級(jí)以上���,簡(jiǎn)化了人員的更衣程序,更方便人員進(jìn)行生產(chǎn)操作�����。已有研究對(duì)使用過(guò)氧化氫進(jìn)行無(wú)菌隔離器滅菌的方法進(jìn)行了驗(yàn)證�����,確認(rèn)其滅菌效果合格 [8—9]�����。因而,無(wú)菌隔離器生產(chǎn)前的滅菌操作可排除其他因素對(duì)人員操作驗(yàn)證結(jié)果的影響���,在此基礎(chǔ)上���,以實(shí)際生產(chǎn)操作為模板設(shè)計(jì)的模擬干預(yù)操作是合理的。
在氣流流型測(cè)試中�����,確認(rèn)靜態(tài)隔離器內(nèi)流型為垂直單向�����,不會(huì)對(duì)產(chǎn)品產(chǎn)生污染�。而在進(jìn)行生產(chǎn)和人員操作的整個(gè)動(dòng)態(tài)過(guò)程中���,無(wú)菌隔離器內(nèi)風(fēng)速穩(wěn)定,且內(nèi)部的流型恒為單向定流�,符合 A 級(jí)要求。
整個(gè)測(cè)試過(guò)程中�����,不產(chǎn)生任何紊流,且無(wú)菌隔離器內(nèi)單向流均勻分布�,不會(huì)產(chǎn)生氣流死角,從而不會(huì)對(duì)產(chǎn)品產(chǎn)生污染 [16]�����。在 APS 中�����,結(jié)合灌裝產(chǎn)品的培養(yǎng)觀察結(jié)果和環(huán)境監(jiān)測(cè)結(jié)果�,確認(rèn)整個(gè) APS 過(guò)程中未對(duì)產(chǎn)品產(chǎn)生污染。驗(yàn)證結(jié)果的合格不僅證明了本車(chē)間產(chǎn)品生產(chǎn)工藝的合理性���,也表明了無(wú)菌隔離器操作人員生產(chǎn)操作的規(guī)范性�。進(jìn)行無(wú)菌隔離器操作的工作人員在上崗前均已進(jìn)行過(guò)嚴(yán)格培訓(xùn)�����,使其在無(wú)菌隔離器內(nèi)的操作緩慢���、干凈�,無(wú)任何多余小動(dòng)作 �����;即使出現(xiàn)設(shè)備故障等異常因素,操作人員進(jìn)行的糾正性操作也符合要求���。
參考文獻(xiàn)
[1] 張 秋.隔離器顛覆傳統(tǒng)潔凈技術(shù)——從新版 GMP 對(duì)無(wú)菌藥品的要求看無(wú)菌隔離器在制藥行業(yè)的應(yīng)用[J].流程工業(yè), 2011, (20): 19.
[2] 李曉雪, 梁 毅.對(duì)無(wú)菌隔離操作器及其結(jié)構(gòu)與確認(rèn)的探討[J].機(jī)電信息, 2015, (23): 24-27.
[3] 中華人民共和國(guó)國(guó)家質(zhì)量監(jiān)督檢驗(yàn)檢疫總局, 中國(guó)國(guó)家標(biāo)準(zhǔn)化管理委員會(huì).潔凈室及相關(guān)受控環(huán)境 第7部分: 隔離裝置(潔凈風(fēng)罩�����、手套箱���、隔離器、微環(huán)境): GB/T 25915.7-2010 [S].北京: 中國(guó)標(biāo)準(zhǔn)出版社, 2011.
[4] 高海燕, 丁恩峰, 趙麗雅, 等.USP對(duì)無(wú)菌檢驗(yàn)隔離器驗(yàn)證的技術(shù)要求[J].醫(yī)藥工程設(shè)計(jì), 2010, 31(2): 29-33.
[5] 袁松范.工業(yè)指南——用無(wú)菌工藝生產(chǎn)的無(wú)菌產(chǎn)品-現(xiàn)行GMP(續(xù))[J].醫(yī)藥工程設(shè)計(jì), 2005, (5): 44-48.
[6] 袁松范.工業(yè)指南 用無(wú)菌工藝生產(chǎn)的無(wú)菌產(chǎn)品-現(xiàn)行GMP[J].醫(yī)藥工程設(shè)計(jì), 2005, (2): 41-46.
[7] 馬 偉, 孫石磊.無(wú)菌隔離器的優(yōu)勢(shì)及其發(fā)展趨勢(shì)[J].機(jī)電信息, 2013, (20): 32-36.
[8] 胡桂蘭, 岳云燕.無(wú)菌隔離系統(tǒng)驗(yàn)證技術(shù)的研究[J].輕工科技, 2018, 34(4): 33-34.
[9] 羅輝艷, 嚴(yán)東珍, 劉家媛, 等.無(wú)菌隔離器滅菌效果研究[J].中國(guó)設(shè)備工程, 2017, (6): 78-79.
[10] 胡敬峰, 韓 瑩.無(wú)菌工藝模擬試驗(yàn)中存在的問(wèn)題與對(duì)策[J].中國(guó)藥事, 33(12): 1395-1399.
[11] 吳 軍.氣流保護(hù)與無(wú)菌工藝操作探討[J].流程工業(yè), 2018, (12): 44-46.
[12] 中華人民共和國(guó)住房和城鄉(xiāng)建設(shè)部, 國(guó)家市場(chǎng)監(jiān)督管理總局.醫(yī)藥工業(yè)潔凈廠房設(shè)計(jì)標(biāo)準(zhǔn): GB 50457-2019 [S].北京: 中國(guó)標(biāo)準(zhǔn)出版社, 2019.
[13] 《〈藥品生產(chǎn)質(zhì)量管理規(guī)范〉解讀》編委會(huì).《藥品生產(chǎn)質(zhì)量管理規(guī)范(2010年修訂)》解讀[M].北京: 中國(guó)醫(yī)藥科技出版社, 2011: 2-5.
[14] 錢(qián)靜杰.粉針劑無(wú)菌工藝驗(yàn)證——培養(yǎng)基模擬灌裝試驗(yàn)[J].醫(yī)藥前沿, 2011, 1(20): 217-219.
[15] 錢(qián)小進(jìn).RABS隔離系統(tǒng)�、FFU以及oRABS的取風(fēng)方式[J].機(jī)電信息, 2013, (11): 31-34.
[16] 吳文蕾.無(wú)菌檢查隔離器的設(shè)備與應(yīng)用要求[J].流程工業(yè), 2017, (6): 28-31.