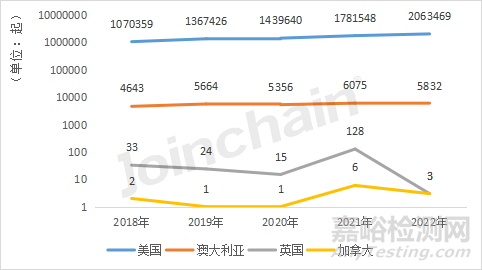
醫(yī)療器械不良事件是指已上市的醫(yī)療器械,在正常使用情況下發(fā)生的��,導致或者可能導致人體傷害的各種有害事件��。不良事件數(shù)據(jù)是醫(yī)療器械上市后監(jiān)管的重要數(shù)據(jù)源之一,目前�,全球各醫(yī)療器械主要國家都建立了不良事件上報制度及不良事件數(shù)據(jù)庫。據(jù)MDCLOUD(醫(yī)械數(shù)據(jù)云)統(tǒng)計����,2018年至2022年,醫(yī)療器械海外不良事件數(shù)量呈逐年遞增的趨勢����,其中,美國報道的不良事件數(shù)由1070359起增至2063469起�;澳大利亞報道的不良事件數(shù)由4643起(2018年)增至6075起(2021年),在2022年有5832起����;英國報道的不良事件報告披露較少��,在2018年至2020年呈波動下降的趨勢��,在2021年由15起(2020年)突增至128起,又在2022年劇減至3起����;加拿大報道的不良事件數(shù)量在近五年維持在個位數(shù)以內(nèi),2019和2020年最低����,均只有1起,2021年最高��,為6起��。
本文將重點對各國2022年的不良事件數(shù)據(jù)進行回顧與統(tǒng)計分析�,以期洞察2022年全球醫(yī)療器械不良事件的宏觀情況。
圖1 全球各主要海外國家近五年的不良事件數(shù)量變化趨勢
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
注:截止2023年1月11日����,澳大利亞藥品管理局披露的醫(yī)療器械不良事件報告的最新時間為2022年9月1日;加拿大藥監(jiān)部門與英國藥監(jiān)機構(gòu)的不良事件報告為不定期披露�。
一、整體情況
1�、美國
(1)2022年不良事件數(shù)同比增長15.8%
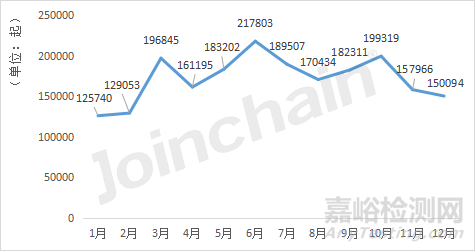
據(jù)MDCLOUD(醫(yī)械數(shù)據(jù)云)統(tǒng)計,2022年美國醫(yī)療器械不良事件數(shù)據(jù)庫(以下簡稱MAUDE數(shù)據(jù)庫)共披露2063469起不良事件�,對比2021年的1781548起,增加了281921起��。2022年一季度的數(shù)量變化趨勢與2021年一季度的基本一致����,1����、2月份的事件數(shù)相對較少��,而后在3月份大幅增加�。2021年4月起�,事件數(shù)量開始下降。2022年3月至10月的不良事件數(shù)呈波動上升趨勢��,6月份達到該年單月事件數(shù)峰值217803起�,為1月事件數(shù)的1.7倍,11�、12月份平緩下降,2022年2��、3季度的不良事件數(shù)相比去年有所增長����。
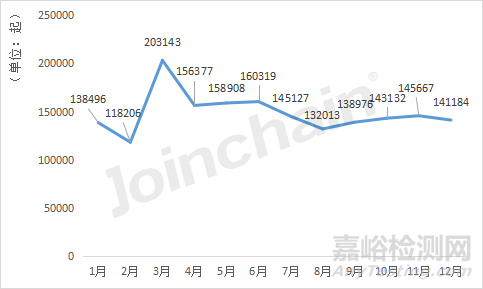
圖2 2022年美國不良事件數(shù)量隨時間變化的趨勢
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
圖3 2021年美國不良事件數(shù)量隨時間變化的趨勢
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
(2)致傷/致死事件占比較往年同期下降
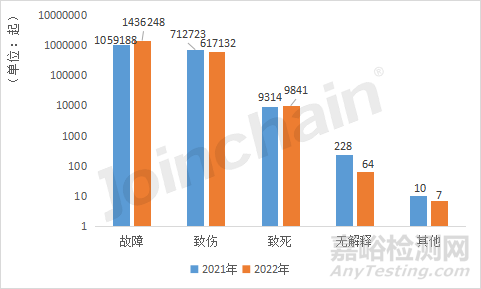
美國不良事件數(shù)據(jù)庫將不良事件的事件類型界定為:故障、致傷��、致死��、無解釋和其他,另有少量事件沒有劃分����。據(jù)MDCLOUD(醫(yī)械數(shù)據(jù)云)統(tǒng)計����,2022年美國不良事件占比最高的事件類型為故障事件,達69.61%��,共發(fā)生1436248起��;其次為致傷事件�,共有617132起,占總數(shù)的29.91%����;致死事件共發(fā)生了9841起,占0.48%�;此外,還有71起不良事件為未解釋及其他事件類型�。對比2021年,2022年美國不良事件的故障事件類型比例增長了約10%�,致傷事件和致死事件類型占比有所減少,分別下降了10.1%和0.04%�。
圖4 2022年和2021年美國各事件類型的不良事件數(shù)量
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
注:2021年有85起不良事件無相關(guān)信息,2022年有177起不良事件無相關(guān)信息,均不列入統(tǒng)計
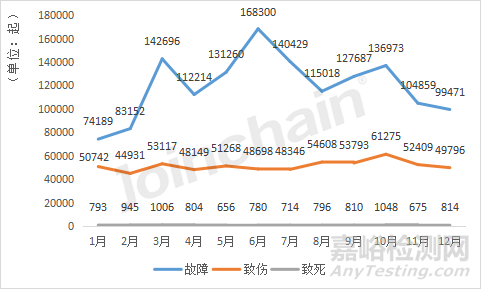
從2022年全年的事件類型數(shù)量變化來看����,美國不良事件的致傷、致死事件數(shù)量變化相對較小����,其中,10月份的致傷事件與致死事件最多��,分別達到了61275起和1048起��。故障事件數(shù)量變化存在波動��,1月份事件數(shù)量為全年最低����,為74189起,6月份達到單月最高�,共168300起,上半年事件數(shù)呈波動上升趨勢�,下半年逐步下降。
圖5 美國致傷�、致死、故障事件報告數(shù)量隨時間變化的趨勢
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
(3)超95%不良事件由制造商主動上報
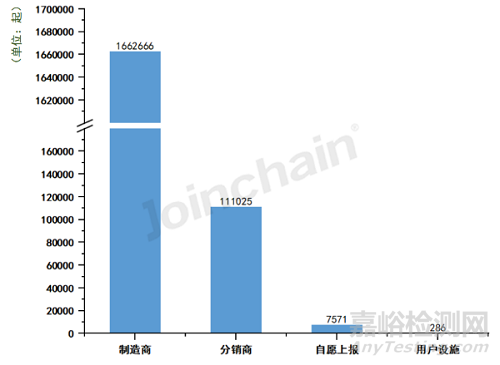
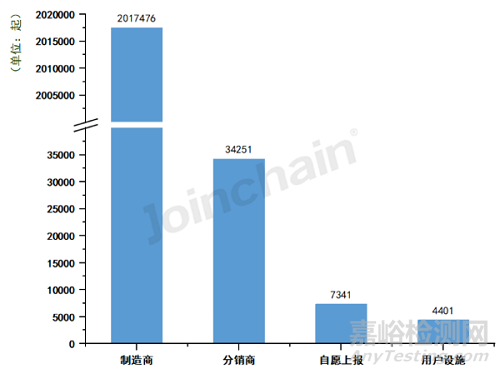
從2022年全年披露的不良事件報告來源來看����,共有2017476起美國不良事件來源于制造商�,其比例高達97.77%����,另有34251起報告來源于分銷商��,7341起為自愿上報����,4401起來自用戶設施,分別占比1.66%����、0.36%、0.21%����。相比2021年,由制造商上報的不良事件報告有1662666起�,占比93.33%,可以看出美國不良事件的上報絕大多數(shù)來源于制造商�,且無論數(shù)量還是占比對比去年都有明顯提升。
圖6 2022年美國各報告來源的事件數(shù)量
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
圖7 2021年美國各報告來源的事件數(shù)量
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
2����、澳大利亞
(1)整體事件數(shù)量變化較平緩
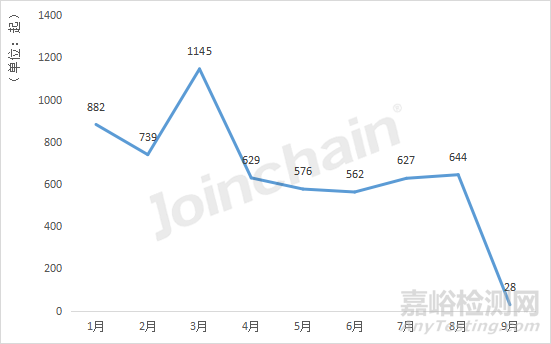
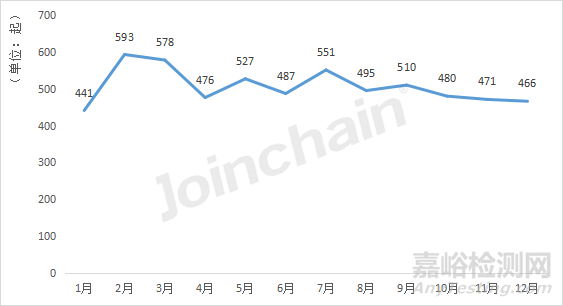
據(jù)MDCLOUD(醫(yī)械數(shù)據(jù)云)統(tǒng)計�,截止2023年1月11日����,2021年與2022年的澳大利亞不良事件數(shù)分別為6075起和5832起。2021年澳大利亞每月的不良事件數(shù)相差不大�,整體較為平穩(wěn);2022年的3月出現(xiàn)上半年的第一個事件數(shù)峰值��,從2月份的739起增加到1145起��,隨后在4月份回落到629起�。但總體上2022年1月至8月的每月不良事件數(shù)波動相對較小,整體趨于平緩����。
圖8 2022年1-9月澳大利亞事件數(shù)量隨時間變化的趨勢
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
注:澳大利亞不良事件數(shù)據(jù)庫最新披露的報告時間為9月1日。
圖9 2021年澳大利亞事件數(shù)量隨時間變化的趨勢
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
(2)引發(fā)致傷的事件占比超7成
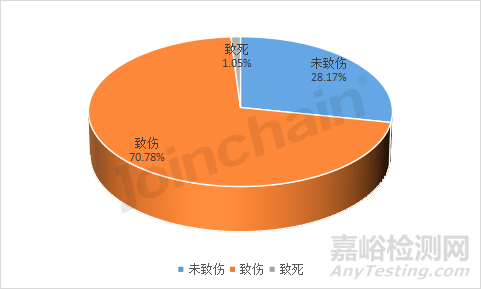
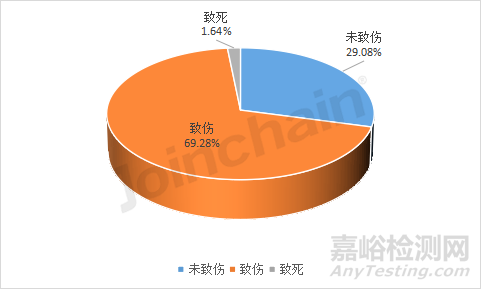
澳大利亞不良事件數(shù)據(jù)對事件引發(fā)后果分為:致傷�、致死和未致傷三類。據(jù)MDCLOUD(醫(yī)械數(shù)據(jù)云)統(tǒng)計�,2022年共有3909起不良事件引發(fā)致傷后果,占總事件數(shù)的70.78%��;1556起未引起致傷��,占28.17%;58起引發(fā)致死后果��,占1.05%����。對比2021年的數(shù)據(jù),2022年引發(fā)致傷后果的事件比例提升了1.5%����,引發(fā)致死后果的事件比例下降0.59%����,全年引發(fā)致傷、致死后果的不良事件占總數(shù)量的三分之二以上�。
圖10 2022年1-9月澳大利亞事件引發(fā)后果類型數(shù)量占比
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
注:有309份不良事件報告無此信息,不列入統(tǒng)計
圖11 2021年澳大利亞事件引發(fā)后果類型數(shù)量占比
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
注:有459份不良事件報告無此信息����,不列入統(tǒng)計
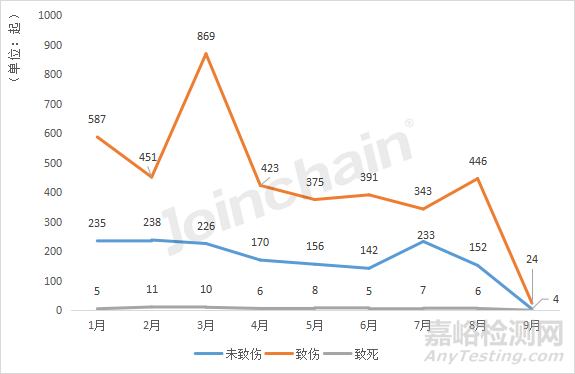
2022年3月,澳大利亞披露的引發(fā)致傷后果的不良事件數(shù)量明顯增加����,達到了869起,相比4月的引發(fā)致傷不良事件數(shù)增長了近1倍�。全年各月份引發(fā)致死后果的不良事件數(shù)維持在11起以下����。
圖12 2022年1-9月澳大利亞引發(fā)不同后果類型的不良事件數(shù)量隨時間變化的趨勢
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
(3)制造商和供應商主動上報比例超90%
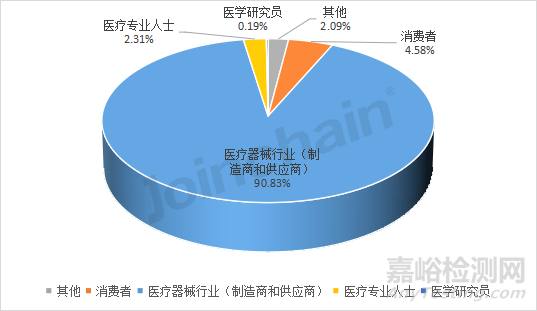
從不良事件報告人的來源類型來看��,2022年澳大利亞的不良事件主要來自醫(yī)療器械行業(yè)的制造商和供應商��,上報數(shù)量為5297起�,占90.83%;267起來自消費者�,占4.58%;135起為來自醫(yī)療專業(yè)人士�,占2.31%;122起來自其他報告人��,占2.09%��;11起來自醫(yī)學研究員�,占0.19%。對比2021年的報告人來源類型占比�,2022年的制造商和供應商上報、消費者上報比例有所提升����,整體以制造商和供應商上報為主。
圖13 2022年報告人的來源類型占比
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
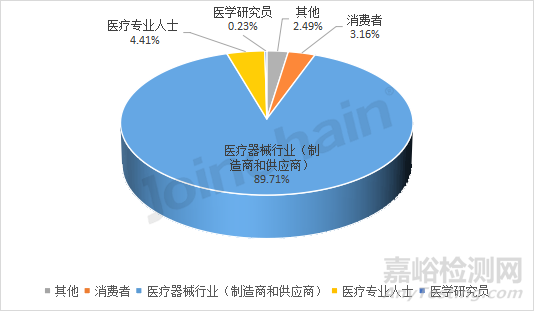
圖14 2021年報告人的來源類型占比
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
3�、英國
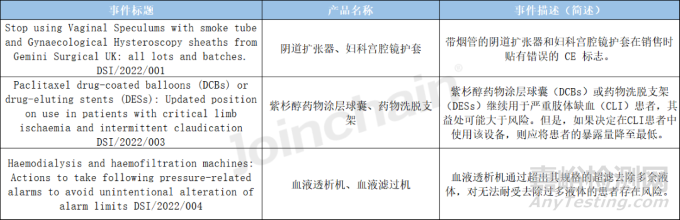
2022年英國醫(yī)療器械署官網(wǎng)僅披露了3起醫(yī)療器械不良事件����,相比2021年(128起)大幅減少��。2022年披露的3起不良事件報告共涉及的產(chǎn)品有陰道擴張器�、婦科宮腔鏡護套、紫杉醇藥物涂層球囊��、藥物洗脫支架����、血液透析機和血液濾過機,不良事件的具體內(nèi)容見表3�。
表3 2022年英國披露的不良事件內(nèi)容
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
4����、加拿大
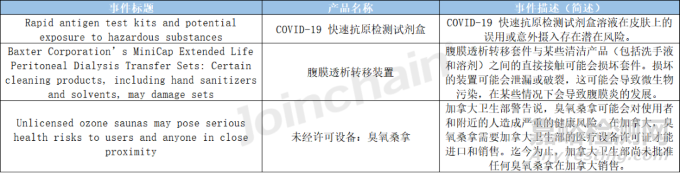
2022年加拿大不良數(shù)據(jù)庫披露了3起醫(yī)療器械不良事件,相比2021年(6起)有所減少��,2022年披露的不良事件中涉及的產(chǎn)品有COVID-19 快速抗原檢測試劑盒��、腹膜透析轉(zhuǎn)移裝置等�,事件詳細內(nèi)容見表4。
表4 2022年加拿大披露的不良事件內(nèi)容
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
二�、產(chǎn)品情況
由于美國和澳大利亞公開披露的不良事件數(shù)據(jù)量相對較大��,故而對這兩個國家不良事件涉及的產(chǎn)品類型及相關(guān)產(chǎn)品故障問題做進一步的統(tǒng)計分析��。
1����、美國
(1)胰島素泵相關(guān)產(chǎn)品報道近48萬起
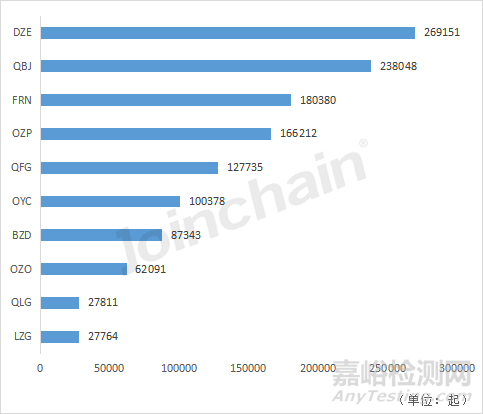
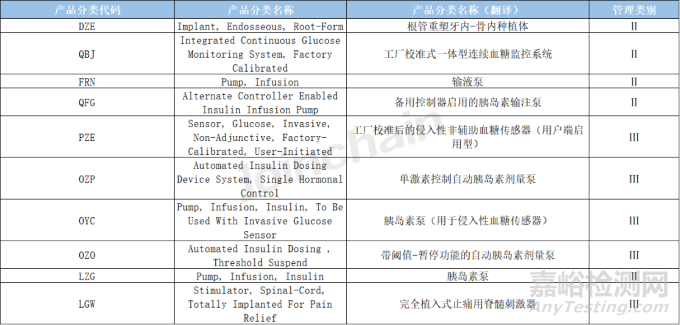
通過統(tǒng)計美國產(chǎn)品分類代碼對應的2022年不良事件數(shù)�,去年不良事件數(shù)量最多的單類產(chǎn)品為根管重塑牙內(nèi)-骨內(nèi)種植體(DZE),報道了近27萬起�;其次為工廠校準式一體型連續(xù)血糖監(jiān)控系統(tǒng)(QBJ)和輸液泵(FRN)。在不良事件數(shù)量前十的產(chǎn)品中��,共有六類產(chǎn)品為胰島素泵相關(guān)產(chǎn)品(OZP�、QFG、OYC��、OZO����、LZG),共計報道了484180起��,有兩類產(chǎn)品為血糖監(jiān)測產(chǎn)品(QBJ����、QLG)����,共有265859起��。
圖15 2022年美國不良事件數(shù)量前十的產(chǎn)品類型
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
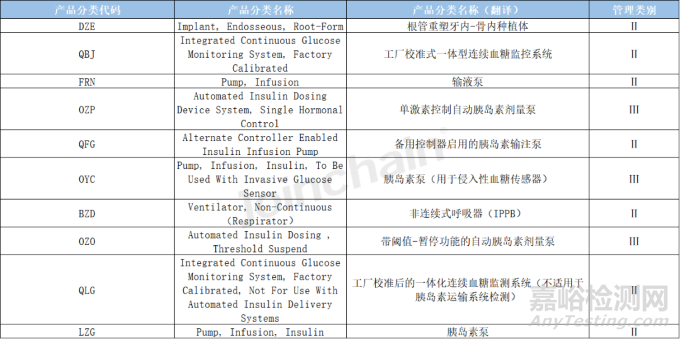
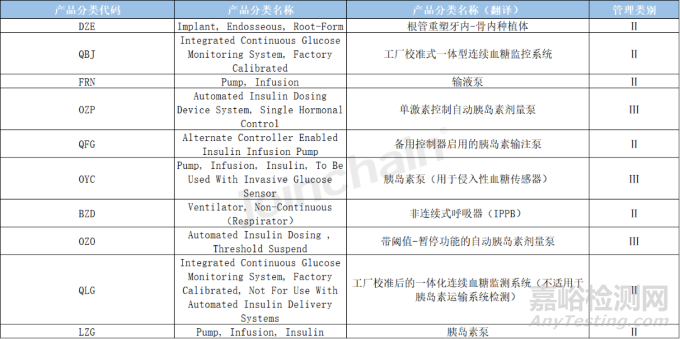
表5 2022年美國事件數(shù)量前十的產(chǎn)品分類信息表
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
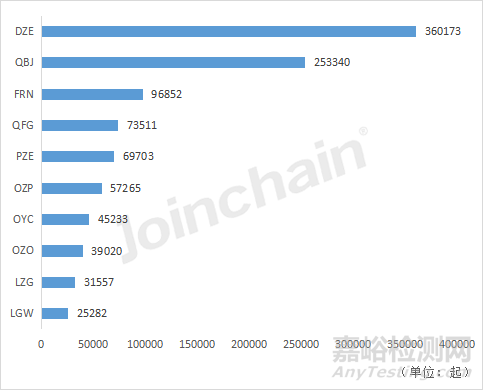
值得關(guān)注的是��,對比2021年不良事件數(shù)前十的產(chǎn)品類別��,可以發(fā)現(xiàn)�,根管重塑牙內(nèi)-骨內(nèi)種植體(DZE)、工廠校準式一體型連續(xù)血糖監(jiān)控系統(tǒng)(QBJ)和輸液泵(FRN)仍是排名前三的產(chǎn)品��,此外2022年不良事件數(shù)前十中的6類胰島素類產(chǎn)品(OZP�、QFG、OYC����、OZO�、LZG)同樣出現(xiàn)在2021年的不良事件數(shù)前十的10類產(chǎn)品中。
圖16 2021年美國不良事件數(shù)量前十的產(chǎn)品類型
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
表6 2021年美國事件數(shù)量前十的產(chǎn)品分類信息表
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
鑒于根管重塑牙內(nèi)-骨內(nèi)種植體(DZE)��、工廠校準式一體型連續(xù)血糖監(jiān)控系統(tǒng)(QBJ)和輸液泵(FRN)這三類產(chǎn)品的不良事件數(shù)相對較多��,故對這三類產(chǎn)品相關(guān)不良事件的設備問題和患者問題進行統(tǒng)計分析��。
(2)種植體、血糖監(jiān)控系統(tǒng)與輸液泵的高頻設備問題
A.根管重塑牙內(nèi)-骨內(nèi)種植體(DZE)
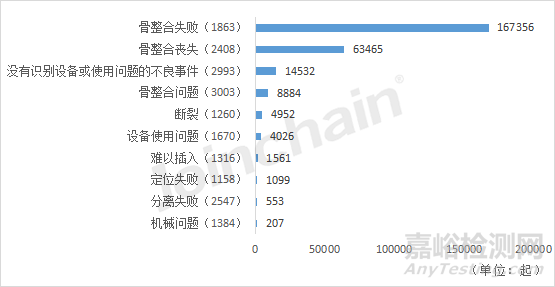
對根管重塑牙內(nèi)-骨內(nèi)種植體(DZE)的不良事件涉及的設備問題進行數(shù)量統(tǒng)計����,排在前5的高頻設備問題分別為:“骨整合失敗(1863)”����、“骨整合喪失(2408)”、“沒有識別設備或使用問題的不良事件(2993)”����、“骨整合問題(3003)”、“斷裂(1260)”�。提示該類產(chǎn)品的不良事件主要與種植體骨整合失敗、減弱或是與骨組織連接出現(xiàn)問題相關(guān)��。
圖17 根管重塑牙內(nèi)-骨內(nèi)種植體相關(guān)不良事件的前十大高頻設備問題
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
B.工廠校準式一體型連續(xù)血糖監(jiān)控系統(tǒng)(QBJ)
對工廠校準式一體型連續(xù)血糖監(jiān)控系統(tǒng)(QBJ)的不良事件涉及的設備問題進行數(shù)量統(tǒng)計�,排在前5的高頻設備問題分別為:“無線通信問題(3283)”、“無設備輸出(1435)”�、“不精確(1307)”、“過早報廢指示器(1480)”����、“意外的應用程序關(guān)閉(4032)”。提示該類產(chǎn)品的不良事件主要與設備的通信故障、信號輸出�、指示器壽命短等問題相關(guān)。
圖18 工廠校準式一體型連續(xù)血糖監(jiān)控系統(tǒng)相關(guān)不良事件的前十大高頻設備問
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
C.輸液泵(FRN)
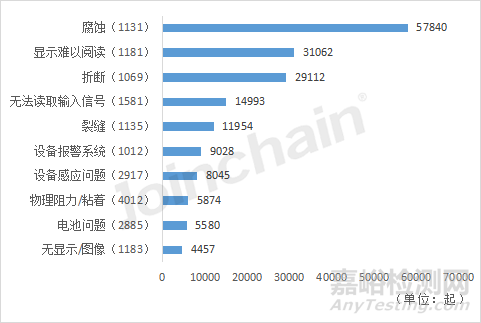
對輸液泵(FRN)的不良事件涉及的設備問題進行數(shù)量統(tǒng)計��,排在前5的高頻設備問題分別為::“腐蝕(1131)”�、“顯示難以閱讀(1181)”��、“折斷(1069)”��、“無法讀取輸入信號(1581)”��、“裂縫(1135)”�。提示該類產(chǎn)品的不良事件主要與產(chǎn)品不耐腐蝕,易折斷����、破損等問題相關(guān)。
圖19 輸液泵相關(guān)不良事件的前十大高頻設備問題
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
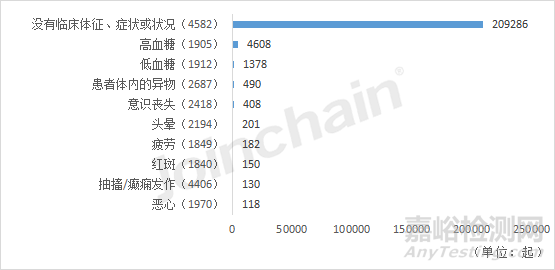
(3)種植體�、血糖監(jiān)控系統(tǒng)與輸液泵的高頻患者問題
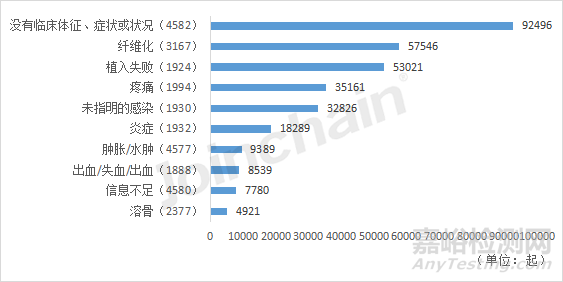
經(jīng)對這三類產(chǎn)品的不良事件涉及的患者問題進行數(shù)量統(tǒng)計,可以看到��,三者最高頻的患者問題均為沒有臨床體征��、癥狀或狀況(4582)����,尤其是血糖監(jiān)控系統(tǒng)與輸液泵,說明這兩類產(chǎn)品的不良事件大多數(shù)并未對患者造成傷害�。種植體由于骨整合出現(xiàn)問題后,會導致種植體周圍纖維化�,乃至植入失敗,造成患者出現(xiàn)疼痛等臨床反應�。
圖20 根管重塑牙內(nèi)-骨內(nèi)種植體相關(guān)不良事件的前十大高頻患者問題
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
圖21 工廠校準式一體型連續(xù)血糖監(jiān)控系統(tǒng)相關(guān)不良事件的前十大高頻患者問題
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
圖22 輸液泵相關(guān)不良事件的前十大高頻患者問題
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
2、澳大利亞
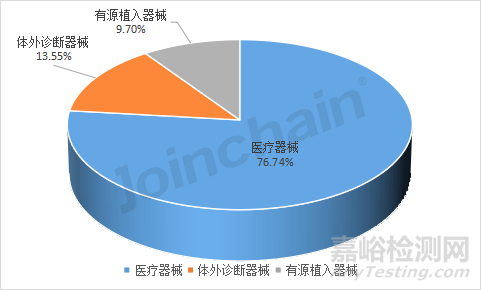
(1)體外診斷器械不良事件數(shù)增長明顯
澳大利亞將器械產(chǎn)品分為:醫(yī)療器械(I類�,Im類,Is類����,Ⅱ類,Ⅲ類)�、體外診斷器械(1類,2類�,3類,4類)和有源植入器械三類����。據(jù)MDCLOUD(醫(yī)械數(shù)據(jù)云)統(tǒng)計,2022年澳大利亞的醫(yī)療器械不良事件有3211起�,占76.74%;體外診斷器械不良事件共567起��,占13.55%;406起有源植入器械不良事件��,占9.70%��。對比2021年的不良事件����,2022年醫(yī)療器械和有源植入器械的事件數(shù)量占比分別減少了8.15%和0.25%,體外診斷器械的事件數(shù)量占比增加9.46%����。
圖23 2022年澳大利亞不同類別產(chǎn)品的不良事件數(shù)量占比
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
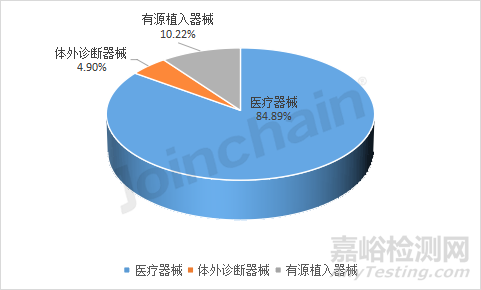
圖24 2021年澳大利亞不同類別產(chǎn)品的不良事件數(shù)量占比
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
注:2021年有682份不良事件報告無產(chǎn)品分類信息,不列入統(tǒng)計
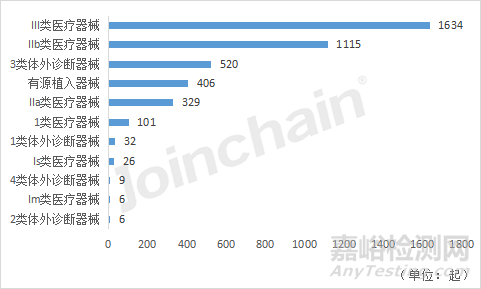
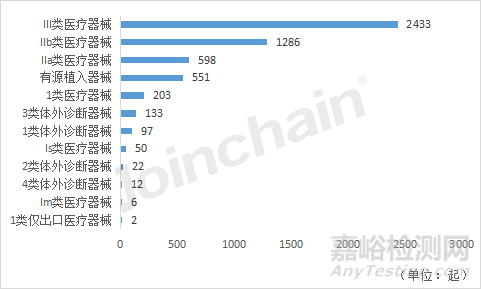
對三類器械的細分管理類別對應的不良事件數(shù)進行統(tǒng)計����,可以看到,無論是2021年和2022年�,Ⅲ類醫(yī)療器械的不良事件數(shù)量最高,其次是IIb類醫(yī)療器械��。值得注意的是�,相較2021年,2022年的Ⅲ類體外診斷器械不良事件數(shù)有明顯上升����,從2021年的133起增長到2022年的520起��。
圖25 2022年澳大利亞各產(chǎn)品類型的不良事件數(shù)量排名
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
注:有1648份不良事件報告無產(chǎn)品分類信息,不列入統(tǒng)計
圖26 2021年澳大利亞各產(chǎn)品類型的不良事件數(shù)量排名
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
注:有682份不良事件報告無產(chǎn)品分類信息����,不列入統(tǒng)計
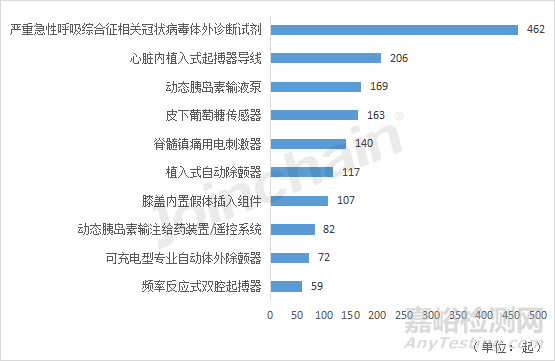
(2)2022年冠狀病毒診斷試劑不良事件激增
2022年,澳大利亞不良事件數(shù)排前三的產(chǎn)品類別分別為嚴重急性呼吸綜合征相關(guān)冠狀病毒體外診斷試劑(462起)�、心臟內(nèi)植入式起搏器導線(206起)、動態(tài)胰島素輸液泵(169起)�。而在2021年,嚴重急性呼吸綜合征相關(guān)冠狀病毒體外診斷試劑的不良事件僅有26起����,該產(chǎn)品的不良事件數(shù)在一年內(nèi)增長了16倍。
圖27 2022年澳大利亞不良事件數(shù)排名前十的產(chǎn)品類別
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
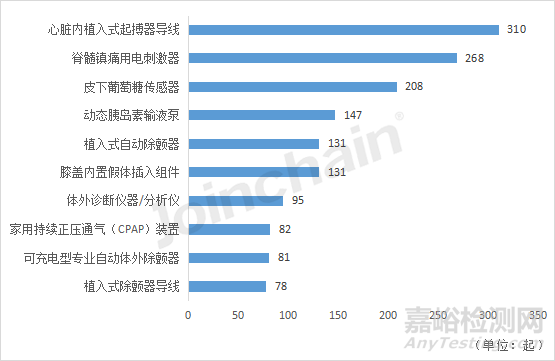
圖28 2021年澳大利亞不良事件數(shù)排名前十的產(chǎn)品類別
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
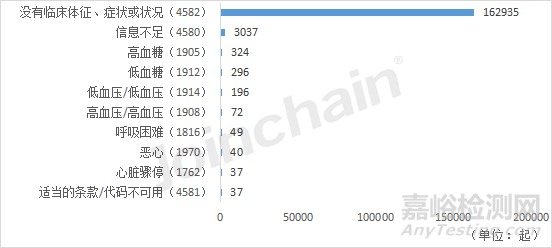
(3)冠狀病毒診斷試劑的高頻事件故障類型
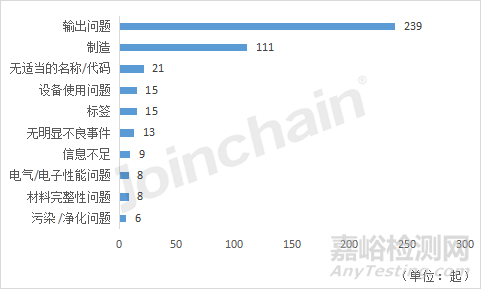
針對2022年不良事件數(shù)激增的嚴重急性呼吸綜合征相關(guān)冠狀病毒體外診斷試劑產(chǎn)品�,對其不良事件中的事件故障類型進行統(tǒng)計�,可以看到高頻的事件故障主要為:輸出問題(239起)��、制造(111起)��、無適當?shù)拿Q/代碼(21起)�、設備使用問題(15起)和標簽(15起)����。
圖29 嚴重急性呼吸綜合征相關(guān)冠狀病毒體外診斷試劑相關(guān)的前十大不良事件故障類型
數(shù)據(jù)來源:MDCLOUD(醫(yī)械數(shù)據(jù)云)
三、總結(jié)
1��、海外醫(yī)療器械不良事件應加強關(guān)注
2022年海外主要國家的醫(yī)療器械不良事件數(shù)據(jù)以美國��、澳大利亞兩國披露的數(shù)據(jù)為主,英國����、加拿大在2022年對醫(yī)療器械產(chǎn)品的不良事件報道大幅減少,且多為監(jiān)管機構(gòu)發(fā)出的產(chǎn)品使用警示報告�。得益于行業(yè)內(nèi)的制造商對不良事件的主動上報�,美國、澳大利亞的不良事件數(shù)據(jù)量相對較大��,字段內(nèi)容更規(guī)范�,數(shù)據(jù)可用度相對較高��,且數(shù)據(jù)量逐年增加����。針對特定產(chǎn)品�,結(jié)合產(chǎn)品的不良事件類型�、設備問題、患者問題等進行統(tǒng)計分析��,進而初步了解產(chǎn)品的安全性。國內(nèi)醫(yī)療器械行業(yè)應加強關(guān)注海外主要國家����,尤其是美、澳兩國的醫(yī)療器械不良事件����,對產(chǎn)品的安全性評估與研發(fā)改進均有幫助��。
2�、糖尿病治療與監(jiān)控產(chǎn)品需重點監(jiān)測
目前����,全球糖尿病人口已超3億,根據(jù)2020年美國全國糖尿病統(tǒng)計報告�,美國全國糖尿病患者共3420萬(包括2690萬確診患者和730萬未確診患者),占美國總?cè)丝诘?0.1%��。近兩年美國不良事件高發(fā)的產(chǎn)品類型多為糖尿病治療相關(guān)器械產(chǎn)品,可能與糖尿病人群增長相關(guān)����;澳大利亞的不良事件高發(fā)產(chǎn)品類型同樣也有胰島素泵�。據(jù)國家衛(wèi)計委報道,我國糖尿病人口在2016年已達1億�,作為糖尿病人口大國對糖尿病治療器械的使用量更為龐大�。對美國、澳大利亞的胰島素泵����、血糖監(jiān)控系統(tǒng)的不良事件進行持續(xù)監(jiān)測����,可為國內(nèi)糖尿病患者在使用同類產(chǎn)品時提供警示參考。
3�、海外高風險產(chǎn)品不良事件值得借鑒分析
對比澳大利亞2021年和2022年的不良事件數(shù)前十產(chǎn)品名單�,可以發(fā)現(xiàn)心臟內(nèi)植入式起搏器導線、動態(tài)胰島素輸液泵����、脊髓鎮(zhèn)痛用電刺激器這三類產(chǎn)品均在這兩年的前五產(chǎn)品名單之中。包括美國2021年和2022年不良事件數(shù)均為前三的牙種植體�、連續(xù)血糖監(jiān)控系統(tǒng)和輸液泵�。重點關(guān)注近兩年海外高風險產(chǎn)品的國內(nèi)同類產(chǎn)品的使用情況,通過對海外重點高風險產(chǎn)品的故障問題和對病人的傷害表現(xiàn)進行分析��,可在國內(nèi)同類產(chǎn)品發(fā)生類似不良事件時����,借鑒相關(guān)的事件處置與故障問題分析等內(nèi)容��。
附表:
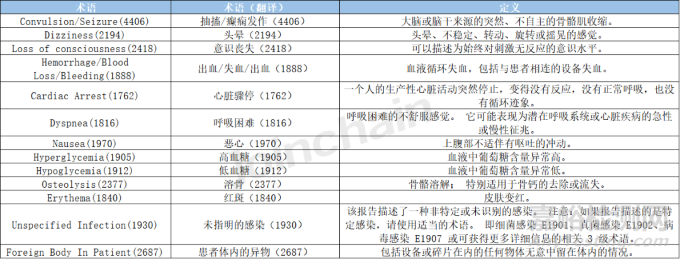
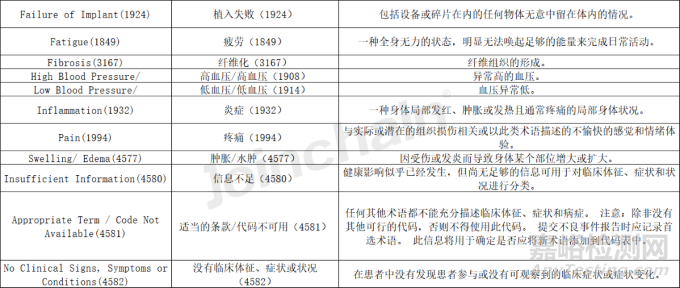
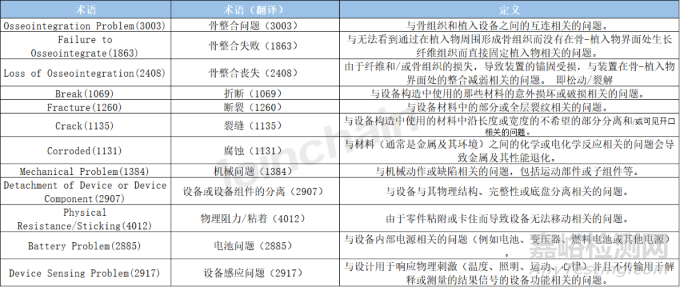
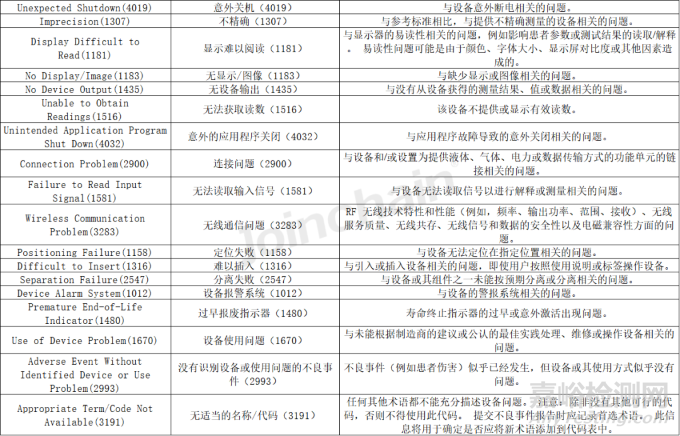
附表1 美國不良事件設備問題術(shù)語定義
來源:美國食品藥品管理局(FDA)官網(wǎng),翻譯僅供參考
附表2 美國不良事件患者問題術(shù)語定義