核醫(yī)療健康產(chǎn)業(yè)是立足于核工業(yè)、助力大健康的戰(zhàn)略性新興產(chǎn)業(yè)��,是促進(jìn)我國(guó)醫(yī)療衛(wèi)生事業(yè)高質(zhì)量發(fā)展的基礎(chǔ)產(chǎn)業(yè)之一����。核醫(yī)學(xué)在多種疾病的診療及預(yù)后判斷方面發(fā)揮著不可替代的作用;放射性藥物(放藥)是核醫(yī)學(xué)發(fā)展的基石�����,相應(yīng)體系化發(fā)展有助于加快放藥創(chuàng)新與應(yīng)用。
中國(guó)工程院趙憲庚院士研究團(tuán)隊(duì)在中國(guó)工程院院刊《中國(guó)工程科學(xué)》2022年第6期發(fā)表《我國(guó)放射性藥物創(chuàng)新體系發(fā)展戰(zhàn)略研究》一文����。文章在深入調(diào)研的基礎(chǔ)上,相對(duì)全面地掌握了放藥研制和應(yīng)用領(lǐng)域的發(fā)展態(tài)勢(shì)與格局����。在分析國(guó)外放藥發(fā)展現(xiàn)狀、技術(shù)水平及趨勢(shì)的基礎(chǔ)上����,總結(jié)了我國(guó)放藥發(fā)展的基本情況并辨識(shí)了面臨的迫切問(wèn)題;從技術(shù)研發(fā)體系��、技術(shù)監(jiān)管體系兩方面闡述了重點(diǎn)建設(shè)內(nèi)容��,提出了放藥靶點(diǎn)研究及靶向結(jié)構(gòu)開發(fā)��,新型放射性標(biāo)記��,放藥自動(dòng)化�����、智能化、規(guī)?���;煽刂苽洌潘庉椛鋭┝繖z測(cè)及評(píng)價(jià)��、放藥聯(lián)合診療等關(guān)鍵技術(shù)突破點(diǎn)����。文章建議,以臨床為導(dǎo)向鼓勵(lì)多學(xué)科交叉融合的創(chuàng)新發(fā)展����,加快放藥技術(shù)創(chuàng)新體系建設(shè),加強(qiáng)放藥研發(fā)專業(yè)化人才隊(duì)伍建設(shè)�����,以此促進(jìn)核醫(yī)學(xué)水平的整體提升��。
一����、前言
黨的二十大報(bào)告指出�����,人民健康是民族昌盛和國(guó)家強(qiáng)盛的重要標(biāo)志,要把保障人民健康放在優(yōu)先發(fā)展的戰(zhàn)略位置�����。核醫(yī)療健康產(chǎn)業(yè)是立足于核工業(yè)�����、助力大健康的戰(zhàn)略性新興產(chǎn)業(yè)����,是促進(jìn)我國(guó)醫(yī)療衛(wèi)生事業(yè)高質(zhì)量發(fā)展的基礎(chǔ)產(chǎn)業(yè)之一。利用放射性核素診斷�����、治療和研究疾病的核醫(yī)學(xué)��,更是核醫(yī)療產(chǎn)業(yè)的重要內(nèi)容��、醫(yī)學(xué)現(xiàn)代化的重要標(biāo)志����,在心血管疾病��、神經(jīng)退行性疾病����、尤其是惡性腫瘤等多種疾病的診斷�����、治療�����、預(yù)后判斷等方面發(fā)揮著不可替代的作用����。根據(jù)國(guó)家癌癥中心的統(tǒng)計(jì)數(shù)據(jù),我國(guó)2016年新增癌癥病例406.4萬(wàn)例�����,新增癌癥死亡人數(shù)約為241.35萬(wàn)人�����,發(fā)病和死亡人數(shù)逐年上升����;惡性腫瘤給社會(huì)和患者帶來(lái)的負(fù)擔(dān)日益嚴(yán)重。癌癥早發(fā)現(xiàn)早治療可明顯降低治療費(fèi)用�����,精準(zhǔn)治療對(duì)患者受益最大��。然而��,截至2019年年底�����,我國(guó)共有正電子顯像設(shè)備427臺(tái)�����、單光子顯像設(shè)備903臺(tái)�����、核醫(yī)學(xué)相關(guān)科室1148個(gè)�����,人均擁有量遠(yuǎn)低于國(guó)際先進(jìn)水平。以核醫(yī)學(xué)臨床診斷用藥比例最高的99mTc藥物為例����,2019年我國(guó)有251萬(wàn)人次開展顯像診斷,而美國(guó)約有1500萬(wàn)人次開展顯像診斷�����。國(guó)際上已規(guī)?���;瘧?yīng)用的多個(gè)靶向治療新藥目前在我國(guó)未進(jìn)入審評(píng)程序,僅在少數(shù)獲得IV類證的單位開展臨床應(yīng)用��。核醫(yī)學(xué)在惡性腫瘤領(lǐng)域診斷與治療的優(yōu)勢(shì)在我國(guó)有待充分發(fā)揮��。
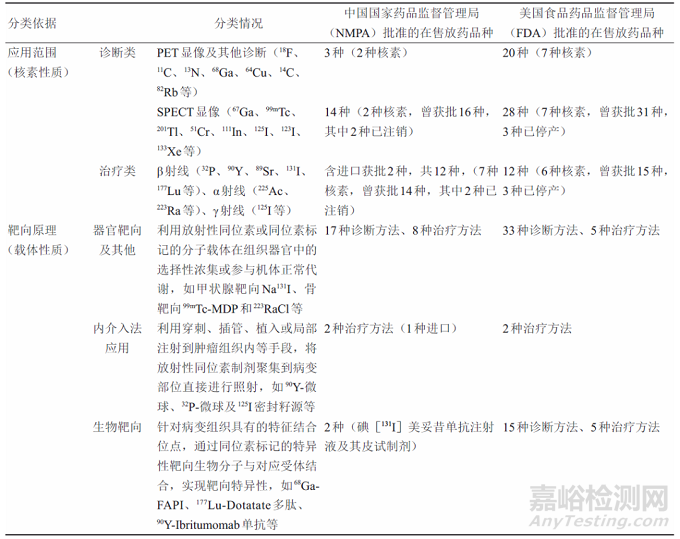
放射性藥物(簡(jiǎn)稱“放藥”)指含有醫(yī)用同位素制劑��、用于疾病診斷或治療的一類特殊藥品����,按用途分為診斷類和治療類(見表1),構(gòu)成了核醫(yī)學(xué)發(fā)展的基石�����。基于診斷類放藥的核醫(yī)學(xué)精準(zhǔn)分子診斷�����,利用示蹤技術(shù)����,在分子層面闡明病變組織的功能變化��、基因異常表達(dá)�����、生化代謝變化等����,具有靈敏度及分辨率高、快速��、準(zhǔn)確等優(yōu)點(diǎn)��,是目前幾乎所有醫(yī)學(xué)診斷技術(shù)中唯一能實(shí)現(xiàn)活體代謝過(guò)程功能顯像的技術(shù)�����,可實(shí)現(xiàn)疾病的早期診斷,可據(jù)此制定更有效的預(yù)防或治療方案��。
診斷類放藥根據(jù)其核素性質(zhì)����,分為兩類:可用于單光子顯像(SPECT)的放藥,主要以99mTc標(biāo)記藥物為主��;用于正電子顯像(PET)的放藥�����,主要以18F����、68Ga標(biāo)記藥物為主。
治療類放藥通過(guò)核素對(duì)病變組織進(jìn)行選擇性和靶向性的治療��,在肝癌�����、前列腺癌��、神經(jīng)內(nèi)分泌腫瘤等惡性腫瘤治療方面具有良好效果,為惡性腫瘤的精準(zhǔn)診治提供了革命性的手段��。此外��,根據(jù)放射性藥品不同的靶向原理����,還可以分為內(nèi)介入法應(yīng)用放藥��、生物靶向放藥和器官靶向放藥及其他放藥(見表1)�����。
2020年��,全球放射性藥品市場(chǎng)規(guī)模為59億美元�����,其中放射性診斷藥物的占比為90%�����;我國(guó)相應(yīng)市場(chǎng)規(guī)模約為44.56億元�����,在全球放藥市場(chǎng)中占比約為8%�����。目前��,我國(guó)放藥依賴進(jìn)口的局面并未打破����,患者用藥成本高昂��,如177Lu標(biāo)記多肽靶向特效藥單個(gè)療程費(fèi)用超過(guò)100萬(wàn)元�����。同時(shí),放藥的半衰期較短����,需要在較短時(shí)間內(nèi)配送到臨床才能保證有效性����。依賴進(jìn)口放藥存在較多的不確定性因素�����,患者穩(wěn)定用藥風(fēng)險(xiǎn)高����,在威脅患者健康��、增加了醫(yī)療資源消耗的同時(shí)�����,為社會(huì)帶來(lái)了沉重負(fù)擔(dān)����。然而,放藥體系化發(fā)展涉及核技術(shù)����、醫(yī)藥學(xué)科技術(shù)的交叉融合,技術(shù)復(fù)雜且極具挑戰(zhàn)性�����。
為提升我國(guó)放藥原始創(chuàng)新能力����,盡快建立和健全放藥研發(fā)體系����,加快自主創(chuàng)新放藥面世與應(yīng)用��,在中國(guó)工程院“國(guó)家核醫(yī)療健康產(chǎn)業(yè)發(fā)展戰(zhàn)略研究”咨詢項(xiàng)目的支持下��,本文圍繞放藥自主供應(yīng)體系化發(fā)展課題,開展國(guó)內(nèi)外放藥研發(fā)�����、轉(zhuǎn)化應(yīng)用�����、體系化發(fā)展模式的梳理和分析,進(jìn)而凝練適應(yīng)國(guó)情的放藥研發(fā)體系發(fā)展目標(biāo)與重點(diǎn)方向��,提出放藥體系化發(fā)展建議��,以期為放藥研發(fā)與應(yīng)用研究����、衛(wèi)生事業(yè)管理研究提供參考�����。
表1 放藥分類及獲批情況對(duì)比
二����、國(guó)外放射性藥物的發(fā)展現(xiàn)狀及趨勢(shì)
(一)放藥品種多樣��,創(chuàng)新藥物不斷面世
國(guó)外已獲批或在研的放藥核素種類較多����,藥物適應(yīng)癥范圍廣,近年來(lái)仍不斷有原研創(chuàng)新放藥獲批上市��。截至2022年3月底�����,經(jīng)美國(guó)FDA批準(zhǔn)上市的放藥有60種(涵蓋18種放射性同位素)�����。在99mTc�����、123I、67Ga和201Tl等核素標(biāo)記的單光子放射性診斷藥物中��,99mTc標(biāo)記藥物是臨床SPECT診斷用的主要藥物����。該類藥物可適用于骨、膽道系統(tǒng)�����、腎����、脾、肺、胃��、心肌等多種組織器官的顯像�����,如99mTc-亞甲基二膦酸鹽(99mTc-MDP)��、99mTc-焦磷酸鹽(99mTc-PYP)用于骨顯像�����,99mTc-亞錫依沙美肟(99mTc-HMPAO)��、99mTc-雙半胱乙酯(99mTc-ECD)用于腦灌注顯像����,99mTc-甲氧異腈(99mTc-MIBI)、99mTc-替曲膦(99mTc-tetrofosmin)用于心肌灌注顯像����,99mTc-聚合白蛋白(99mTc-MAA)用于肺灌注顯像��,99mTc-硫膠體(99mTc-sulfur colloid)用于肝顯像����,99mTc-巰替肽(99mTc-MAG3)、99mTc-噴替酸鹽(99mTc-penetettate)用于腎顯像�����,99mTc-紅細(xì)胞(99mTc-RBC)用于心血池顯像��,99mTc-tilmanocept用于前哨淋巴結(jié)顯像等。此外��,還包括腦顯像劑123I-鹽酸非他胺(123I-IMP)��、123I-苯甲酰胺(123I-IBZM)����,心肌顯像劑123I-β-甲基-p-碘苯基十五烷酸(123I-BMIPP)�����、123I-碘苯基十五酸(123I-IPPA)����,軟組織臟器的腫瘤顯像劑67Ga-枸櫞酸(67Ga-gallium citrate)��,神經(jīng)內(nèi)分泌瘤(NETs)顯像劑111In-奧曲肽注射液(111In-DTPA-pentetreotide)及最早的心肌灌注顯像劑201Tl-氯化鉈(201Tl-thallous chloride)等單光子藥物均已在臨床診斷中廣泛應(yīng)用����。
近幾年����,國(guó)外基于18F��、11C��、13N����、15O����、68Ga和64Cu等核素標(biāo)記的正電子放射性診斷藥物在臨床實(shí)踐中獲得廣泛應(yīng)用并不斷更新。除用于腫瘤診斷��、冠狀動(dòng)脈疾病與心室功能評(píng)估及其他糖代謝異常等的經(jīng)典PET診斷劑18F-氟脫氧葡萄糖(18F-FDG)外�����,還獲批上市了包括氟[18F]貝他吡(18F-florbetapir)、18F-他莫(18F-flutemetamol)及18F-比他班(18F-florbetaben)等多個(gè)用于阿爾茨海默病的診斷藥物��。2020年����,美國(guó)FDA還批準(zhǔn)了64Cu-Dotatate注射液上市��,豐富了NETs顯像劑可用的核素品種�����。隨著68Ge/68Ga發(fā)生器及相關(guān)靶向藥研發(fā)技術(shù)的日趨成熟與普及����,68Ga標(biāo)記藥物也相繼上市。2016年,F(xiàn)DA批準(zhǔn)了用于生長(zhǎng)抑素受體(SSTR)陽(yáng)性神經(jīng)內(nèi)分泌瘤的顯像劑68Ga-DOTA-TATE(商品名為Netspot)��,不久后同樣適應(yīng)癥的顯像藥物68Ga-DOTA-TOC先后在歐盟(2016年)及美國(guó)(2019年)獲批上市;2021年12月��、2022年3月又分別批準(zhǔn)了兩家公司的68Ga-PSMA-11用于前列腺特異性膜抗原陽(yáng)性的前列腺癌診斷�����。
基于治療核素131I、32P��、198Au、90Y��、89Sr����、186/188Re����、153Sm����、177Lu、223Ra�����、225Ac等研發(fā)的放射性治療藥物中��,碘[131I]化鈉口服溶液是用于甲狀腺癌等疾病治療的經(jīng)典藥物����。90Y-微球及90Y標(biāo)記的Ibritumomab單抗(Zevalin)都是較早獲批上市的;Zevalin是第一個(gè)獲批的靶向單抗治療藥物(2002年)��,主要用于非霍奇金淋巴瘤的治療��。α核素治療藥物的代表之一是2013年FDA獲批的氯化鐳[223Ra]注射液(223Ra-氯化鐳),用于治療有骨轉(zhuǎn)移的晚期去勢(shì)抵抗性前列腺癌(mCRPC)患者��。2017年和2018年歐洲藥品管理局(EMA)�����、FDA先后批準(zhǔn)了Lutathera(177Lu-Dotatate)用于治療胃腸胰神經(jīng)內(nèi)分泌腫瘤(GEP-NETs)��,成為首個(gè)獲批用于治療GEP-NETs的靶向放藥��。177Lu作為國(guó)際原子能機(jī)構(gòu)(IAEA)推薦的治療核素�����,在2022年3月又獲批上市了針對(duì)轉(zhuǎn)移性mCRPC的治療放藥177Lu-PSMA-617����,具有良好的臨床治療療效及耐受性。
國(guó)外正在開展臨床或臨床前研究的放藥種類與國(guó)內(nèi)相比�����,更加豐富����。僅美國(guó)國(guó)立衛(wèi)生研究院(NIH)分子數(shù)據(jù)庫(kù)中就有200多種單光子核素標(biāo)記及近500種正電子核素標(biāo)記的顯像藥物,覆蓋了64Cu�����、124I����、76Br和89Zr等較長(zhǎng)半衰期核素在內(nèi)的幾十種顯像核素。相關(guān)放藥不僅具有臨床診斷應(yīng)用前景����,還能用于研究單抗等代謝時(shí)間較長(zhǎng)的靶向藥物的體內(nèi)生物過(guò)程。針對(duì)不同適應(yīng)癥的臨床或臨床前在研放射性治療藥物也很多�����,如90Y-Clivatuzumab用于治療胰腺癌已進(jìn)入臨床實(shí)驗(yàn)��;177Lu-EDTMP作為可媲美89SrCl2或153Sm-EDTMP的藥物��,在價(jià)格和療效方面均具有優(yōu)勢(shì)�����,并且等劑量的177Lu骨髓抑制毒性較89Sr和153Sm低,因此�����,將有較好的社會(huì)和經(jīng)濟(jì)效益��。177Lu/90Y-pentixather CXCR4靶向放射療法有助于治療多發(fā)性骨髓瘤��,也是晚期多發(fā)性骨髓瘤很有前景的治療方法�����?����;?alpha;治療核素也有多個(gè)在研放藥����,如225Ac-Dotatate、225Ac-Lintuzumab單抗����、212Pb/212Bi-TCMC-曲妥珠單抗�����、212Pb/212Bi-DOTAMTATE等。
(二)科學(xué)前沿技術(shù)在放藥研發(fā)中的廣泛應(yīng)用
國(guó)外在放射性靶向治療新藥方面充分借鑒了普藥研發(fā)及其他科學(xué)前沿技術(shù)��,如抗體偶聯(lián)藥物(ADC)技術(shù)����、預(yù)靶向技術(shù)(PRIT)、高通量分子庫(kù)篩選技術(shù)等����,推動(dòng)了多種靶向藥物在惡性腫瘤診療領(lǐng)域的放射性新藥研發(fā)進(jìn)程。核素抗體偶聯(lián)藥物(RAC)與ADC的結(jié)構(gòu)非常類似����,由靶向抗體、連接子����、發(fā)揮效應(yīng)作用的核素(ADC中為毒素分子)等主要結(jié)構(gòu)組成。在開發(fā)RAC時(shí)��,用于核素標(biāo)記的配體修飾到靶向活性抗體上的比例�����,即藥物抗體偶聯(lián)比(DAR)同樣是影響靶向放藥的靶向活性、體內(nèi)代謝��、療效等決定藥物研發(fā)成功率的關(guān)鍵因素����。國(guó)外利用ADC研發(fā)采用的Thiomab技術(shù)、ThioBridge技術(shù)��、引入非天然氨基酸方法����、酶催化法等定點(diǎn)偶聯(lián)技術(shù),可得到DAR可控��、均一性高��、藥物活性及藥代動(dòng)力學(xué)均明顯提高的靶向放藥����。
在1960年提出的雙特異性抗體(簡(jiǎn)稱“雙抗”)成為當(dāng)前免疫靶向藥物研發(fā)的一個(gè)重要方向。雙抗擁有可發(fā)揮靶向結(jié)合��、介導(dǎo)結(jié)合作用的兩個(gè)不同的抗原結(jié)合位點(diǎn),能實(shí)現(xiàn)誘導(dǎo)免疫細(xì)胞靶向腫瘤��,體內(nèi)結(jié)合信號(hào)傳導(dǎo)配體或結(jié)合其他因子產(chǎn)生反應(yīng)等�����。雙抗技術(shù)在放藥領(lǐng)域被擴(kuò)展應(yīng)用形成了預(yù)靶向策略技術(shù)(PRIT)��,將抗體的靶向性能與小分子藥物優(yōu)良的藥代動(dòng)力學(xué)特性結(jié)合起來(lái)��,避免了傳統(tǒng)放射免疫治療(RIT)中核素直接標(biāo)記抗體導(dǎo)致的血液高毒性�����,降低了健康組織高劑量照射的風(fēng)險(xiǎn)����,實(shí)現(xiàn)低毒高效的目的����。經(jīng)過(guò)多年發(fā)展,PRIT還形成了親和素 ? 生物素(avidin-biotin)結(jié)合策略����,體內(nèi)正交反應(yīng)與脫氧核糖核酸(DNA)類似物策略等。其中,雙特異性抗體策略與體內(nèi)正交反應(yīng)策略已有多個(gè)臨床在研藥物����,如以111In/177Lu-IMP288為效應(yīng)結(jié)合子的抗人癌胚抗原相關(guān)的細(xì)胞黏附分子5(anti-CEACAM5)及抗半抗原(anti-hapten)雙抗。
此外����,國(guó)外越來(lái)越多地研究利用核醫(yī)學(xué)影像技術(shù)與輻射劑量學(xué),結(jié)合放射醫(yī)學(xué)��、腫瘤學(xué)�����、蛋白與基因組學(xué)��、分子生物學(xué)生命科學(xué)��、藥學(xué)等多學(xué)科前沿技術(shù)為放藥研發(fā)中的輻射生物效應(yīng)研究方向提供了更科學(xué)全面的解析手段��,相關(guān)研究成果又能在放藥作用機(jī)理����、療效評(píng)價(jià)、安全性及毒理評(píng)估分析����、臨床方案設(shè)計(jì)等放藥研發(fā)與應(yīng)用的關(guān)鍵參數(shù)研究中發(fā)揮重要作用��,進(jìn)一步加快了放藥的臨床轉(zhuǎn)化進(jìn)程��,提高研發(fā)成功率����?�;诨蚪M學(xué)及大數(shù)據(jù)分析等技術(shù)�����,能夠從分子水平上了解人體生長(zhǎng)����、發(fā)育����、正常生理活動(dòng)的本質(zhì)和基礎(chǔ),通過(guò)對(duì)健康人和病人組學(xué)大數(shù)據(jù)的比較��,找到各種疾病在分子水平的病因����,在尋找適用于放藥研發(fā)的新靶點(diǎn)��、新藥物分子等方面起到重要作用��。
(三)放藥研發(fā)形成體系化發(fā)展模式����,平臺(tái)鏈條完善
放藥創(chuàng)制是一個(gè)專業(yè)性強(qiáng)�����、涉及學(xué)科范圍廣��、基于數(shù)據(jù)密集型科學(xué)的研究過(guò)程��,參與主體包括研究機(jī)構(gòu)(或高校)�����、醫(yī)藥公司����、醫(yī)院等,需要依賴反應(yīng)堆�����、加速器等大型尖端裝置,投入大量的人力����、物力、資本����、時(shí)間等要素。國(guó)外擁有反應(yīng)堆和加速器的研究機(jī)構(gòu)與藥企�����、醫(yī)院在行業(yè)上下游進(jìn)行了“產(chǎn)學(xué)研用”的深度融合��,建立了成熟高效的放藥研發(fā)體系及應(yīng)用推廣模式�����。具備反應(yīng)堆或加速器核素自主化的國(guó)家��,圍繞核素資源建設(shè)了一批具備核醫(yī)藥創(chuàng)制����、核醫(yī)學(xué)臨床、療養(yǎng)康復(fù)等綜合功能的中心平臺(tái)����。在放藥創(chuàng)制過(guò)程中,反應(yīng)堆起到了核心樞紐作用��。以美國(guó)密蘇里大學(xué)研究反應(yīng)堆(MURR)為例�����,其核心任務(wù)之一是放射性同位素及藥物創(chuàng)制����,可以生產(chǎn)多種診療放射性同位素,并且還持續(xù)進(jìn)行166Ho��、186Re��、153Sm�����、198Au等核素研發(fā)�����,保障了藥物研發(fā)的核素資源。在放藥創(chuàng)制中��,MURR擁有專注于開發(fā)癌癥及其他慢性疾病靶向診療放藥的研究小組�����。在放藥創(chuàng)制后端��,MURR與其他國(guó)家實(shí)驗(yàn)室及醫(yī)藥公司合作����,已經(jīng)成功開發(fā)了3種經(jīng)FDA批準(zhǔn)的放藥。同時(shí)�����,MURR還建立了符合藥品生產(chǎn)質(zhì)量管理規(guī)范(GMP)的放射性同位素����、藥物生產(chǎn)基地及質(zhì)量體系��,在保障醫(yī)用同位素穩(wěn)定供應(yīng)����、防止供應(yīng)鏈斷裂等方面發(fā)揮了巨大作用��。
國(guó)外在放藥創(chuàng)制全產(chǎn)業(yè)鏈中�����,除了具有體系化的流程與產(chǎn)業(yè)轉(zhuǎn)化路徑外����,各階段的參與主體也具有較大優(yōu)勢(shì)��。一是依托眾多具備放射性操作能力的機(jī)構(gòu)����,國(guó)外的放藥基礎(chǔ)研究一直走在科學(xué)與技術(shù)前沿,層出不窮的研究成果為藥物發(fā)現(xiàn)����、臨床前研究等階段提供了堅(jiān)實(shí)的基礎(chǔ)。二是在臨床研究與產(chǎn)業(yè)化方面�����,國(guó)外具有眾多專業(yè)或綜合性的公司或機(jī)構(gòu)可提供專業(yè)化的����、強(qiáng)有力的支持�����,如占全球治療放藥市場(chǎng)份額42%的諾華(Novartis)集團(tuán)(瑞士)以及緊隨其后的拜耳(Bayer)集團(tuán)(德國(guó))�����;從事放藥經(jīng)營(yíng)的企業(yè)Curium Pharma以及主要從事放藥開發(fā)����、制造和商業(yè)化的Jubilant DraxImage Inc.等����;在醫(yī)療設(shè)備方面,有橫跨核醫(yī)學(xué)醫(yī)療設(shè)備����、藥物兩大領(lǐng)域的通用電氣公司醫(yī)療集團(tuán)(GE Healthcare)、以核醫(yī)學(xué)成像為核心業(yè)務(wù)的億比亞公司(IBA Molecular)等��;在流通領(lǐng)域����,有目前運(yùn)營(yíng)著全美最大的放藥生產(chǎn)�����、銷售網(wǎng)絡(luò)的卡地納健康(Cardinal Health)集團(tuán)等。三是在應(yīng)用端��,國(guó)外具有較高的核醫(yī)學(xué)醫(yī)療水平及放藥臨床應(yīng)用普及率�����,進(jìn)一步推動(dòng)放藥創(chuàng)制形成了良性循環(huán)����。總體而言�����,國(guó)外放藥體系化發(fā)展模式為放藥創(chuàng)制提供了良好的產(chǎn)業(yè)化路徑����、形成了結(jié)構(gòu)合理且創(chuàng)新能力強(qiáng)的研究團(tuán)隊(duì),取得的成果顯著推動(dòng)了醫(yī)療水平的改善以及科技����、經(jīng)濟(jì)水平的提高。
三、我國(guó)放射性藥物的發(fā)展現(xiàn)狀與趨勢(shì)
2021年�����,國(guó)家原子能機(jī)構(gòu)聯(lián)合多個(gè)部門正式發(fā)布了核技術(shù)在醫(yī)藥領(lǐng)域的綱領(lǐng)性文件《醫(yī)用同位素中長(zhǎng)期發(fā)展規(guī)劃(2021—2035年)》����。這表明,我國(guó)醫(yī)用核素高度依賴進(jìn)口的問(wèn)題已受到國(guó)家重視�����,我國(guó)核素自主化研制進(jìn)入了良性發(fā)展階段��,131I��、177Lu����、89Sr等多種核素已實(shí)現(xiàn)自主供給。自此�����,我國(guó)放藥研發(fā)逐步進(jìn)入發(fā)展機(jī)遇期�����,但研發(fā)與應(yīng)用進(jìn)程較為緩慢,與國(guó)際先進(jìn)差距明顯�����。截至2022年3月底�����,NMPA已批準(zhǔn)的放藥有30種��,其中有6種藥物已進(jìn)行了藥品批準(zhǔn)文號(hào)注銷(退出市場(chǎng))����,即目前僅有24種已上市的放藥��,包括14種診斷藥物和10種治療藥物(含進(jìn)口藥物2種)�����;近10余年�����,沒有原研創(chuàng)新藥獲批上市。本文通過(guò)文獻(xiàn)調(diào)研及實(shí)地走訪多家國(guó)內(nèi)核醫(yī)療行業(yè)相關(guān)企業(yè)��、高校����、研究院所及醫(yī)院,邀請(qǐng)行業(yè)專家開展咨詢研討交流會(huì)等方式�����,進(jìn)一步分析了我國(guó)放藥發(fā)展現(xiàn)狀����,并通過(guò)對(duì)比國(guó)內(nèi)外差距梳理了我國(guó)放藥未來(lái)發(fā)展的趨勢(shì)。
(一)放藥研發(fā)進(jìn)入快速發(fā)展期�����,臨床用放藥品種少�����,缺乏原創(chuàng)新藥
在診斷方面����,國(guó)內(nèi)應(yīng)用最廣泛的放藥是18F-FDG�����、99mTc-MDP等����;一部分診斷類放藥雖然未獲批����,但依托放射性藥品使用許可證(四類)已在醫(yī)療機(jī)構(gòu)內(nèi)部使用�����,如11C-腦多巴胺轉(zhuǎn)運(yùn)體(11C-CFT)�����、18F-雌激素類似物(18F-FES)�����、68Ga-成纖維細(xì)胞活化蛋白特異性酶抑制劑(68Ga-FAPI)����、68Ga-PSMA-11��、68Ga-DOTA-TOC和68Ga-DOTA-TATE等����;還有部分藥物已進(jìn)入臨床研究�����,如肝臟顯像劑99mTc-GSA(注射用亞錫半乳糖酰人血清白蛋白二亞乙基三胺五乙酸鹽)�����,前哨淋巴結(jié)顯像99mTc-rituxumab��,腫瘤顯像劑99mTc-RGD和99mTc-HYNIC-PSMA����,血池、淋巴及腫瘤顯像劑68Ga-DOTA-Evans blue等�����。在治療方面��,我國(guó)臨床批準(zhǔn)的治療用放藥較少����,臨床可用的有碘[131I]化鈉口服溶液�����、89Sr-氯化鍶��、125I粒子�����、90Y-樹脂微球��、223Ra-氯化鐳等。碘[131I]腫瘤細(xì)胞核嵌合單克隆抗體注射液(131I-chTNT)可用于放化療不能控制或復(fù)發(fā)的中晚期肺癌患者����,但該藥物已經(jīng)注銷藥品批準(zhǔn)文號(hào)并退市。131I標(biāo)記的單抗美妥昔HAb18F(ab’)2用于不能手術(shù)切除或者術(shù)后復(fù)發(fā)的原發(fā)性肝癌��。
我國(guó)著力布局放藥研發(fā)與進(jìn)口��,放藥發(fā)展進(jìn)入快速上升期�����。近年來(lái),我國(guó)不斷有進(jìn)口放藥獲批�����,如223Ra-氯化鐳�����、90Y-樹脂微球����。醫(yī)藥企業(yè)、高校����、研究院所等加強(qiáng)聯(lián)動(dòng),積極開展放藥研發(fā)與轉(zhuǎn)化應(yīng)用����,如68Ga-PSMA-11、177Lu-Dotatate�����、177Lu-PSMA-617�����、68Ga-PD-L1抗體、188Re-HEDP等多個(gè)放藥啟動(dòng)臨床申請(qǐng)或臨床研究����。整體而言,我國(guó)臨床應(yīng)用的放藥多為仿制藥�����,臨床在研放藥以診斷藥物為主��,治療放藥品種數(shù)量少����,適應(yīng)癥單一且具有自主知識(shí)產(chǎn)權(quán)的放藥甚少。雖然我國(guó)放藥目前仍處于仿制�����、創(chuàng)制的結(jié)合階段�����,但臨床前研究的百花齊放也為放藥的體系化發(fā)展打下了堅(jiān)實(shí)基礎(chǔ)��。
(二)放藥研發(fā)已有較好技術(shù)支撐基礎(chǔ)�����,但前沿技術(shù)應(yīng)用較少����,基礎(chǔ)研究水平不高
隨著分子生物學(xué)、免疫學(xué)等學(xué)科的發(fā)展��,國(guó)內(nèi)在普藥研發(fā)領(lǐng)域發(fā)展迅速����,尤其是在靶向治療領(lǐng)域掌握了相應(yīng)的生物技術(shù)。2020年以來(lái)�����,我國(guó)已經(jīng)先后上市了恩美曲妥珠單抗(商品名為“赫賽萊”)����、Seagen/ 武田的維布妥昔單抗(商品名為“安適利”)、注射用維迪西妥單抗(商品名為“愛地希”)等抗體偶聯(lián)藥物����。不同于國(guó)外將多個(gè)新技術(shù)��、新策略大量應(yīng)用于放射性靶向新藥研發(fā)�����,我國(guó)在將前沿技術(shù)應(yīng)用于放藥時(shí)較為謹(jǐn)慎��,放藥研發(fā)依然側(cè)重仿制藥����,自主研發(fā)的放藥多用于基礎(chǔ)研究�����,原始創(chuàng)新的治療放藥研發(fā)偏少��。
將預(yù)靶向策略等新設(shè)計(jì)應(yīng)用到放藥中��,涉及復(fù)雜的研究體系及更多的關(guān)鍵影響因素��,需要全面認(rèn)識(shí)其作用機(jī)制與科學(xué)規(guī)律����,我國(guó)在此領(lǐng)域雖然起步晚,但已顯現(xiàn)了部分基礎(chǔ)研究成果����。例如,利用體內(nèi)正交反應(yīng)策略��,結(jié)合硼氨酸與靶向蛋白載體實(shí)現(xiàn)體內(nèi)可控釋放的雙靶向系統(tǒng)�����,并用核醫(yī)學(xué)影像技術(shù)揭示了細(xì)胞焦亡的免疫過(guò)程��?�?紤]到預(yù)靶向策略可以有效解決放藥輻射損傷等主要副作用這一瓶頸問(wèn)題����,該類技術(shù)方法在放藥研發(fā)中具有較大的應(yīng)用轉(zhuǎn)化前景。
我國(guó)放藥研發(fā)工作還未充分利用大數(shù)據(jù)等新技術(shù)來(lái)支撐適宜靶點(diǎn)的探索及龐大數(shù)據(jù)庫(kù)的分析等工作�����,對(duì)放藥用于臨床中涉及的劑量推算����、輻射生物效應(yīng)等方面的科學(xué)認(rèn)識(shí)不全面��,多數(shù)數(shù)據(jù)來(lái)源于外照射的放射治療��,缺乏體系化的科學(xué)指導(dǎo)�����。這在一定程度上制約了放藥新藥的多元化開發(fā)及臨床前/臨床研究����,放藥研發(fā)水平難以滿足國(guó)內(nèi)日益增長(zhǎng)的臨床治療需求��。
(三)放藥研發(fā)體系已具備全鏈條各環(huán)節(jié)要素�����,但尚未形成體系化發(fā)展模式
我國(guó)在放藥研發(fā)領(lǐng)域起步較早����,但由于研發(fā)不連貫,目前放藥研發(fā)技術(shù)整體處于落后局面�����。從放藥體系化發(fā)展的全鏈條來(lái)看�����,我國(guó)已經(jīng)初步具備各環(huán)節(jié)要素��,在部分具備核素自主化資源的地區(qū)也逐步形成了相似的全鏈條模式平臺(tái)��,但仍未形成良好的體系化發(fā)展模式�����,具有小�����、弱�����、散的特點(diǎn)����,放藥研發(fā)體系化發(fā)展模式仍需進(jìn)一步完善。
在放藥創(chuàng)制的前端����,近年來(lái)隨著關(guān)注度的提升��,北京師范大學(xué)����、蘇州大學(xué)����、廈門大學(xué)、四川大學(xué)����、北京大學(xué)、中國(guó)科學(xué)院上海藥物研究所等在放藥研發(fā)領(lǐng)域投入更多資源�����,但受限于核素來(lái)源及研究硬件條件限制�����,創(chuàng)新藥物研究更多圍繞18F��、68Ga�����、99mTc等加速器或發(fā)生器可獲取核素的診斷藥物。例如����,北京大學(xué)主研的99mTc-3PRGD2多肽獲批1類化學(xué)藥品臨床試驗(yàn)批件,至今已完成III期臨床試驗(yàn)����;北京師范大學(xué)自主研發(fā)的99mTc標(biāo)記葡萄糖類衍生物(99mTc-CNDG)能有效診斷肺癌�����、胰腺癌等多種腫瘤����,已經(jīng)進(jìn)入1類新藥申報(bào)階段。相關(guān)進(jìn)展表明����,我國(guó)診斷類放藥的自主化研制具備一定的原創(chuàng)競(jìng)爭(zhēng)力,但大多數(shù)研究尤其是治療類放藥仍止步于基礎(chǔ)研究����,并未推向應(yīng)用。然而����,臨床上對(duì)放射性治療藥物的需求越發(fā)明顯��,由于核素來(lái)源受限��,專注開展此類放藥基礎(chǔ)研究的團(tuán)隊(duì)也較少��,科研原創(chuàng)水平不高��。中國(guó)工程物理研究院依托中國(guó)綿陽(yáng)研究堆的核素生產(chǎn)能力��,開展了治療類放藥的仿制工作和原創(chuàng)研究�����,除已推向市場(chǎng)并臨床應(yīng)用的碘[131I]化鈉口服溶液外�����,其他藥物還尚未進(jìn)行臨床應(yīng)用�����。在放藥創(chuàng)制的后端�����,國(guó)內(nèi)外藥企紛紛部署放藥創(chuàng)制����,如國(guó)外藥企Novartis集團(tuán)以及Bayer集團(tuán),國(guó)內(nèi)藥企原子高科股份有限公司��、煙臺(tái)東誠(chéng)藥業(yè)集團(tuán)股份有限公司����、江蘇華益科技有限公司����、天津賽德生物制藥有限公司、北京先通國(guó)際醫(yī)藥科技股份有限公司等��。但我國(guó)相關(guān)企業(yè)多注重產(chǎn)品開發(fā)的時(shí)效性與經(jīng)濟(jì)性��,優(yōu)先選擇對(duì)國(guó)外已有藥物進(jìn)行仿制或采取合同加工外包(CMO)模式為國(guó)外藥企進(jìn)行代工生產(chǎn)�����。在臨床應(yīng)用端��,我國(guó)雖然已經(jīng)建立有兼顧教學(xué)��、診斷、治療和科研的核醫(yī)學(xué)科室�����,但相關(guān)醫(yī)院的設(shè)備����、技術(shù)、管理水平參差不齊��,限制了放藥創(chuàng)制體系的良性發(fā)展�����。
近幾年來(lái)��,在國(guó)家政策支撐及戰(zhàn)略規(guī)劃的引導(dǎo)下��,我國(guó)核醫(yī)學(xué)行業(yè)是相關(guān)機(jī)構(gòu)����、企業(yè)在“產(chǎn)學(xué)研用”融合發(fā)展上進(jìn)行了有益的嘗試和探索。例如����,中國(guó)工程物理研究院獲批成立了國(guó)家原子能機(jī)構(gòu)核技術(shù)(放射性同位素及藥物)研發(fā)中心����,并與相關(guān)企業(yè)合作開展了治療用放藥的聯(lián)合項(xiàng)目�����,逐步形成了集“產(chǎn)學(xué)研用”一體的放藥綜合研發(fā)平臺(tái)��;煙臺(tái)東誠(chéng)藥業(yè)集團(tuán)股份有限公司與中國(guó)科學(xué)院近代物理研究所進(jìn)行戰(zhàn)略合作��,在醫(yī)用回旋加速器��、新型核素�����、相關(guān)核藥的研發(fā)等領(lǐng)域開展合作�����;南京市第一醫(yī)院基于長(zhǎng)期的核醫(yī)學(xué)臨床診療經(jīng)驗(yàn)和開創(chuàng)性的治療工作����,設(shè)立了區(qū)域性核醫(yī)學(xué)中心,逐步發(fā)展藥物制備與研發(fā)能力�����。西南醫(yī)科大學(xué)附屬醫(yī)院聯(lián)合中國(guó)工程物理研究院�����、四川大學(xué)原子核科學(xué)技術(shù)研究所等�����,開展了177Lu-Dotatate����、177Lu-PSMA、225Ac-PSMA等臨床治療研究����,是我國(guó)首個(gè)開展α核素臨床治療的機(jī)構(gòu)?�?傮w上��,我國(guó)放藥合作平臺(tái)�����、機(jī)制及研發(fā)模式還處于萌芽階段,缺乏標(biāo)志性產(chǎn)品的面世����,專業(yè)研發(fā)團(tuán)隊(duì)組成較為單一,已有平臺(tái)未發(fā)揮作用優(yōu)勢(shì)��,力量仍較為薄弱�����。
整體來(lái)看�����,我國(guó)放藥發(fā)展仍存在自主化核素品種少�����、新興核素缺乏研發(fā)經(jīng)驗(yàn)����、生物靶向藥物開發(fā)技術(shù)未在放藥領(lǐng)域得到發(fā)揮�����、放藥規(guī)模化生產(chǎn)制備缺乏規(guī)范性等瓶頸問(wèn)題��,我國(guó)在獲批放藥的核素類型及適用范圍上均與國(guó)外市場(chǎng)存在顯著差距��。但從國(guó)內(nèi)已經(jīng)啟動(dòng)臨床研究或在研的創(chuàng)新放藥來(lái)看����,我國(guó)核醫(yī)療正在從放射性仿制藥、單一用藥研發(fā)的角度轉(zhuǎn)型為以臨床需求為導(dǎo)向的放射性創(chuàng)新藥開發(fā)��。自主創(chuàng)新才能真正實(shí)現(xiàn)我國(guó)放藥的體系化發(fā)展��,未來(lái)需要從更多新興核素的開發(fā)與應(yīng)用����、放藥靶點(diǎn)與靶向載體的設(shè)計(jì)創(chuàng)新、放藥可控��、智能制備技術(shù)突破����、放藥臨床應(yīng)用及評(píng)價(jià)技術(shù)完善等方面全面加速提升。
四��、我國(guó)放射性藥物發(fā)展面臨的挑戰(zhàn)
(一)放藥基礎(chǔ)研究薄弱,原始創(chuàng)新能力不足
放藥研發(fā)涉及多學(xué)科合作����、多單位協(xié)同,是高門檻��、高投入��、高風(fēng)險(xiǎn)的技術(shù)領(lǐng)域�����。長(zhǎng)期以來(lái)�����,我國(guó)對(duì)放藥研發(fā)基礎(chǔ)研究的投入有限�����,缺乏穩(wěn)定支持��,基礎(chǔ)研究薄弱��,制約了創(chuàng)新藥的發(fā)展��。同時(shí)����,藥物設(shè)計(jì)仍停留于經(jīng)驗(yàn)與以往的開發(fā)基礎(chǔ),而生物創(chuàng)新藥領(lǐng)域已大量采用的定點(diǎn)偶聯(lián)技術(shù)�����、高通量篩選��、基因大數(shù)據(jù)等新興科學(xué)技術(shù)還未在該領(lǐng)域得到普遍應(yīng)用��。放藥研發(fā)大多仍處于“跟隨”階段����,缺乏針對(duì)新靶點(diǎn)、新作用機(jī)制的突破性首創(chuàng)新藥��。
(二)發(fā)展模式單一����,難以滿足臨床實(shí)際需求
放藥研發(fā)與轉(zhuǎn)化平臺(tái)不完善,缺乏“產(chǎn)學(xué)研用”一體化創(chuàng)新體系��。學(xué)科協(xié)作薄弱��,藥企、科研院所和臨床核醫(yī)學(xué)結(jié)合程度不高����,核醫(yī)學(xué)與專業(yè)臨床需求缺乏深入銜接;目標(biāo)導(dǎo)向及臨床應(yīng)用反饋不及時(shí)��,難以形成具有科學(xué)指導(dǎo)意義的體系化知識(shí)積累��,尤其是在靶向治療藥物領(lǐng)域�����,對(duì)輻射及生物效應(yīng)機(jī)制等認(rèn)識(shí)不足�����。臨床專業(yè)需求難以轉(zhuǎn)化為放藥研發(fā)需求�����,導(dǎo)致研發(fā)水平提升不足����,科研成果轉(zhuǎn)化較慢。
(三)專業(yè)化人才隊(duì)伍建設(shè)不足限制了放藥研發(fā)與管理水平提升
放藥研發(fā)涉及放射化學(xué)、分子生物學(xué)��、腫瘤學(xué)����、藥學(xué)����、核醫(yī)學(xué)、各種臨床醫(yī)學(xué)等多個(gè)學(xué)科�����,臨床轉(zhuǎn)化還需要核醫(yī)學(xué)物理師和化學(xué)師等行業(yè)人才�����。優(yōu)秀復(fù)合型人才的缺乏制約了放藥研發(fā)進(jìn)程����。一方面,科研院校專業(yè)課程的設(shè)計(jì)與放藥研發(fā)生產(chǎn)過(guò)程相脫節(jié)����,課堂教學(xué)多以書本為主,知識(shí)更新較慢;另一方面�����,醫(yī)院和企業(yè)參與人才培養(yǎng)的積極性不高��,缺乏足夠的創(chuàng)新人才培養(yǎng)基地�����。同時(shí)�����,醫(yī)院核醫(yī)學(xué)科醫(yī)師隊(duì)伍薄弱��,導(dǎo)致放藥臨床需求牽引力不強(qiáng)����,制約了放藥研制的高質(zhì)量發(fā)展。
五��、我國(guó)放射性藥物體系化發(fā)展目標(biāo)��、重點(diǎn)方向與關(guān)鍵技術(shù)
(一)發(fā)展目標(biāo)
面向2025年:實(shí)現(xiàn)部分關(guān)鍵醫(yī)用同位素的自主化制備��,啟動(dòng)多品種的仿制及原創(chuàng)放藥研發(fā)項(xiàng)目,已開發(fā)的放藥實(shí)現(xiàn)臨床應(yīng)用自主化��,初步形成具有示范作用的放藥研發(fā)與轉(zhuǎn)化的技術(shù)創(chuàng)新中心或核醫(yī)療綜合體��。
面向2035年:全面實(shí)現(xiàn)放藥所需主要醫(yī)用同位素的自主化制備��,實(shí)現(xiàn)已有多品種放藥的臨床應(yīng)用自主化��,構(gòu)建示范性放藥研發(fā)與轉(zhuǎn)化技術(shù)創(chuàng)新中心或核醫(yī)療綜合體�����。
面向2050年:實(shí)現(xiàn)原研創(chuàng)新放藥成果應(yīng)用及自主化����,放藥創(chuàng)制達(dá)到國(guó)外同等水平��;放藥研發(fā)與轉(zhuǎn)化的技術(shù)創(chuàng)新中心或核醫(yī)療綜合體等平臺(tái)運(yùn)行成熟��,顯著支撐我國(guó)放藥發(fā)展�����,形成完善的放藥相關(guān)監(jiān)管機(jī)制����。
(二)重點(diǎn)方向
1. 放藥技術(shù)研發(fā)體系
放藥技術(shù)研發(fā)體系建設(shè)在瞄準(zhǔn)臨床��、高發(fā)病率�����、高致死率及無(wú)藥可用疾病的潛在需求��,構(gòu)建多種治療核素為基石����、生物藥前沿技術(shù)為支撐的多元化新藥研發(fā)技術(shù)創(chuàng)新體系��。在分子影像�����、診療一體化����、放射性核素靶向治療等方面開展從基礎(chǔ)研究到應(yīng)用、研發(fā)到轉(zhuǎn)化的一系列全鏈條研發(fā)��。重視分子影像放射性探針和精準(zhǔn)靶向治療藥物在腫瘤��、心血管、神經(jīng)系統(tǒng)疾病的診斷����、療效評(píng)價(jià)及指導(dǎo)治療方面的研究。
針對(duì)國(guó)外已上市或臨床結(jié)果優(yōu)異的藥物����,開展仿制藥研制轉(zhuǎn)化,如123I/131I�����、68Ga�����、177Lu等既有核素來(lái)源保障又已開發(fā)出能在分化型甲狀腺癌����、嗜鉻細(xì)胞瘤�����、神經(jīng)內(nèi)分泌腫瘤��、前列腺癌等疾病的診療一體化臨床應(yīng)用中發(fā)揮良好作用的藥物,積極推動(dòng)仿制藥在國(guó)內(nèi)上市��;加快更多經(jīng)典藥物如治療轉(zhuǎn)移性骨腫瘤的89Sr-氯化鍶��、223Ra-氯化鐳����、90Y-玻璃微球等的自主化供給。針對(duì)臨床亟需的藥物�����,開展放射性靶向創(chuàng)新藥物研發(fā)�����,引入并優(yōu)化放射化學(xué)�����、分子生物學(xué)�����、藥學(xué)��、免疫學(xué)、腫瘤學(xué)��、核醫(yī)學(xué)��、臨床醫(yī)學(xué)等交叉領(lǐng)域的新思路與新技術(shù)����,重點(diǎn)在放藥適宜靶點(diǎn)發(fā)現(xiàn)與前藥設(shè)計(jì)、新標(biāo)記方法開發(fā)��、新診療策略設(shè)計(jì)與應(yīng)用��、構(gòu)效關(guān)系與協(xié)同效應(yīng)科學(xué)規(guī)律研究及新機(jī)制闡述等方向��,在定點(diǎn)標(biāo)記技術(shù)��、規(guī)?����;c自動(dòng)化制備技術(shù)����、藥品質(zhì)控技術(shù)等方面突破放藥創(chuàng)新發(fā)展必須解決的關(guān)鍵技術(shù)瓶頸問(wèn)題��,提高放藥整體創(chuàng)新水平。
積極構(gòu)建形成多方合作的綜合研發(fā)與轉(zhuǎn)化平臺(tái)��,為臨床用藥多元化發(fā)展打下基礎(chǔ)��。同時(shí)為了防止源頭“卡脖子”情況的發(fā)生��,保障放藥醫(yī)用核素的資源供給��,提前布局規(guī)劃反應(yīng)堆與加速器建設(shè)��,形成資源協(xié)調(diào)機(jī)制也是建設(shè)完善的放藥研發(fā)體系不可或缺的一環(huán)����,助力加快放射性新藥轉(zhuǎn)化應(yīng)用的進(jìn)程。
2. 放藥技術(shù)監(jiān)管體系
放藥技術(shù)監(jiān)管體系主要包括放藥評(píng)審和放藥相關(guān)制度管理��。尤其是針對(duì)臨床應(yīng)用�����、生產(chǎn)規(guī)范等制度的優(yōu)化完善��,需充分考慮放藥特殊性����,推進(jìn)和加快放藥研發(fā)到轉(zhuǎn)化應(yīng)用的進(jìn)程��,從科學(xué)規(guī)律��、科學(xué)原理����、科學(xué)技術(shù)可行性上進(jìn)一步優(yōu)化與完善放藥研發(fā)和評(píng)價(jià)技術(shù)導(dǎo)則及技術(shù)評(píng)審制度��、臨床試驗(yàn)與應(yīng)用規(guī)范����、放藥生產(chǎn)質(zhì)量與運(yùn)輸規(guī)范等制度體系。通過(guò)政策優(yōu)化�����,加快實(shí)現(xiàn)我國(guó)多個(gè)放藥的評(píng)審上市�����,滿足臨床應(yīng)用需求����,服務(wù)國(guó)家“健康中國(guó)”發(fā)展戰(zhàn)略�����。進(jìn)一步加強(qiáng)放藥的推廣應(yīng)用,形成示范效應(yīng)��,帶動(dòng)形成一批國(guó)際領(lǐng)先的診斷與治療放射性創(chuàng)新藥物��,形成放藥研發(fā)體系可持續(xù)發(fā)展的良性循環(huán)����,滿足人民健康日益增長(zhǎng)的需要。
(三)關(guān)鍵技術(shù)
1. 放藥靶點(diǎn)研究及靶向結(jié)構(gòu)開發(fā)技術(shù)
放藥對(duì)靶向效率�����、識(shí)別特異性�����、靶向結(jié)合穩(wěn)定性的要求更高��,并且靶向載體的自身藥代性質(zhì)對(duì)放藥診療效果影響顯著����。針對(duì)放藥應(yīng)用的需求特點(diǎn),借鑒已有靶點(diǎn)及前沿生物技術(shù),瞄準(zhǔn)高危高發(fā)臨床適應(yīng)癥����,開拓放藥診療適用的靶點(diǎn)。同時(shí)�����,開發(fā)適用于放射性靶向藥物機(jī)理研究的技術(shù)方法����,完成放藥靶向機(jī)理研究,有效指導(dǎo)靶向放藥的結(jié)構(gòu)設(shè)計(jì)����,支撐放藥創(chuàng)制的自主化發(fā)展。
2. 放射性標(biāo)記創(chuàng)新技術(shù)
靶向放藥在核素選擇上呈現(xiàn)多元化��,新興核素212Pb��、212Bi�����、225Ac����、211At等均顯現(xiàn)廣泛的應(yīng)用前景。圍繞新興核素�����,設(shè)計(jì)和開發(fā)更穩(wěn)定的標(biāo)記配體�����,建立更高效�����、安全可控的靶向放藥標(biāo)記技術(shù)對(duì)新藥的研發(fā)至關(guān)重要��。借鑒二硫鍵還原����、氨基酸插入或蛋白構(gòu)象選擇等定點(diǎn)標(biāo)記技術(shù),開發(fā)放射性標(biāo)記藥物�����,有選擇性地將核素定位修飾到遠(yuǎn)離靶向活性中心的位點(diǎn)��,降低對(duì)靶向結(jié)構(gòu)的生物活性影響。因此����,有必要研究標(biāo)記技術(shù)對(duì)靶向放藥的各項(xiàng)參數(shù)的影響,開發(fā)適用于放藥特點(diǎn)的創(chuàng)新標(biāo)記分子與技術(shù)����。
3. 放藥自動(dòng)化、智能化��、規(guī)?����;煽刂苽浼夹g(shù)
現(xiàn)有放藥制備技術(shù)多為人工或半自動(dòng)操作模式��,自動(dòng)化水平低�����,少數(shù)加速器藥物或177Lu/68Ga靶向多肽藥物利用模塊化組件實(shí)現(xiàn)自動(dòng)一體化合成��,存在規(guī)模較小��、缺乏數(shù)字化跟蹤溯源等問(wèn)題�����,難以滿足大規(guī)模臨床應(yīng)用需求。有必要針對(duì)上述問(wèn)題�����,開發(fā)對(duì)應(yīng)的技術(shù)系統(tǒng)與生產(chǎn)裝置��。放藥相關(guān)制備技術(shù)的突破有利于加速放藥的臨床應(yīng)用�����,推進(jìn)我國(guó)核醫(yī)療的現(xiàn)代化發(fā)展����。
4. 放藥輻射劑量檢測(cè)及評(píng)價(jià)技術(shù)
放藥的藥效及安全性評(píng)價(jià)與其輻射劑量直接相關(guān)�����,缺乏準(zhǔn)確的內(nèi)照射輻射劑量檢測(cè)技術(shù)是阻礙輻射劑量研究的瓶頸之一?����,F(xiàn)有的放藥臨床輻射劑量評(píng)價(jià)主要是通過(guò)核醫(yī)學(xué)影像獲取放藥分布����,或利用合適的動(dòng)物模型開展治療放藥的生物分布研究��。針對(duì)新興核素(225Ac����、212Pb�����、177Lu��、161Tb����、166Ho等)開發(fā)的放藥,因缺乏有效的����、準(zhǔn)確的劑量評(píng)價(jià)模型,導(dǎo)致難以科學(xué)指導(dǎo)藥品審評(píng)中的藥效及安全性評(píng)價(jià)����。有必要系統(tǒng)地開展放射創(chuàng)新藥的體內(nèi)劑量學(xué)研究,構(gòu)建更精準(zhǔn)的輻射檢測(cè)技術(shù)方法與劑量估算模型����。
5. 放藥聯(lián)合診療技術(shù)
放療與免疫治療����、化療����、光動(dòng)力治療及物理療法等手段聯(lián)合�����,會(huì)產(chǎn)生良好的協(xié)同治療效果��,但放藥與以上治療手段聯(lián)合使用的協(xié)同機(jī)制還不明確��,限制了相關(guān)聯(lián)合診療技術(shù)的臨床應(yīng)用和推廣�����。結(jié)合多學(xué)科技術(shù)與方法�����,重點(diǎn)開發(fā)免疫療法 ? 放藥聯(lián)用�����、輔助藥物 ? 放藥聯(lián)用、光聲光動(dòng)力藥物 ? 放藥聯(lián)用����、物理療法(如超聲微泡等) ? 放藥聯(lián)用的策略及創(chuàng)新診療技術(shù)與方法,進(jìn)一步提高放藥臨床診療效果��。
六����、對(duì)策建議
(一)以臨床為導(dǎo)向,鼓勵(lì)多學(xué)科交叉融合的創(chuàng)新發(fā)展
建議設(shè)立放藥創(chuàng)制專項(xiàng)�����,加強(qiáng)多學(xué)科交叉融合下的協(xié)同創(chuàng)新和臨床轉(zhuǎn)化研究��。鼓勵(lì)研發(fā)機(jī)構(gòu)提前布局��,瞄準(zhǔn)高發(fā)病率��、高致死率及無(wú)藥可用疾病的潛在臨床需求��,探索適于放藥的優(yōu)異靶點(diǎn)、構(gòu)建以多種治療核素為基石��、生物藥前沿技術(shù)為支撐的多品種����、系列化新藥研發(fā)技術(shù)創(chuàng)新體系。針對(duì)在臨床中有顯著應(yīng)用潛力的核素(如225Ac����、212Pb、177Lu����、161Tb��、166Ho)�����,可基于成熟靶點(diǎn)或藥物進(jìn)行優(yōu)化��,利用核素性質(zhì)差異擴(kuò)展相關(guān)藥物的適用范圍����,提高臨床診療效果。此外����,建議借鑒普藥靶向藥物的前沿技術(shù)及研究經(jīng)驗(yàn)����,如靶點(diǎn)篩選技術(shù)����、靶向結(jié)構(gòu)分子庫(kù)構(gòu)建技術(shù)、藥效評(píng)價(jià)技術(shù)等����,結(jié)合放藥特點(diǎn)開展針對(duì)肺癌、胰腺癌等難治惡性疾病的靶向診療放藥開發(fā)����。從發(fā)病機(jī)制、病灶發(fā)展過(guò)程��、靶點(diǎn)識(shí)別特征等方面��,開展以小分子��、多肽��、單抗等多類型靶向載體結(jié)構(gòu)為基礎(chǔ)的創(chuàng)新放藥研發(fā)。鼓勵(lì)臨床積極采用核醫(yī)療手段��,尤其是在無(wú)藥可用且放藥能發(fā)揮重大作用的心腦血管診斷及腫瘤診療領(lǐng)域����,針對(duì)具有潛力的放藥,可適時(shí)組建基礎(chǔ)研究與臨床醫(yī)生的協(xié)同團(tuán)隊(duì)����,共同推動(dòng)臨床研究的開展及放藥的轉(zhuǎn)化應(yīng)用。
(二)加快放藥技術(shù)創(chuàng)新體系建設(shè)
鼓勵(lì)以現(xiàn)有原子能機(jī)構(gòu)創(chuàng)新中心等平臺(tái)為依托�����,建設(shè)以科研院所和高校為主的源頭創(chuàng)新����,以企業(yè)為主的技術(shù)創(chuàng)新��,“政產(chǎn)學(xué)研用”深度融合的網(wǎng)格化創(chuàng)新體系�����?����?蛇M(jìn)一步選擇基礎(chǔ)條件較好、研究方向明確��、資金投入穩(wěn)定和研發(fā)隊(duì)伍實(shí)力較強(qiáng)的企業(yè)�����,建設(shè)創(chuàng)新型放藥孵化基地��,加快放藥創(chuàng)新產(chǎn)出進(jìn)程�����。建議支持原始創(chuàng)新和基礎(chǔ)理論研究����,重點(diǎn)發(fā)展放藥相關(guān)原創(chuàng)靶點(diǎn)探索、放藥在分子及細(xì)胞水平的輻射效應(yīng)機(jī)制研究��、放藥微劑量檢測(cè)�����、多組學(xué)分析等新技術(shù)開發(fā)�����、診療一體化及放藥聯(lián)用等創(chuàng)新策略開發(fā)等方面,形成科學(xué)認(rèn)識(shí)與技術(shù)研發(fā)的豐富儲(chǔ)備基礎(chǔ)�����,更好的支撐放藥創(chuàng)新體系建設(shè)����。
(三)加強(qiáng)放藥研發(fā)專業(yè)化人才隊(duì)伍建設(shè)
建議適當(dāng)擴(kuò)充國(guó)內(nèi)放藥研究機(jī)構(gòu)和高校的研究生招生規(guī)模,在有條件的高校和科研院所設(shè)定專項(xiàng)計(jì)劃����,培養(yǎng)放藥方向的研究人才。加強(qiáng)放藥研發(fā)后備人才培養(yǎng)力度����,試點(diǎn)推行醫(yī)工結(jié)合的創(chuàng)新人才培養(yǎng)機(jī)制,形成具有原創(chuàng)意識(shí)和能力的專業(yè)化人才隊(duì)伍�����。建立校企協(xié)作的技術(shù)人才培訓(xùn)基地����,以產(chǎn)業(yè)發(fā)展需求帶動(dòng)人才培養(yǎng)建設(shè)。設(shè)立國(guó)際交流與合作資助計(jì)劃��,支持鼓勵(lì)放藥方向?qū)W生的國(guó)際化培養(yǎng)����。改進(jìn)和完善放藥領(lǐng)域相關(guān)人才發(fā)展的環(huán)境,注重國(guó)內(nèi)培養(yǎng)和國(guó)外引進(jìn)放藥領(lǐng)域的領(lǐng)軍人物����。建議實(shí)施以核醫(yī)學(xué)醫(yī)生為重點(diǎn)的醫(yī)師隊(duì)伍建設(shè)培養(yǎng)工程,并在若干三甲醫(yī)院構(gòu)建放藥在重大疾病診療中發(fā)揮顯著作用的多學(xué)科診療模式(MDT團(tuán)隊(duì))機(jī)制����,加強(qiáng)專業(yè)、復(fù)合型醫(yī)師人才隊(duì)伍建設(shè)����。健全符合放藥研發(fā)生產(chǎn)成本和技術(shù)含量的薪酬體系,切實(shí)增加放藥從業(yè)人員的崗位吸引力��。