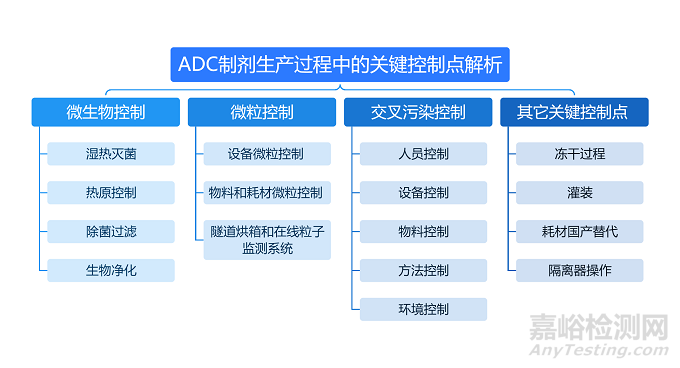
抗體偶聯(lián)藥物(ADC)兼具抗體的高特異性和細(xì)胞毒素的高抗腫瘤活性,對制劑生產(chǎn)也提出了更高要求�。在ADC制劑生產(chǎn)中的經(jīng)驗(yàn),ADC制劑生產(chǎn)過程中的關(guān)鍵控制點(diǎn)�,從微生物控制、微粒控制�、交叉污染控制以及其它關(guān)鍵點(diǎn)控制。
本次講詳細(xì)解析ADC制劑生產(chǎn)過程中的“微生物控制”���。
ADC制劑生產(chǎn)過程中的微生物控制
ADC制劑的生產(chǎn)和其他大分子的生產(chǎn)有很多相通之處���,比如對微生物的控制。微生物控制主要包含濕熱滅菌���、熱原控制���、除菌過濾、生物凈化四個(gè)方面:
一�、濕熱滅菌
濕熱滅菌主要針對滅菌柜做器具滅菌,其中有五個(gè)注意點(diǎn):
(一)滅菌柜性能:CD開發(fā)是確定滅菌柜性能的重要手段�。平衡時(shí)間、BD測試和泄露率測試�,這些性能測試也是考量滅菌柜質(zhì)量的重要因素。
(二)針對滅菌柜的驗(yàn)證:包括空載熱分布����、裝載熱穿透、BI挑戰(zhàn)以及最大裝載/最小裝載���。滅菌柜在所有驗(yàn)證項(xiàng)目達(dá)到合格標(biāo)準(zhǔn)后才能投入生產(chǎn)使用�。
(三)裝載策略設(shè)計(jì):這一部分考量的是裝載的代表性以及涵蓋范圍。如果裝載發(fā)生變化���,應(yīng)當(dāng)在前期驗(yàn)證過程中盡可能地考量到,僅通過一個(gè)評估就能將變化涵蓋����,從而減少驗(yàn)證的工作量。裝載發(fā)生變化后�,需要重新驗(yàn)證的時(shí)間節(jié)點(diǎn),也是設(shè)計(jì)裝載時(shí)需要重點(diǎn)考量的部分���。
(四)生產(chǎn)實(shí)際過程中的運(yùn)行參數(shù):驗(yàn)證通常采用Worse case參數(shù)����,所以生產(chǎn)過程中會采用更加保守的策略�。例如:驗(yàn)證時(shí),滅菌條件為121℃����、30min,而在實(shí)際生產(chǎn)中�,可以考慮用122℃���、30min的參數(shù)進(jìn)行生產(chǎn)。這樣可以保證在生產(chǎn)過程中�,滅菌柜的溫度即使低于122度,但只要高于121度���,驗(yàn)證依然有效�,可使風(fēng)險(xiǎn)降到最低���。
(五)考慮Holding Time:通過相應(yīng)的驗(yàn)證來確定滅菌后的存放時(shí)限�。例如一些器具滅菌以后存放多長時(shí)間�。該時(shí)限的確定通常有兩個(gè)策略:一是通過相應(yīng)的時(shí)限驗(yàn)證來確定,二是通過模擬灌裝挑戰(zhàn)來確定�。
濕熱滅菌的第二部分主要針對凍干機(jī)的SIP。
首先���,CIP站作為為凍干機(jī)清洗提供介質(zhì)的裝置�,需要考量是否進(jìn)行相應(yīng)的SIP����。純化水罐可以不進(jìn)行滅菌,WFI罐則需要滅菌或至少進(jìn)行蒸汽消毒處理����,目的是控制微生物的限度����。此外���,凍干機(jī)SIP時(shí)需保證滅菌溫度和時(shí)間�,以符合滅菌的要求�。
其次���,凍干機(jī)的SIP過程一般采用過度殺滅����。由于CIP結(jié)束后����,凍干機(jī)并非處于干燥狀態(tài),導(dǎo)致微生物滋長���,之后再進(jìn)行SIP會有失敗的風(fēng)險(xiǎn)�,所以CIP后不要放置太長的時(shí)間����,應(yīng)盡快進(jìn)行SIP���。在SIP中,也要關(guān)注凍干機(jī)的通氣過濾器�。
第三是SIP的驗(yàn)證。該驗(yàn)證一般通過風(fēng)險(xiǎn)評估來確定探頭的數(shù)量以及BI的數(shù)量和點(diǎn)位�,如對于凍干箱箱體的板層、內(nèi)壁和大門�,就需要通過風(fēng)險(xiǎn)評估來考慮在哪些地方布置探頭和BI。SIP的管路和過濾器則必須布置探頭和BI���,以此確保管路和過濾器能夠達(dá)到無菌效果����。BI在布置的過程中一定要牢固���,且不能堵塞管路����。如果布置不合適���,可能導(dǎo)致SIP結(jié)束后����,BI被蒸汽沖走,產(chǎn)生引入污染的風(fēng)險(xiǎn)����,或者堵塞管路,最終造成SIP的失敗�。
最后是SIP的時(shí)效性。與滅菌器柜相同���,需要考察其Holding Time�。該考察可以通過驗(yàn)證來確定�,也可以進(jìn)行三批模擬灌裝來確定滅菌的時(shí)效性����。通氣過濾器的滅菌次數(shù)也很關(guān)鍵,要根據(jù)過濾器的耐受次數(shù)以及實(shí)際的生產(chǎn)情況來綜合考察����。
二、熱原控制
微生物控制第二部分是熱原控制�,主要涉及隧道烘箱,可以從五個(gè)方面來解析:
(一)隧道烘箱的運(yùn)行模式����。在生產(chǎn)過程中采用的生產(chǎn)模式通常叫日間模式�;在生產(chǎn)停止過程中����,恰當(dāng)?shù)姆绞绞乔袚Q成夜間模式,保持隧道烘箱的送風(fēng)�,防止因送風(fēng)關(guān)閉造成隧道烘箱污染。
(二)冷卻段滅菌����。一般每批生產(chǎn)前需要對冷卻段進(jìn)行滅菌,保證冷卻段的無菌環(huán)境���。
(三)冷卻段壓差梯度的設(shè)計(jì)����。特別是對于ADC的生產(chǎn)����,一般會使用隔離器來保證活性藥物生產(chǎn)的安全性,所以隧道烘箱的出口段壓差比普通隧道烘箱高�。這對隧道烘箱的挑戰(zhàn)較大,需要防止隔離器的風(fēng)灌到隧道烘箱,還要防止冷卻段的風(fēng)灌到加熱段���。采用雙級的壓差梯度可以避免冷卻段對高溫段的影響�。
(四)隧道烘箱本身各段的壓差���。要與設(shè)計(jì)保持一致���。在實(shí)際運(yùn)行中不能偏離設(shè)計(jì),否則可能造成倒灌�,進(jìn)而影響除熱原的效果。
(五)溫度和網(wǎng)帶速度���。這個(gè)時(shí)候要考察不同規(guī)格的西林瓶對應(yīng)的除熱原溫度����、網(wǎng)帶速度存在差別�,這些參數(shù)需要通過驗(yàn)證來確定���。
三���、除菌過濾
微生物控制需要考慮的第三部分是除菌過濾,主要是藥液的除菌過濾。
具體包含以下六個(gè)方面:
(一)濾膜材質(zhì)和膜面積的選擇���。目前在市面上���,濾膜材質(zhì)多用PVDF和PES。在實(shí)際操作中���,材質(zhì)的選擇要根據(jù)藥液的特性確定����,通常是根據(jù)藥液的兼容性選擇���。膜面積的選擇要留有緩沖余地�,如果僅通過計(jì)算的值來選擇���,沒有留有緩沖�,可能會造成濾器的堵塞和破損���,尤其要注意高粘度����、高濃度、有蛋白聚集的情況����,可以考慮采用預(yù)過濾和多級濾器并聯(lián)的方式來有效降低風(fēng)險(xiǎn)。
(二)時(shí)限研究���?��;靹蚝笾吝^濾前一定要考察時(shí)限,還要考慮藥液整體的過濾時(shí)間���、藥液過濾后的存放時(shí)間���。
(三)影響藥液除菌過濾效能的因素����。其中最主要的是藥液本身的性質(zhì),此外還有過濾工藝參數(shù)����,如過濾的壓力���、以及過濾器和藥液相互的作用�,還有過濾量和使用周期���。
(四)無菌連接���。無菌連接器市面上也有很多種。此時(shí)要重點(diǎn)考察廠家對無菌連接器是否進(jìn)行了相應(yīng)驗(yàn)證���、驗(yàn)證資料是否齊全����、整體的密封性以及無菌連接器輻照滅菌驗(yàn)證資料是否齊備���。因?yàn)檫^濾的時(shí)候要考量濾器前后端的壓差,所以也要有相應(yīng)的壓力監(jiān)測系統(tǒng)�,還要有相應(yīng)的記錄及進(jìn)行相應(yīng)的計(jì)量。
(五)一次性系統(tǒng)����。根據(jù)EU GMP規(guī)范����,使用前要進(jìn)行完整性測試���。這時(shí)候要考量的是在無菌狀態(tài)下,做完整性測試過程中的通氣����、通水經(jīng)過相應(yīng)的過濾,應(yīng)當(dāng)怎樣收集過濾的水���。
(六)微生物負(fù)荷。需要重點(diǎn)考察的是取樣量���。法規(guī)要求是10CFU / 100ml���。ADC和其他大分子藥物附加值比較高,通常會采用折中的方案���。例如取3ml���,規(guī)定定量的CFU���。微生物負(fù)荷的取樣時(shí)間�,也是一個(gè)考量點(diǎn)�。一般的取樣會在除菌過濾前。如果除菌過濾是持續(xù)的過程���,那就要在除菌過濾前的最后時(shí)間點(diǎn)進(jìn)行取樣���。
四���、生物凈化
第四部分就是ADC制劑生產(chǎn)過程中微生物控制的非常重要的一部分���,即生物凈化,通常指隔離器VHP����。
隔離器VHP需要重點(diǎn)關(guān)注四個(gè)方面:
(一)CD/CV的開發(fā)���。隔離器的溫度���、濕度���、壓差以及蒸發(fā)盤的溫度、過氧化氫的注入量�、持續(xù)時(shí)間,都是在CD/CV開發(fā)過程中重點(diǎn)考量的參數(shù)����。
(二)BI的選擇與處理����。BI的選擇重點(diǎn)考慮D值;BI的保存要注意溫濕度以及避免裸手接觸BI���。驗(yàn)證過程可考慮分?jǐn)?shù)法���,每個(gè)點(diǎn)布置3個(gè)BI���,防止出現(xiàn)個(gè)別陽性的情況���。
(三)VHP實(shí)施過程中的控制。要關(guān)注幾個(gè)點(diǎn):一是VHP的起始階段,即除濕后的濕度����。還要關(guān)注VHP過程中(提升階段)過氧化氫達(dá)到的濃度,該濃度需達(dá)到一定的數(shù)值�,且經(jīng)過驗(yàn)證�。如驗(yàn)證的時(shí)候達(dá)到400PPM才能達(dá)到殺滅的效果�,但如果實(shí)際過程中,濃度沒有達(dá)到400PPM則會造成風(fēng)險(xiǎn)�,這就不是成功的VHP過程。凈化階段持續(xù)時(shí)間也很重要�,比如驗(yàn)證過程中進(jìn)行的是85分鐘的驗(yàn)證,生產(chǎn)過程中就會更保守�,延長時(shí)間,真正對無菌保證起到雙保險(xiǎn)的作用����。
(四)過氧化氫排殘����。一般要配備高低濃度探頭,有的設(shè)備商只配了一種探頭���,并宣稱高低濃度均可監(jiān)測���。實(shí)際上這種探頭對高濃度比較精確�,而低濃度時(shí)誤差非常大����,所以并不適宜���。比較適宜的做法是分開設(shè)置濃度探頭���,并且要確認(rèn)低濃度探頭的精度范圍。很多時(shí)候���,低濃度探頭在1ppm的精度不高���,排殘的時(shí)候顯示到了1ppm����,如果以更精確的便攜式監(jiān)測的話,可能有幾個(gè)ppm���,這對于敏感性高的藥品有一定影響����。同時(shí),低濃度探頭的安裝位置也很重要�。
在排殘時(shí)需要在驗(yàn)證過程中做實(shí)驗(yàn),保證過氧化氫的濃度達(dá)到實(shí)際的數(shù)值���,而不是在隔離器本身的探頭里面顯示的數(shù)值。因?yàn)樘筋^精度有限���,一些特殊藥品對過氧化氫的敏感度非常高,此時(shí)需要單獨(dú)考察���,考察時(shí)要做到:一是延長排殘時(shí)間���,二是以相應(yīng)的方法進(jìn)行確認(rèn)。