今日頭條
深圳賽嵐腫瘤表觀遺傳療法獲批臨床�����。賽嵐醫(yī)藥宣布其基于新一代表觀遺傳機(jī)理研發(fā)的潛在“first-in-class”抗腫瘤候選藥物CTS2190膠囊獲FDA臨床試驗(yàn)許可�����,即將開(kāi)展Ⅰ期臨床評(píng)估用于晚期實(shí)體瘤患者的安全性與初步療效�����。在臨床前研究中,CTS2190已顯示出對(duì)多種實(shí)體瘤和血液瘤的細(xì)胞�����、CDX���、PDO和PDX模型的有效抑制效果�����,而且具有良好的藥代動(dòng)力學(xué)和安全性���,有望為腫瘤治療提供有力的創(chuàng)新手段�。
國(guó)內(nèi)藥訊
1.武漢濱會(huì)溶瘤病毒擬納入突破性治療品種���。濱會(huì)生物1類生物制品重組人GM-CSF溶瘤II型單純皰疹病毒(OH2)注射液(Vero細(xì)胞)獲CDE擬納入突破性治療品種���,針對(duì)適應(yīng)癥為:經(jīng)至少二線以上標(biāo)準(zhǔn)治療失敗的不能手術(shù)切除或轉(zhuǎn)移性的黑色素瘤患者。該產(chǎn)品可選擇性感染腫瘤細(xì)胞并在其中復(fù)制���,最終裂解�����、殺死腫瘤細(xì)胞�����,并釋放出抗原物質(zhì)誘導(dǎo)特異性抗腫瘤免疫反應(yīng)���。在美國(guó)�,F(xiàn)DA已授予該新藥孤兒藥資格���,用于治療IIb期至IV期黑色素瘤�����。
2.衛(wèi)材&渤健Aβ單抗擬納入優(yōu)先審評(píng)���。衛(wèi)材與渤健聯(lián)合開(kāi)發(fā)的1類新藥侖卡奈單抗注射液的上市申請(qǐng)獲國(guó)家藥監(jiān)局?jǐn)M納入優(yōu)先審評(píng),擬用于治療早期阿爾茨海默病(AD)�。侖卡奈單抗(lecanemab,BAN2401)是一款抗淀粉樣蛋白(Aβ)原纖維抗體�����,已在今年1月獲FDA批準(zhǔn)用于治療AD�。兩項(xiàng)Ⅲ期臨床(EMERGE和ENGAGE)擴(kuò)展研究顯示,aducanumab治療兩年后能持續(xù)降低患者大腦中的Aβ水平和血漿中的p-tau181水平���。
3.歌禮PD-L1單抗慢性乙肝II期臨床積極。歌禮制藥皮下注射PD-L1抗體恩沃利單抗(ASC22)治療慢性乙型肝炎的最新臨床數(shù)據(jù)公布于亞太肝臟研究協(xié)會(huì)2023年年會(huì)上。24周治療數(shù)據(jù)顯示�,在基線HBsAg≤100 IU/mL的患者亞組中,42.9% (3/7)的患者在治療期間實(shí)現(xiàn)了HBsAg清除(HBsAg低于檢測(cè)下限�����,即LLOQ<0.05 IU/mL)���,并在24周或41周隨訪結(jié)束時(shí)保持HBsAg清除�,顯示ASC22具有慢乙肝功能性治愈潛力�����。ASC22總體耐受性良好�����。
4.尚健CLDN18.2/CD47雙抗獲批臨床���。尚健生物自研創(chuàng)新CLDN18.2/CD47雙抗SG1906注射液獲國(guó)家藥監(jiān)局批準(zhǔn)臨床�,擬開(kāi)發(fā)用于CLDN18.2陽(yáng)性晚期惡性實(shí)體腫瘤�。SG1906能同時(shí)特異性結(jié)合CLDN18.2和CD47分子,介導(dǎo)ADCC���、ADCP以及通過(guò)阻斷CD47和SIRPα相互作用�����,具有協(xié)同抗腫瘤效應(yīng)�����。在CLDN18.2中低表達(dá)的PDX腫瘤模型中���,SG1906顯示出積極的抑瘤效果�����,未見(jiàn)明顯的靶點(diǎn)相關(guān)不良反應(yīng)�����。2022年10月�,F(xiàn)DA已批準(zhǔn)該新藥在美國(guó)開(kāi)展臨床試驗(yàn)�。
5.博奧明賽IgG1單抗報(bào)乙肝IND。博奧明賽1類生物制品BM012注射液的臨床試驗(yàn)申請(qǐng)獲得CDE受理�。BM012是一種具有多重機(jī)制抗乙肝病毒(HBV)的IgG1全人源單克隆抗體藥物,已在臨床前研究顯示出比同類產(chǎn)品 (Vir3434) 更好的抑制S抗原的活性以及抗病毒藥效�����,并在GLP毒理研究中展示出良好的安全性。BM012注射液的首個(gè)適應(yīng)癥為慢性乙型肝炎病毒感染���。
國(guó)際藥訊
1.首個(gè)IgA腎病非免疫抑制療法獲批上市。Travere公司內(nèi)皮素/血管緊張素受體拮抗劑(DEARA)Filspari(sparsentan)獲FDA加速批準(zhǔn)上市���,用于在有高風(fēng)險(xiǎn)出現(xiàn)疾病進(jìn)展的IgA腎病患者中降低蛋白尿�����。在一項(xiàng)Ⅲ期PROTECT研究中�,sparsentan治療組36周后患者蛋白尿較基線平均減少49.8%�����,活性對(duì)照組平均減少15.1%(p<0.0001)�。Filspari也是FDA批準(zhǔn)針對(duì)IgA腎病的首個(gè)非免疫抑制療法。
2.首款A(yù)M酶替代療法獲批上市�����。Chiesi Global Rare Diseases公司重組人α-甘露糖苷酶Lamzede(velmanase alfa-tycv)獲FDA批準(zhǔn)上市���,用于治療α-甘露糖苷貯積癥(AM)的非中樞神經(jīng)系統(tǒng)表現(xiàn)�����。Lamzede也是FDA批準(zhǔn)針對(duì)該疾病的首款酶替代療法�,旨在提供或補(bǔ)充天然α-甘露糖苷酶,以降解富含甘露糖的寡糖并防止其在體內(nèi)各種組織中蓄積�。2018年3月,歐盟委員會(huì)已批準(zhǔn)Lamzede用于治療輕中度AM患者的非神經(jīng)系統(tǒng)表現(xiàn)�����。
3.眼科雙環(huán)肽療法獲批治療GA���。Apellis公司靶向補(bǔ)體C3的聚乙二醇化雙環(huán)肽療法Syfovre(pegcetacoplan)獲FDA批準(zhǔn)�����,用于治療由年齡相關(guān)性黃斑變性(AMD)引起的地圖樣萎縮(GA)�����。來(lái)自III期DERBY和OAKS研究的24個(gè)月療效數(shù)據(jù)顯示�����,每個(gè)月或每?jī)蓚€(gè)月一次的pegcetacoplan治療�,皆具一致性的療效與安全性。2021年5月���,pegcetacoplan已獲得FDA批準(zhǔn)上市�����,用于治療陣發(fā)性睡眠性血紅蛋白尿癥(PNH)。
4.K藥聯(lián)合化療治療胃癌III期臨床積極�����。默沙東PD-1抑制劑Keytruda聯(lián)合PF(5-氟尿嘧啶+順鉑)或CAPOX(卡培他濱+奧利沙鉑)一線治療HER2陰性晚期胃癌或胃食管交界處 (GEJ) 腺癌的III期KEYNOTE-859結(jié)果積極�。中位隨訪為31.0個(gè)月時(shí),Keytruda組患者的OS較安慰劑組顯著延長(zhǎng)(12.9vs11.5個(gè)月)���,死亡風(fēng)險(xiǎn)降低22%(HR=0.78���;95% CI, 0.70-0.87;P<0.0001)���;兩組患者PFS(6.9vs5.6個(gè)月)和DOR(8.0vs5.7個(gè)月)顯著延長(zhǎng)�����,疾病進(jìn)展或死亡風(fēng)險(xiǎn)降低24%�;兩組3-5級(jí)治療相關(guān)不良事件(TRAEs)發(fā)生率亦相似。
5.Moderna公布四價(jià)流感疫苗III期數(shù)據(jù)�����。Moderna公司公布季節(jié)性流感mRNA疫苗mRNA-1010在成年人中開(kāi)展的關(guān)鍵III期臨床中期結(jié)果�。與傳統(tǒng)疫苗相比,mRNA-1010在甲型H1N1和甲型H3N2的血清轉(zhuǎn)化率上取得優(yōu)效結(jié)果�,在H3N2的幾何平均滴度比上也具有優(yōu)效性,在H1N1的幾何平均滴度比上具有非劣效性���。但在乙型Victoria和乙型Yamagata的血清轉(zhuǎn)化率和抗體滴度方面則均未達(dá)到非劣效性���。mRNA-1010與傳統(tǒng)疫苗的不良反應(yīng)發(fā)生率分別為70%和48%。
6.OSE公司癌癥疫苗獲批注冊(cè)性III期臨床���。OSE公司宣布癌癥疫苗Tedopi同時(shí)獲得FDA和EMA同意開(kāi)展關(guān)鍵性III期臨床���,用于二線治療HLA-A2陽(yáng)性晚期非小細(xì)胞肺癌(NSCLC)。此前�,Tedopi已在三線治療NSCLC患者的III期臨床中獲得積極結(jié)果���。結(jié)果顯示,與標(biāo)準(zhǔn)治療(SOC)相比�,Tedopi組患者的1年OS率更高(44.4%vs27.5%);3-5級(jí)治療期間不良事件(TEAE)發(fā)生率更低(11%vs35%)�����。
醫(yī)藥熱點(diǎn)
1.廣東鄉(xiāng)村醫(yī)生每人每年補(bǔ)貼2萬(wàn)元�����。近日���,廣東高度重視基層醫(yī)療衛(wèi)生服務(wù)能力建設(shè),陸續(xù)出臺(tái)政策�����、加大投入���。廣東省衛(wèi)健委已推動(dòng)下發(fā)4.8億多資金���,用于2023年在崗�����、離崗村醫(yī)的補(bǔ)助�����。無(wú)論是持有執(zhí)業(yè)(助理)醫(yī)師證書(shū)���,還是鄉(xiāng)村醫(yī)生執(zhí)業(yè)證書(shū),只要在村衛(wèi)生站工作�,均可領(lǐng)取補(bǔ)貼,補(bǔ)貼標(biāo)準(zhǔn)為鄉(xiāng)村醫(yī)生每人每年2萬(wàn)元���。
2.廣州構(gòu)建居家腹膜透析治療體系�。近日�����,由廣東省廣州市衛(wèi)健委主辦�、南方醫(yī)科大學(xué)南方醫(yī)院承辦的廣州市居家腹膜透析治療示范體系建設(shè)項(xiàng)目在南方醫(yī)院舉行試點(diǎn)單位授牌活動(dòng)。該項(xiàng)目為衛(wèi)生健康領(lǐng)域重點(diǎn)發(fā)展的“院士工程”�����,安排專門(mén)資金推動(dòng),旨在探索社區(qū)腎臟替代治療廣覆蓋���。該項(xiàng)目吸納了21家醫(yī)療衛(wèi)生機(jī)構(gòu)參與�,包括1個(gè)項(xiàng)目示范中心(南方醫(yī)院)���,3個(gè)分中心(中山大學(xué)孫逸仙紀(jì)念醫(yī)院�����、廣州醫(yī)科大學(xué)附屬第一醫(yī)院�����、廣州市第一人民醫(yī)院),以及17家基層醫(yī)療衛(wèi)生機(jī)構(gòu)�。
3.吉林打造四級(jí)臨床重點(diǎn)專科�����。近日�,吉林省衛(wèi)健委出臺(tái)《吉林省臨床重點(diǎn)專科建設(shè)“十四五”規(guī)劃》,提出到2025年���,力爭(zhēng)建設(shè)國(guó)家臨床重點(diǎn)?��??0個(gè)、省級(jí)臨床重點(diǎn)?��??0個(gè)���、市級(jí)臨床重點(diǎn)專科110個(gè)�����、縣級(jí)臨床重點(diǎn)???10個(gè),形成資源均衡�����、分工協(xié)作�����、縱向貫通、橫向聯(lián)通的臨床?��?品?wù)體系�。
評(píng)審動(dòng)態(tài)
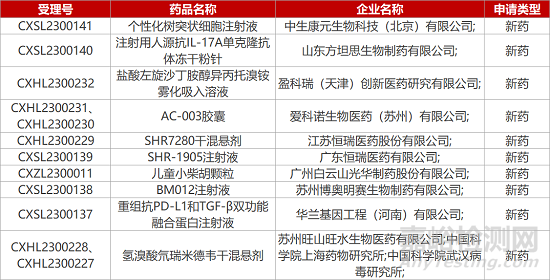
1. CDE新藥受理情況(02月18日)
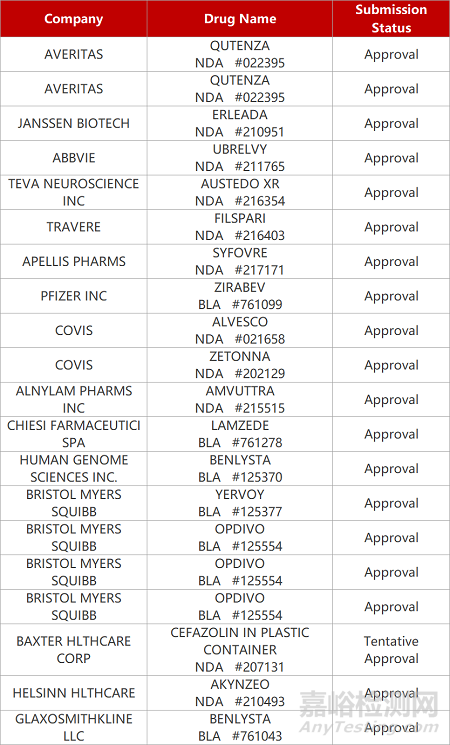
2. FDA新藥獲批情況(北美02月17日)
 ..
..

 ..
..