今日頭條
廣州蘇庇罕見病新藥獲批上市��。蘇庇醫(yī)藥與Swedish Orphan Biovitrum AB(SOBI)公司合作開發(fā)的尼替西農(nóng)膠囊以及口服混懸液獲國家藥監(jiān)局批準(zhǔn)上市���,結(jié)合酪氨酸和苯丙氨酸飲食限制���,用于治療成人和兒科患者的遺傳性酪氨酸血癥I型(HT-1)��。這是一種常染色體隱性遺傳的罕見病��,由15號染色體基因缺陷導(dǎo)致���。尼替西農(nóng)是一款4-羥苯丙酮酸雙氧酶可逆抑制劑。
國內(nèi)藥訊
1.艾伯維JAK1抑制劑在華獲批治療UC��。艾伯維JAK1抑制劑烏帕替尼緩釋片獲國家藥監(jiān)局批準(zhǔn)新適應(yīng)癥���,用于治療對一種或多種腫瘤壞死因子抑制劑應(yīng)答不佳或不耐受或禁忌的中重度活動性潰瘍性結(jié)腸炎(UC)成人患者���。這也烏帕替尼緩釋片在華獲批的第四個適應(yīng)癥。在U-ACHIEVE和U-ACCOMPLISH誘導(dǎo)研究中��,烏帕替尼的臨床緩解率為26%(vs5%)和33%(vs4%)���;在U-ACHIEVE維持治療研究中,烏帕替尼的臨床緩解率分別為42%和52%,而安慰劑僅有12%���。
2.君實PD-1抑制劑三陰乳癌III期臨床積極。君實生物PD-1抑制劑特瑞普利單抗(拓益®)聯(lián)合注射用紫杉醇(白蛋白結(jié)合型)用于治療首診IV期或復(fù)發(fā)轉(zhuǎn)移性三陰性乳腺癌的III期TORCHLIGHT研究(NCT04085276)達(dá)到主要終點���。與紫杉醇相比,聯(lián)合治療顯著延長PD-L1陽性患者的無進展生存期�����,而且次要終點總生存期也顯示明顯獲益趨勢���。臨床中未發(fā)現(xiàn)新的安全性信號�����。
3.康希諾新冠mRNA疫苗IIb期研究積極��。康希諾新冠mRNA疫苗CS-2034用于18歲及以上已完成3劑新冠滅活疫苗接種的成年人序貫加強的IIb期臨床結(jié)果積極���。序貫加強1劑CS-2034后,14��、28天mRNA異源加強組針對BA.5株的抗體幾何平均滴度(GMT)約為滅活疫苗組的34.7及14.4倍,幾何平均滴度增長倍數(shù)(GMI)約為滅活組的38及15.7倍�����,陽轉(zhuǎn)率約為滅活組的25.5及5.2倍�����,GMT及陽轉(zhuǎn)率均達(dá)優(yōu)效性��;且疫苗的不良反應(yīng)發(fā)生率及嚴(yán)重程度低于目前已上市mRNA疫苗��。
4.康弘膠質(zhì)瘤創(chuàng)新藥獲孤兒藥資格��。康弘藥業(yè)旗下弘合生物自研創(chuàng)新藥KH617獲FDA授予孤兒藥資格���,擬用于膠質(zhì)母細(xì)胞瘤的治療。在臨床前研究中。KH617已在幾種疾病模型中顯示出對多種實體瘤的良好抑瘤作用��,尤其在膠質(zhì)母細(xì)胞瘤原位模型中藥效更為顯著。2022年9月���,KH617已獲得CDE臨床許可,針對適應(yīng)癥為晚期實體瘤患者(包括成人彌漫性膠質(zhì)瘤)��。
5.人福選擇性阿片受體激動劑獲批臨床��。人福醫(yī)藥子公司宜昌人福開發(fā)的選擇性阿片受體激動劑RFUS144注射液獲FDA臨床批件,擬開發(fā)用于治療疼痛和瘙癢���。在臨床前研究中,RFUS144已顯示出高選擇性的鎮(zhèn)痛效果���,并具有良好的安全性和耐受性��,無成癮�����、心臟�����、呼吸抑制等不良反應(yīng)�����。國內(nèi)目前尚無同類型產(chǎn)品上市。
6.智康弘義WEE1激酶抑制劑在美獲批臨床�����。智康弘義WEE1激酶小分子抑制劑SC0191獲FDA批準(zhǔn)開展Ⅰ/Ⅱ期臨床�����,擬單藥和聯(lián)合化療用于治療晚期實體瘤�����。細(xì)胞周期調(diào)節(jié)蛋白WEE1激酶是細(xì)胞周期中G2/M檢查點的關(guān)鍵調(diào)控因子���,能夠調(diào)控G2/M期發(fā)生阻滯�����,為DNA修復(fù)提供時間��。在中國��,該新藥已先后獲批多項臨床試驗���,適應(yīng)癥包括晚期實體瘤�����,以及與吉西他濱或紫杉醇等化療藥物聯(lián)合治療晚期卵巢癌。
國際藥訊
1.Mirum公司膽汁淤積癥新藥報sNDA���。Mirum公司宣布遞交口服回腸膽汁酸轉(zhuǎn)運蛋白(IBAT)抑制劑maralixibat(Livmarl)的補充新藥申請(sNDA)�����,用于治療兩個月及以上進行性家族性肝內(nèi)膽汁淤積癥(PFIC)患者的膽汁淤積性瘙癢癥狀���。在Ⅲ期研究MARCH PFIC中���,maralixibat較安慰劑顯著改善患者瘙癢程度(p<0.0001);血清膽汁酸水平較基線也顯著下降�����。2021年10月���,F(xiàn)DA已批準(zhǔn)Livmarl用于治療1歲及以上Alagille綜合征(ALGS)患者的膽汁淤積性瘙癢癥��。
2.眼科類病毒偶聯(lián)藥物Ⅱ期結(jié)果積極��。Aura Biosciences公司類病毒偶聯(lián)藥物(VDC)Bel-sar(AU-011)一線治療早期脈絡(luò)膜黑色素瘤的Ⅱ期試驗(NCT04417530)中期結(jié)果積極�����。藥物通過脈絡(luò)膜上腔注射并進行三個周期的治療���。Bel-sar平均腫瘤控制率達(dá)到89%���,患者的視敏度保存率為88%;藥物的總體耐受性良好�����,沒有出現(xiàn)劑量限制毒性���、治療相關(guān)的SAEs或重大的不良事件��。詳細(xì)數(shù)據(jù)將在黃斑學(xué)會(Macula Society)第46屆年會上公布�����。
3.奧拉帕利治療mCRPC的Ⅲ期研究新進展。阿斯利康與默沙東在ASCO2023 年會上公布PARP抑制劑奧拉帕利(Lynparza)聯(lián)合標(biāo)準(zhǔn)治療(阿比特龍和潑尼松/潑尼松龍)一線治療轉(zhuǎn)移性去勢抵抗性前列腺癌(mCRPC)的III期PROpel研究關(guān)鍵次要終點結(jié)果。與安慰劑聯(lián)合標(biāo)準(zhǔn)治療相比���,Lynparza聯(lián)合治療提高患者的總生存期(OS)���,兩組患者中位OS分別為42.1個月和34.7個月(成熟度47.9%��,HR 0.81;95% CI 0.67-1.00���;p=0.0544)�����,中位OS未達(dá)到統(tǒng)計學(xué)差異���。臨床中沒有發(fā)現(xiàn)新的長期安全問題。
4.磷酸化靶向嵌合體分子臨床前研究積極�����。耶魯大學(xué)Craig M. Crews教授團隊開發(fā)的磷酸化靶向嵌合體PhosTACs分子在體外細(xì)胞實驗中評估降低Tau蛋白磷酸化水平的臨床前研究結(jié)果積極�����。實驗結(jié)果顯示��,PhosTACs能夠誘導(dǎo)生成穩(wěn)定的三元結(jié)構(gòu)���,特異性去除Tau蛋白的過度磷酸化,并降低Tau蛋白水平��。PhosTACs分子有望用于治療阿爾茨海默病和其它Tau蛋白病。
5.安斯泰來更年期藥物上市審批延期。FDA延長安斯泰來公司NK3(神經(jīng)激肽3)受體拮抗劑fezolinetant用于治療更年期相關(guān)的中重度血管舒縮癥狀(VMS)的上市申請審查期,新的PDUFA日期為2023年5月22日。Fezolinement旨在通過阻斷NKB的信號通路���,調(diào)控下視丘溫度調(diào)節(jié)中心的神經(jīng)活動,以降低絕經(jīng)相關(guān)中重度VMS的頻率和嚴(yán)重程度�����。如果獲批���,fezolinant將成為這類患者的“first-in-class”的非激素治療選擇�����。
6.AR靶向RIPTAC臨床前數(shù)據(jù)積極。Halda公司在2023 ASCO GU會議上公布其靶向AR的調(diào)節(jié)誘導(dǎo)接近靶向嵌合體(RIPTAC)H001治療前列腺癌的完整臨床前數(shù)據(jù)��。H001通過參與細(xì)胞轉(zhuǎn)錄調(diào)節(jié)的蛋白(EP)與AR連接成一個穩(wěn)定的三元復(fù)合物���,從而抑制EP的功能,導(dǎo)致AR陽性細(xì)胞的選擇性死亡���。在前列腺癌小鼠模型中�����,H001治療較標(biāo)準(zhǔn)療法恩雜魯胺顯示出優(yōu)效的抑制活性�����,以及廣泛活性��,有望為耐藥性的患者帶來希望���。
醫(yī)藥熱點
1.徐景和當(dāng)選全球醫(yī)療器械法規(guī)協(xié)調(diào)會主席。2月16日���,國家藥監(jiān)局副局長徐景和成功當(dāng)選第27屆全球醫(yī)療器械法規(guī)協(xié)調(diào)會(GHWP)主席��。這在我國醫(yī)療器械監(jiān)管國際化進程中具有重要意義���。徐景和表示,他將與GHWP的各位成員一道���,繼續(xù)推進全球醫(yī)療器械監(jiān)管法規(guī)的協(xié)調(diào)工作��,促進成員間監(jiān)管能力的共同提升�����。
2.鄭大一附院神經(jīng)外科重癥監(jiān)護病房成立。2月21日��,鄭州大學(xué)第一附屬醫(yī)院神經(jīng)外科重癥監(jiān)護病房揭牌開診及神經(jīng)外科新病房喬遷儀式在南院區(qū)2號樓五樓舉行��。這是鄭大一附院成立的首個神經(jīng)外科重癥監(jiān)護病房,旨在建立健全神經(jīng)外科亞專業(yè)學(xué)科體系的重要組成部分,必將進一步提升醫(yī)院神經(jīng)外科診療服務(wù)水平���,提高河南省神經(jīng)外科專業(yè)競爭力,為廣大神經(jīng)外科患者提供精準(zhǔn)���、科學(xué)�����、高質(zhì)量的醫(yī)療服務(wù)。
3.第八批國家藥品集采啟動。2月20日起�����,我國第八批國家組織藥品集中采購相關(guān)藥品信息填報工作正式展開。本次集采涵蓋全身用抗感染藥物�����、心腦血管系統(tǒng)藥物、血液和造血系統(tǒng)藥物�����、神經(jīng)系統(tǒng)藥物等治療領(lǐng)域��。此次共有41個品種�����、181個品規(guī)的藥品進入集采�����。41個品種中�����,27個為注射劑��,和歷次國家集采相比,占比首次超過60%��;口服常釋劑型有11個�����;顆粒劑���、緩釋控釋劑型及口服溶液劑各有1個。
評審動態(tài)
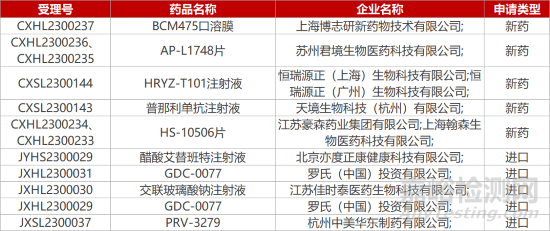
1. CDE新藥受理情況(02月21日)
2. FDA新藥獲批情況(北美02月17日)