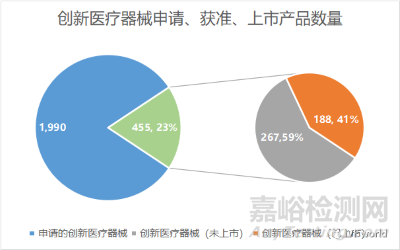
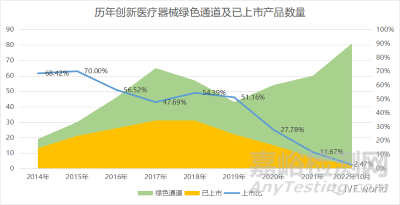
作者近期對中國歷史所有獲準進入“綠色通道”的創(chuàng)新醫(yī)療器械進行了梳理��,從2014年創(chuàng)新醫(yī)療器械“綠色通道”開設以來,截至2022年12月31日�����,八年間��,中國藥品監(jiān)督管理局醫(yī)療器械審評中心(CDE)總計收到了1990份創(chuàng)新醫(yī)療器械申請�,其中455款醫(yī)療器械獲準進入綠色通道����,得以公示,占比約22.86%����。
而在已經(jīng)進入“綠色通道”的455款創(chuàng)新醫(yī)療器械(名單見附錄1)中��,目前已經(jīng)完成上市的產(chǎn)品約占41%,即總計有188款創(chuàng)新醫(yī)療器械(名單見附錄2)產(chǎn)品通過綠色通道已經(jīng)上市�����。而仍有267款(約59%)創(chuàng)新醫(yī)療器械產(chǎn)品仍在審批路上����。
我們對這8年時間���、455款創(chuàng)新醫(yī)療器械�����,從年份��、地區(qū)���、審批時長、產(chǎn)品類型�����、獲準率����、上市比等十余個維度進行了逐一研究分析,發(fā)現(xiàn)了如下趨勢:
1�����、創(chuàng)新醫(yī)療器械的申請通過率在24%左右��,并在提高;
2�、33%創(chuàng)新醫(yī)療器械1年后完成上市�,但這個速度正在變慢����;
3��、創(chuàng)新醫(yī)療器械產(chǎn)品類型最多的是“13無源植入器械”����;
4��、創(chuàng)新醫(yī)療器械產(chǎn)品最多的省份在北京���,其次是上海����;
5�����、旗下創(chuàng)新醫(yī)療器械產(chǎn)品數(shù)量最多的企業(yè)是【品馳醫(yī)療】和【微創(chuàng)集團】����;
6��、綠色通道中“優(yōu)先審批”比“創(chuàng)新醫(yī)療器械”申請門檻更高����;
7����、2022年創(chuàng)新醫(yī)療器械上市數(shù)量增長率最高�����,達到了54%���。
一�����、什么是醫(yī)療器械的綠色通道�����?
“綠色通道”是國家為優(yōu)秀醫(yī)療器械專設的審批加速渠道。中國藥品監(jiān)督管理局醫(yī)療器械審評中心(CDE)每年有上萬醫(yī)療器械項目等待審評��,單個項目從申請到獲批上市平均需要3-5年不等����。為了讓具有顯著臨床價值����、國內(nèi)首創(chuàng)����、國際領先的醫(yī)療器械項目能夠更快進入臨床造?���;颊?�,NMPA在2014年和2017年分別開設了“創(chuàng)新醫(yī)療器械特別審查”和“醫(yī)療器械優(yōu)先審批”兩條綠色通道���。
“創(chuàng)新醫(yī)療器械”通道比“優(yōu)先審批”通道擁擠����。“創(chuàng)新醫(yī)療器械”要求研發(fā)方必須擁有核心技術發(fā)明專利��,強調(diào)產(chǎn)品的技術創(chuàng)新性與領先性��;而“醫(yī)療器械優(yōu)先審批”則側重于項目臨床價值的急迫性����,對于尚無獲批產(chǎn)品的針對罕見病����、惡性腫瘤等未滿足臨床需求的醫(yī)療器械則可適用優(yōu)先程序���。
“優(yōu)先審批”比“創(chuàng)新醫(yī)療器械”申請門檻更高
二者相較,“創(chuàng)新醫(yī)療器械”申請門檻更低一些���,“優(yōu)先審批”則往往需要通過國家科技重大專項等渠道進入。這也讓每年創(chuàng)新醫(yī)療器械申請量遠遠多于申請優(yōu)先審批的醫(yī)療器械數(shù)量�����。
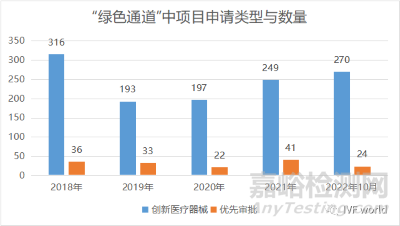
從上表我們可以看到����,每年“創(chuàng)新醫(yī)療器械”基本保持數(shù)百申請量�,而“醫(yī)療器械優(yōu)先審批”申請量基本都是幾十項����;平均來看,創(chuàng)新醫(yī)療器械的申請量是優(yōu)先審批的7倍以上�,在2022年(官方數(shù)據(jù)更新至2022年10月)這個倍差達到最大的11.25倍�����。
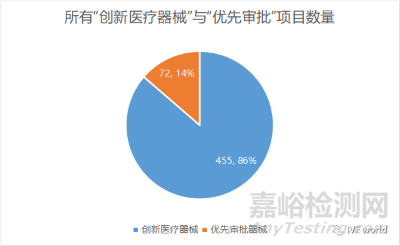
最終又有多少進入綠色通道呢?截至2022年12月31日�,獲得創(chuàng)新醫(yī)療器械審批資格的產(chǎn)品有455款�����,而進入優(yōu)先審批名額的醫(yī)療器械僅有72款��。當然���,也要考慮到創(chuàng)新醫(yī)療器械本身起源更早����。
不過��,從每年申請及其獲批數(shù)量的維度看�,創(chuàng)新醫(yī)療器械平均每年申請量為238家�,通過量均值為51家���,通過率約為22%;優(yōu)先審批平均每年申請量為33家�,通過量均值為12家��,通過率約為38%��,反而其通過率更高����。
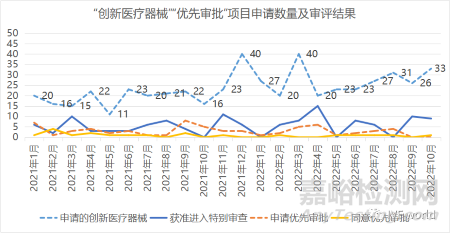
從上表我們也可以看出��,CDE每月獲準的創(chuàng)新醫(yī)療器械數(shù)量與每月企業(yè)申請的優(yōu)先審批數(shù)量在同一個數(shù)量級,而同意優(yōu)先審批的醫(yī)療器械更是鳳毛麟角����。所以作者這次對總量更大��、數(shù)據(jù)更全的創(chuàng)新醫(yī)療器械進行梳理分析����,以此反映中國創(chuàng)新醫(yī)療器械發(fā)展趨勢����,以饗讀者���。
二����、從申請到獲準:平均24%的申請通過率,2022年提高到30%
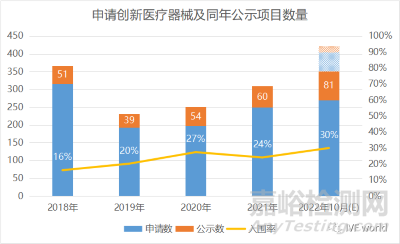
平均來看����,每4個申請項目��,有1個能獲準進入創(chuàng)新醫(yī)療器械的綠色通道����。根據(jù)CDE公示最新數(shù)據(jù)計算���,從2014年至2022年10月底,總計有1990個醫(yī)療器械產(chǎn)品申請進入創(chuàng)新通道����,455個產(chǎn)品作為創(chuàng)新醫(yī)療器械被納入該通道�����,涉及約349家醫(yī)療器械廠商入圍��。項目申請每年的平均通過率在23.57%左右����,意味著每4個申請項目中將有1個項目成功入選��。
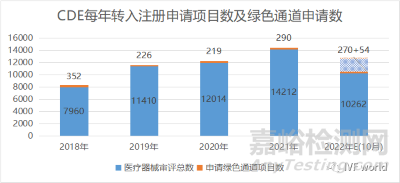
創(chuàng)新醫(yī)療器械申請熱情不減,申請量逐年提升�。2018年至2022年10月,CDE分別收到316份��、193份��、197份、249份及270份申請���,而同年公示進入創(chuàng)新通道的醫(yī)療器械分別對應51個、39個��、54個����、60個和81個���。
創(chuàng)新醫(yī)療器械審批程序最新規(guī)定要求,各省藥品監(jiān)督管理局在收到創(chuàng)新醫(yī)療器械申請后���,需在20個工作日完成初審,40個工作日內(nèi)NMPA出具審查意見�。也就是說,從提交到公示最長僅需2個月��。如果忽略這兩個月的時間差��,以同年申請同年公告來推算,目前2022年的創(chuàng)新醫(yī)療器械申請通過率是最高的���,達到了30%;最低是2018年���,僅有16.14%的通過率����。
三���、從審批到上市:多維度分析188款上市創(chuàng)新醫(yī)療器械
綠色通道助力“提速”而非“降準”。
《創(chuàng)新醫(yī)療器械特別審批程序》指出�����,創(chuàng)新醫(yī)療器械的特別審批程序并不獨立于醫(yī)療器械的一般審批程序,所以并未減少審批環(huán)節(jié)或降低審批標準����,而是在審批程序的諸多環(huán)節(jié)中��,按照早期介入�����、專人負責�、科學審批的原則����,對創(chuàng)新醫(yī)療器械予以優(yōu)先辦理����,從而加快其審批進程���,加強與申請人的溝通交流����。
從官方文件上理解或許比較抽象����,一家已經(jīng)進入綠色通道的醫(yī)療器械廠商告訴作者�����,進入通道后能夠與審評專家不限次數(shù)的點對點溝通,相較于一般審批程序只能有限次數(shù)的“盲對盲”溝通�,專人負責機制不僅節(jié)約了審批時間�,還能降低審評環(huán)節(jié)中因信息差導致的多次試驗成本。
不僅如此��,國家還會對創(chuàng)新醫(yī)療器械企業(yè)增設“輔導員”����。2021年4月底���,CDE發(fā)布通告明確,對于已納入創(chuàng)新�����、優(yōu)先審評通道的醫(yī)療器械��,在原溝通交流機制保持不變的基礎上��,各CDE分中心需指派“輔導員”主動服務、全程指導醫(yī)療器械注冊工作����。
1����、時長:綠通加速后�,平均1.65年完成上市���,2022年放緩至2.7年
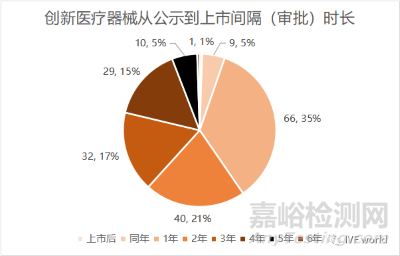
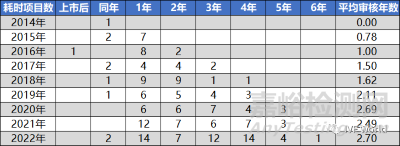
進入綠通后能提速多少呢�?基于188款已上市的創(chuàng)新醫(yī)療器械數(shù)據(jù)�����,作者用它們的上市年份減去該產(chǎn)品剛進入綠通時的公示年份�,得出該產(chǎn)品進入綠通后的審批時長��,發(fā)現(xiàn)最短的即在公示同年即完成了上市��,最長的則仍達6年之久才完成上市。
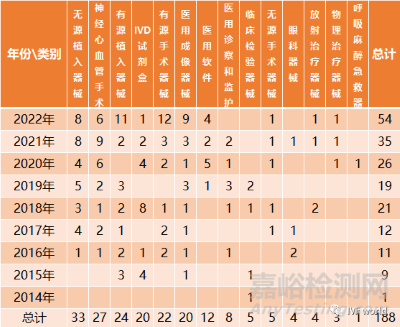
數(shù)據(jù)統(tǒng)計顯示�,創(chuàng)新醫(yī)療器械平均審評時長為1.65年��。從我們的統(tǒng)計結果看��,僅有9款創(chuàng)新醫(yī)療器械的公示年份與上市年份同年����,獲批創(chuàng)新醫(yī)療器械一半以上都在1-2年內(nèi)完成了注冊上市�����,其中33%的創(chuàng)新醫(yī)療器械在隔年完成注冊��,21%創(chuàng)新醫(yī)療器械在公示的第二年完成注冊上市。剩余37%的創(chuàng)新醫(yī)療器械注冊用時3-5年���。
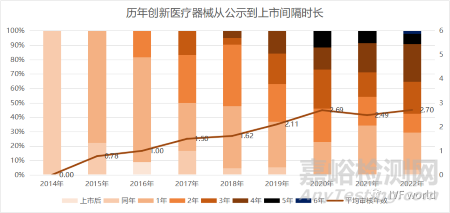
平均提速1-2年,但這個數(shù)字正在變小�����。這188款涉及153家醫(yī)療器械廠商�����,我們對其從公司創(chuàng)新醫(yī)療器械產(chǎn)品公示到其獲批上市的時間間隔以年為單位進行了統(tǒng)計。
由上圖可以看到,綠通內(nèi)平均審核的年份時長正在增加��,也就意味著綠通的加速正在放緩��。其背后原因不難推測�����,隨著中國科技水平的提升�,越來越多的創(chuàng)新項目如雨后春筍����,據(jù)統(tǒng)計CDE每年接入的創(chuàng)新醫(yī)療器械申請數(shù)正以約20%的增速�����、進入創(chuàng)新醫(yī)療器械綠色通道的數(shù)量也以約24%的增速同步增加����,無疑給監(jiān)管體系帶來了壓力����,審批排隊等待時長越來越長,也就意味著醫(yī)療器械“綠色通道”的加速度正在放緩���。
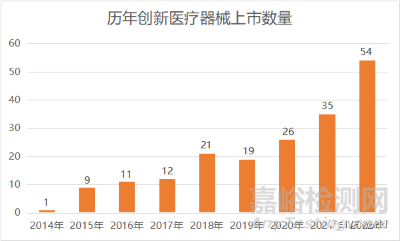
2���、年份:2022年上市55款創(chuàng)新醫(yī)療器械,位居年份最多
截至2022年12月31日�����,我們對已經(jīng)完成上市的188款創(chuàng)新醫(yī)療器械進行了整理,首先從年份維度進行了比對分析:
可以看到����,每年上市的創(chuàng)新醫(yī)療器械數(shù)量基本保持增長的趨勢��,除了在2019年上市的創(chuàng)新醫(yī)療器械數(shù)量略低于2018年����,其余年份基本都是正增長����,并在2022年達到了最高的55個。其中��,2018年的增長率最高���,一度達到了75%。
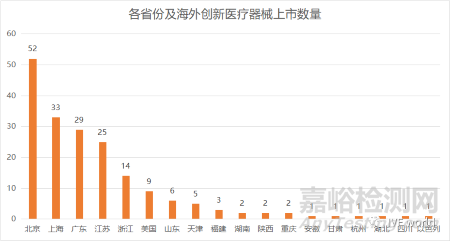
3����、地區(qū):北京已上市的創(chuàng)新醫(yī)療器械達到52款�,位居全國榜首
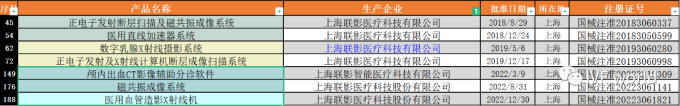
我們對這188款上市的創(chuàng)新醫(yī)療器械其注冊地址進行了分析,發(fā)現(xiàn)其中有52款產(chǎn)品都來自北京的注冊公司�����,其次是上海����、廣東和江蘇�,分別有著33款、29款和25款創(chuàng)新醫(yī)療器械上市����。
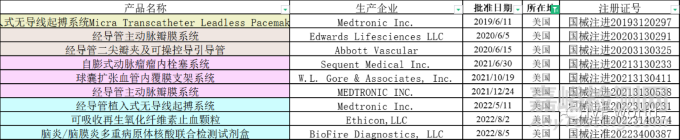
值得一提的是���,來自美國的創(chuàng)新醫(yī)療器械也有9款已經(jīng)獲得上市�����,其中Medtronic(美敦力)一家就占據(jù)了3款,而有6款產(chǎn)品是以注冊進口方式上市�����,分別如下圖:
這些創(chuàng)新醫(yī)療器械都是屬于最高監(jiān)管級別的三類醫(yī)療器械。
4�����、類型:高技術壁壘的植入類器械更容易順利成為創(chuàng)新醫(yī)療器械��,完成上市
根據(jù)中國最新的醫(yī)療器械目錄分類�,醫(yī)療器械整體可分為01 有源手術器械 02 無源手術器械 03 神經(jīng)和心血管手術器械 05 放射治療器械 06 醫(yī)用成像器械 07 醫(yī)用診察和監(jiān)護器械 08 呼吸�����、麻醉和急救器械 09 物理治療器械 09 物理治療器械 10 輸血�、透析和體外循環(huán)器械 11 醫(yī)療器械消毒滅菌器械 12 有源植入器械 13 無源植入器械 14 注輸�、護理和防護器械 15 患者承載器械 16 眼科器械 17 口腔科器械 18 婦產(chǎn)科��、輔助生殖和避孕器械 19 醫(yī)用康復器械 20 中醫(yī)器械 21 醫(yī)用軟件 22 臨床檢驗器械 以及體外診斷醫(yī)療器械總計23類�����。
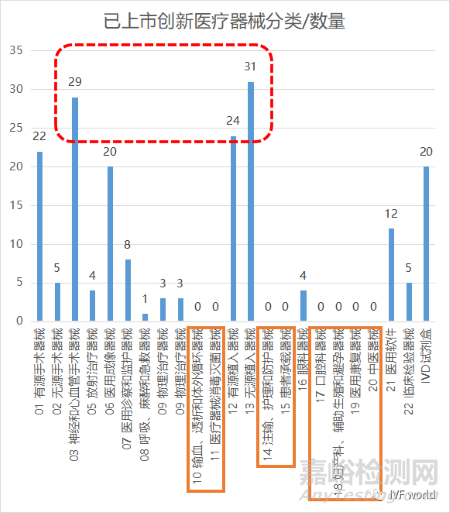
同樣對這188款已上市的創(chuàng)新醫(yī)療器械進行逐一分類�����,我們發(fā)現(xiàn)“13無源植入器械”類型的創(chuàng)新醫(yī)療器械產(chǎn)品最多����,達到了31款���,其次是“03神經(jīng)和心血管手術器械”有29款上市�����,都是屬于高技術壁壘的醫(yī)療器械�����,也能看出創(chuàng)新醫(yī)療器械的上市趨勢,更具有臨床價值和技術壁壘的產(chǎn)品更容易獲批進入市場��。
如果從器械的侵入與否來看��,植入型的創(chuàng)新醫(yī)療器械已經(jīng)有55款獲得上市�,占比所有上市創(chuàng)新醫(yī)療器械的29%����,成為最多�����!
而目前還沒有“10 輸血��、透析和體外循環(huán)器械 11 醫(yī)療器械消毒滅菌器械 14 注輸����、護理和防護器械 15 患者承載器械 17 口腔科器械 18 婦產(chǎn)科�����、輔助生殖和避孕器械 19 醫(yī)用康復器械20 中醫(yī)器械”這九大類的創(chuàng)新醫(yī)療器械產(chǎn)品上市�,具體原因此處就不做分析了��。
對每年上市的創(chuàng)新醫(yī)療器械類型再進行細化�����,可以看到隨著上市的創(chuàng)新醫(yī)療器械越來越多����,“13無源植入器械”和“03神經(jīng)和心血管手術器械”基本每年都保持著產(chǎn)品上市。(*研究統(tǒng)計中�,我們將不同注冊證書的配套使用產(chǎn)品視為獨立產(chǎn)品計數(shù))
5�、數(shù)量:微創(chuàng)集團22款創(chuàng)新醫(yī)療器械����,品馳醫(yī)療創(chuàng)新醫(yī)療器械上市比例最高
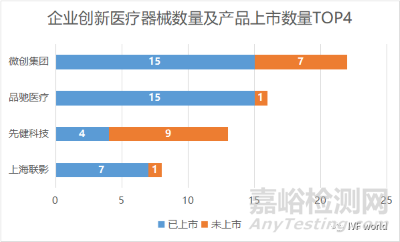
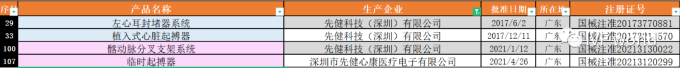
創(chuàng)新醫(yī)療器械數(shù)量最多的TOP4企業(yè)分別是微創(chuàng)集團、品馳醫(yī)療��、先健科技����、上海聯(lián)影��。
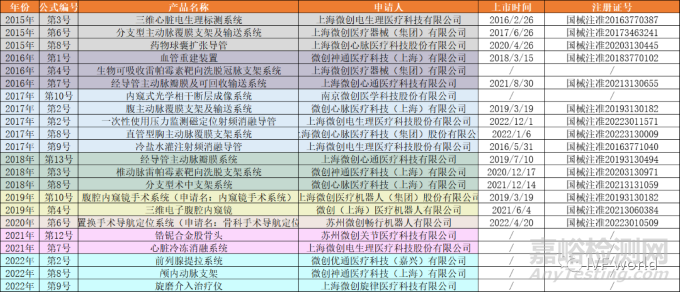
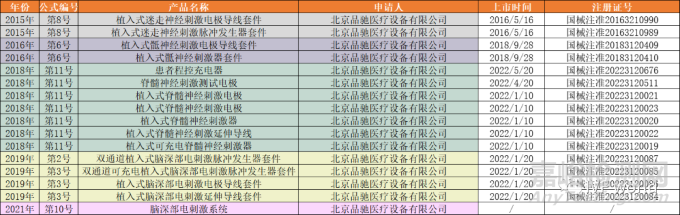
其中�,微創(chuàng)集團有22款產(chǎn)品進入了創(chuàng)新醫(yī)療器械的綠色通道��,其中有15款產(chǎn)品已經(jīng)完成上市��,它們分別是:
緊隨其后的是品馳醫(yī)療,旗下16款創(chuàng)新醫(yī)療器械也已經(jīng)有15款獲得了上市許可:
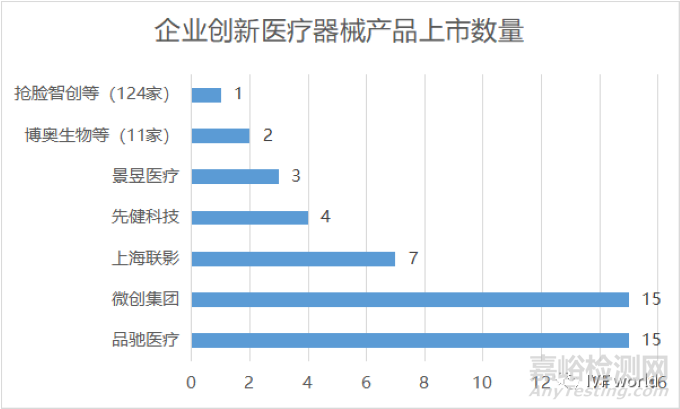
而如果從整體的企業(yè)上市創(chuàng)新醫(yī)療器械數(shù)量來看����,微創(chuàng)集團和品馳醫(yī)療仍然是異軍突起��,都實現(xiàn)了15款創(chuàng)新醫(yī)療器械上市:
從整體看��,在總計涉及153家醫(yī)療器械公司中�,我們將不同名但同一個主體集團公司的企業(yè)(如微創(chuàng)心通和微創(chuàng)心脈都屬于微創(chuàng)集團)進行并列,還剩140家公司�,而這其中,124家企業(yè)(約88%)只有一款創(chuàng)新醫(yī)療器械產(chǎn)品上市����,11家(約9%)企業(yè)名下有兩款創(chuàng)新醫(yī)療器械上市�。除此之外,就是聯(lián)影集團有7款創(chuàng)新醫(yī)療器械上市位列TOP3��,先健科技有4款上市位列TOP4����,景昱醫(yī)療3款上市為TOP5��。

四�、附錄
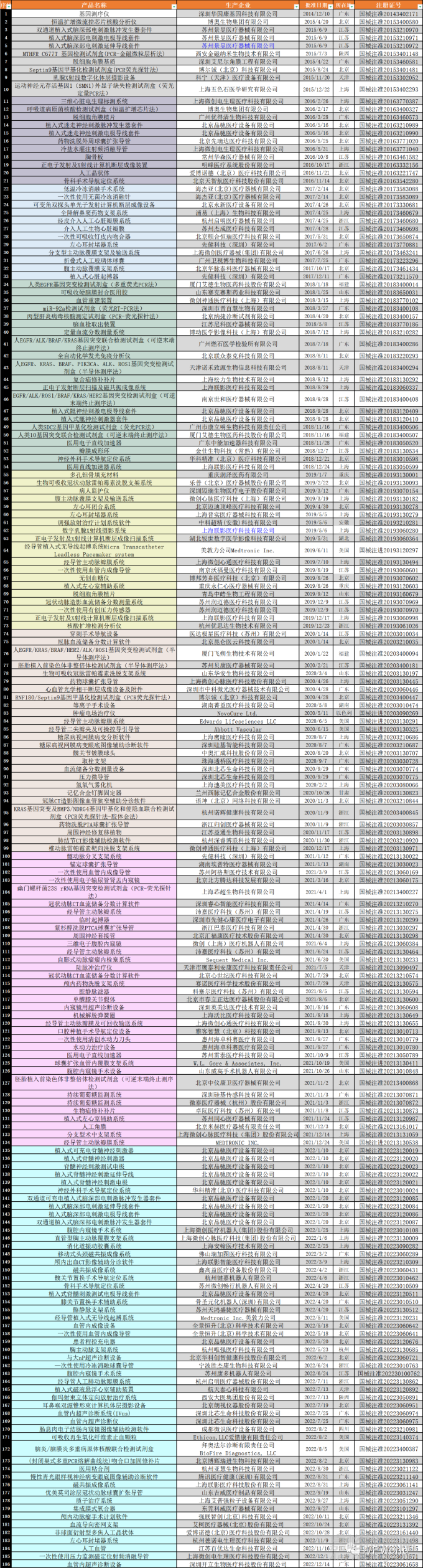
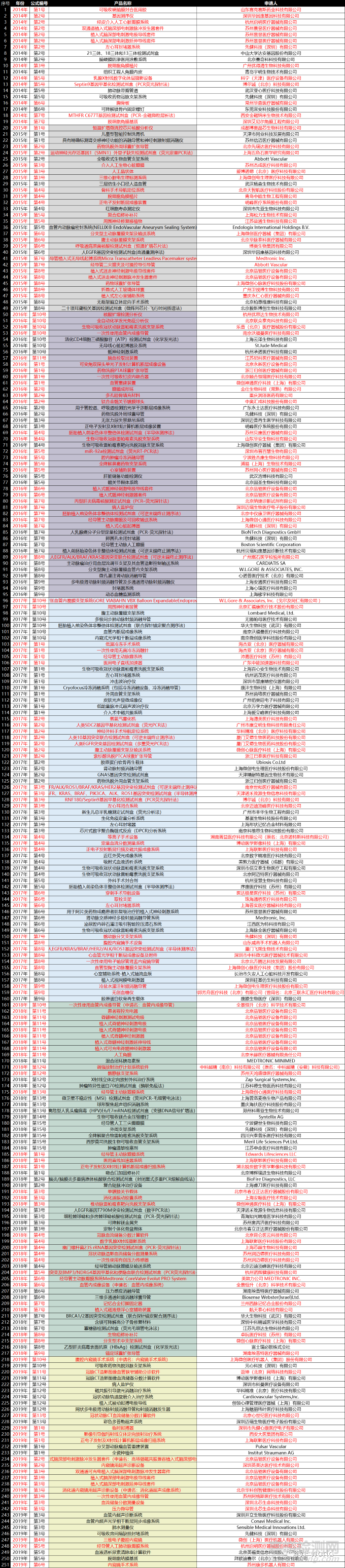
附錄1:455款創(chuàng)新醫(yī)療器械
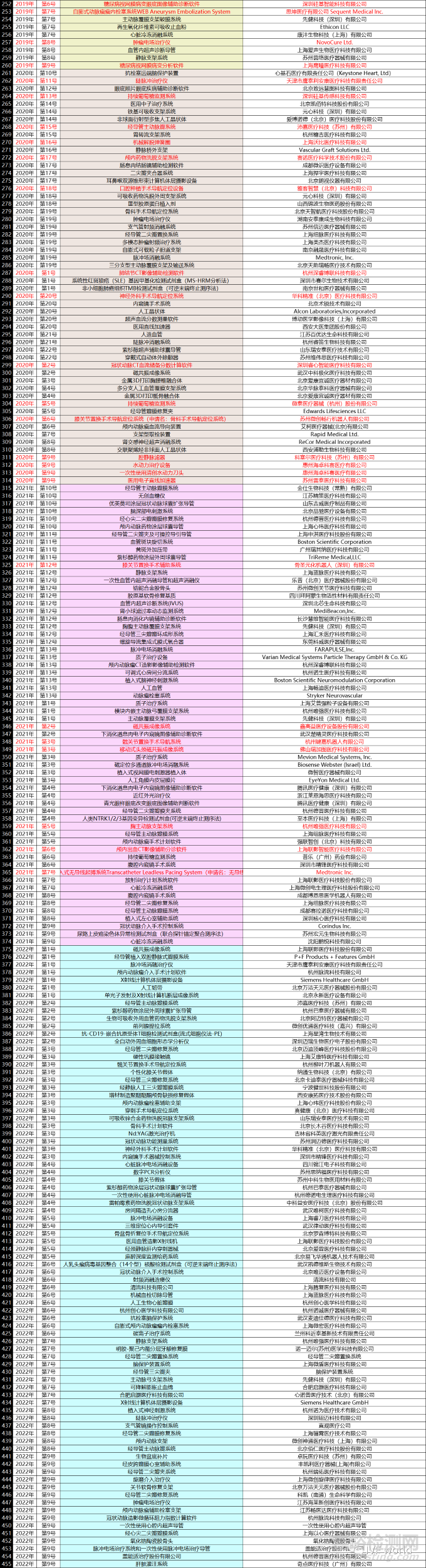
附錄2:188款已上市創(chuàng)新醫(yī)療器械