今日頭條
新元素醫(yī)藥痛風(fēng)新藥Ⅱa期臨床積極����。新元素醫(yī)藥尿酸轉(zhuǎn)運(yùn)蛋白1(URAT1)抑制劑ABP-671治療痛風(fēng)或高尿酸血癥患者的中國Ⅱa期臨床結(jié)果積極。在每天一次服用1mg ABP-671劑量組�,86%的患者sUA水平低于6mg/dL;在每天一次服用6mg和12mg ABP-671的兩個(gè)劑量組�,100%的患者sUA水平降至5mg/dL以下,且分別有57%和100%的患者sUA水平低于4mg/dL����;研究結(jié)果與此前在澳大利亞開展的Ⅱa期試驗(yàn)結(jié)果一致。
國內(nèi)藥訊
1.恒瑞PDL1單抗獲批治療小細(xì)胞肺癌。恒瑞醫(yī)藥1類新藥PD-L1單抗SHR-1316(阿得貝利單抗注射液)獲國家藥監(jiān)局批準(zhǔn)上市�,聯(lián)合化療一線治療廣泛期小細(xì)胞肺癌。發(fā)表在《柳葉刀-腫瘤學(xué)》上的Ⅲ期研究(CAPSTONE-1)結(jié)果顯示����,與化療相比,SHR-1316聯(lián)合化療一線治療顯著提高患者總生存期(中位OS:15.3個(gè)月vs12.8個(gè)月)和無疾病進(jìn)展期���,顯著降低患者疾病進(jìn)展風(fēng)險(xiǎn)33%�?���;颊叩?年生存率達(dá)31.3%(vs17.2%)。
2.默沙東九價(jià)HPV疫苗新適應(yīng)癥在華報(bào)產(chǎn)�。默沙東九價(jià)人乳頭瘤病毒(HPV)疫苗(釀酒酵母)Gardasil 9新適應(yīng)癥上市申請獲CDE受理。Gardasil 9采用三劑免疫程序���,適用于預(yù)防HPV16���、18、31�、33、45�、52和58型引起的宮頸癌����;HPV6����、11、16����、18、31���、33����、45����、52和58型引起的宮頸上皮內(nèi)瘤樣病變以及宮頸原位腺癌����;以及HPV6、11����、16�、18���、31����、33�、45、52和58型引起的持續(xù)感染����。2022年8月,國家藥監(jiān)局已批準(zhǔn)Gardasil 9由適用人群從19-26歲拓展至9-45歲適齡女性����。
3.歐康維視干眼癥新藥上II期臨床。歐康維視I類新藥OT202滴眼液正式啟動(dòng)II期臨床����,評估治療中重度干眼癥的安全性和有效性。OT-202是一款脾酪氨酸激酶(Syk)與血管內(nèi)皮生長因子受體-2雙靶點(diǎn)抑制劑���,在治療干眼癥方面可產(chǎn)生協(xié)同作用���,從而抑制炎癥反應(yīng)���。I期臨床結(jié)果顯示,OT-202在健康成人受試者中表現(xiàn)出良好的安全性和耐受性特征�。
4.創(chuàng)勝CLDN18.2免疫PET探針見刊JPA。創(chuàng)勝集團(tuán)開發(fā)的用于胃腸道腫瘤無創(chuàng)成像的靶向CLDN18.2免疫PET探針[89Zr]Zr-DFO-TST001的研究成果日前發(fā)布于期刊Journal of Pharmaceutical Analysis上���。研究顯示���,探針不僅在細(xì)胞水平上表現(xiàn)出良好的特異性,且在24到96小時(shí)內(nèi)呈現(xiàn)出快速而持續(xù)的腫瘤蓄積趨勢�。該研究為實(shí)時(shí)監(jiān)測腫瘤患者的抗體治療療效提供一種有潛力的無創(chuàng)影像工具。TST001是創(chuàng)勝集團(tuán)開發(fā)的一款CLDN18.2單抗����,正在中美兩國開展臨床試驗(yàn)。
5.聯(lián)邦RASP抑制劑獲批干眼癥臨床�。聯(lián)邦制藥1類新藥TUL12101滴眼液獲國家藥監(jiān)局臨床試驗(yàn)?zāi)驹S可�,擬開發(fā)用于干眼的治療。TUL12101是新一代小分子活性醛(RASP)抑制劑����。RASP是炎癥的前細(xì)胞因子介質(zhì)�,通過與蛋白質(zhì)上的硫醇和胺殘基結(jié)合�,增強(qiáng)細(xì)胞因子釋放,激活炎性小體����。TUL12101通過可共價(jià)結(jié)合游離醛并降低過量的RASP水平,降低眼部活性醛的含量和緩解炎癥反應(yīng)���。
國際藥訊
1.禮來CDK4/6抑制劑獲批擴(kuò)大使用人群�。禮來CDK4/6抑制劑阿貝西利獲FDA批準(zhǔn)擴(kuò)大適應(yīng)癥����,聯(lián)合內(nèi)分泌治療(ET)用于HR+/HER2-、淋巴結(jié)陽性�、高復(fù)發(fā)風(fēng)險(xiǎn)的早期乳腺癌成年患者的輔助治療。阿貝西利是首個(gè)獲批用于乳腺癌輔助治療的CDK4/6抑制劑����,F(xiàn)DA已于2021年批準(zhǔn)阿貝西利聯(lián)合ET方案,用于輔助治療HR+/HER2-�、淋巴結(jié)陽性、高復(fù)發(fā)風(fēng)險(xiǎn)且Ki-67≥20%早期乳腺癌患者���。
2.GSK佐劑RSV疫苗獲FDA推薦批準(zhǔn)����。FDA疫苗與相關(guān)生物制品產(chǎn)品咨詢委員會(huì)(VRBPAC)推薦批準(zhǔn)葛蘭素史克呼吸道合胞病毒(RSV)疫苗RSVPreF3 OA上市,用于預(yù)防60歲及以上成人因RSV引起的下呼吸道疾病����。RSVPreF3 OA由RSV融合前F糖蛋白(RSVPreF3)與佐劑組成。在Ⅲ期臨床AReSVi-006中���,該疫苗在≥60歲老年人中的保護(hù)效力達(dá)到82.6%(96.95% CI:57.9-94.1)���。歐盟和日本監(jiān)管部門已受理該疫苗的上市申請。
3.Checkpoint公司PD-L1單抗報(bào)BLA�。Checkpoint公司PD-L1抗體cosibelimab的生物制品許可申請(BLA)獲FDA受理,用于治療轉(zhuǎn)移性或局部晚期皮膚鱗狀細(xì)胞癌(cSCC)患者����。PDUFA日期為2024年1月3日。在臨床試驗(yàn)中����,cosibelimab在轉(zhuǎn)移性cSCC患者中達(dá)到47.4%(95% CI:36.0, 59.1)的客觀緩解率(ORR);在晚期cSCC患者中ORR為54.8%(95% CI:36.0, 72. 7)����。cSCC是美國第二大常見的皮膚癌類型,每年發(fā)病患者達(dá)180萬例�。
4.VMAT2抑制劑治療TD長期療效積極。Neurocrine公司VMAT2抑制劑Ingrezza(valbenazine)治療遲發(fā)性運(yùn)動(dòng)障礙(TD)年長患者的最新結(jié)果積極�。Ingrezza旨在通過減少多巴胺量來調(diào)節(jié)TD患者的神經(jīng)信號。48周治療數(shù)據(jù)顯示���,在≥65歲的患者中����,達(dá)成異常不自主運(yùn)動(dòng)量表(AIMS)反應(yīng)改善≥50%的患者比例超過80%���。詳細(xì)數(shù)據(jù)將公布于2023年美國老年精神病學(xué)協(xié)會(huì)(AAGP)年會(huì)當(dāng)中����。
5.HPV DNA疫苗III期臨床積極����。Inovio公司DNA治療性疫苗VGX-3100(ABC-3100)治療成年女性中高危型HPV-16/18感染相關(guān)的宮頸高級別鱗狀上皮內(nèi)病變(HSIL)的III期臨床(Reveal 2)數(shù)據(jù)積極。匯總分析顯示�,在所有研究人群中,VGX-3100組和安慰劑組達(dá)到主要終點(diǎn)的患者比例分別為25.0%和9.8%(p<0.001)�;在生物標(biāo)志物陽性患者中,兩組這一數(shù)值分別為54.4%和12.5%(p<0.001)。臨床中����,沒有與治療相關(guān)的嚴(yán)重不良事件。北京東方略擁有該藥的中國權(quán)益����。
6.氨甲蝶呤玻璃體內(nèi)注射配方報(bào)NDA。Aldeyra公司非復(fù)合型的氨甲蝶呤玻璃體內(nèi)注射配方ADX-2191(methotrexate injection)的新藥申請(NDA)獲FDA受理���,用以治療原發(fā)性玻璃體視網(wǎng)膜淋巴瘤���。FDA同時(shí)授予其優(yōu)先審評資格。PDUFA日期為今年6月21日����。去年10月,ADX-2191在治療增生性玻璃體視網(wǎng)膜病變的Ⅲ期臨床GUARD達(dá)到主要終點(diǎn)����,與歷史對照組(無治療例行手術(shù)治療)相比����,ADX-2191顯著降低患者的視網(wǎng)膜脫落情形(P=0.024)����;且藥物總體耐受性良好�。
醫(yī)藥熱點(diǎn)
1.安徽省首家醫(yī)療機(jī)構(gòu)“生物銀行”獲批����。近日�,安徽省婦幼保健院(合肥市婦幼保健院)生物樣本庫順利獲批中國人類遺傳資源保藏行政許可�,成為安徽省首家獲得行政許可的,擁有生物樣本庫的醫(yī)療衛(wèi)生機(jī)構(gòu)����。樣本庫主要面向母嬰自然人群、妊娠高血壓����、妊娠糖尿病、不良生育史的夫婦���,以及兒童罕見病和婦科腫瘤患者等����,能為相關(guān)疾病的臨床研究提供科研材料,為疾病早期的實(shí)驗(yàn)技術(shù)提供支持����。
2.全國政協(xié)委員曹菲建議醫(yī)院設(shè)置上門看診。2023年全國“兩會(huì)”召開����,政協(xié)委員曹菲建議“醫(yī)院設(shè)置上門看診,協(xié)助設(shè)置家庭病房���;社區(qū)建立24小時(shí)響應(yīng)體系�,搭建護(hù)工(每天4-6次)����、護(hù)士(每周一次)、醫(yī)生(雙休或每月一次)三層級分時(shí)不同頻度的巡視的體系����;制定相應(yīng)標(biāo)準(zhǔn),完善居家養(yǎng)老設(shè)施”���。
3.張文宏呼吁進(jìn)一步加強(qiáng)社區(qū)醫(yī)衛(wèi)體系建設(shè)���。3月4日����,全國政協(xié)十四屆一次會(huì)議首場“委員通道”集體采訪舉行����。全國政協(xié)委員張文宏教授在接受采訪時(shí)呼吁,我國目前已進(jìn)入疫情舒緩階段����,國家應(yīng)繼續(xù)強(qiáng)化基層醫(yī)療衛(wèi)生體系�。他期待未來三級醫(yī)院既能賦能基層醫(yī)療衛(wèi)生機(jī)構(gòu),又能與之相互分級����、分層、分流�,打造出一個(gè)上下聯(lián)動(dòng)、平急轉(zhuǎn)換�,既有彈性又有韌性的醫(yī)療衛(wèi)生體系。
4.全球藥企TOP10名單出爐����。隨著2022年財(cái)報(bào)的披露,全球TOP10藥企排名正式出爐�。按照公司總收入,全球藥企TOP10分別為輝瑞���、強(qiáng)生���、羅氏、默沙東����、艾伯維、拜耳���、諾華�、BMS����、賽諾菲和阿斯利康。按照制藥業(yè)務(wù)收入���,全球藥企TOP10分別為輝瑞���、艾伯維、強(qiáng)生�、默沙東���、諾華、羅氏����、BMS、阿斯利康�、賽諾菲和GSK。按照公司市值�,全球藥企TOP10分別為強(qiáng)生、諾和諾德�、禮來�、默沙東、艾伯維����、羅氏、輝瑞����、阿斯利康、諾華和BMS�。
評審動(dòng)態(tài)
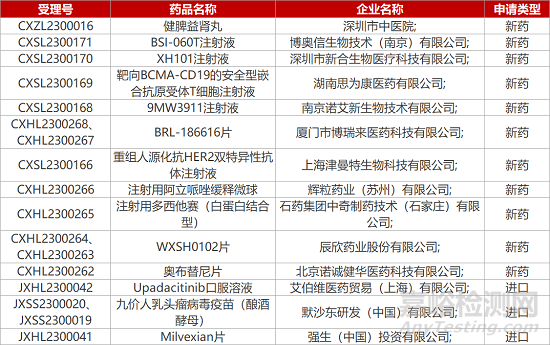
1. CDE新藥受理情況(03月04日)
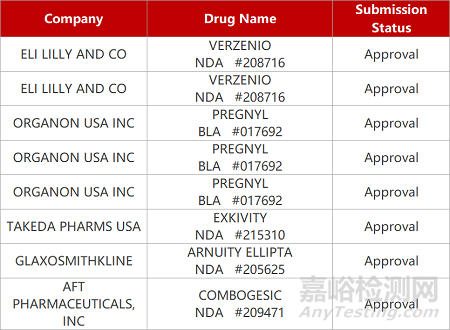
2. FDA新藥獲批情況(北美03月03日)