近日����,澳大利亞TGA更新了部分醫(yī)療器械重新分類(lèi)的指南,該指南旨在幫助作為引入體內(nèi)物質(zhì)的醫(yī)療器械的制造商履行其義務(wù)����,并概述了過(guò)渡期安排,以幫助遵守新法規(guī)����。
新法規(guī)涵蓋的醫(yī)療器械
新法規(guī)涵蓋的醫(yī)療器械范圍如下:
適用于通過(guò)孔口引入體內(nèi)的器械:那些在應(yīng)用時(shí)傾向于局部分散并依靠其固有的物理或機(jī)械性能來(lái)執(zhí)行其治療功能的器械。雖然其中一些裝置在配方和物理屬性上可能與藥品相似�����,但重要的區(qū)別在于它們不能通過(guò)藥理學(xué)�����,代謝或免疫學(xué)手段實(shí)現(xiàn)其主要預(yù)期作用。
適用于涂抹在皮膚上并被皮膚吸收的物質(zhì):傾向于能夠被局部吸收的物質(zhì)����。通過(guò)全身吸收起作用的物質(zhì)通常是藥物,盡管為了安全起見(jiàn)�����,應(yīng)該考慮能夠被全身吸收的物質(zhì)��。
以下器械不在本法規(guī)范圍內(nèi):
旨在通過(guò)穿透(通常不會(huì)局部分散)并且依賴(lài)外部作用或操作來(lái)實(shí)現(xiàn)其預(yù)期目的的身體孔口來(lái)使用的侵入性醫(yī)療器械(例如�����,壓舌器����,牙科印模材料或胃內(nèi)球囊)。
外科侵入性醫(yī)療器械(例如手術(shù)器械��、可吸收縫線)
制造商打算用于接觸受損皮膚或未被吸收的粘膜的非侵入性醫(yī)療器械(例如傷口敷料)
ARTG過(guò)渡期安排
① 2021年11月25日之前已納入ARTG的醫(yī)療器械
如果制造商的醫(yī)療器械由擬通過(guò)身體孔口進(jìn)入人體或在ARTG中應(yīng)用于皮膚的物質(zhì)組成��,且開(kāi)始日期為2021年11月25日之前��,則會(huì)做出過(guò)渡安排��,以確保可以在根據(jù)新分類(lèi)申請(qǐng)將其納入ARTG時(shí)繼續(xù)在澳大利亞市場(chǎng)供應(yīng)�����。
如果制造商需要繼續(xù)向澳大利亞供應(yīng)醫(yī)療器械�����,則必須:
通知TGA:2022年5月25日之前�����,您有一個(gè)需要重新分類(lèi)的器械申請(qǐng)納入ARTG�����。
提交申請(qǐng):在2024年11月1日之前����,您的器械將以正確的分類(lèi)納入ARTG中����。
② 2021年11月25日之前提交的將醫(yī)療器械納入ARTG的申請(qǐng)
如果制造商已在ARTG中提交了一份醫(yī)療器械的申請(qǐng),該醫(yī)療器械由通過(guò)身體孔口進(jìn)入人體或應(yīng)用于皮膚的物質(zhì)組成��,則TGA將對(duì)制造商的器械申請(qǐng)進(jìn)行評(píng)估,并根據(jù)舊的分類(lèi)規(guī)則將該器械納入ARTG��。
要獲得根據(jù)新分類(lèi)規(guī)則對(duì)器械進(jìn)行重新分類(lèi)的過(guò)渡安排的資格�����,制造商必須:
通知TGA:您有一個(gè)需要重新分類(lèi)的器械申請(qǐng)納入ARTG�����,以較晚的日期為準(zhǔn):
— 2022年5月25日前
— 自ARTG項(xiàng)目開(kāi)始之日起2個(gè)月內(nèi)
提交申請(qǐng):在2024年11月1日之前����,您的器械將以正確的分類(lèi)納入ARTG中。
如果制造商沒(méi)有在2022年5月25日之前或在您的ARTG項(xiàng)目開(kāi)始日期(以較晚的日期為準(zhǔn))的兩個(gè)月內(nèi)通知TGA并申請(qǐng)通過(guò)以新分類(lèi)規(guī)則將器械納入ARTG中�����,制造商將不再有資格獲得過(guò)渡安排:
從2022年5月25日起停止供應(yīng)您的器械
取消ARTG納入的資格
如果制造商在到期日之前通知TGA�����,但沒(méi)有在2024年11月1日之前提交將納入ARTG的正確分類(lèi)申請(qǐng)��,則必須:
從2024年11月1日起停止供應(yīng)器械
取消ARTG納入的資格
③ 2021年11月25日或之后在ARTG中加入新醫(yī)療器械的申請(qǐng)
2021年11月25日或之后提交給TGA的任何尚未包含在ARTG中的新器械��,必須根據(jù)新的分類(lèi)規(guī)則使用正確的分類(lèi)進(jìn)行提交ARTG納入申請(qǐng)。
如果制造商需要繼續(xù)在澳大利亞市場(chǎng)上銷(xiāo)售醫(yī)療器械����,則必須在2024年11月1日之前提交申請(qǐng),以將其納入ARTG�����,以根據(jù)新的分類(lèi)規(guī)則進(jìn)行正確的器械分類(lèi)�����。
如果制造商在此日期之前提交了申請(qǐng)����,但TGA尚未完成��,則可以繼續(xù)使用現(xiàn)有的ARTG條目提供器械�����,直到TGA對(duì)制造商的納入申請(qǐng)做出決定��。
如何提交重新分類(lèi)申請(qǐng)
1. 從eBS門(mén)戶中的菜單創(chuàng)建"New Device Appliacation"
2. 從提供的第一個(gè)下拉列表中選擇"Medical Device - Included"
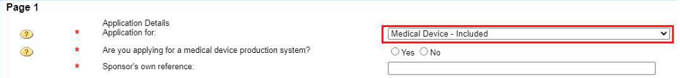
3. 選擇"Reclassify an existing register entry"選項(xiàng)
4. 搜索要重新分類(lèi)的ARTG編號(hào):例如130099(僅示例)
5. 點(diǎn)擊"Clone"按鈕�����。
6. 允許系統(tǒng)將與ARTG條目相關(guān)的信息克隆到應(yīng)用程序中
7. 從"New classification"提供的下拉列表中選擇新分類(lèi)






