摘要:與傳統(tǒng)注射劑和口服制劑相比,透皮貼劑具有避免首過(guò)消除效應(yīng)���、維持穩(wěn)定的血藥濃度以及提高患者的用藥依從性等許多優(yōu)勢(shì)�����,其研發(fā)和產(chǎn)業(yè)化發(fā)展近年來(lái)受到了廣泛的關(guān)注����,但經(jīng)皮吸收這一過(guò)程的存在使得透皮貼劑的生物利用度難以達(dá)到臨床要求����。因此,如何改善藥物的經(jīng)皮滲透以及如何評(píng)價(jià)藥物的體外滲透成為透皮貼劑開(kāi)發(fā)的關(guān)鍵和難點(diǎn)��。本文結(jié)合國(guó)內(nèi)外相關(guān)文獻(xiàn)將現(xiàn)階段透皮貼劑的促透方法及其機(jī)制進(jìn)行歸納�,為開(kāi)發(fā)新的促透方法,提高藥物的生物利用度提供思路����;同時(shí)總結(jié)了體外滲透試驗(yàn)主要方法及常用皮膚模型、用于體外滲透分析的成像技術(shù)等�����,為解決目前關(guān)于透皮貼劑滲透性存在的諸多問(wèn)題與挑戰(zhàn)�,制定更為完善的關(guān)于透皮貼劑滲透性的要求和標(biāo)準(zhǔn)提供參考。
貼劑系指原料藥物與適宜的材料制成的供貼敷在皮膚上的�,可產(chǎn)生全身性或局部作用的一種薄片狀柔性制劑,可用于完整皮膚表面�����,也可用于有疾患或不完整的皮膚表面��,其中用于完整皮膚表面能將藥物輸送透過(guò)皮膚進(jìn)入血液循環(huán)系統(tǒng)起全身作用的貼劑稱為透皮貼劑[1]����。透皮貼劑起源于美國(guó)1979年上市的東莨菪堿透皮貼劑(商品名:Transderm Scop®),此后�,尼古丁、可樂(lè)定��、雌二醇等的透皮貼劑產(chǎn)品陸續(xù)上市����。與傳統(tǒng)注射劑和口服制劑相比��,透皮貼劑具有許多顯著優(yōu)勢(shì)[2]��,例如:①可避免肝臟的首過(guò)消除效應(yīng)�����,提高治療效率�;②避免藥物對(duì)胃腸道的刺激�����;③維持穩(wěn)定的血藥濃度����,從而降低毒副作用的發(fā)生;④減少給藥次數(shù)�����,提高患者的用藥依從性�,特別適合嬰兒、老人以及有昏迷等情況的患者�;⑤出現(xiàn)問(wèn)題可及時(shí)中斷給藥等。
對(duì)于透皮貼劑及其他經(jīng)皮給藥制劑來(lái)說(shuō),皮膚都是一道難以透過(guò)的屏障����,皮膚致密的角質(zhì)層結(jié)構(gòu)的存在����,使大部分藥物不能被吸收進(jìn)入體內(nèi),而被滯留在皮膚內(nèi)��,生物利用度達(dá)不到臨床要求��。經(jīng)皮吸收這一過(guò)程的存在也使得傳統(tǒng)的藥物釋放方法并不完全適用于透皮貼劑等經(jīng)皮給藥制劑��。因此���,如何改善藥物的經(jīng)皮滲透以及如何評(píng)價(jià)藥物的體外滲透成為透皮貼劑開(kāi)發(fā)的關(guān)鍵和難點(diǎn)��。
1�����、皮膚的構(gòu)造和生理功能
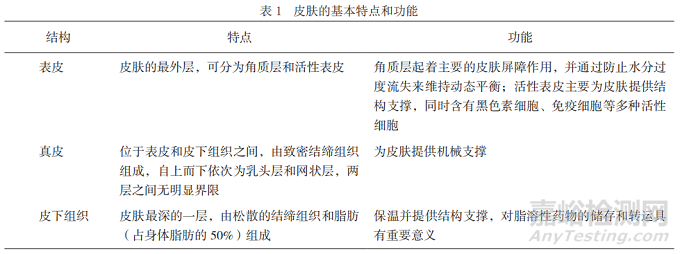
人體最大的器官就是皮膚���,約占體重的15%,抵御外源性暴露的屏障特性和維持動(dòng)態(tài)平衡是皮膚的兩大主要功能。皮膚可分為表皮�����、真皮和皮下組織���,是一個(gè)復(fù)雜的多層結(jié)構(gòu)體���,盡管皮膚在整個(gè)身體結(jié)構(gòu)上是連續(xù)的,但根據(jù)個(gè)體的年齡和解剖部位不同���,皮膚的厚度也會(huì)有所不同���,皮膚各層的基本特點(diǎn)和功能見(jiàn)表1[3]。
2��、 透皮貼劑中藥物促滲方法
藥物作為外源性物質(zhì)��,需要通過(guò)經(jīng)皮吸收才能進(jìn)入體內(nèi)�����,由于皮膚屏障的存在�����,特別是角質(zhì)層的存在,大多數(shù)藥物無(wú)法直接透過(guò)皮膚進(jìn)入體內(nèi)�,在生物利用度上透皮貼劑很難與其他制劑相同,這就在一定程度上限制了它的發(fā)展����,為了擴(kuò)展用藥范圍����,誕生了許多促透方法。
2.1 物理方法
常用的物理促透方法包括電穿孔����、離子導(dǎo)入法以及超聲導(dǎo)入法。電穿孔是通過(guò)電脈沖使細(xì)胞膜等脂質(zhì)雙分子層形成暫時(shí)�����、可逆的親水性孔道���,藥物經(jīng)過(guò)孔道進(jìn)入皮膚而被吸收的技術(shù)[4]��;離子導(dǎo)入是通過(guò)電位差��,使藥物通過(guò)電滲流移動(dòng)����,不破壞皮膚屏障[5];超聲導(dǎo)入法是指利用超聲波的能量使藥物透過(guò)皮膚��,可實(shí)現(xiàn)在短時(shí)間內(nèi)增加藥物透皮吸收[6]�。Vaidya等[7]自制了甲氨蝶呤貼劑,比較了甲氨蝶呤貼劑與3種物理促滲方法(超聲導(dǎo)入��、電穿孔和冷激光)相結(jié)合后的滲透情況���,依次是超聲導(dǎo)入>電穿孔>冷激光��,相關(guān)藥效學(xué)試驗(yàn)也表明在類風(fēng)濕性關(guān)節(jié)炎的治療中��,使用超聲導(dǎo)入作為促滲技術(shù)配合甲氨蝶呤貼劑有著更為顯著的效果�����。
2.2 化學(xué)滲透促進(jìn)劑
化學(xué)滲透促進(jìn)劑是透皮貼劑常用的促透方法�����,原理一般是削弱角質(zhì)層的屏障作用從而增強(qiáng)藥物的滲透能力�����?�;瘜W(xué)滲透促進(jìn)劑可以進(jìn)入到角質(zhì)層�,并與其成分相互作用,暫時(shí)降低角質(zhì)層的屏障作用����,而不會(huì)對(duì)細(xì)胞造成重大損害。另一方面����,化學(xué)滲透促進(jìn)劑也可以改變配方的性質(zhì)以促進(jìn)藥物滲透�����。第一個(gè)專門用來(lái)作為化學(xué)滲透促進(jìn)劑而設(shè)計(jì)的化合物是月桂氮卓酮�����,于1976年獲得專利���。理想的化學(xué)滲透促進(jìn)劑應(yīng)具備以下條件[8]:①特異性(增加藥物的滲透性�����,而不在體內(nèi)有其他藥理活性)���;②無(wú)毒性�����、無(wú)刺激性���、無(wú)過(guò)敏性;③起效快�����、去除后角質(zhì)層能恢復(fù)其屏障作用����;④不對(duì)內(nèi)源性物質(zhì)造成損傷;⑤與藥物和配方輔料相容��。按照促透劑的結(jié)構(gòu)�,可將化學(xué)滲透促進(jìn)劑分為亞砜類、脂肪酸類及其酯類���、酰胺類��、醇類���、表面活性劑等��。常見(jiàn)化學(xué)滲透促進(jìn)劑及其應(yīng)用藥物見(jiàn)表2[9]�����。
2.3 新型載體的應(yīng)用
使用物理方法促進(jìn)藥物滲透��,患者依從性較差�����,成本昂貴;促滲劑的使用可能會(huì)引起皮膚刺激和皮膚損傷�����,而通過(guò)制劑技術(shù)研究的新型載體可以提高藥物的溶解度���、改變藥物的結(jié)構(gòu)或者使用特定結(jié)構(gòu)包裹藥物�����,從而增強(qiáng)藥物透過(guò)皮膚能力的性能�,使更多的藥物能夠開(kāi)發(fā)成透皮貼劑。常見(jiàn)的透皮貼劑載體主要有立方納米載體���、脂質(zhì)體����、微針等����。
立方納米載體是由單油酸甘油酯構(gòu)成的納米顆粒,具有晶格膜結(jié)構(gòu)��,穩(wěn)定性高���。立方納米載體促進(jìn)藥物滲透的機(jī)制可能是它可以擾亂皮膚角質(zhì)層結(jié)構(gòu)的有序性�����,提高皮膚角質(zhì)層流動(dòng)性[10]���。另外���,立方納米載體與皮膚的結(jié)構(gòu)相似,皮膚中也可能存在完整結(jié)構(gòu)的立方納米載體�����,并在藥物經(jīng)皮吸收中發(fā)揮重要作用���,所以立方納米載體促進(jìn)藥物滲透很可能依賴于整個(gè)載體的“攜帶”作用[11]���。Salah等[12]構(gòu)建了一種依托度酸立方納米載體,通過(guò)經(jīng)皮給藥途徑在靶點(diǎn)提供穩(wěn)定的依托度酸濃度�,持續(xù)時(shí)間更長(zhǎng),給藥頻率低�,具有良好的控釋性,與口服給藥相比����,依托度酸立方納米載體提高了依托度酸的生物利用度�。Mohyeldin等[13]以黃體酮為模型藥物,制備了4種納米載體:立方納米載體��、納米脂質(zhì)體��、納米乳劑和納米膠束,并采用Franz擴(kuò)散池進(jìn)行了體外皮膚滲透���,證明了與其他納米載體相比���,立方納米載體具有較高的經(jīng)皮滲透能力,同時(shí)通過(guò)激光共聚焦掃描顯微鏡和組織病理學(xué)發(fā)現(xiàn)立方納米載體能夠穿透整個(gè)皮膚層且具有良好的生物相容性�����。
脂質(zhì)體是由兩親分子組成的具有雙層構(gòu)象的囊泡�,具有較高的親水性和親脂性、無(wú)毒可生物降解并且容易大規(guī)模制備�����,類似于生物膜�����,主要成分通常是磷脂��。脂質(zhì)體是改善難溶性和大分子藥物經(jīng)皮遞送的有利載體�����,脂質(zhì)體的表面電荷、膜流動(dòng)性和脂質(zhì)組成等會(huì)對(duì)藥物的經(jīng)皮滲透造成影響����,但傳統(tǒng)脂質(zhì)體通常容易聚集在角質(zhì)層,無(wú)法穿透完整的皮膚��,可考慮制成可變形脂質(zhì)體如醇質(zhì)體���、轉(zhuǎn)移體等促進(jìn)其經(jīng)皮滲透�。此外�,還可考慮將物理促透方法如離子導(dǎo)入等與脂質(zhì)體結(jié)合,為透過(guò)皮膚屏障提供驅(qū)動(dòng)力[14]���。Salimi等[15]將脂質(zhì)體作為利斯的明經(jīng)皮給藥系統(tǒng)的載體��,采用薄膜水化法和超聲法制備了50~150 nm的利斯的明脂質(zhì)體并進(jìn)行了處方優(yōu)化���,優(yōu)化后的利斯的明脂質(zhì)體在外用48 h后有90%以上的藥物通過(guò)皮膚,并且由于脂雙層的存在對(duì)藥物釋放有阻隔作用���,可實(shí)現(xiàn)在較長(zhǎng)時(shí)間內(nèi)釋放利斯的明���。Abd El-Alim等[16]開(kāi)發(fā)了2種二氟尼柳經(jīng)皮納米囊泡載體:醇質(zhì)體和轉(zhuǎn)移體,并與傳統(tǒng)脂質(zhì)體進(jìn)行了比較�,結(jié)果表明,二氟尼柳的2種載體在皮膚滲透時(shí)有著顯著的優(yōu)越性�����,并且分布更廣�,表現(xiàn)出顯著的治療疼痛和抗炎作用,被認(rèn)為是二氟尼柳經(jīng)皮給藥有希望的載體����。
微針穿透皮膚角質(zhì)層進(jìn)入皮膚后可形成微小孔道,藥物通過(guò)這些微小孔道進(jìn)入皮膚��,從而達(dá)到促進(jìn)經(jīng)皮滲透的效果��。Lopez-Ramirez等[17]構(gòu)建了一種主動(dòng)微針遞送平臺(tái)�,采用加載在微針貼片中一種金屬微粒作為引擎,實(shí)現(xiàn)更深�����、更快的皮膚遞送��。他們也提出了一種雙作用組合可編程微針貼片,與傳統(tǒng)微針貼片相比���,該組合貼片可在幾分鐘內(nèi)更快地傳遞藥物并且釋放可調(diào)節(jié)[18]����。微針在突破皮膚屏障的同時(shí)極大地減輕了患者給藥時(shí)的痛苦����,在促進(jìn)藥物透皮吸收領(lǐng)域中的應(yīng)用越來(lái)越廣泛,但仍有一些問(wèn)題需要解決�����,例如微針是否能滯留在皮膚里以及滯留的時(shí)間長(zhǎng)短���、對(duì)皮膚的刺激較大��、可能發(fā)生過(guò)敏反應(yīng)等[19]����。
3�、 透皮貼劑的體外滲透試驗(yàn)
體外滲透試驗(yàn)是為了模擬藥品在生理?xiàng)l件下的透皮過(guò)程,以部分地反映藥品的質(zhì)量與臨床治療的有效性��,是透皮貼劑質(zhì)量控制中的重要一環(huán),開(kāi)發(fā)合理的體外滲透性檢測(cè)方法也是透皮貼劑質(zhì)量評(píng)價(jià)過(guò)程中的重要內(nèi)容��。目前透皮貼劑體外滲透試驗(yàn)主要方法是Franz擴(kuò)散池法�。
3.1 常用擴(kuò)散池的種類
目前用于體外滲透試驗(yàn)的擴(kuò)散池有靜態(tài)擴(kuò)散池和動(dòng)態(tài)擴(kuò)散池兩種��。靜態(tài)擴(kuò)散池包括立式擴(kuò)散池和水平式擴(kuò)散池�,均由供給室、接收室��、取樣口�����、溫度控制夾套和攪拌裝置五部分組成��。立式擴(kuò)散池一般指Franz擴(kuò)散池(Franz Diffusion Cell)����,是體外滲透試驗(yàn)的常用裝置,該裝置中供給室和接收室上下對(duì)合而成���,上層為供給室���,下層為接收室���,兩室之間用合成膜、動(dòng)物皮膚或人的皮膚隔開(kāi)���,接收室的接收介質(zhì)恰好與合成膜或者皮膚的真皮層接觸�����,接收室中存在的攪拌裝置以一定速率攪拌接收介質(zhì)�����,使藥物與接收介質(zhì)能夠混合充分[20]�����。水平式擴(kuò)散池一般指Vilia-Chien擴(kuò)散池(Vilia-ChienDiffusion Cell)���,供給室和接收室由左右兩個(gè)對(duì)稱的玻璃半室組成,均有溫度控制夾套和攪拌裝置以保證兩室的溫度和攪拌速度相同�����,常用于藥物在皮膚中的擴(kuò)散系數(shù)和滲透系數(shù)的測(cè)定[21]��。動(dòng)態(tài)擴(kuò)散池一般指流通式擴(kuò)散池(Flow Through Cell),由供給室�����、接收室和泵組成�����,泵的存在可以實(shí)現(xiàn)接收室內(nèi)介質(zhì)的持續(xù)流動(dòng)��,優(yōu)化漏槽條件的同時(shí)可以更好地模擬皮膚內(nèi)的微環(huán)境��,對(duì)于溶解度較低的樣品具有重要意義[22]���。
此外,還可以采用MIVO®(Multi In Vitro OrganDevice)等新型的流體動(dòng)力學(xué)平臺(tái)進(jìn)行體外滲透試驗(yàn)�����。MIVO®是一種一次性細(xì)胞培養(yǎng)室�,能夠在生理?xiàng)l件下容納活組織(細(xì)胞層、3D重建組織等)或人造膜�,進(jìn)行體外滲透試驗(yàn)時(shí)可用皮膚或皮膚代替物將該系統(tǒng)隔成供給室、接收室�,接收室連接可引起單向流動(dòng)的蠕動(dòng)泵�,同時(shí)可設(shè)置合適的流速模擬真實(shí)的生理?xiàng)l件[23]�����。
3.2 皮膚模型的選擇
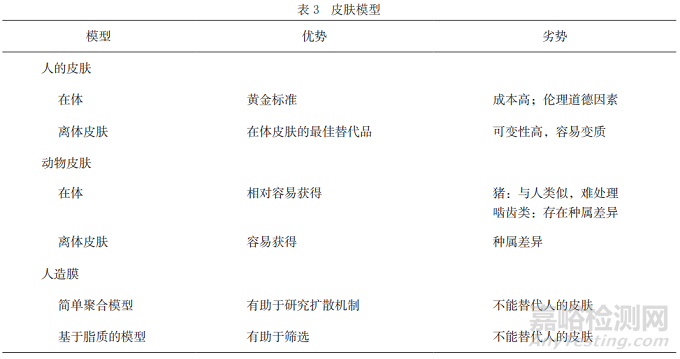
體外滲透是評(píng)價(jià)透皮貼劑的一個(gè)重要方面�����,如果藥物是為了給人類使用�����,體外滲透試驗(yàn)最合適的皮膚模型就是人體皮膚�����。但是�����,由于道德或者經(jīng)濟(jì)方面的原因��,特別是在藥物研發(fā)的早期階段�����,這幾乎是不可能的。因此����,找到與人類皮膚接近的代用品是非常必要的。表3[24]列出了一些常用于評(píng)價(jià)藥物體外滲透的皮膚模型��。
目前���,常使用動(dòng)物皮膚模型來(lái)評(píng)估藥物的體外滲透����,這些動(dòng)物主要包括豬�����、小鼠����、大鼠��、豚鼠和蛇�����,其中豬皮和鼠皮較為常用,豬皮在組織學(xué)上與人類皮膚相似并且相對(duì)容易獲得���,嚙齒動(dòng)物中大鼠皮膚在結(jié)構(gòu)上與人體皮膚最為相似�,但通常比人體皮膚更具滲透性�����。動(dòng)物皮膚模型在前期的一些基礎(chǔ)研究中發(fā)揮重要作用��,使我們對(duì)各種藥物穿過(guò)皮膚屏障的過(guò)程����、途徑和驅(qū)動(dòng)力有更好的理解。然而���,由于不同物種間差異的存在以及所使用的試驗(yàn)方法的差異���,結(jié)果可能存在較大的差別,例如皮膚部位����、皮膚溫度、皮膚厚度等都會(huì)對(duì)試驗(yàn)結(jié)果造成影響,從而影響進(jìn)一步的分析�����。
此外�����,用于透皮貼劑體外滲透研究的還包括基于硅樹(shù)脂的人工膜�����,這種人工膜易于處理和儲(chǔ)存��,可重復(fù)性高�,是體外皮膚的理想替代品。但人工膜通常缺乏類似角質(zhì)層的屏障特性�,所以并不能完全替代人類或動(dòng)物皮膚來(lái)預(yù)測(cè)皮膚吸收。
3.3 溫度及接受液的選擇
在體外滲透試驗(yàn)中����,接收液的目的是代替皮膚的微環(huán)境��,所以接收液的溫度一般設(shè)定為皮膚表面溫度32 ℃或者人體溫度37 ℃��。理想的接收液要求滿足漏槽條件以及盡量接近皮膚微環(huán)境,人體血漿的正常pH值一般在7.35~7.45���,接收液的pH值應(yīng)盡量接近此范圍���,并結(jié)合藥物的理化性質(zhì)、處方工藝等因素綜合考慮���。此外,還要根據(jù)給藥時(shí)間的長(zhǎng)短考慮是否在接收液中加入合適的防腐劑����,以防止藥物或皮膚被微生物污染[25]�����。
4��、利用成像技術(shù)分析體外滲透
透皮貼劑在皮膚中的滲透行為不僅影響其滲透速率�����,還可以反映其安全性和有效性�����,然而相關(guān)的理論和試驗(yàn)并不能完整地反映滲透行為�����。利用成像技術(shù)可以獲得藥物經(jīng)皮吸收后在皮膚中的空間分布信息,以探索透皮增強(qiáng)機(jī)制��,揭示局部藥物與皮膚相互作用的機(jī)理���,幫助更好地了解透皮吸收這一動(dòng)態(tài)過(guò)程。但并不是所有的成像技術(shù)都可以用于分析透皮貼劑的體外滲透行為�����,例如熒光標(biāo)記雖然能夠追蹤待測(cè)物的動(dòng)態(tài)過(guò)程�����,但其熒光標(biāo)記的分子量通常遠(yuǎn)高于透皮貼劑藥物的分子量,并且熒光標(biāo)記不可避免地會(huì)改變待測(cè)物的動(dòng)態(tài)行為���,對(duì)結(jié)果造成干擾�����;光聲成像��、光學(xué)相干斷層掃描��、高頻超聲成像等可以說(shuō)明皮膚形態(tài)結(jié)構(gòu),但不能對(duì)待測(cè)物進(jìn)行特征分析�����,目前用于分析透皮貼劑體外滲透行為的成像技術(shù)主要有紅外光譜�、拉曼光譜以及質(zhì)譜成像[26]���。
4.1 紅外光譜成像
傅立葉變換紅外光譜成像(Fourier TransformInfrared Spectroscopy���,F(xiàn)T-IR)是傳統(tǒng)紅外光譜學(xué)的擴(kuò)展����,將FT-IR光譜儀與配有陣列檢測(cè)器的光學(xué)顯微鏡結(jié)合���,可以評(píng)估待測(cè)物在皮膚、組織和細(xì)胞內(nèi)的相對(duì)數(shù)量和分布[27]�。應(yīng)用FT-IR時(shí)��,不同波長(zhǎng)的紅外光會(huì)被皮膚或組織中的不同化學(xué)鍵(例如C=O���、C-H等)吸收�,而這些化學(xué)鍵與生物分子(例如脂質(zhì)�、DNA���、蛋白質(zhì)等)的存在和組成有關(guān)�����,F(xiàn)T-IR圖像中包含完整的紅外(IR)光譜,不同的峰對(duì)應(yīng)于不同的生物分子���,同時(shí)還可以獲得這些分子的空間信息�,其中衰減全反射(AttenuatedTotal Reflection�,ATR)FT-IR還具有高分辨成像的特點(diǎn)[28]。Andanson等[29]應(yīng)用FT-IR成像技術(shù)���,測(cè)量了12種液體樣品的皮膚的滲透性�����,并比較相同條件下幾種促滲劑的透皮過(guò)程�����,可幫助研究促滲劑的促透動(dòng)力學(xué)與相關(guān)的分子機(jī)制����。Kong等[30]使用 FT-IR成像測(cè)量化學(xué)成分以及空間結(jié)構(gòu)隨時(shí)間的變化�����,以表征豬皮作為人類皮膚模型的特征���,證明了豬皮在光譜學(xué)上類似于人類皮膚,同時(shí)考察了豬皮透皮擴(kuò)散能力和穩(wěn)定性�����,結(jié)果表明,豬皮對(duì)藥物透皮滲透的研究有很大的幫助����。
4.2 拉曼光譜成像
分子對(duì)光的拉曼散射���,是1923年Smekal通過(guò)經(jīng)典量子理論預(yù)測(cè)的��,并于1928年由Raman和Krishnan在實(shí)驗(yàn)中觀察到。拉曼光譜的出現(xiàn)和發(fā)展對(duì)生物和醫(yī)學(xué)領(lǐng)域產(chǎn)生了極大的影響��,因?yàn)樗且环N無(wú)標(biāo)記且化學(xué)選擇性高的光譜成像技術(shù)����,對(duì)于透皮貼劑而言�����,可以使用拉曼光譜獲取皮膚中待測(cè)物組成和濃度變化的詳細(xì)信息并將其可視化�,以顯示待測(cè)物在皮膚中的空間分布[31]。目前常用的拉曼技術(shù)主要有相干反斯托克斯拉曼散射(CoherentAnti-Stokes Raman Scattering�,CARS)、表面增強(qiáng)拉曼散射(Surface-enhanced Raman Scattering�,S E R S ) 、 受 激 拉 曼 散 射 ( S t i m u l a t e d R a m a nScattering����,SRS)���。
CARS顯微鏡是一種基于拉曼散射的無(wú)標(biāo)記化學(xué)成像方法,它可以利用化學(xué)鍵的拉曼振動(dòng)頻率產(chǎn)生對(duì)比度圖像�,與傳統(tǒng)的拉曼信號(hào)相比�����,CARS的高對(duì)比度圖像具有明顯的優(yōu)勢(shì)�,CARS是一個(gè)三階非線性四波混頻過(guò)程,由2個(gè)脈沖激光組成��,2個(gè)不同波長(zhǎng)的脈沖激光與樣品相互作用����,在反斯托克斯頻率下產(chǎn)生分子的相干激發(fā),產(chǎn)生的信號(hào)通常是自發(fā)拉曼散射的106倍�����,但會(huì)出現(xiàn)與拉曼位移無(wú)關(guān)的非共振背景對(duì)測(cè)定結(jié)果造成干擾[32]�����。
傳統(tǒng)拉曼光譜的主要缺陷是拉曼散射信號(hào)非常弱��,可能無(wú)法檢測(cè)到低濃度的分子,從而限制了拉曼光譜的發(fā)展�,SERS是一種可將拉曼信號(hào)增強(qiáng)幾個(gè)數(shù)量級(jí)的拉曼光譜技術(shù),將分析物放置在相對(duì)粗糙的金屬表面(最常用的金屬材料是金和銀)即可實(shí)現(xiàn)�,SERS增強(qiáng)拉曼信號(hào)的機(jī)制主要是電磁場(chǎng)增強(qiáng)以及通過(guò)金屬表面和分析物之間的電荷轉(zhuǎn)移進(jìn)行化學(xué)增強(qiáng)[33]�����。
SRS是一個(gè)相干四波非線性光學(xué)混頻過(guò)程���,可提供比自發(fā)拉曼光譜更強(qiáng)的信號(hào),SRS過(guò)程取決于泵浦光束和斯托克斯光束��,通常是將調(diào)諧到斯托克斯頻率的外部輻射源與泵浦光束串聯(lián)來(lái)激發(fā)這種效應(yīng)��,并且可通過(guò)泵浦輻射的能量增強(qiáng)斯托克斯信號(hào)�����,使其快速填充最終振動(dòng)態(tài)[34]��。Ito等[35]提出了一種新的成像方法——相位調(diào)制 SRS(PM-SRS)�,具有定量測(cè)量能力和高靈敏度����,使用相位調(diào)制和時(shí)間分辨檢測(cè)來(lái)去除背景信號(hào)��,他們分別使用PMSRS與調(diào)幅SRS(AM-SRS)兩種SRS模式對(duì)四氫嘧啶進(jìn)行了體外滲透試驗(yàn),通過(guò)PM-SRS模式獲得的光譜具有接近零水平的背景信號(hào)基線并且PM-SRS信號(hào)與四氫嘧啶濃度成正比��。
4.3 質(zhì)譜成像
質(zhì)譜成像(Mass Spectrometry Imaging��,MSI)技術(shù)起源于20世紀(jì)70年代�����,具有高特異性和高靈敏度�����,在過(guò)去的幾十年里得到了迅速發(fā)展��,MSI可用于觀察內(nèi)源性和外源性化合物的分布,包括脂類����、蛋白質(zhì)、藥物和代謝物����,而不需要使用熒光標(biāo)記或放射性標(biāo)記化合物。MSI的主要技術(shù)包括二次離子質(zhì)譜(Secondary-ion Mass Spectrometry����,SIMS)、基質(zhì)輔助激光解吸電離(Matrix-assistedLaser Desorption Ionization���,MALDI)��、解吸電噴霧電離(Desorption Electrospray Ionization�����,DESI)��、液體萃取表面分析(Liquid Extraction SurfaceAnalysis�����,LESA)����、激光消融電噴霧電離(LaserAblation Electrospray Ionization���,LAESI)、激光解吸電離(Laser Desorption Postionization���,LDPI)和飛秒激光解吸電離(Femtosecond Laser DesorptionPostionization�,fs-LDPI)��,其中MALDI-MSI被廣泛應(yīng)用于透皮研究中���,可對(duì)全身或不同器官動(dòng)物切片的各種藥物的空間分布進(jìn)行分析��。
MALDI-MSI是一種基于激光照射從表面解吸和電離待測(cè)物��,然后對(duì)電離分子進(jìn)行質(zhì)譜分析���,以獲得目標(biāo)化合物的空間分布圖像的技術(shù)[36]��。MALDI-MSI已成為無(wú)標(biāo)記生物分析的關(guān)鍵技術(shù)�����,可以對(duì)生物分子����、藥物和其他外來(lái)物質(zhì)在組織切片中的空間分布進(jìn)行分析�����,在應(yīng)用MALDI-MSI分析時(shí)��,待測(cè)物電離的性質(zhì)很大程度上取決于待測(cè)物和組織的實(shí)體��,同一分子在不同組織中或在同一組織中可能會(huì)受到不同的離子抑制效應(yīng)從而引起離子信號(hào)的變化���,這可能是開(kāi)發(fā)MALDI-MSI作為定量質(zhì)譜成像(Quantitative Mass SpectrometryImaging�,QMSI)方法時(shí)需要解決的主要問(wèn)題[37]。應(yīng)用MALDI-MSI進(jìn)行定量分析需要考慮多方面的影響��,因?yàn)槿魏位贛S的分析�,待測(cè)物的強(qiáng)度都會(huì)同時(shí)受到幾個(gè)因素的影響,包括待測(cè)物的提取效率�����、電離效率和其與基質(zhì)共結(jié)晶的一致性���,此外����,離子抑制也是MALDI-MSI定量分析的一個(gè)重要因素[38]��。
MALDI-MSI是一種能夠同時(shí)檢測(cè)多種化合物的成像技術(shù)����,應(yīng)用非常廣泛,據(jù)報(bào)道[39]已成功地應(yīng)用于分析藥物在豬皮的空間分布情況�����,同時(shí)可以比較作用于局部的藥物的滲透能力���。當(dāng)MALDI-MSI應(yīng)用于透皮貼劑時(shí)���,皮膚作為定量試驗(yàn)的靶器官,組織成分對(duì)MSI信號(hào)響應(yīng)的影響具有重要意義��。在透皮貼劑的研究中,可將Franz擴(kuò)散池與MALDIMSI技術(shù)結(jié)合來(lái)對(duì)滲透行為進(jìn)行分析��,增加對(duì)皮膚、輔料和藥物分子之間復(fù)雜相互作用的理解��,從而對(duì)透皮貼劑的體外滲透與體內(nèi)分布作出更加科學(xué)和全面的分析。Handler等[40]應(yīng)用Franz擴(kuò)散池法對(duì)3種處方的托法替尼進(jìn)行了體外滲透試驗(yàn)���,并用MALDI-MSI定量測(cè)定藥物在皮膚中的滲透性���,為了解托法替尼在皮膚中的分布提供了有價(jià)值的信息�。
5、總結(jié)與展望
透皮貼劑的滲透性研究主要包括如何改善透皮貼劑中藥物的滲透性以及如何評(píng)價(jià)透皮貼劑體外滲透性�����。改善透皮貼劑中藥物的滲透性�����,提高其生物利用度�,這就需要我們對(duì)各種促透方法的機(jī)制有一個(gè)全面而深入的了解�,在此基礎(chǔ)上開(kāi)發(fā)兩種或幾種促透方法的聯(lián)用技術(shù)����,揚(yáng)長(zhǎng)避短�,尋找最為適合的促透方法�����。而如何評(píng)價(jià)透皮貼劑體外滲透性�����,例如進(jìn)行滲透試驗(yàn)時(shí)皮膚模型的選擇�����、體外滲透結(jié)果的分析等�����,就需要相關(guān)部門加大研發(fā)水平,完善相應(yīng)的標(biāo)準(zhǔn)和要求���。