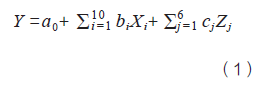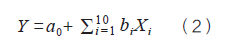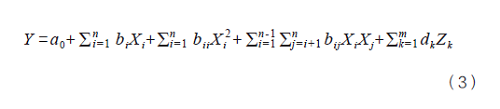摘 要 / Abstract
目的:針對(duì)中藥制藥過(guò)程參數(shù)控制中存在的共性關(guān)鍵問(wèn)題��,提出一種中藥制藥過(guò)程質(zhì)量控制方法��。方法:以三七總皂苷生產(chǎn)制造為例���,在簡(jiǎn)述物料傳遞流程基礎(chǔ)上�����,對(duì)原料藥材屬性參數(shù)、產(chǎn)品質(zhì)量標(biāo)準(zhǔn)以及生產(chǎn)流程各單元工藝環(huán)節(jié)物料屬性參數(shù)進(jìn)行檢測(cè),辨識(shí)關(guān)鍵物料質(zhì)控參數(shù)及其合理限度���;設(shè)計(jì)預(yù)置過(guò)程參數(shù)并用10批次以上原料考察制藥過(guò)程�����,根據(jù)實(shí)驗(yàn)結(jié)果辨識(shí)出關(guān)鍵過(guò)程參數(shù)��,進(jìn)而擇優(yōu)確定關(guān)鍵過(guò)程參數(shù)的取值范圍�����。結(jié)果與結(jié)論:工業(yè)生產(chǎn)實(shí)踐表明��,上述方法能確保三七總皂苷產(chǎn)品質(zhì)量���,并適宜推廣應(yīng)用。
Objective: A quality control method for the manufacturing process of traditional Chinese medicine is proposed for tackling the common key problems in the control of manufacturing parameters. Methods: A case study was done on the manufacturing of Notoginseng Total Saponins(NTS). Based on the brief description of the material transfer steps, tests were taken in terms of the indices of medicinal materials, the quality standards of finished products, and material property parameters of each unit during the production process, so as to identify the key material quality control parameters and their reasonable ranges. Process parameters were preset and the pharmaceutical process was investigated with more than 10batches of medicinal materials. Critical process parameters(CPPs) were identified according to the experimental results. Then the ranges of CPPs were optimized. Results and Conclusion: The industrial practice verifies that the proposed method can ensure the product quality of NTS and the proposed method is suitable for popularization and application.
中成藥化學(xué)組成十分復(fù)雜���,其質(zhì)量檢驗(yàn)不僅技術(shù)難度大,而且檢測(cè)成本很高[1]�����。中藥制藥過(guò)程質(zhì)量控制對(duì)于確保中藥安全性、有效性及質(zhì)量一致性具有重要的現(xiàn)實(shí)意義[2]��。盡管《中國(guó)藥典》在“制法”項(xiàng)中規(guī)定了單元工藝先后順序以及必要的工藝參數(shù)取值等�����,但仍然不夠縝密���,需進(jìn)一步完善。放眼國(guó)際��,美國(guó)等發(fā)達(dá)國(guó)家的藥品監(jiān)管部門均倡導(dǎo)在深入研究并認(rèn)知制藥過(guò)程規(guī)律的基礎(chǔ)上���,加強(qiáng)制藥過(guò)程質(zhì)量控制[3]��。
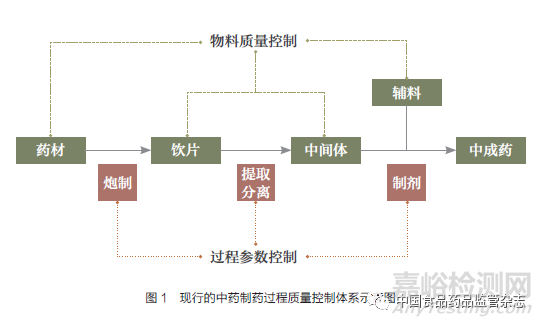
先進(jìn)的制藥過(guò)程質(zhì)量控制系統(tǒng)能夠適時(shí)檢測(cè)關(guān)鍵物料質(zhì)量參數(shù)和過(guò)程狀態(tài)參數(shù),及時(shí)調(diào)整關(guān)鍵過(guò)程參數(shù)���,保障所產(chǎn)藥品質(zhì)量與原定的藥品質(zhì)量概貌一致��,從而“免檢”實(shí)時(shí)放行藥品[3]。因此�����,科學(xué)構(gòu)建中藥制藥過(guò)程質(zhì)量控制體系是解決中藥工業(yè)領(lǐng)域當(dāng)今“最緊急��、最緊迫”問(wèn)題的關(guān)鍵技術(shù)路徑。現(xiàn)行的中藥制藥過(guò)程質(zhì)量控制體系如圖1所示�����,一般包括物料質(zhì)量控制及過(guò)程參數(shù)控制�����。
中藥生產(chǎn)物料包括藥材���、飲片、輔料和中間體等���,《中國(guó)藥典》一部規(guī)定了藥材���、飲片和部分提取物的質(zhì)量標(biāo)準(zhǔn)��,而四部規(guī)定了輔料的質(zhì)量標(biāo)準(zhǔn)。由于在中藥生產(chǎn)制造中涉及相當(dāng)多的過(guò)程參數(shù)��,且往往存在關(guān)鍵過(guò)程參數(shù)不明確�����、與產(chǎn)品質(zhì)量相關(guān)參數(shù)的優(yōu)選值不清楚等情況��,會(huì)出現(xiàn)符合法定標(biāo)準(zhǔn)的藥材及物料難以生產(chǎn)出質(zhì)量可靠的中藥產(chǎn)品等問(wèn)題��。此外��,中藥生產(chǎn)制造一般通過(guò)檢測(cè)單個(gè)物理量(如溫度、壓力��、密度���、pH值等)判斷制藥過(guò)程狀態(tài),造成產(chǎn)品質(zhì)量風(fēng)險(xiǎn)難以防控�����,但若要檢測(cè)更多化學(xué)或生物活性指標(biāo)��,就存在設(shè)備價(jià)格高、分析結(jié)果不直觀等問(wèn)題���。
本文以三七總皂苷生產(chǎn)制造為例��,提出一種中藥制藥過(guò)程質(zhì)量控制方法��,其技術(shù)步驟為:①研究量值傳遞規(guī)律���,在此基礎(chǔ)上完善藥材的質(zhì)量檢測(cè)指標(biāo)�����,解決藥材應(yīng)該“測(cè)什么”的問(wèn)題�����。②根據(jù)制藥過(guò)程參數(shù)對(duì)物料量值傳遞的影響�����,設(shè)置藥材質(zhì)檢指標(biāo)的內(nèi)控標(biāo)準(zhǔn)�����,解決藥材“怎么控”的問(wèn)題。③聯(lián)合考察多個(gè)單元工藝并考慮原料批次間質(zhì)量變化情況���,篩選關(guān)鍵過(guò)程參數(shù)�����,解決生產(chǎn)過(guò)程“控什么”的問(wèn)題。④考慮原料批次間質(zhì)量變化情形,提出過(guò)程參數(shù)的優(yōu)值范圍��,解決過(guò)程參數(shù)“如何控”的問(wèn)題��。
1��、三七總皂苷制藥過(guò)程質(zhì)量控制方法研究
1.1 根據(jù)量值傳遞規(guī)律設(shè)定原料內(nèi)控指標(biāo)
量值傳遞一般是指中藥生產(chǎn)規(guī)程中物料平衡的遞次量傳以及關(guān)鍵物料質(zhì)控參數(shù)的量測(cè)值在制藥全流程各環(huán)節(jié)的逐級(jí)傳遞。這里可以采用單位質(zhì)量藥材為基準(zhǔn)的指標(biāo)性成分含量���、大類成分含量以及總固體的產(chǎn)量等指標(biāo)定量表征相關(guān)物質(zhì)在中藥生產(chǎn)規(guī)程中的傳遞��。
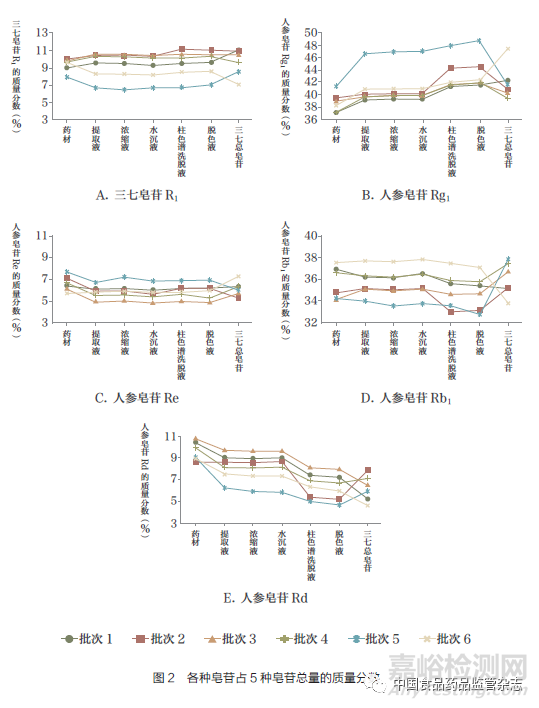
根據(jù)國(guó)家藥典委員會(huì)相關(guān)規(guī)定���,三七總皂苷是采用三七藥材��,經(jīng)過(guò)粉碎、醇提���、水沉�����、柱色譜��、脫色��、精制、濃縮和干燥等一系列單元工藝制得���。筆者曾考察了不同批次三七生產(chǎn)三七總皂苷過(guò)程中的量值傳遞情況[4]。分別檢測(cè)了6批次三七藥材���、提取液���、濃縮液、水沉液���、柱色譜洗脫液�����、脫色液以及三七總皂苷產(chǎn)品中三七皂苷R1��、人參皂苷Rg1��、人參皂苷Re���、人參皂苷Rb1和人參皂苷Rd 5種皂苷含量。計(jì)算了各個(gè)物料中每種皂苷在這5種皂苷總量中的質(zhì)量分?jǐn)?shù)��,具體結(jié)果如圖2所示��。
從圖2中可知���,在提取過(guò)程中人參皂苷Rg1的質(zhì)量分?jǐn)?shù)略有增加�����,而人參皂苷Rd的質(zhì)量分?jǐn)?shù)略有下降��,但改變量大多在3%以下��。提取后的各單元工藝處理后��,除人參皂苷Rd的質(zhì)量分?jǐn)?shù)稍有下降外��,其他皂苷的質(zhì)量分?jǐn)?shù)總體變化不大��。這意味著�����,最終所得三七總皂苷確實(shí)主要是從藥材提取分離“傳遞”而來(lái)���,而非化學(xué)反應(yīng)“轉(zhuǎn)化”而來(lái)�����。那么��,作為原料的三七質(zhì)控指標(biāo)應(yīng)該考慮控制上述5種皂苷的含量���。
《中國(guó)藥典》2020年版規(guī)定三七藥材中含人參皂苷Rg1���、人參皂苷Rb1���、三七皂苷R1的總量不得少于5.0%,沒(méi)有規(guī)定人參皂苷Re和人參皂苷Rd的含量要求��。根據(jù)量值傳遞研究結(jié)果���,人參皂苷Re和人參皂苷Rd主要是從藥材中提取分離而來(lái)。因此��,如果是作為工業(yè)生產(chǎn)三七總皂苷的原料�����,三七藥材內(nèi)控標(biāo)準(zhǔn)中應(yīng)考慮將人參皂苷Re和人參皂苷Rd含量作為質(zhì)量參數(shù)�����,每批進(jìn)行檢測(cè)��。
《中國(guó)藥典》2020年版規(guī)定了三七總皂苷中5種皂苷的含量下限�����,實(shí)際上對(duì)原料藥材中這些皂苷的含量提出了要求�����。例如,5種皂苷中含量最低的是人參皂苷Re�����,假設(shè)三七藥材中人參皂苷Re含量為0.1%��,并且提取分離過(guò)程中人參皂苷Re無(wú)損失(轉(zhuǎn)移率為100%),為了達(dá)到三七總皂苷中2.5%人參皂苷Re的最低標(biāo)準(zhǔn)��,那么5種皂苷的總得率只能是低于4.0%���。這意味著合格三七藥材中很多皂苷都未能充分利用�����。因此�����,如果希望5種皂苷的總得率不低于8.0%,那么三七藥材中人參皂苷Re含量就不宜低于0.2%���。類似地�����,人參皂苷Rd�����、三七皂苷R1��、人參皂苷Rg1和人參皂苷Rb1的含量分別不宜低于0.4%�����、0.4%、2.0%和2.4%�����。
若考慮提取分離過(guò)程中5種皂苷存在一定損失���,那么采購(gòu)三七藥材時(shí)上述5種皂苷的含量下限還需要進(jìn)一步提高�����。比如,PAN等[5]的研究結(jié)果顯示�����,人參皂苷Re��、人參皂苷Rd��、三七皂苷R1��、人參皂苷Rg1和人參皂苷Rb1從藥材傳遞到三七總皂苷的轉(zhuǎn)移率約為82.3%、69.9%�����、79.0%�����、80.7%和77.8%�����。以上述轉(zhuǎn)移率進(jìn)行估算��,藥材中人參皂苷Re�����、人參皂苷Rd���、三七皂苷R1���、人參皂苷Rg1和人參皂苷Rb1的含量下限分別為0.243%�����、0.572%�����、0.506%�����、2.48%��、3.08%。
從上面的分析可以看到��,工業(yè)生產(chǎn)中所用三七的內(nèi)控標(biāo)準(zhǔn)會(huì)比藥典標(biāo)準(zhǔn)更高��,不僅需要檢測(cè)更多皂苷成分�����,且對(duì)各皂苷含量下限有要求��。目前已有文獻(xiàn)報(bào)道了三七藥材中5種皂苷含量的液相色譜檢測(cè)方法[6-7]�����,可參考這些方法進(jìn)行檢測(cè)。檢測(cè)后可以考慮進(jìn)一步采用混批調(diào)配的方法降低原料質(zhì)量波動(dòng)�����。
1.2 辨析關(guān)鍵過(guò)程參數(shù)
中藥制藥過(guò)程參數(shù)的類型較多��,通常包括工藝參數(shù)、物料屬性參數(shù)�����、狀態(tài)參數(shù)���、設(shè)備參數(shù)和環(huán)境參數(shù)等[8]。其中�����,工藝參數(shù)通常是指在國(guó)家藥品標(biāo)準(zhǔn)的制法項(xiàng)或工藝規(guī)程中規(guī)定的參數(shù)(比如�����,工藝規(guī)程中調(diào)p H值的目標(biāo)范圍就是工藝參數(shù));物料屬性參數(shù)是用來(lái)表征中藥生產(chǎn)原輔料或中間體特性的參數(shù)�����,包括物理���、化學(xué)或生物特性參數(shù),影響藥品質(zhì)量的物料屬性參數(shù)稱為物料質(zhì)量參數(shù)���;質(zhì)控參數(shù)是指用于確保藥品質(zhì)量而進(jìn)行控制的過(guò)程參數(shù)��;狀態(tài)參數(shù)是反映制藥過(guò)程狀態(tài)的參數(shù),其可能不用數(shù)字變量而用語(yǔ)言變量(比如,用“未沸騰”或“沸騰”描述中藥煎煮過(guò)程狀態(tài)�����,又如���,用“未達(dá)終點(diǎn)”或“達(dá)終點(diǎn)”描述滲漉提取過(guò)程狀態(tài))�����;設(shè)備參數(shù)通常指制藥相關(guān)設(shè)備的參數(shù)(比如�����,計(jì)量泵的電機(jī)轉(zhuǎn)速)���;表征制藥流程所處環(huán)境的參數(shù)一般稱為環(huán)境參數(shù)��,常見(jiàn)的有環(huán)境溫度���、濕度、壓力�����、潔凈度等�����。
目前���,對(duì)已上市中成藥可根據(jù)生產(chǎn)數(shù)據(jù)��、檢驗(yàn)數(shù)據(jù)和文獻(xiàn)報(bào)道等,采用風(fēng)險(xiǎn)評(píng)估等可行方法直接確定關(guān)鍵過(guò)程參數(shù)�����。常用的風(fēng)險(xiǎn)評(píng)估方法包括風(fēng)險(xiǎn)排序及過(guò)濾��、失效模式及效應(yīng)分析�����、故障樹(shù)分析等�����。如果有實(shí)驗(yàn)研究數(shù)據(jù)或者工業(yè)生產(chǎn)數(shù)據(jù),可采用適當(dāng)統(tǒng)計(jì)學(xué)方法確定關(guān)鍵過(guò)程參數(shù)�����,如多元線性回歸法[9]���、逐步回歸法[9]��、標(biāo)準(zhǔn)偏回歸系數(shù)法[9]��、加權(quán)決定系數(shù)法[10]等���。
筆者曾采用確定性篩選設(shè)計(jì)(definitive screening design)安排了32個(gè)實(shí)驗(yàn)用于研究提取���、濃縮��、水沉和柱色譜4個(gè)步驟中的10個(gè)參數(shù)��,并且在實(shí)驗(yàn)中隨機(jī)搭配了16個(gè)不同批次的三七藥材[5]。測(cè)定了每種藥材中以特定提取條件提取的5種皂苷量和總固體量作為藥材屬性參數(shù)��。得到柱色譜洗脫液后���,測(cè)定了5種皂苷的純度、總固體產(chǎn)量��、總皂苷產(chǎn)量作為過(guò)程評(píng)價(jià)指標(biāo)(Y)。以逐步回歸法精簡(jiǎn)公式(1)獲得關(guān)鍵過(guò)程參數(shù)為提取所用乙醇濃度��、洗脫液乙醇濃度�����、洗脫時(shí)間�����。
式中�����,X為實(shí)驗(yàn)中考察的過(guò)程參數(shù)��,Z為藥材屬性參數(shù)�����,a0為擬合所得常數(shù)項(xiàng)�����,bi和cj均為擬合所得偏回歸系數(shù)��。
上述工作與多數(shù)參數(shù)篩選工作的區(qū)別點(diǎn)在于:篩選關(guān)鍵過(guò)程參數(shù)時(shí)考慮了藥材屬性參數(shù)的變化�����,獲得關(guān)鍵過(guò)程參數(shù)時(shí)也確定了藥材質(zhì)量參數(shù)。此外���,還對(duì)比了不考慮藥材屬性參數(shù)變化的情況���,即采用逐步回歸法精簡(jiǎn)公式(2)獲得關(guān)鍵過(guò)程參數(shù)。
對(duì)比結(jié)果見(jiàn)表1���。從中可知:考慮三七屬性參數(shù)變化篩選所得關(guān)鍵過(guò)程參數(shù)與不考慮時(shí)不同���。考慮三七屬性參數(shù)所得模型的決定系數(shù)數(shù)值更高���,說(shuō)明部分三七屬性參數(shù)確實(shí)對(duì)過(guò)程評(píng)價(jià)指標(biāo)有影響���。因?yàn)楣I(yè)生產(chǎn)中三七藥材批次間質(zhì)量差異總是存在���,考慮三七屬性參數(shù)變化所得關(guān)鍵過(guò)程參數(shù)應(yīng)該更為可靠。
1.3 確定參數(shù)操作范圍
ICH Q8《藥物開(kāi)發(fā)》(Pharmaceutical Development)要求構(gòu)建設(shè)計(jì)空間(design space)以保障制藥過(guò)程質(zhì)量。構(gòu)建設(shè)計(jì)空間的本質(zhì)是優(yōu)化制藥過(guò)程參數(shù)到合適的范圍��,而非一個(gè)操作點(diǎn)��,以便為生產(chǎn)提供更大靈活性��,減少不必要的監(jiān)管��。制藥過(guò)程中過(guò)程參數(shù)數(shù)量很多���,優(yōu)化其中關(guān)鍵過(guò)程參數(shù)的操作范圍是構(gòu)建設(shè)計(jì)空間最核心的內(nèi)容。
設(shè)計(jì)空間的概念中提示優(yōu)化過(guò)程參數(shù)取值范圍時(shí)應(yīng)將物料質(zhì)量參數(shù)考慮在內(nèi)�����。因此筆者采用公式(3)建立了關(guān)鍵過(guò)程參數(shù)和工藝評(píng)價(jià)指標(biāo)之間的定量模型[5]���。
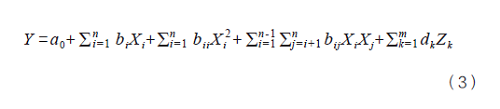
式中���,Z為物料質(zhì)量參數(shù),n為除物料質(zhì)量參數(shù)以外的關(guān)鍵過(guò)程參數(shù)個(gè)數(shù)��,m為物料質(zhì)量參數(shù)個(gè)數(shù)���,i、j��、k用于區(qū)別不同的偏回歸系數(shù)���。建立數(shù)學(xué)模型后計(jì)算獲得設(shè)計(jì)空間�����。設(shè)計(jì)空間以列表的形式給出���。驗(yàn)證后發(fā)現(xiàn)模型預(yù)測(cè)結(jié)果準(zhǔn)確�����,設(shè)計(jì)空間范圍可靠���。
除關(guān)鍵過(guò)程參數(shù)外,其他過(guò)程參數(shù)也應(yīng)有操作范圍��。選擇其他參數(shù)具體運(yùn)行值時(shí)�����,應(yīng)考慮節(jié)能�����、降耗��、增效等原則���。例如���,在確保樹(shù)脂充分吸附三七皂苷的前提下,可以適當(dāng)增加上樣速度以提高生產(chǎn)效率���;在確保洗滌除去雜質(zhì)的前提下,洗滌水用量應(yīng)盡量少些;在確保樹(shù)脂再生效果的前提下���,酸堿液洗滌的用量應(yīng)盡量少些。
2��、研究結(jié)果與討論
2.1 基于量值傳遞規(guī)律判斷關(guān)鍵工藝
確定制藥過(guò)程關(guān)鍵工藝環(huán)節(jié)的意義在于明確實(shí)施制藥過(guò)程質(zhì)量控制的重點(diǎn)��,縮小關(guān)鍵過(guò)程參數(shù)的搜索范圍��。根據(jù)量值傳遞研究結(jié)果可以確定關(guān)鍵單元工藝��。
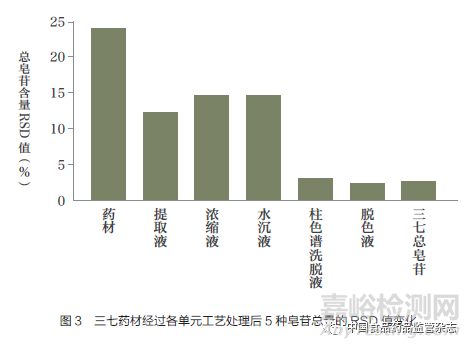
筆者測(cè)定了各單元工藝處理后6批次三七5種皂苷總量的相對(duì)標(biāo)準(zhǔn)偏差(RSD)[4]���,如圖3所示���。該數(shù)值體現(xiàn)了三七5種皂苷總量在生產(chǎn)過(guò)程中精密度的變化,體現(xiàn)了各單元工藝對(duì)提升三七總皂苷批次間一致性的貢獻(xiàn)大小���。從圖3可知��,藥材中5種皂苷總量相差較大�����,RSD超過(guò)20%��。經(jīng)過(guò)提取工藝后���,RSD下降到15%以下�����。經(jīng)過(guò)柱色譜工藝后���,RSD更是下降到5%以下���。這說(shuō)明當(dāng)處理多批次三七時(shí),柱色譜工藝對(duì)提升產(chǎn)品質(zhì)量一致性貢獻(xiàn)最大�����,是影響其精密制造的關(guān)鍵工藝��,提取工藝的貢獻(xiàn)次之���。
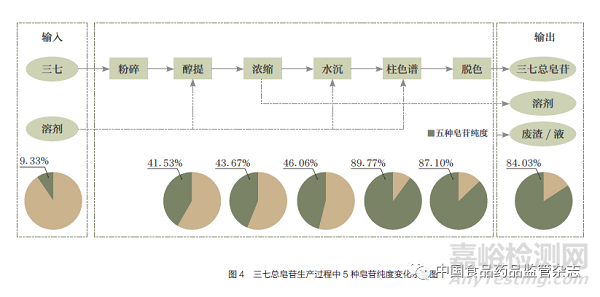
研究中也發(fā)現(xiàn)提取工藝和柱色譜工藝都較大程度地改變了體系中化學(xué)成分組成���,具體體現(xiàn)為5種皂苷占總固體的質(zhì)量分?jǐn)?shù)大幅上升,即純度明顯提高�����。提取后5種皂苷純度從不足10%提升到約40%��,柱色譜后純度從不足50%提升到超過(guò)80%,如圖4所示��。柱色譜工藝后所得藥液的抗凝血酶活性也有較大變化�����。因此���,柱色譜工藝是三七總皂苷生產(chǎn)的首要關(guān)鍵單元工藝��,提取工藝是次要關(guān)鍵單元工藝���。
2.2 關(guān)鍵過(guò)程參數(shù)辨析策略的選擇
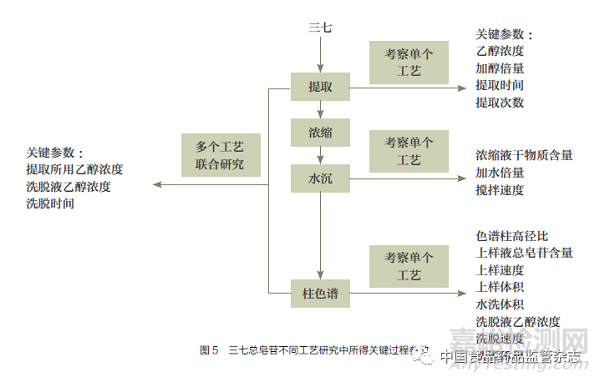
目前多數(shù)研究都是針對(duì)某個(gè)具體單元工藝�����,實(shí)驗(yàn)研究后辨析關(guān)鍵過(guò)程參數(shù)。需要注意的是���,逐個(gè)考察單元工藝所得關(guān)鍵過(guò)程參數(shù)數(shù)量往往會(huì)多于聯(lián)合考察多個(gè)單元工藝���。圖5列出了這2種研究策略所得參數(shù)的差別���。
逐個(gè)研究提取�����、水沉和柱色譜工藝時(shí)共找到關(guān)鍵過(guò)程參數(shù)15個(gè)���。但聯(lián)合研究提取、濃縮�����、水沉、柱色譜4個(gè)單元工藝時(shí)���,關(guān)鍵過(guò)程參數(shù)只有提取所用乙醇濃度、洗脫液乙醇濃度��、洗脫時(shí)間3個(gè)��。所得關(guān)鍵過(guò)程參數(shù)均集中于提取和柱色譜工藝��,也證實(shí)2.1節(jié)基于量值傳遞研究所得關(guān)鍵工藝是準(zhǔn)確的�����。因此��,聯(lián)合研究多個(gè)單元工藝不僅效率較高��,且能從更接近全局的視角中獲得制藥過(guò)程真正的關(guān)鍵過(guò)程參數(shù)���。聯(lián)合研究多個(gè)單元工藝需要同時(shí)考察較多過(guò)程參數(shù)��,建議采用足夠分辨率的篩選試驗(yàn)設(shè)計(jì)以減少實(shí)驗(yàn)次數(shù)���。
2.3 實(shí)驗(yàn)設(shè)計(jì)方法的選擇
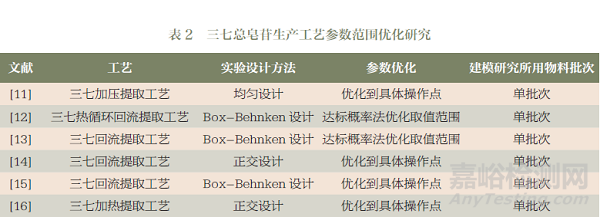
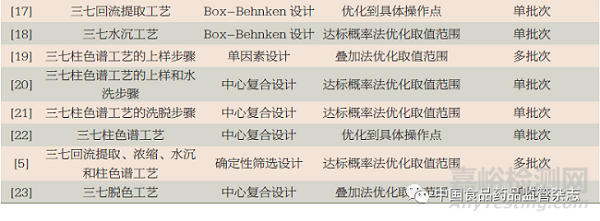
表2中列出了三七總皂苷生產(chǎn)工藝相關(guān)文獻(xiàn)報(bào)道中的實(shí)驗(yàn)設(shè)計(jì)方法���。實(shí)驗(yàn)設(shè)計(jì)方法包括:中心復(fù)合設(shè)計(jì)、Box-Behnken設(shè)計(jì)�����、確定性篩選設(shè)計(jì)���、單因素設(shè)計(jì)、正交設(shè)計(jì)和均勻設(shè)計(jì)���。實(shí)驗(yàn)設(shè)計(jì)方法的選擇和待研究參數(shù)個(gè)數(shù)及后續(xù)建模方法有關(guān)�����。若考慮采用二階多項(xiàng)式建模�����,用前3個(gè)實(shí)驗(yàn)設(shè)計(jì)方法較好�����。當(dāng)所研究的參數(shù)超過(guò)5個(gè)時(shí),中心復(fù)合設(shè)計(jì)和Box-Behnken設(shè)計(jì)的實(shí)驗(yàn)次數(shù)都較多�����,建議采用確定性篩選設(shè)計(jì)�����。
2.4 優(yōu)化方式的選擇
表2中列出了三七總皂苷生產(chǎn)工藝研究中的參數(shù)優(yōu)化工作。雖然很多研究者將參數(shù)優(yōu)化到最優(yōu)點(diǎn)��,但將參數(shù)優(yōu)化到特定范圍會(huì)更有利于提升制藥過(guò)程的穩(wěn)健性。目前不少研究工作在優(yōu)化時(shí)都計(jì)算了達(dá)標(biāo)概率��,以達(dá)標(biāo)概率定量表示在優(yōu)化范圍內(nèi)運(yùn)行參數(shù)時(shí)制藥過(guò)程質(zhì)量能得到的保障��。達(dá)標(biāo)概率計(jì)算時(shí)可以考慮過(guò)程參數(shù)��、實(shí)驗(yàn)結(jié)果或模型預(yù)測(cè)結(jié)果的不確定度���,所得參數(shù)優(yōu)化范圍會(huì)更為可靠。MODDE或Matlab等軟件均可用于計(jì)算獲得基于達(dá)標(biāo)概率的較優(yōu)參數(shù)范圍��。
另一種參數(shù)優(yōu)化思路是前饋控制�����,即根據(jù)三七藥材質(zhì)量參數(shù)變化針對(duì)性地調(diào)整參數(shù)���。應(yīng)用該思路調(diào)整參數(shù)要注意合規(guī)���。JIANG等[24]用Yoon-Nelson模型關(guān)聯(lián)了三七水沉后上樣液中皂苷濃度�����、上樣液流速和柱色譜穿透曲線���,能根據(jù)每次柱色譜上樣液中皂苷含量高低靈活調(diào)整柱色譜上樣時(shí)間���。王曉宇等[25]建立了三七藥材近紅外光譜主成分、提取過(guò)程參數(shù)及指標(biāo)成分提取量的定量模型��,通過(guò)掃描藥材快速獲得光譜信息�����,然后針對(duì)性地調(diào)整提取過(guò)程參數(shù)���,可以減少三七質(zhì)量差異造成的提取液質(zhì)量波動(dòng)�����。
采用適當(dāng)?shù)闹扑庍^(guò)程檢測(cè)技術(shù)確定狀態(tài)參數(shù),然后針對(duì)性地調(diào)整后續(xù)過(guò)程參數(shù)則是反饋控制的思路�����。JIANG等[26]將在線近紅外光譜和紫外光譜所得數(shù)據(jù)相融合��,建立了三七柱色譜上樣流出液中三七皂苷濃度的定量模型���,可用于實(shí)時(shí)監(jiān)測(cè)流出液皂苷濃度;若觀察到流出液皂苷濃度過(guò)高,則考慮停止上樣�����。蔣程[27]采集三七柱色譜過(guò)程在線紫外光譜數(shù)據(jù)���,以多變量統(tǒng)計(jì)過(guò)程控制的方法評(píng)價(jià)過(guò)程批次一致性��,能檢測(cè)出藥液中皂苷濃度和流速的異常�����;進(jìn)一步可根據(jù)異常情況確定處理方案���。
2.5 中間體和其他物料的內(nèi)控標(biāo)準(zhǔn)設(shè)定
中藥生產(chǎn)中往往會(huì)有多個(gè)中間體,針對(duì)關(guān)鍵中間體設(shè)置內(nèi)控標(biāo)準(zhǔn)有利于保障后續(xù)制藥過(guò)程質(zhì)量和藥品質(zhì)量。設(shè)置關(guān)鍵中間體內(nèi)控標(biāo)準(zhǔn)的原則:放行符合內(nèi)控標(biāo)準(zhǔn)的中間體后,后續(xù)加工應(yīng)能得到合格藥品�����。
確定關(guān)鍵中間體時(shí)需要考慮上游的控制情況��,取樣是否方便��、檢測(cè)工作量大小等�����。比如�����,三七飲片由藥材粉碎制得���,如果藥材已按照1.1節(jié)中5種皂苷含量?jī)?nèi)控標(biāo)準(zhǔn)進(jìn)行了放行控制,那么飲片可不作為關(guān)鍵物料��。三七提取液在工業(yè)生產(chǎn)中往往存放于多個(gè)儲(chǔ)罐��,各儲(chǔ)罐中提取液濃度不同��,取樣檢測(cè)工作量大���,不適合作為關(guān)鍵物料��。三七提取液濃縮所得的濃縮液通常放置在同一儲(chǔ)罐中���,體系均勻性好���,取樣和檢測(cè)都較方便��,更適合作為關(guān)鍵中間體。確定關(guān)鍵中間體的質(zhì)量參數(shù)及其范圍可以采用類似于1.1節(jié)的方法�����。也可以先建立中間體質(zhì)量參數(shù)和后續(xù)制藥過(guò)程評(píng)價(jià)指標(biāo)之間的定量模型�����,再根據(jù)評(píng)價(jià)指標(biāo)的要求反算出中間體質(zhì)量參數(shù)的控制標(biāo)準(zhǔn)��。類似思路已用于設(shè)置丹參水提液[28]�����、黃芪濃縮液[29]等中間體質(zhì)量標(biāo)準(zhǔn)�����。
除了原料藥材和關(guān)鍵中間體���,其他物料也需要有其內(nèi)控標(biāo)準(zhǔn)�����。例如���,三七柱色譜工藝中使用的樹(shù)脂�����,應(yīng)保證每次使用前都洗凈上個(gè)生產(chǎn)周期中吸附的成分。又如��,采用三七醇提液或者柱色譜洗脫液的回收乙醇用于下一批生產(chǎn)���,應(yīng)保證不產(chǎn)生批次間交叉污染��。因此��,這些物料也需要有合適的內(nèi)控標(biāo)準(zhǔn)判斷其品質(zhì)是否合格��。
2.6 制藥過(guò)程設(shè)備和設(shè)施管理的重要性
制藥設(shè)備性能與運(yùn)行狀態(tài)對(duì)藥品質(zhì)量及生產(chǎn)效率均有較大影響���,因此需要科學(xué)管理中成藥生產(chǎn)制造所涉及的設(shè)備和設(shè)施��。國(guó)際制藥工程協(xié)會(huì)(International Society for Pharmaceutical Engineering,ISPE)發(fā)布了《良好工程管理規(guī)范》(Good Engineering Practice,GEP),其中一項(xiàng)重要的內(nèi)容是“操作與維護(hù)”�����,其目標(biāo)是將設(shè)備和設(shè)施維持在較優(yōu)狀態(tài)。
生產(chǎn)中除了采集物料和參數(shù)數(shù)據(jù)�����,還應(yīng)采集設(shè)備相關(guān)數(shù)據(jù)�����,以反映設(shè)備當(dāng)前運(yùn)行狀態(tài)��。建議對(duì)關(guān)鍵單元工藝對(duì)應(yīng)的設(shè)備增加故障預(yù)警預(yù)報(bào)模塊��,定期檢測(cè)其運(yùn)行狀態(tài)�����,并實(shí)施科學(xué)干預(yù),確保設(shè)備長(zhǎng)期穩(wěn)定工作��,促使生產(chǎn)處于受控狀態(tài)��。
2.7 制藥過(guò)程質(zhì)量控制持續(xù)改進(jìn)的重要性
在整個(gè)藥品生命周期內(nèi)���,都應(yīng)不斷積累中藥產(chǎn)品和制藥過(guò)程的知識(shí)��,采用風(fēng)險(xiǎn)管理方法���,持續(xù)完善中成藥質(zhì)量標(biāo)準(zhǔn)和提升過(guò)程質(zhì)量控制水平���。具體的,如果獲得三七總皂苷制劑的臨床數(shù)據(jù),建議結(jié)合制劑質(zhì)檢數(shù)據(jù)和臨床反饋信息等進(jìn)行回顧分析�����,根據(jù)分析結(jié)果調(diào)整三七總皂苷的質(zhì)量參數(shù)及其控制要求���。在此基礎(chǔ)上,重新分析確定關(guān)鍵過(guò)程參數(shù)及其控制范圍�����、關(guān)鍵物料及其質(zhì)量參數(shù)控制范圍。如果采集了工業(yè)大數(shù)據(jù)���,可以進(jìn)一步采用合適方法���,依靠數(shù)據(jù)驅(qū)動(dòng)預(yù)判產(chǎn)品質(zhì)量風(fēng)險(xiǎn)���,提升整體管理水平。
3��、結(jié) 論
本文針對(duì)當(dāng)前中藥制藥過(guò)程質(zhì)量控制技術(shù)方面的難點(diǎn)問(wèn)題��,以三七總皂苷生產(chǎn)為例��,提出了一種中藥制藥過(guò)程質(zhì)量控制方法并用于工業(yè)生產(chǎn)���,可有效提高三七總皂苷產(chǎn)品合格率。