抗體藥物研發(fā)�����、申報和生產(chǎn)過程均伴隨著對產(chǎn)品的質(zhì)量研究和質(zhì)量控制?����?贵w藥物質(zhì)量分析涉及多個方面�����,歐洲藥品管理局(EMA)和國際協(xié)調(diào)會議(ICH)指南Q6B[1,2]都要求對抗體藥物進(jìn)行表征�����,從理化�����、結(jié)構(gòu)性質(zhì)和雜質(zhì)等方面進(jìn)行廣泛而全面的質(zhì)量屬性表征研究�����,為生物技術(shù)產(chǎn)品的表征提供了一套統(tǒng)一的國際公認(rèn)原則�����,以支持抗體藥物的市場應(yīng)用?����?贵w藥物的結(jié)構(gòu)表征通常包括以下幾個方面�����,見表1�����。
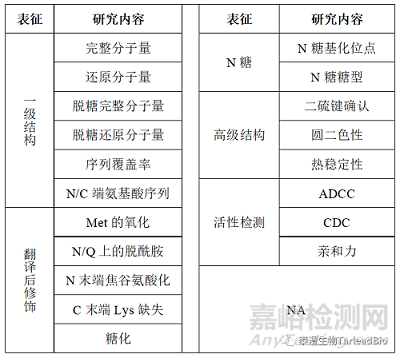
表1 表征研究內(nèi)容
1. 一級結(jié)構(gòu)
1.1. 分子量
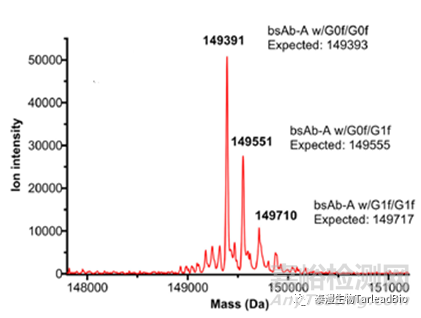
分子量分為完整分子量和還原分子量分子量�����,從整體來表征抗體分子�����,確認(rèn)抗體分子是否有片段缺失�����、錯配(圖1)�����。對于雙抗或其他多抗�����,目的分子和錯配分子(如同源二聚體)之間的分子量相差不大�����,小到相差十幾個Da�����,理化性質(zhì)差別小�����,用常規(guī)的色譜方法無法區(qū)分雙抗的錯配情況�����,需要用液相色譜-串聯(lián)質(zhì)譜(LC-MS/MS)檢測出的精確分子量來檢測錯配比例�����,指導(dǎo)早期CMC工藝的開發(fā)。此外�����,還可以用特異的N/O糖酶(PNGase F和O-糖酶)切掉抗體上的N/O糖�����,消除糖型對分子量檢測的影響�����,從而可以更準(zhǔn)確的表征抗體分子特性�����。
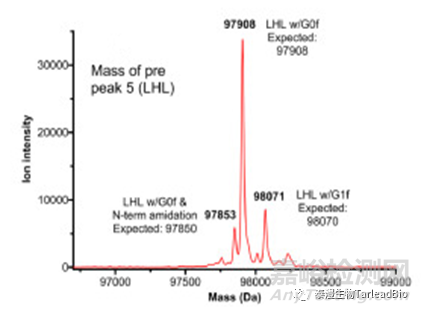
圖1 雙抗樣本的分子量[3]
上:目的分子的完整分子量�����;下:錯配類型(LHL型)的分子量
1.2. 氨基酸序列覆蓋率與N/C端序列確認(rèn)
除了分子量�����,還需要用肽圖來表征目的分子的氨基酸序列�����。樣本經(jīng)變性還原和烷基化后�����,加特異性酶酶切�����,經(jīng)LC-MS檢測分析�����,與理論序列比對�����,得到抗體的序列覆蓋率�����。常用的酶有胰蛋白酶(trypsin)�����、Glu-C和糜蛋白酶(chymotrypsin)等,根據(jù)各酶的特異性酶切位點選擇合適的酶(表2)�����。結(jié)合多種酶切結(jié)果�����,可以達(dá)到100%的序列覆蓋率�����,確認(rèn)抗體氨基酸序列(圖2)[4]�����。N/C端序列可以結(jié)合氨基酸覆蓋率結(jié)構(gòu)來分析�����,確認(rèn)末端序列與目的序列一致�����。
表2 常用蛋白酶的酶切位點
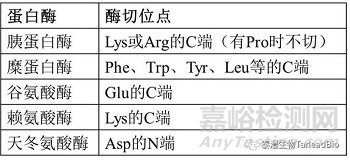
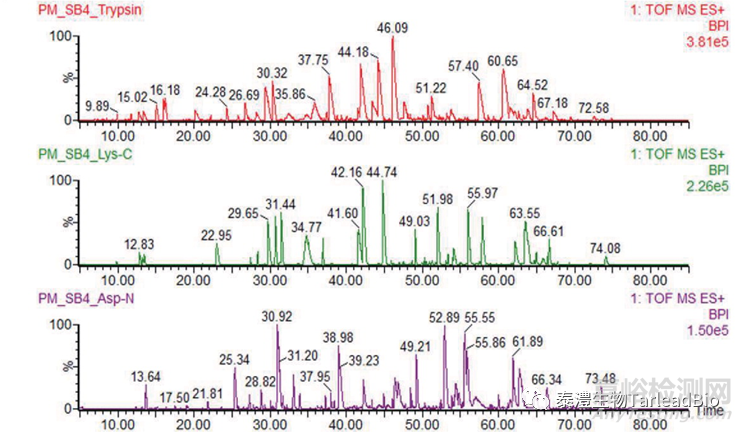
圖2 抗體的肽圖
從上至下分別為胰蛋白酶�����、賴氨酸酶和天冬氨酸酶酶切的肽圖
2.翻譯后修飾
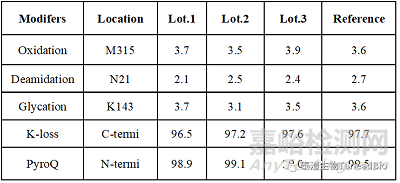
抗體分子在分泌�����、表達(dá)�����、純化和貯存過程中�����,受細(xì)胞內(nèi)和細(xì)胞外環(huán)境的影響�����,會發(fā)生翻譯后修飾�����,常見的修飾有甲硫氨酸(Met)上的氧化(oxidation)�����、天冬酰胺(N)上的脫酰胺(deamidation)、N末端Q上的環(huán)化(pyroQ)和C末端丟失賴氨酸(K loss)等�����。這些修飾會引起抗體的局部構(gòu)象和電荷發(fā)生變化�����,在IEF上表現(xiàn)出不同比例的酸堿峰�����。發(fā)生在CDR的修飾會影響活性�����,引起抗體藥物治療效果的下降�����。分析翻譯后修飾和序列覆蓋率的樣本酶解方式相差不大�����,根據(jù)序列比對結(jié)果�����,計算翻譯后修飾的位點和比例�����。翻譯后修飾是酸堿峰表征和產(chǎn)品可比性研究中常見的檢測項目�����。以某項目為例�����,在三批次產(chǎn)品的可比性研究中�����,對翻譯后修飾進(jìn)行表征�����,結(jié)果顯示�����,三個批次產(chǎn)品和參比品之間的修飾類型和比例保持一致(表3)。值得注意的是�����,樣本在處理過程中可能也會引入修飾�����,造成假陽性修飾�����,此時�����,可以使用低pH酶解條件等來降低樣本處理引入的修飾�����。
表3 可比性研究中不同批次之間的翻譯后修飾比例
3.N糖
單抗在重鏈CH2的N297位有保守的N糖基化位點(保守序列為NX-S/T)�����,多抗和重組蛋白通常有更多的N糖基化位點�����?����?贵w在內(nèi)質(zhì)網(wǎng)中開始N糖基化�����,達(dá)到高爾基體(Golgi)后進(jìn)一步糖基化�����,最終生成復(fù)雜的N糖糖型�����?����?贵w中常見的N糖糖型有G0、G0F�����、G1F�����、G2�����、G2F�����、Man5和Man8等�����。有研究顯示�����,在IgG1中�����, 沒有巖藻糖核心的糖(G0,G1等)�����,會增強抗體與FcRIIa的結(jié)合�����,進(jìn)而提高ADCC活性�����,因此�����,針對此特點可以開發(fā)不同巖藻糖化水平的抗體�����,控制ADCC活性�����。當(dāng)高甘露糖(Man5�����,Man8等)比例高時�����,抗體在人體內(nèi)的清除變快�����,降低抗體的治療效果�����。
表征中確認(rèn)N糖基化位點時�����,樣本先用N糖苷酶PNGase F切掉N糖�����,糖基化位點的天冬酰胺殘基發(fā)生脫氨基化�����,造成0.9840 Da的質(zhì)量增加,經(jīng)過酶解和LC-MS/MS分析�����,尋找發(fā)生+0.9840Da的天冬酰胺�����,確認(rèn)N糖糖基化位點�����。
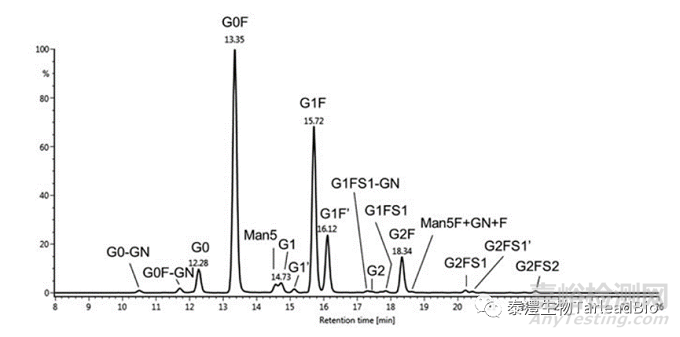
N糖糖型檢測時使用特異性的N糖苷酶PNGase F切掉N糖�����,因為N糖本身不能發(fā)熒光�����,需要用熒光試劑標(biāo)記N糖�����。常用的熒光標(biāo)記試劑有2-AB�����、2-AA�����、RapiFulor-MS和InstantPC等�����,市面上均有成熟的試劑盒�����,也可以自己配制使用�����。用HILIC分離熒光標(biāo)記的N糖�����,質(zhì)譜檢測分子量用于確定糖型�����,熒光檢測器檢測熒光強度用于定量,確定抗體的糖型和比例�����。圖3是一個IgG1類型抗體的N糖糖型熒光光譜[5]�����。
圖3 IgG1類型抗體的N糖糖型
4.高級結(jié)構(gòu)
4.1.二硫鍵確認(rèn)
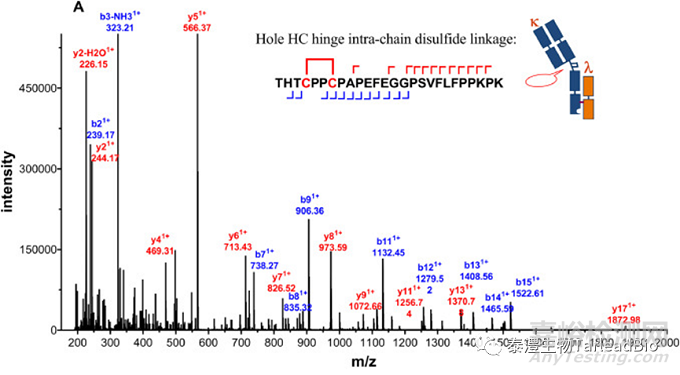
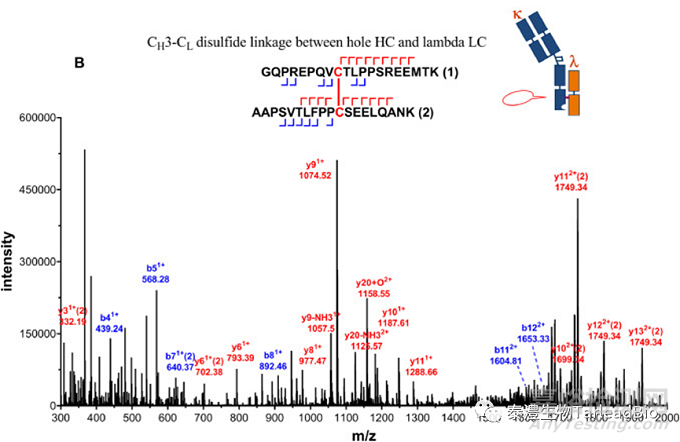
抗體的不同鏈之間通過二硫鍵鏈接�����,鏈內(nèi)也有二硫鍵存在�����,以維持抗體的空間結(jié)構(gòu)和活性�����。通常IgG1類型單抗有16個二硫鍵�����,雙抗和多抗擁有更多的二硫鍵�����,重組蛋白的二硫鍵更錯綜復(fù)雜�����,鏈接形式也更加多樣�����。二硫鍵鏈接方式直接和抗體的活性有關(guān)�����,錯配會導(dǎo)致活性完全喪失�����,因此有必要利用質(zhì)譜技術(shù)來表征樣本的二硫鍵鏈接方式�����。樣本在非還原狀態(tài)下經(jīng)過特異性酶切�����,在LC-MS上檢測分析,利用串級數(shù)據(jù)�����,得到二硫鍵配對結(jié)果(圖4)[3]�����。
圖4 用LC MS/MS方法確認(rèn)抗體的鉸鏈區(qū)(A)及重鏈-輕鏈鏈間(B)二硫鍵
4.2. 圓二色性
抗體的高級結(jié)構(gòu)是由主鏈折疊產(chǎn)生�����,如α螺旋�����、β折疊�����、轉(zhuǎn)角等�����,這些不對稱結(jié)構(gòu)使得抗體具有圓二色性�����。圓二色譜(Circular Dichroism�����,CD)法利用抗體的圓二色性和分子的不對稱性�����,根據(jù)左右偏振光吸收的不同來解析抗體的高級結(jié)構(gòu)�����。遠(yuǎn)紫外區(qū)(190-230mm)光譜可反映抗體的二級結(jié)構(gòu)�����,α螺旋�����、β折疊、轉(zhuǎn)角和不規(guī)則卷曲的比例�����。近紫外區(qū)(250-350mm)光譜反映抗體的三級結(jié)構(gòu)變化�����,側(cè)鏈生色基團(tuán)如色氨酸�����、苯丙氨酸�����、酪氨酸的排布信息和二硫鍵微環(huán)境的變化�����。
4.3. 熱穩(wěn)定性
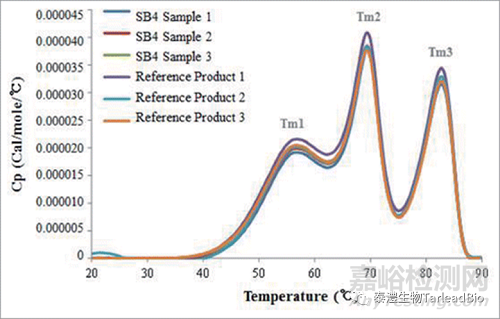
通常用DSC(differential scanning calorimetry)來表征抗體的熱穩(wěn)定性�����,用Tm(溶解溫度)表示�����,Tm越高表示抗體分子越穩(wěn)定�����。圖5是生物類似藥與原研藥表征時Tm的比較[4]�����,兩者有類似的Tm1�����、Tm2和Tm3�����,說明類似藥與原研藥的高級結(jié)構(gòu)一致�����。
圖5 生物類似藥與原研藥的Tm值比較
5.生物學(xué)活性
抗體活性可以分為Fc相關(guān)的親和力活性和細(xì)胞活性�����,是抗體發(fā)揮腫瘤殺傷活性的的發(fā)生機制。親和力結(jié)合活性比如Fc片段與FcγRIa�����、FcγRIIa�����、FcγRIIb�����、FcγRIIIa�����、FcγRIIIb�����、FcRn和C1q的結(jié)合活性�����,依據(jù)抗體的MOA設(shè)計實驗�����?����?贵w依賴的細(xì)胞毒性ADCC是抗體的Fc端與效應(yīng)細(xì)胞(主要是NK)表面的Fc受體(如FcγRIIIa/CD16)結(jié)合�����,介導(dǎo)效應(yīng)細(xì)胞殺傷腫瘤細(xì)胞�����。補體依賴的細(xì)胞毒性CDC是抗體Fc與補體系統(tǒng)的C1q結(jié)合�����,激活經(jīng)典補體通路�����,經(jīng)過一系列的信號放大�����,在靶細(xì)胞表面形成膜攻擊復(fù)合物,引起靶細(xì)胞裂解�����。常見的活性檢測方法有表面等離子共振和生物膜干涉等方法�����。
參考文獻(xiàn)
1.EMA. Guideline on Development, Production, Characterization and Specifications for Monoclonal Antibodies and Related Products (London, Dec. 2008).
2.ICH. Q6B Test Procedures and Acceptance Criteria for Biotechnological/Biological Products (1999).
3.Cao MY, et al. Characterization and Monitoring of a Novel Light-heavy-light Chain Mispair in a Therapeutic Bispecific Antibody. Journal of Pharmaceutical Sciences, 2021(110):2904-2915
4.Cho IH,et al. Evaluation of the structural, physicochemical, and biological characteristics of SB4, a biosimilar of etanercept. mAbs, 2016(8):1136-1155
5.Upton R,et al. Evaluating N-Glycosylation of a Therapeutic Monoclonal Antibody Using UHPLC-FLR-MS with RapiFluor-MS Labeling. Mass Spectrometry of Glycoproteins:189-203