近日����,國家藥監(jiān)局網(wǎng)站發(fā)布了八家醫(yī)療器械企業(yè)召回通告,其中涉及中國市場的只有三家企業(yè)�,對于該三家企業(yè)的召回產(chǎn)品及批次均未在國內(nèi)進口和銷售��,其他企業(yè)召回均不涉及中國地區(qū)。詳細信息見文章附件����。
通過召回信息的查看,我們關(guān)注到對于不同的情形召回級別不同��,有三級召回�、二級召回等區(qū)分,在召回報告中還需明確產(chǎn)品名稱�、注冊證或備案憑證、涉及地區(qū)和國家�、涉及產(chǎn)品批次和數(shù)量、召回原因��、糾正行動等內(nèi)容��。
接下來帶大家來回顧下醫(yī)療器械召回的法規(guī)要求��,對于國內(nèi)醫(yī)療器械產(chǎn)品的召回主要執(zhí)行《醫(yī)療器械召回管理辦法》����。
醫(yī)療器械召回,是指醫(yī)療器械生產(chǎn)企業(yè)按照規(guī)定的程序?qū)ζ湟焉鲜袖N售的某一類別��、型號或者批次的存在缺陷的醫(yī)療器械產(chǎn)品�,采取警示、檢查、修理�、重新標簽、修改并完善說明書�、軟件更新、替換�、收回、銷毀等方式進行處理的行為�。
2.醫(yī)療器械召回情形:
醫(yī)療器械召回有 主動召回、責令召回兩種情形�。
3.醫(yī)療器械召回缺陷:
召回所稱的存在缺陷的醫(yī)療器械產(chǎn)品包括:
(一)正常使用情況下存在可能危及人體健康和生命安全的不合理風險的產(chǎn)品;
(二)不符合強制性標準��、經(jīng)注冊或者備案的產(chǎn)品技術(shù)要求的產(chǎn)品�;
(三)不符合醫(yī)療器械生產(chǎn)、經(jīng)營質(zhì)量管理有關(guān)規(guī)定導致可能存在不合理風險的產(chǎn)品�;
(四)其他需要召回的產(chǎn)品。
4.召回的嚴重程度劃分:
根據(jù)醫(yī)療器械缺陷的嚴重程度��,醫(yī)療器械召回分為:
(一)一級召回:使用該醫(yī)療器械可能或者已經(jīng)引起嚴重健康危害的����;
(二)二級召回:使用該醫(yī)療器械可能或者已經(jīng)引起暫時的或者可逆的健康危害的����;
(三)三級召回:使用該醫(yī)療器械引起危害的可能性較小但仍需要召回的。
5. 召回時限的要求:
醫(yī)療器械生產(chǎn)企業(yè)作出醫(yī)療器械召回決定的,一級召回應當在1日內(nèi)����,二級召回應當在3日內(nèi),三級召回應當在7日內(nèi)��,通知到有關(guān)醫(yī)療器械經(jīng)營企業(yè)�、使用單位或者告知使用者。
附件:國家藥監(jiān)局網(wǎng)站召回通告�。
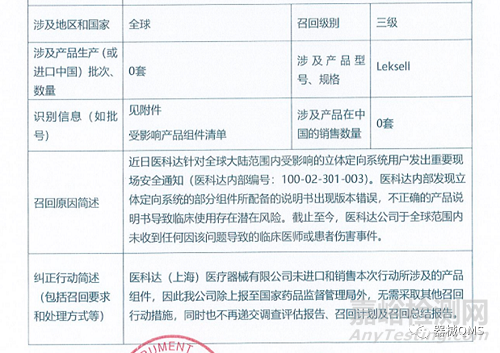
醫(yī)科達(上海)醫(yī)療器械有限公司報告,由于部分組件所配備的說明書出現(xiàn)版本錯誤�,生產(chǎn)商醫(yī)科達(瑞典)醫(yī)療器械有限公司Elekta Instrument AB對立體定向系統(tǒng)(國械注進20142056130)主動召回。召回級別為三級召回�。涉及產(chǎn)品的型號、規(guī)格及批次等詳細信息見《醫(yī)療器械召回事件報告表》�。
沃芬醫(yī)療器械商貿(mào)(北京)有限公司報告,由于特定批次不符合當前標簽上標示的24小時有效期的穩(wěn)定性聲明��,生產(chǎn)商儀器實驗室公司Instrumentation Laboratory Co.對活化的部分凝血活酶時間測定試劑盒(凝固法)HemosIL SynthAsil(國械注進20162404613)主動召回��。召回級別為二級召回�。涉及產(chǎn)品的型號、規(guī)格及批次等詳細信息見《醫(yī)療器械召回事件報告表》�。
奧森多醫(yī)療器械貿(mào)易(中國)有限公司報告,由于在某些情況下MicroTip試劑包可能會因其開蓋器組件的運行而損壞����,生產(chǎn)商奧森多臨床診斷(美國)股份有限公司Ortho-Clinical Diagnostics, Inc.對全自動生化免疫分析儀(國械注進20232220063)主動召回�。召回級別為三級召回����。涉及產(chǎn)品的型號、規(guī)格及批次等詳細信息見《醫(yī)療器械召回事件報告表》��。


賽諾龍(北京)醫(yī)療科技有限公司報告��,由于可能存在特定批次Picoway設備的變焦手柄的鏡片在組裝過程中錯誤倒置的問題�,生產(chǎn)商凱德朗公司Candela Corporation對Nd:YAG皮秒激光治療儀PicoWay Laser system(國械注進20173092289, 國械注進20173242289)主動召回。召回級別為三級召回����。涉及產(chǎn)品的型號、規(guī)格及批次等詳細信息見《醫(yī)療器械召回事件報告表》�。
徠卡顯微系統(tǒng)(上海)貿(mào)易有限公司報告,由于產(chǎn)品標簽上顯示了錯誤的有效期��,生產(chǎn)商徠卡生物系統(tǒng)(紐卡斯爾)有限公司Leica Biosystems Newcastle Ltd對清洗液 Bond Wash Solution 10X Concentrate(國械備20150492)主動召回�。召回級別為三級召回�。涉及產(chǎn)品的型號、規(guī)格及批次等詳細信息見《醫(yī)療器械召回事件報告表》�。
碧迪醫(yī)療器械(上海)有限公司報告�,由于軟件問題可能導致不正確的信息處理�,生產(chǎn)商碧迪科斯化有限公司 BD Kiestra B.V.對全自動微生物樣本處理系統(tǒng) BD Kiestra™ InoqulA+™ TLA(國械備20220143)主動召回。召回級別為二級召回��。涉及產(chǎn)品的型號�、規(guī)格及批次等詳細信息見《醫(yī)療器械召回事件報告表》。
奧林巴斯貿(mào)易(上海)有限公司報告��,由于電子氣管插管內(nèi)窺鏡的510(K) 追加信息中的再處理參數(shù)與之前銷售的電子氣管插管內(nèi)窺鏡標簽信息不一致�,生產(chǎn)商奧林巴斯醫(yī)療株式會社對電子氣管插管內(nèi)窺鏡(國械注進20183062428)主動召回。召回級別為三級召回����。涉及產(chǎn)品的型號、規(guī)格及批次等詳細信息見《醫(yī)療器械召回事件報告表》��。
奧林巴斯貿(mào)易(上海)有限公司報告����,由于部分地區(qū)發(fā)行的清洗消毒手冊中錯誤地描述了4K攝像頭可用高壓方式滅菌,生產(chǎn)商奧林巴斯醫(yī)療株式會社對內(nèi)窺鏡攝像系統(tǒng)(國械注進20182220250)主動召回�。召回級別為三級召回。涉及產(chǎn)品的型號�、規(guī)格及批次等詳細信息見《醫(yī)療器械召回事件報告表》。