背景
腦膠質(zhì)瘤是神經(jīng)外科治療中最棘手的難治性腫瘤之一���,膠質(zhì)母細(xì)胞瘤(GBM)是最高級(jí)別以及惡性程度最高(Ⅳ級(jí))的腦膠質(zhì)瘤,占顱內(nèi)原發(fā)性惡性腫瘤的45%���,中國每年確診的膠質(zhì)母細(xì)胞瘤患者超過45000例�����,常見療法是切除腫瘤��,再采取放療和化療手段延長壽命���。不過,膠質(zhì)母細(xì)胞瘤是神經(jīng)外科治療中最棘手的難治性腫瘤之一�����,患者的5年生存率不到5%。
腫瘤細(xì)胞非常的狡猾�����,即便目前的靶向和免疫治療已經(jīng)能夠非常精準(zhǔn)有效的殺傷一部分腫瘤細(xì)胞�����,但是���,它們還是會(huì)產(chǎn)生新的突變讓靶向藥不再起效��,或者偽裝自己讓免疫治療無法起效���,但不管癌細(xì)胞如何變化,它都有一個(gè)最基本特征-快速惡性分裂�����!如果能找到一種專門靶向這些快速分裂的癌細(xì)胞的治療方式���,就能有效的殺滅腫瘤并且不會(huì)傷及我們的正常細(xì)胞。
在2000年�����,以色列理工學(xué)院生理學(xué)和生物物理學(xué)榮譽(yù)教授Yoram Palti博士開辟了這種全新抗癌療法-電場(chǎng)治療,并成立了Novocure公司��,專門研究利用交替的低強(qiáng)度電場(chǎng)���,精準(zhǔn)的摧毀處于快速分裂的腫瘤細(xì)胞的新療法���,同時(shí)減少健康組織損傷,可很好地避免副作用影響患者生活質(zhì)量���。產(chǎn)品命名為optune��,中文名愛普盾�����,可穿戴治療設(shè)備���。
2011年和2015年,愛普盾先后獲得美國食品藥品監(jiān)督管理局批準(zhǔn)�����,用于治療復(fù)發(fā)和新診斷的膠質(zhì)母細(xì)胞瘤(GBM)成人患者。
2020年5月�����,Optune順利通過了在中國正式被國家藥品監(jiān)督管理局(NMPA)批準(zhǔn)上市���!用于治療組織學(xué)證實(shí)的復(fù)發(fā)性多形性膠質(zhì)母細(xì)胞瘤(GBM)的成年患者(22歲或以上)�����,以及與替莫唑胺聯(lián)合治療新診斷膠質(zhì)母細(xì)胞瘤���。中文名為愛普盾。TTFields具有局部有效��、全身毒副作用小���、牽一發(fā)動(dòng)全身的優(yōu)勢(shì)���,但TTFields仍需繼續(xù)克服其需長期佩戴、價(jià)格高且未進(jìn)醫(yī)保���、局部皮炎不良反應(yīng)等缺點(diǎn)��。


腫瘤電場(chǎng)由電場(chǎng)發(fā)生器 (TFH9100)���、電場(chǎng)貼片(INE9000、INE9000�����、WINF9020�����、INE9020W)電源適配器 (SPS9100) ��、電池(IBH9100)�����、電池充電器 (ICH9100) ��、連接電纜接線盒(CAD9100) 和選配件組成�����?��?蛇x配件:電池?cái)y帶包���、電場(chǎng)發(fā)生器攜帶包��、電場(chǎng)治療計(jì)劃軟件 (NovaTAL)��。其中電場(chǎng)貼片為一次性使用��,輻照滅菌��,有效期9個(gè)月�����。
它通過體外貼敷式電極片�����,向體內(nèi)病灶傳遞中頻(100-300kHz)�����、低場(chǎng)強(qiáng)(1-3V/cm)的交變電場(chǎng)���,破壞處于快速分裂狀態(tài)的腫瘤細(xì)胞���,是一種便攜���、低副反應(yīng)的新型局部治療方式�����。
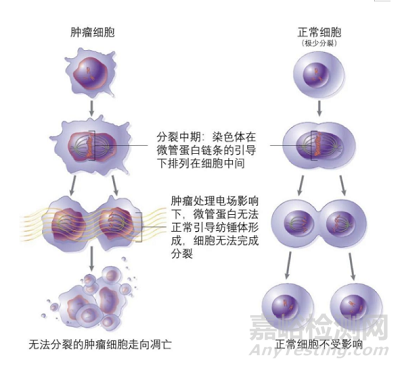
癌細(xì)胞是一群快速有絲分裂���,不受控制惡性增殖的細(xì)胞。在癌細(xì)胞分裂的中期�����,電場(chǎng)影響微管蛋白聚集成簇��,阻止紡錘體形成��,導(dǎo)致染色體無法正常分離��;在癌細(xì)胞分裂的末期�����,電場(chǎng)將電荷推向分裂細(xì)胞的頸部,破壞癌細(xì)胞結(jié)構(gòu)���。這兩種作用機(jī)制導(dǎo)致的最終結(jié)果都是抑制癌細(xì)胞正常分裂��,最終出現(xiàn)表面膜起泡��,癌細(xì)胞破裂�����,死亡��。
腫瘤電場(chǎng)現(xiàn)狀和市場(chǎng)情況
多年來��,膠質(zhì)母細(xì)胞瘤的治療方案更新緩慢��,直至腫瘤電場(chǎng)治療創(chuàng)新器械在中國內(nèi)地獲批��,成為15年來我國首個(gè)膠質(zhì)母細(xì)胞瘤突破性新療法�����,“手術(shù)+放化療+腫瘤電場(chǎng)治療”成為新的標(biāo)準(zhǔn)治療方案���。由于腫瘤電場(chǎng)治療需要長期佩戴��,膠質(zhì)母細(xì)胞瘤患者還需承擔(dān)相對(duì)較高的治療費(fèi)用��。
在國外�����,Optune 每個(gè)月的治療費(fèi)用是 21000 美元,主要用于購買一次性貼片��。目前���,Optune 在國外的收費(fèi)模式是患者購買治療療程�����,支付月治療費(fèi)用��,根據(jù)Novocure公司2015年披露的招股書�����,患者每月使用Optune費(fèi)用為2.1萬美金�����。也就是說���,一個(gè)患者接受Optune治療一年�����,費(fèi)用高達(dá)25.2萬美金�����,超過100萬人民幣�����。
國內(nèi)上市后�����,單片定價(jià)約3325元�����,一個(gè)月大約需要使用40片���,月治療費(fèi)超過13萬元�����,可申請(qǐng)分期付款���。通過保險(xiǎn)的方式,部分地區(qū)可以報(bào)銷60%-80%���。為了提高產(chǎn)品的可及性,針對(duì)低?��;颊咛峁┝舜壬品桨?��,低保患者可以無償獲得最多 6 盒(每盒 20 片)貼片�����。對(duì)于低收入患者進(jìn)行分期援助�����,第一期自費(fèi)使用 2 盒,免費(fèi)獲得 2 盒���,后續(xù)自費(fèi)使用 4 盒�����,可免費(fèi)獲得 8 盒�����。盡管已經(jīng)推出優(yōu)惠方案�����,但對(duì)于大多數(shù)患者而言��,腫瘤電場(chǎng)治療的價(jià)格依舊難以承受�����,如何進(jìn)一步提高患者可及性依舊是腫瘤電場(chǎng)研發(fā)企業(yè)不得不面對(duì)的問題��。另一方面�����,腫瘤電場(chǎng)治療對(duì)于患者的依從性要求很高���,患者每天都需要連續(xù)佩戴電極貼片18小時(shí)以上���,佩戴時(shí)間越長效果越好,睡覺也不能摘下��。由于極片需要產(chǎn)生電場(chǎng)��,而此過程中也會(huì)產(chǎn)熱��,高時(shí)可達(dá)41℃���,如果耐受不好的話很容易出現(xiàn)皮膚損傷,這也是實(shí)際使用中最常出現(xiàn)的副作用���。雖然皮損和腦腫瘤比起來輕得多��,還可通過糖皮質(zhì)激素軟膏等方式進(jìn)行緩解�����,不過相同位置的皮膚短期內(nèi)便不能再貼附極片��,移動(dòng)位置則會(huì)影響電場(chǎng)的覆蓋區(qū)域���,從而影響治療效果�����。
腫瘤電場(chǎng)發(fā)展趨勢(shì)
一方面�����,除了膠質(zhì)瘤��,如今腫瘤電場(chǎng)治療有四個(gè)重要的實(shí)體瘤適應(yīng)癥正在研發(fā)進(jìn)程中��,包括聯(lián)合吉西他濱治療胰腺癌��;聯(lián)合多西他賽或免疫檢查點(diǎn)抑制劑治療肺癌�����;序貫標(biāo)準(zhǔn)立體定向放射治療(SRS)治療非小細(xì)胞肺癌造成的腦轉(zhuǎn)移�����;聯(lián)合紫杉醇治療卵巢癌�����。針對(duì)中國人高發(fā)的胃腸道腫瘤的臨床試驗(yàn)也在籌劃中��。
另一方面���,處于十億美金的風(fēng)口��。據(jù)西格瑪醫(yī)學(xué)內(nèi)部數(shù)據(jù)顯示���,國內(nèi)一些新創(chuàng)企業(yè)也正在陸續(xù)開展臨床試驗(yàn)中或者處于試驗(yàn)結(jié)束階段。江蘇海萊新創(chuàng)��,湖南安泰康成�����,深圳等多家企業(yè)的研發(fā)�����,突破專利及生產(chǎn)壁壘���。預(yù)計(jì)未來幾年���,市場(chǎng)至少有 3-4家的企業(yè)及產(chǎn)品上市。南京西格瑪醫(yī)學(xué)作為臨床研究的 CRO 公司���,在方案設(shè)計(jì)���,臨床操作,數(shù)據(jù)管理和統(tǒng)計(jì)分析方面��,積累了豐富的經(jīng)驗(yàn)���。
臨床試驗(yàn)方案設(shè)計(jì)舉例
一���、試驗(yàn)?zāi)康模涸u(píng)價(jià)腫瘤電場(chǎng)治療儀用于新診斷幕上膠質(zhì)母細(xì)胞瘤治療的有效性和安全性臨床試驗(yàn)
二、入選標(biāo)準(zhǔn):
1.經(jīng)組織學(xué)/分子病理學(xué)確診的新診斷幕上膠質(zhì)母細(xì)胞瘤(WHO IV級(jí))或星形細(xì)胞瘤(WHO IV級(jí))患者(包括單發(fā)和多發(fā)病灶��,分級(jí)依據(jù)2016年WHO中樞神經(jīng)系統(tǒng)腫瘤分類與分級(jí)標(biāo)準(zhǔn)或cIMPACT-NOW update5)��;
2.腫瘤切除術(shù)(包括全切���、部分切除���、活檢)后6周內(nèi)(≤6周)開始同步TMZ放化療��,目前已完成腫瘤切除術(shù)和同步TMZ放化療(約60Gy)�����;
3.自愿參加本臨床試驗(yàn)�����,并已簽署知情同意書���。
三、排除標(biāo)準(zhǔn):
1.體內(nèi)已有或需使用電子植入物者��,包括但不限于心臟起搏器�����、植入型心律轉(zhuǎn)復(fù)除顫器���、胰島素泵���、腦部刺激器、脊髓刺激器�����、迷走神經(jīng)刺激器等��;
2.基線檢查時(shí)有以下表現(xiàn)者:
(1)血小板減少癥(血小板計(jì)數(shù)<80×10^9/L)���;
(2)中性粒細(xì)胞減少(中性粒細(xì)胞絕對(duì)計(jì)數(shù)<1.0×10^9/L)�����;
(3)CTCAE4級(jí)非血液學(xué)毒性(脫發(fā)���、惡心、嘔吐除外)���;
(4)顯著的肝功能損害(AST或ALT>正常上限的3倍)���;
(5)總膽紅素>正常上限的2倍;
(6)顯著的腎臟損害(血肌酐>1.7 mg/dL)���。
3.合并急性重癥感染���;
4.合并嚴(yán)重的心功能不全者��;
5.CT或MRI等影像學(xué)檢查有明顯顱內(nèi)壓升高表現(xiàn)(如中線結(jié)構(gòu)移位超過5mm�����,有臨床意義的視神經(jīng)乳頭水腫��,嘔吐�����,惡心或意識(shí)水平下降)��;
6.替莫唑胺過敏史��;年齡18-65 歲的患者, 性別不限�����。要求患者無嚴(yán)重心��、肝�����、腎及血液系統(tǒng)合并癥�����,無嚴(yán)重并發(fā)癥及嚴(yán)重全身感染���,無急性代謝紊亂,無嚴(yán)重免疫系統(tǒng)疾病��,伴有糖尿病者須控制血糖≤10mmol/L且保持該水平2周以上���。排除妊娠�����、哺乳期婦女和對(duì)銀有過敏史者�����,排除依從性差或生命垂危及不能完成療程者��。
四���、主要指標(biāo):無進(jìn)展生存期��。




