納米抗體����,1989年比利時(shí)科學(xué)家是從駱駝科家族中發(fā)現(xiàn)的僅含重鏈抗體HCAb的可變區(qū)(VHH)��。由于其體積小,結(jié)構(gòu)簡(jiǎn)單�,抗原結(jié)合親和力高����,以及在極端條件下的高穩(wěn)定性����。因此��,納米體在各種研究領(lǐng)域����,特別是在疾病的診斷和治療方面引起了極大的興趣�。從2018年����,世界上第一個(gè)基于納米抗體的藥物(卡普拉珠單抗)獲得批準(zhǔn),到2022年世界第一款雙特異性納米抗體Ozoralizumab獲批上市��。此外�,從國(guó)內(nèi)維度來(lái)看,康寧杰瑞的KN-035產(chǎn) (PD-L1靶點(diǎn)����,單鏈抗體FC融合)以及傳奇生物的首款納米抗體CAR-T細(xì)胞分別于2021以及2022年獲批上市,由此可見(jiàn)納米抗體正逐漸在生物制藥領(lǐng)域占有重要地位��。
1����、納米抗體的獨(dú)特結(jié)構(gòu)特征
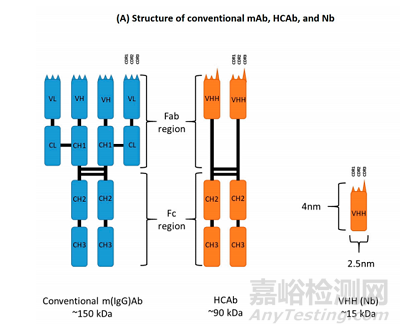
駝科動(dòng)物僅含重鏈的抗體(HCAb)由一個(gè)片段結(jié)晶區(qū)(Fc)�,直接連接到一個(gè)由單結(jié)構(gòu)域(VHH)組成的Fab片段。由于缺少輕鏈以及CH1區(qū)域納米抗體的分子量比傳統(tǒng)單克隆抗體減少了90 kDa��。其中HCAb的VHH片段��,大小約為2.5*4 nm, 分子量約為15 kDa����,可以結(jié)合廣泛抗原庫(kù),又稱(chēng)納米抗體(Nbs)。與傳統(tǒng)抗體的可變區(qū)(VH)類(lèi)似��,納米抗體VHH(Nbs)由四個(gè)保守區(qū)域(FR)和三個(gè)負(fù)責(zé)決定抗原特異性的高變互補(bǔ)決定區(qū)(CDR)組成��。與此同時(shí)納米抗體VHH與單克隆抗體的VH區(qū)域也存在一系列的差別����,首先由于缺乏輕鏈��,納米抗體通過(guò)三個(gè)CDR區(qū)域與抗原結(jié)合��,而單克隆抗體通常需要六個(gè)CDR區(qū)域才能與抗原結(jié)合。從結(jié)構(gòu)上看�,盡管納米抗體缺失了輕鏈����,但是其CDR1區(qū)域的結(jié)構(gòu)變異和CDR3區(qū)域長(zhǎng)度的增加,極大促進(jìn)了其抗原結(jié)合的多樣性��。此外��,傳統(tǒng)單抗VH結(jié)構(gòu)域的FR2主要由的疏水氨基酸殘基組成����,即V37/G44/L45/W47�,而納米抗體的FR2通常由親水性氨基酸殘基組成,即F37/E44/R45/G47����,這也就使得其能以可溶性單體的形式存在����。
圖1 單克隆抗體及僅含重鏈抗體以及納米抗體示意
2����、納米抗體單克隆抗體相比的優(yōu)勢(shì)以劣勢(shì)
與傳統(tǒng)單克隆抗體相比����,納米抗體的獨(dú)特結(jié)構(gòu)具有多種優(yōu)勢(shì)�。它們的小尺寸、凸形狀和延伸的CDR3賦予了它們的傘形結(jié)構(gòu)特征��,可以結(jié)合抗原的凹部分��,這些凹部分通常被認(rèn)為是阻塞的��,而分子量較大的單克隆抗體無(wú)法接近如��。與此同時(shí)納米抗體的微小尺寸并不妨礙結(jié)合親和力�,并且表現(xiàn)出與單克隆抗體相當(dāng)?shù)目乖Y(jié)合力�。此外,較小尺寸的納米抗體����,展現(xiàn)出較好的組織穿透性����,納米抗體-藥物偶聯(lián)物,可以穿透腫瘤,而傳統(tǒng)抗體-藥物偶聯(lián)物無(wú)法穿透腫瘤�。因此�,納米抗體展現(xiàn)出優(yōu)異的藥物遞送能力。
除了由于體積較小而已經(jīng)賦予它們的優(yōu)勢(shì)外��,納米抗體還具有一系列有利的生化特性。首先�,納米抗體在長(zhǎng)時(shí)間暴露于高溫下時(shí)表現(xiàn)出顯著的穩(wěn)定性����,這部分是由于其延長(zhǎng)的CDR3和變性后重新折疊的能力所造成的�。其次��,納米抗體由于其含有親水性FR2而具有高可溶性�,從而防止聚集并允許其作為單體發(fā)揮功能,而且它們還能夠在蛋白酶存在下保持穩(wěn)定����,并表現(xiàn)出對(duì)pH變化的抵抗力,因此納米抗體展現(xiàn)出口服給藥以及腹腔給藥的潛力。此外多項(xiàng)研究表明����,納米抗體具有較低的免疫原性,成為藥物開(kāi)發(fā)的理想潛在候選物�。此外,還可以通過(guò)將納米抗體的駱駝特異性氨基酸序列突變?yōu)槿祟?lèi)VH對(duì)應(yīng)序列(即人源化)從而進(jìn)一步降低發(fā)生副作用的風(fēng)險(xiǎn)��。最后�,傳統(tǒng)的單克隆抗體結(jié)構(gòu)復(fù)雜,需要繁瑣的純化步驟����,而納米抗體的生產(chǎn)和純化相對(duì)更簡(jiǎn)單,可以通過(guò)添加組氨酸標(biāo)簽��,使用固定金屬親和層析(IMAC)進(jìn)行純化。
雖然納米抗體具有許多令人滿意的特性�,但仍有一定的局限性。由于腎小球?yàn)V過(guò)的閾值為50-60 kDa�,其15 kDa的小尺寸導(dǎo)致血清持續(xù)時(shí)間低或腎臟清除迅速����,因此在診斷篩查和治療應(yīng)用方面存在劣勢(shì)�。一種解決策略是將納米抗體偶聯(lián)到聚乙二醇(PEG)或白蛋白上。其次����,納米抗體缺乏Fc區(qū)����,因此不能發(fā)揮與該部分相關(guān)的效應(yīng)功能����。然而,這個(gè)問(wèn)題可以通過(guò)偶聯(lián)到Fc區(qū)來(lái)增加治療能力來(lái)解決。
3、納米抗體開(kāi)發(fā)和生產(chǎn)
3.1 納米抗體發(fā)現(xiàn)
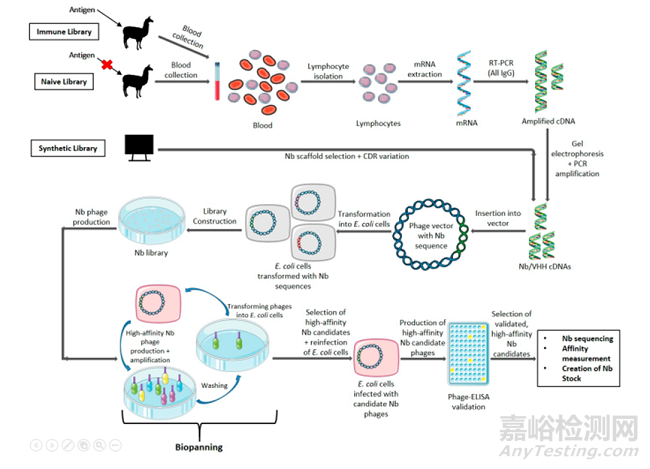
抗原特異性納米抗體可以從三個(gè)不同的來(lái)源中選擇��,即免疫動(dòng)物����、天然來(lái)源和文庫(kù)篩選�。免疫文庫(kù)通常由目標(biāo)抗原對(duì)駱駝科動(dòng)物(如羊駝或單峰駱駝)進(jìn)行免疫,通常在兩個(gè)月內(nèi)至少四次��。然后從提取的血液中純化淋巴細(xì)胞�,提取mRNA,然后進(jìn)行cDNA逆轉(zhuǎn)錄��。然后采用兩步聚合酶鏈反應(yīng)(PCR)方法��,首先從所有IgG的先導(dǎo)序列擴(kuò)增到CH2結(jié)構(gòu)域內(nèi)的保守區(qū)域�,然后瓊脂糖凝膠電泳選擇來(lái)自HCAb的序列,最后通過(guò)引物靶向活性限制性內(nèi)切酶位點(diǎn)擴(kuò)增VHH序列��。最后����,將獲得的擴(kuò)增子連接到載體中,并轉(zhuǎn)化為適當(dāng)?shù)谋磉_(dá)系統(tǒng)��,通常是大腸桿菌。一個(gè)典型的理想免疫庫(kù)應(yīng)該包含至少107個(gè)獨(dú)特轉(zhuǎn)化�。
一旦獲得納米抗體庫(kù),最常用的方法是利用噬菌體展示技術(shù)進(jìn)行篩選��,用M13噬菌體感染納米抗體文庫(kù)細(xì)胞����,產(chǎn)生含有納米抗體DNA序列的噬菌體。此外��,這些噬菌體將展示融合在其外殼蛋白上的納米抗體��,然后將其引入帶有粘附目標(biāo)抗原的微滴板�。通過(guò)pH沖擊洗脫陽(yáng)性結(jié)合物。多輪篩選丟棄親和性較弱的噬菌體�,從而排除非特異性結(jié)合納米抗體。接下來(lái)����,噬菌體再次被轉(zhuǎn)染到新的大腸桿菌細(xì)胞中�,在培養(yǎng)基中培養(yǎng),使用相應(yīng)抗生素為選擇標(biāo)記����。便于挑選出大量培養(yǎng)陽(yáng)性結(jié)合物�,此外它們可以通過(guò)酶聯(lián)免疫吸附試驗(yàn)(ELISA)進(jìn)行驗(yàn)證�,然后進(jìn)行測(cè)序以確定納米抗體核苷酸序列。最后����,為了確定親和力最高的結(jié)合劑,采用表面等離子體共振(SPR)����,進(jìn)行進(jìn)一步的篩選。含有最終序列的大腸桿菌用甘油進(jìn)行保菌����。
圖2 納米抗體發(fā)現(xiàn)流程-噬菌體展示技術(shù)
3.2 納米抗體表達(dá)與純化
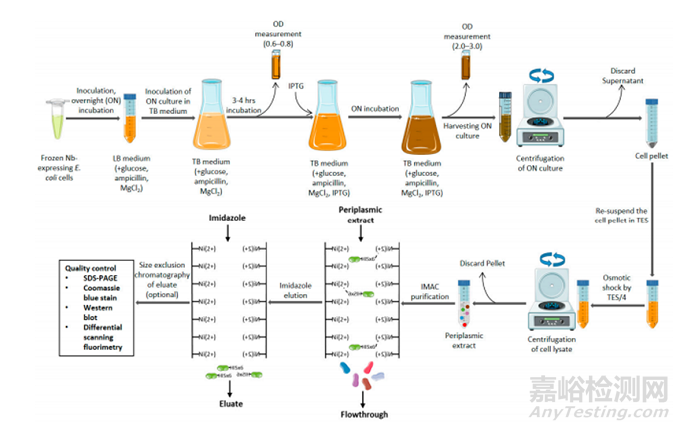
納米抗體的標(biāo)準(zhǔn)生產(chǎn)通常采用大腸桿菌表達(dá)系統(tǒng),用表達(dá)納米抗體的大腸桿菌細(xì)胞的甘油原液接種到(LB)培養(yǎng)基�,孵育過(guò)夜,然后依次接種到 (TB)培養(yǎng)基��。在達(dá)到足夠的生長(zhǎng)(OD:0.6-0.8)后����,通過(guò)添加1Mm IPTG進(jìn)行誘導(dǎo)納米抗體表達(dá),然后進(jìn)一步過(guò)夜孵育�。然后通過(guò)離心收集細(xì)胞(微球),通過(guò)裂解大腸桿菌獲得納米抗體上清液��,納米抗體的純化通常使用IMAC靶向與納米抗體初級(jí)序列相連的組氨酸標(biāo)簽,最后通過(guò)添加(0.5 M)咪唑溶液洗脫納米抗體��。
圖3 納米抗體表達(dá)與純化
4����、臨床研究進(jìn)展
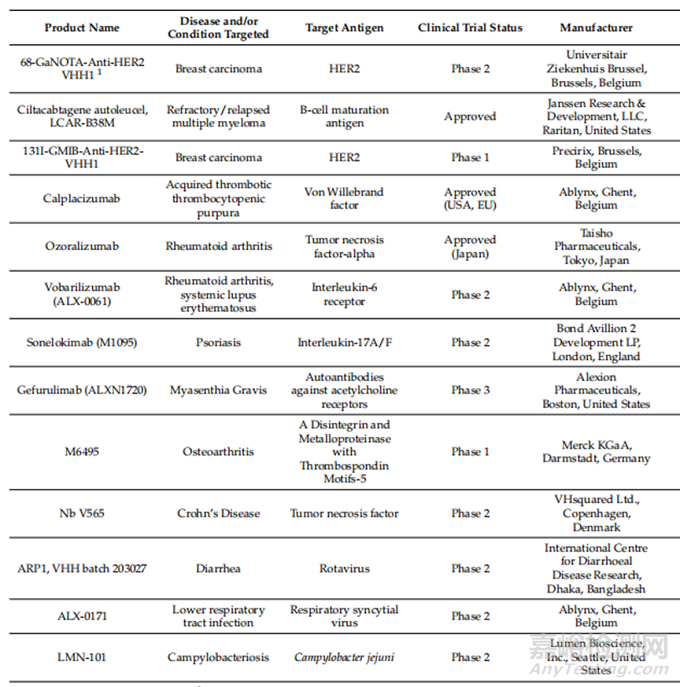
如表1所示,目前已有三種治療性納米抗體獲批�,多種納米抗體處于臨床實(shí)驗(yàn)階段。
4.1 納米抗體用于癌癥治療
納米抗體優(yōu)異的腫瘤穿透能力����、識(shí)別獨(dú)特抗原的能力等優(yōu)勢(shì)使其成為癌癥治療領(lǐng)域的一個(gè)有極大潛力的候選者。納米抗體癌癥治療的一個(gè)途徑是開(kāi)發(fā)CAR-T細(xì)胞��,表達(dá)腫瘤抗原特異性的納米抗體����。從患者體內(nèi)提取T細(xì)胞并對(duì)其進(jìn)行基因修飾,使其表達(dá)腫瘤抗原特異性納米抗體�,然后再注入患者體內(nèi),從而使T細(xì)胞通過(guò)釋放細(xì)胞毒性分子��、通過(guò)腫瘤壞死因子受體識(shí)別誘導(dǎo)細(xì)胞凋亡��、分泌炎性細(xì)胞因子等機(jī)制結(jié)合并中和腫瘤細(xì)胞��。2018年�,針對(duì)癌癥生物標(biāo)志物B細(xì)胞成熟抗原的Nb CAR -T 細(xì)胞候選物治療難治性/復(fù)發(fā)性多發(fā)性骨髓瘤的I期臨床試驗(yàn)結(jié)果顯示出令人滿意的結(jié)果。它成功地完成了I期臨床試驗(yàn)�,并進(jìn)行了進(jìn)一步的II期試驗(yàn),在首次給藥4年后進(jìn)行的隨訪研究也顯示,CAR-T細(xì)胞具有良好的長(zhǎng)期安全性和持久性����。基于I期和II期臨床試驗(yàn)的成功��,這種Nb CAR-T細(xì)胞候選藥物(更名為Ciltacabtagene autoeucel)于2022年2月被FDA批準(zhǔn)用于治療多發(fā)性骨髓瘤����。
4.2 納米抗體用于自身免疫疾病的治療
納米抗體在治療應(yīng)用方面取得最大成功的領(lǐng)域是自身免疫性疾病的治療。2018年����,Caplacizumab被歐盟批準(zhǔn)用于治療獲得性血小板減少紫癜(一種罕見(jiàn)的凝血疾病),這是納米抗體治療領(lǐng)域的里程碑式成功��。不久之后��,在2019年�,Caplacizumab也被美國(guó)FDA批準(zhǔn)用于消費(fèi)者處方。另一種已經(jīng)進(jìn)入商業(yè)市場(chǎng)的納米抗體治療藥物是Ozoralizumab,截至2022年9月�,以TNF- α為靶點(diǎn)的Ozoralizumab在日本被批準(zhǔn)用于治療類(lèi)風(fēng)濕性關(guān)節(jié)炎。
4.3 納米抗體用于抗感染
與腫瘤和自身免疫性疾病的廣泛候選納米抗體相反��,幾乎沒(méi)有針對(duì)病毒��、細(xì)菌和寄生蟲(chóng)引起的傳染病的治療候選納米抗體����。然而,也有一些針對(duì)傳染病的納米抗體治療藥物的報(bào)道�,如針對(duì)輪狀病毒的VHH 203027治療腹瀉和用于治療呼吸道合胞病毒下呼吸道感染的ALX-0171。目前暫未獲得積極進(jìn)展����。此外,一種用于治療空腸彎曲桿菌感染的納米抗體候選藥物L(fēng)MN-101已被報(bào)道�,目前正在進(jìn)行2期試驗(yàn)。治療性納米抗體的缺乏并不意味著納米抗體不適合開(kāi)發(fā)治療病毒��、細(xì)菌或寄生蟲(chóng)的療法����,而是表明這一領(lǐng)域在很大程度上仍處于起步階段。
表1 納米抗體臨床應(yīng)用進(jìn)展
5.總結(jié)
自從30多年前它們被偶然發(fā)現(xiàn)以來(lái)�,納米抗體的應(yīng)用領(lǐng)域呈指數(shù)級(jí)增長(zhǎng)納米抗體與傳統(tǒng)單克隆抗體相比具有許多優(yōu)勢(shì)��,這推動(dòng)了研究的發(fā)展����,此外�,在過(guò)去幾年中��,納米抗體治療癌癥和自身免疫性疾病的多種療法獲得批準(zhǔn)��,推動(dòng)了商業(yè)和工業(yè)的興趣�。因此,這一領(lǐng)域?qū)⒃诓痪玫膶?lái)進(jìn)一步發(fā)展��。此外�,納米抗體治療傳染病的潛力也已被證明明顯存在,但仍需要大量的研究和開(kāi)發(fā)����。因此,可以肯定的是����,在未來(lái)的幾年里,納米抗體將在下一代診斷工具和治療方法的發(fā)展中發(fā)揮重要作用�。
參考文獻(xiàn)
[1]Jin, B.-k.; Odongo, S.; Radwanska, M.; Magez, S. Nanobodies: A Review of Generation, Diagnostics and Therapeutics. Int. J. Mol. Sci. 2023, 24, 5994. https:// doi.org/10.3390/ijms24065994
[2]Bailon Calderon, H.; Yaniro Coronel, V.O.; Cáceres Rey, O.A.; Colque Alave, E.G.; Leiva Duran, W.J.; Padilla Rojas, C.; Montejo Arevalo, H.; García Neyra, D.; Galarza Pérez, M.; Bonilla, C.; et al. Development of Nanobodies Against Hemorrhagic and Myotoxic Components of Bothrops atrox Snake Venom. Front. Immunol. 2020, 11, 655
[3]Zimmermann, I.; Egloff, P.; Hutter, C.A.J.; Kuhn, B.T.; Bräuer, P.; Newstead, S.; Dawson, R.J.P.; Geertsma, E.R.; Seeger, M.A. Generation of synthetic nanobodies against delicate proteins. Nat. Protoc. 2020, 15, 1707–1741