據(jù)《醫(yī)療器械監(jiān)督管理條例》規(guī)定,第Ⅱ��、Ⅲ類醫(yī)療器械采用產(chǎn)品注冊管理方式����。
境內(nèi)第二類醫(yī)療器械由省、自治區(qū)�、直轄市藥監(jiān)局審查,批準后發(fā)給醫(yī)療器械注冊證��。
境內(nèi)第三類醫(yī)療器械由國家藥監(jiān)局審查����,批準后發(fā)給醫(yī)療器械注冊證。
進口第二類�、第三類醫(yī)療器械由國家藥監(jiān)局審查,批準后發(fā)給醫(yī)療器械注冊證�。香港、澳門��、臺灣地區(qū)醫(yī)療器械的注冊��、備案����,參照進口醫(yī)療器械辦理����。
2023年4月注冊備案信息匯總統(tǒng)計:
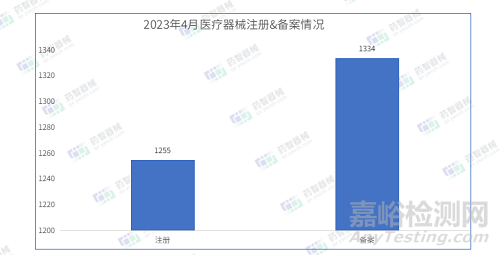
4月注冊批準醫(yī)療器械數(shù)量1255項
4月備案批準醫(yī)療器械數(shù)量1334項
4月優(yōu)先審批注冊醫(yī)療器械產(chǎn)品2項
4月創(chuàng)新審批注冊醫(yī)療器械產(chǎn)品12項
據(jù)最新統(tǒng)計����,2023年4月NMPA共批準注冊醫(yī)療器械1255項,同比減少7.4%��,其中優(yōu)先審批注冊2項����,創(chuàng)新審批注冊12項��;審批備案醫(yī)療器械數(shù)量1334項�,同比減少24.7%。
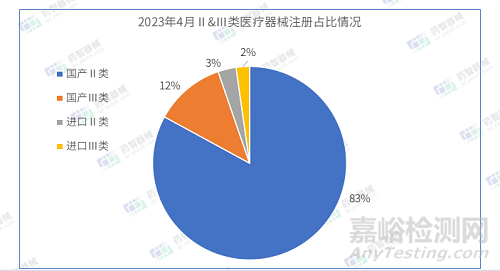
2023年4月����,國家藥監(jiān)局共批準注冊醫(yī)療器械產(chǎn)品1255項。其中�,國產(chǎn)第Ⅱ類醫(yī)療器械產(chǎn)品1041項,國產(chǎn)第Ⅲ類醫(yī)療器械產(chǎn)品148項����,進口第Ⅱ類醫(yī)療器械產(chǎn)品38項��,進口第Ⅲ類醫(yī)療器械產(chǎn)品28項�,國產(chǎn)占比94.7%����。
從產(chǎn)品類別來看,2023年4月注冊醫(yī)療器械中�,體外診斷試劑(363件),注輸�、護理和防護器械(268件)、及口腔科器械(91件)注冊數(shù)量排名前三�。
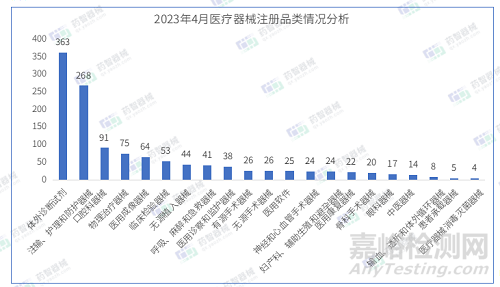
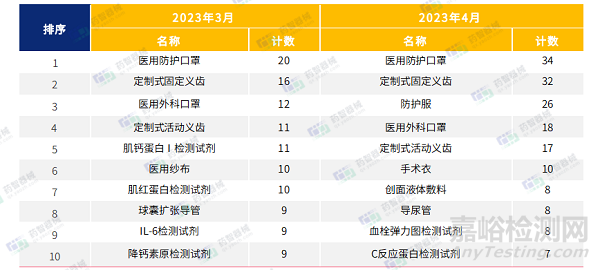
2023年3月-4月,醫(yī)用口罩等最重要的防護類醫(yī)療器械依舊是占據(jù)了醫(yī)療器械注冊產(chǎn)品數(shù)量排名第一的位置��。此外�,4月口腔科器械和創(chuàng)面液體敷料注冊數(shù)量較前兩月明顯增加。
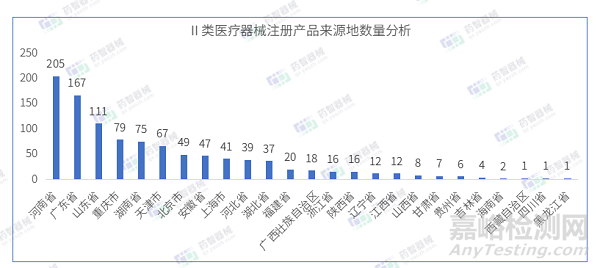
從Ⅱ類醫(yī)療器械注冊產(chǎn)品來源地分布來看�,國內(nèi)4月共有25個省市(不包括中國港澳臺)注冊Ⅱ類醫(yī)療器械,其中河南省注冊醫(yī)療器械數(shù)量最多�,占全部Ⅱ類醫(yī)療器械數(shù)量的19.6%。
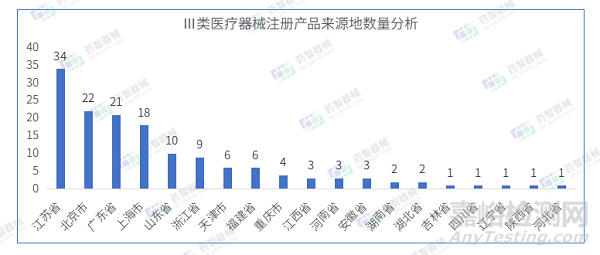
從Ⅲ類醫(yī)療器械注冊產(chǎn)品來源地分布來看��,國內(nèi)4月共有19個省市(不包括中國港澳臺)注冊Ⅲ類醫(yī)療器械�,其中江蘇省注冊醫(yī)療器械數(shù)量最多����,占全部Ⅲ類醫(yī)療器械數(shù)量的22.9%��。
據(jù)《醫(yī)療器械監(jiān)督管理條例》規(guī)定�,第一類醫(yī)療器械采用產(chǎn)品備案管理方式。
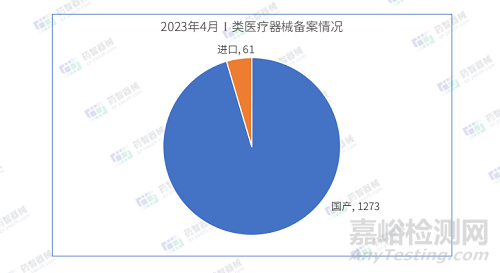
2023年4月國產(chǎn)Ⅰ類醫(yī)療器械備案批準數(shù)量1273項�,同比減少25.4%。同時��,進口第一類醫(yī)療器械備案批準數(shù)量61項����,同比減少7.5%。
4月醫(yī)療器械創(chuàng)新及優(yōu)先審批
根據(jù)《創(chuàng)新醫(yī)療器械特別審批程序(試行)》�,我國醫(yī)療器械創(chuàng)新審批是為了保障醫(yī)療器械的安全、有效����,鼓勵醫(yī)療器械的研究與創(chuàng)新����,促進醫(yī)療器械新技術(shù)的推廣和應(yīng)用,推動醫(yī)療器械產(chǎn)業(yè)發(fā)展的特殊審批通道����。
2023年4月����,全國創(chuàng)新審批注冊產(chǎn)品共計12項�,均為國產(chǎn)創(chuàng)新醫(yī)療器械產(chǎn)品。
從產(chǎn)品類別來看:12項均為器械產(chǎn)品��,無試劑產(chǎn)品����。
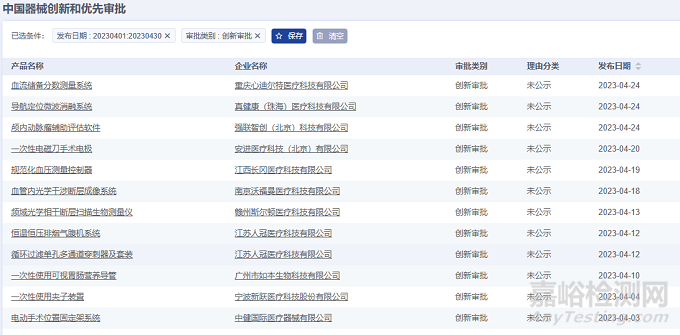
2023年4月共有六個省市注冊創(chuàng)新審批醫(yī)療器械,其中江蘇省和北京市注冊數(shù)量排名并列第一��。
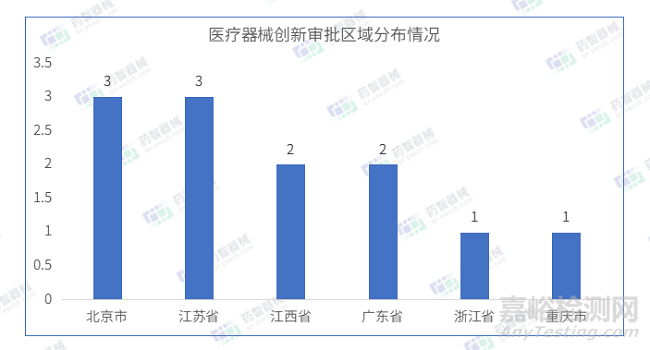
2016年10月25日����,國家藥監(jiān)局發(fā)布《醫(yī)療器械優(yōu)先審批程序》,于2017年1月1日起施行�。根據(jù)《醫(yī)療器械優(yōu)先審批程序》,對下列醫(yī)療器械實施優(yōu)先審批:
一是診斷或治療罕見病��、惡性腫瘤且具有明顯臨床優(yōu)勢的醫(yī)療器械��,診斷或治療老年人特有和多發(fā)疾病且尚無有效診斷或治療手段的醫(yī)療器械��,專用于兒童且具有明顯臨床優(yōu)勢的醫(yī)療器械;
二是列入國家科技重大專項或國家重點研發(fā)計劃的醫(yī)療器械����。
此外,將根據(jù)各方面情況和意見��,組織專家審查后�,確定對“其他應(yīng)當(dāng)優(yōu)先審批的醫(yī)療器械”予以優(yōu)先審批。
2023年4月��,全國優(yōu)先審批注冊產(chǎn)品共計2項�,均為國產(chǎn)醫(yī)療器械產(chǎn)品。從產(chǎn)品類別來看:均為器械產(chǎn)品��,無試劑產(chǎn)品��。
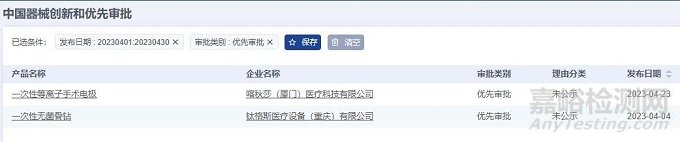
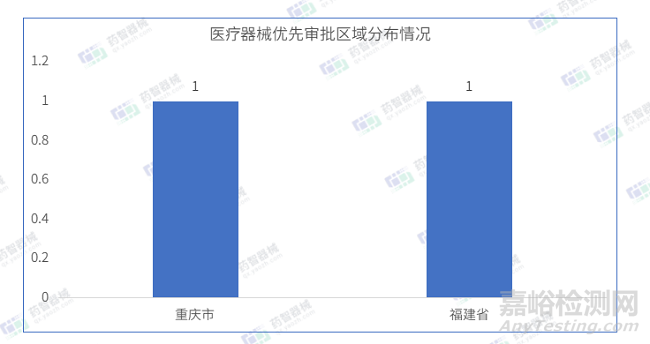
2023年4月共有2個省市注冊醫(yī)療器械進入優(yōu)先審批����,產(chǎn)品注冊數(shù)量均為1項。
4月醫(yī)療器械注冊企業(yè)分析
2023年4月國內(nèi)注冊醫(yī)療器械企業(yè)達675家����。排行前十的企業(yè)中�,排名前三的分別是:鄭州藍躍生物科技股份有限公司��、雅博捷銳(重慶)醫(yī)療科技有限公司��、安陽國醫(yī)扁鵲健康科技有限公司����,排行前十的企業(yè)情況如下圖所示�。
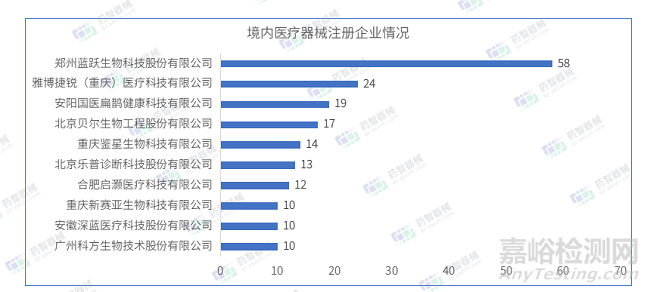
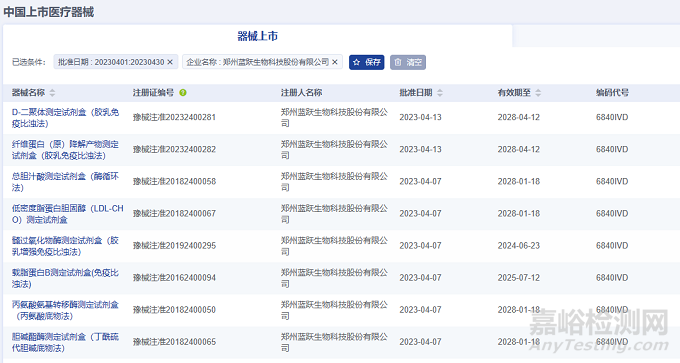
2023年4月,鄭州藍躍生物科技股份有限公司在北京市藥監(jiān)局完成了58項醫(yī)療器械��,注冊產(chǎn)品數(shù)量排名第一��,均為Ⅱ類IVD診斷試劑產(chǎn)品����。
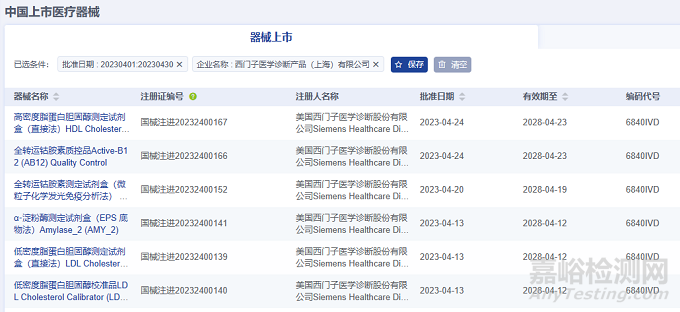
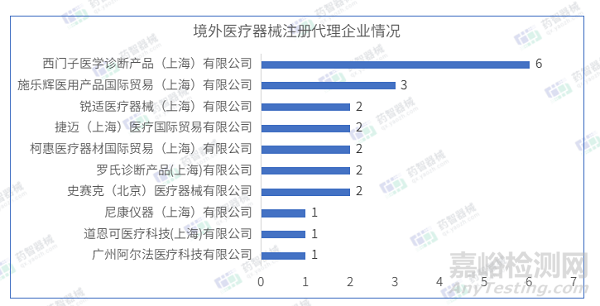
2023年4月進口醫(yī)療器械注冊代理人企業(yè)達54家。排行前十的企業(yè)中��,排名前三的分別是:西門子醫(yī)學(xué)診斷產(chǎn)品(上海)有限公司����、施樂輝醫(yī)用產(chǎn)品國際貿(mào)易(上海)有限公司、銳適醫(yī)療器械(上海)有限公司�,排行前十的企業(yè)情況如下圖所示。
西門子醫(yī)學(xué)診斷產(chǎn)品(上海)有限公司代理6項進口醫(yī)療器械����,均為Ⅱ類體外診斷試劑產(chǎn)品����。