2023年5月24日�,識林聯(lián)合北京大學(xué)知識工程與監(jiān)管科學(xué)實驗室�,在浙江省藥品監(jiān)督管理局的指導(dǎo)以及臺州市局的支持下�����,在臺州舉辦了“《藥品GMP指南》(原料藥和質(zhì)量控制實驗室與物料系統(tǒng)分冊)研討交流會”。
在本次研討會中���,識林知識平臺研究員�����,藥品GMP指南(第2版)項目課題組王國旭博士做了《原料藥企業(yè)的FDA檢查缺陷研究》專題報告,報告分為五個部分�����,分別為:原料藥高頻檢查缺陷分析���、原料藥特有的高頻檢查缺陷和舉例�����、中國原料藥企業(yè)常見檢查缺陷分析、原料藥企業(yè)檢查員舉例分析��、如何應(yīng)對檢查 – GMP審計工具簡介���。本文介紹第三部分:中國原料藥企業(yè)常見檢查缺陷分析。
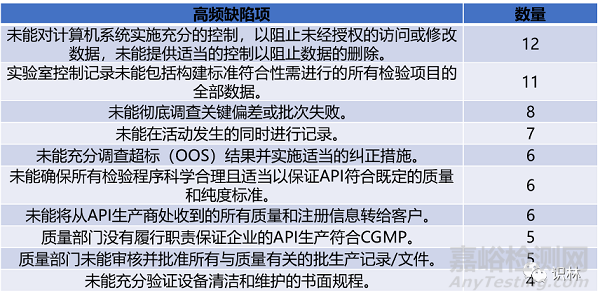
王國旭博士統(tǒng)計分析了識林警告信數(shù)據(jù)庫中2013年至今40封中國原料藥中譯警告信�,在這40封警告信中����,缺陷項總數(shù)為104條��,其中出現(xiàn)頻率最高的10類缺陷項,總數(shù)為70條�,占比達(dá)到67.3%���。下表統(tǒng)計了出現(xiàn)頻率最高的10類缺陷項的描述��,以及在這40封警告信中出現(xiàn)的數(shù)量��?����?梢钥吹?,中國原料藥企業(yè)差異大���,top10缺陷項分布較為平均。
表1. 中國原料藥企業(yè)高頻檢查缺陷項:top10
隨后,王國旭博士將此前統(tǒng)計的原料藥企業(yè)top10缺陷項與中國原料藥企業(yè) top10缺陷項進(jìn)行了對比��,來分析FDA對中國原料藥企業(yè)檢查的重點(見表2)。
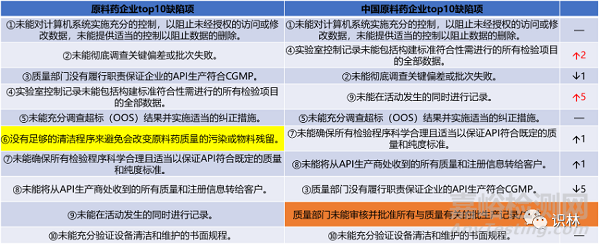
表2. 原料藥企業(yè)vs中國原料藥企業(yè) top10缺陷項對比
從表2中可以看到�,中國原料藥企業(yè)與原料藥企業(yè)總體 top10缺陷項類別多數(shù)是相同的��。不同之處主要有以下幾個方面:
“沒有足夠的清潔程序來避免會改變原料藥質(zhì)量的污染或物料殘留”這一缺陷項沒有出現(xiàn)在中國原料藥企業(yè) top10缺陷項中,取而代之的是“質(zhì)量部門未能審核并批準(zhǔn)所有與質(zhì)量有關(guān)的批生產(chǎn)記錄/文件”這一缺陷項�,說明FDA對中國原料藥企業(yè)質(zhì)量部門對批生產(chǎn)和文件記錄的審核是比較關(guān)注的����。
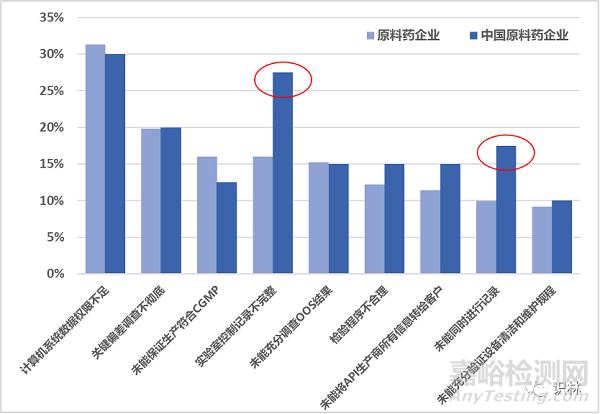
“實驗室控制記錄未能包括構(gòu)建標(biāo)準(zhǔn)符合性需進(jìn)行的所有檢驗項目的全部數(shù)據(jù)”這一缺陷項在中國原料藥企業(yè)中排名上升了兩位,“未能在活動發(fā)生的同時進(jìn)行記錄”排名上升了5位之多��。從圖1中也可以看到���,這兩類缺陷項在中國原料藥企業(yè)警告信中出現(xiàn)的比例顯著高于原料藥企業(yè)總體�。由此可見����,實驗室控制記錄完整性����、同步記錄等數(shù)據(jù)可靠性問題是FDA對中國原料藥企業(yè)檢查的重點。
此外����,偏差調(diào)查和OOS調(diào)查無論是否在中國原料藥企業(yè)�,都始終是FDA檢查關(guān)注的重點��。
圖1. 高頻缺陷項在原料藥企業(yè)和中國原料藥企業(yè)警告信中出現(xiàn)的比例對比
通過以上分析可以得出結(jié)論:1. 中國原料藥企業(yè)與原料藥企業(yè)高頻缺陷項總體差別不大。2. 數(shù)據(jù)可靠性問題仍是FDA對中國原料藥企業(yè)關(guān)注的重點�。