導(dǎo) 讀
本篇內(nèi)容詳細(xì)介紹了作為人工器官潛在的治療方法之3D生物打印���,詳細(xì)介紹了目前在研究階段的3D打印技術(shù)以及技術(shù)對(duì)比���,其次介紹了打印所用的天然材料和高分子材料及相應(yīng)的優(yōu)缺點(diǎn)���,最后介紹了材料結(jié)合細(xì)胞的打印方式��。
(一)3D打印技術(shù)
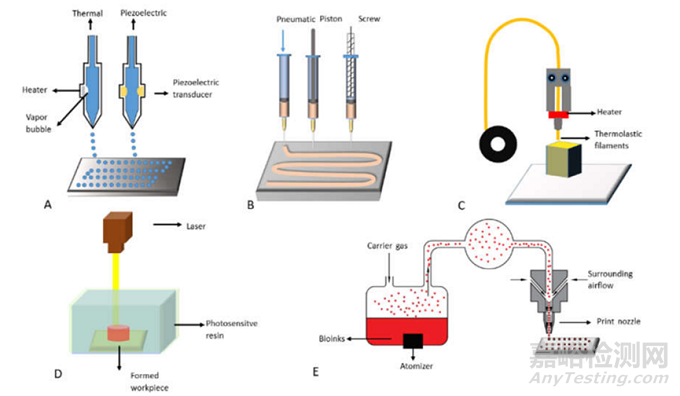
與傳統(tǒng)制造技術(shù)相比���,3D打印技術(shù)在生物人工器官制造方面具有諸多優(yōu)勢(shì)�����,尤其適用于快速���、精準(zhǔn)��、定制化的生物醫(yī)學(xué)應(yīng)用�����。如下圖所示是目前研究中常用的3D打印技術(shù):
(A)噴墨3D打?�。↖nkjet 3D printing)��;基于噴墨的 3D 打印是一種非接觸式增材制造(AM)技術(shù)�����,改編自工業(yè) 2D 打印機(jī)��。在傳統(tǒng)的 2D 打印中��,一層液滴被選擇性地沉積���,而在 3D 生物打印中,可以通過改變“生物墨水”和沉積層的內(nèi)容���,將細(xì)胞和蛋白質(zhì)打印成所需的器官形狀�����。按需噴墨打印機(jī)是最常用的設(shè)備��,由聲學(xué)���、熱學(xué)���、壓電或靜電噴墨噴嘴組成。噴墨打印機(jī)通常用于打印用于細(xì)胞接種的組織工程支架���。但打印分辨率差��、打印速度慢等問題極大地限制了其保真度和臨床推廣1��;
( B ) 基于擠壓的 3D 打?����。‥xtrusion based 3D printing);與 FDM 類似���,基于擠壓的 3D 打印將“生物墨水”從注射器或噴嘴沉積到基于 CAD 模型的構(gòu)建平臺(tái)上���,但該過程不涉及任何加熱過程��。含有細(xì)胞�����、生長(zhǎng)因子和其他生物活性劑的聚合物溶液或水凝膠可以通過氣動(dòng)壓力或物理壓力的方式通過噴嘴擠出��。
與其他3D打印工藝相比��,基于擠壓的3D打印技術(shù)提供了更高的打印速度���。隨著擠壓3D 打印技術(shù)的發(fā)展,多種細(xì)胞類型可以以非常高的細(xì)胞密度與不同的生物相容性聚合物溶液/水凝膠一起沉積��。聚合物溶液或水溶膠的固化是通過一系列物理和化學(xué)方法��,如物理交聯(lián))��、聚合���、化學(xué)交聯(lián)和酶促反應(yīng)2��。
打印后的細(xì)胞活力在40%到80%的范圍內(nèi)�����。通過優(yōu)化打印參數(shù)�����,如沉積速率�����、壓力和溫度��,可以提高細(xì)胞存活率3��。
( C ) 熔融沉積成型(Fused deposition modeling��,F(xiàn)DM)��;通過一個(gè)或多個(gè)帶有小孔的加熱擠壓頭��,以特定的鋪設(shè)模式逐層沉積熔融熱塑性聚合物���,也被稱為“熱塑性擠出”��。在 FDM 中���,將熱塑性聚合物熔化成半液態(tài),然后將半液態(tài)聚合物逐層擠出到平臺(tái)上�����。擠出前的熱塑性聚合物一般呈絲狀或顆粒狀���。當(dāng)熱塑性聚合物被加熱到高于其熔點(diǎn)的溫度時(shí)�����,它會(huì)變成流體并從噴嘴中流出��。一旦塑料聚合物從噴嘴中流出�����,它就會(huì)硬化并與下面的層結(jié)合��。一旦構(gòu)建了一層���,降低平臺(tái)或升高噴嘴��,擠出噴嘴沉積另一層4���。FDM技術(shù)在器官3D打印領(lǐng)域的致命缺點(diǎn)之一是細(xì)胞、生長(zhǎng)因子和其他生物活性劑不能在高聚合物熔化溫度下直接打印�����。
( D )立體光刻(Stereolithography���,SLA)��;最早出現(xiàn)的 3D 打印技術(shù)�����,SLA 是最成熟的 3D 打印方式�����,在業(yè)界得到廣泛應(yīng)用���。在 SLA 中,主要利用紫外激光為光源,再用振鏡系統(tǒng)來控制激光光斑掃描��,激光束會(huì)在液體樹脂表面上先畫出一個(gè)物件形狀��,隨后打印平臺(tái)會(huì)下降一定距離���,再讓平臺(tái)浸入液體樹脂中,如此反復(fù)���,形成實(shí)體打印��。
與其他傳統(tǒng)方法相比���,光固化生物3D打印具有靈活性高、分辨率高���、制造速度快等特點(diǎn)���。這些特性使其廣泛應(yīng)用于角膜基質(zhì)組織再生、胰島素輸送�����、組織工程支架制造等領(lǐng)域5。
目前SLA的缺點(diǎn)也很明顯6:
打印技術(shù)局限性:不同的SLA技術(shù)對(duì)燈管波長(zhǎng)��、打印尺寸�����、“生物墨水”黏度要求不同�����,難以標(biāo)準(zhǔn)化�����。
材料局限性:可用作“生物墨水”的光固化生物材料較少���,且具有所需的低粘度�����。
成本限制:SLA儀器及其打印的生物材料價(jià)格昂貴���,導(dǎo)致臨床試驗(yàn)受限。
( E ) 氣溶膠噴射打?����。ˋerosol jet printing):氣溶膠噴射打印是一種非接觸式打印方法,具有高分辨率和靈活性�����。“生物墨水”被放置在霧化發(fā)生器中�����,并通過超聲波或氣動(dòng)霧化成氣溶膠顆粒�����,然后通過惰性氣體輸送到打印噴嘴7��。
該方法可以打印在金屬�����、半導(dǎo)體���、聚合物等多種基材上,產(chǎn)品廣泛應(yīng)用于電子領(lǐng)域��。醫(yī)療設(shè)備主要是對(duì)柔性、可拉伸和可穿戴電子產(chǎn)品的探索�����。但研究表明���,超聲處理可使DNA變性�����,限制了其在生物醫(yī)學(xué)領(lǐng)域的應(yīng)用���。到目前為止,除了心臟補(bǔ)片工程和蛋白質(zhì)檢測(cè)外��,很少有使用該方法進(jìn)行 3D 打印器官的研究8���。
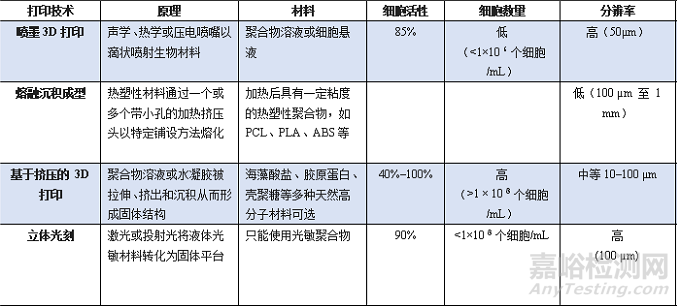
表 打印技術(shù)對(duì)比
(二)3D生物材料墨水
生物墨水是指位于 3D 或生物材料內(nèi)的細(xì)胞或細(xì)胞聚集體���。在生物打印領(lǐng)域,生物墨水指的是載有細(xì)胞�����,生物材料墨水單純指材料即無細(xì)胞。因此��,構(gòu)成生物墨水的生物材料必須作為細(xì)胞載體�����,生物材料墨水可以打印���,但只能在打印后播種細(xì)胞�����。如下圖所示9:
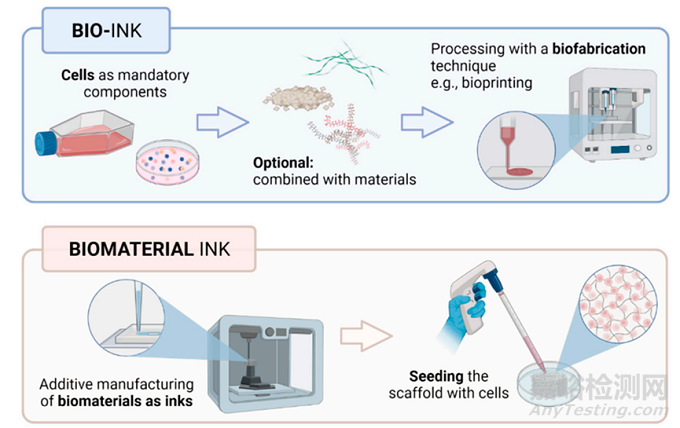
3D打印材料作為承載細(xì)胞以及相關(guān)因子的重要載體���,材料必須具有如下的特點(diǎn)10:
a.可打印性:即用于打印的材料必須可以在一定的時(shí)間內(nèi)精確地沉積在所指定的空間內(nèi)�����,該性能直接關(guān)系到3D打印產(chǎn)品是否能取得期望的結(jié)構(gòu)與尺寸精度���;打印參數(shù)如噴頭尺寸�����,會(huì)直接影響到材料內(nèi)細(xì)胞所受到的剪切應(yīng)力及材料沉積形成3D結(jié)構(gòu)所需的時(shí)間��,需要同時(shí)考慮對(duì)細(xì)胞活性的保護(hù)能力���;
b.生物相容性:從最初的要求材料能夠與組織器官共存���,且不引起宿主任何不良的局部或系統(tǒng)反應(yīng),發(fā)展到植入材料需要與宿主產(chǎn)生積極的相互作用���,包括與宿主組織和/或免疫系統(tǒng)的相互作用�����,以達(dá)到調(diào)控宿主細(xì)胞���、組織和器官活性與功能的目的;生物相容性主要受材料的化學(xué)組成�����、結(jié)構(gòu)形態(tài)(如多孔結(jié)構(gòu)/絲狀結(jié)構(gòu))���、表面特性(如親疏水性)��、表面電荷以及材料的力學(xué)性能��、物理化學(xué)特性等因素的影響�����;
c.力學(xué)穩(wěn)定性:材料具有一定的力學(xué)強(qiáng)度�����,能夠一定程度上抵抗外界作用力�����,維持打印物的形貌結(jié)構(gòu)��,在3D打印構(gòu)建組織器官的相關(guān)研究中���,應(yīng)根據(jù)不同靶組織器官(如皮膚、肝臟���、軟骨��、骨等)所需的結(jié)構(gòu)力學(xué)環(huán)境���,選用具有相應(yīng)力學(xué)特性的打印材料���;
d.降解特性:理想的生物打印材料,植入體內(nèi)后應(yīng)當(dāng)隨著細(xì)胞的增殖及細(xì)胞外基質(zhì)(ECM)的產(chǎn)生而逐漸降解���,且降解速率應(yīng)當(dāng)與細(xì)胞產(chǎn)生ECM替換植入材料的速率�����,及新組織生成的速率相匹配��,同時(shí)降解產(chǎn)物應(yīng)該無毒�����。易于代謝���,能夠快速代謝排除體外;
f.仿生學(xué)特性:材料仿生學(xué)特性有利于刺激細(xì)胞響應(yīng).在生物材料中摻入生物活性組分可對(duì)內(nèi)源或外源細(xì)胞的粘附�����、遷移、增殖及功能表達(dá)產(chǎn)生積極作用�����,材料表面性質(zhì)如化學(xué)基團(tuán)的修飾���、粗糙度�����、親疏水性�����、微納米結(jié)構(gòu)等直接影響到細(xì)胞的鋪展形狀�����、分化過程���、運(yùn)動(dòng)、取向���、細(xì)胞骨架的組裝,甚至是細(xì)胞內(nèi)部的相關(guān)信號(hào)通路��。11
1、生物打印材料
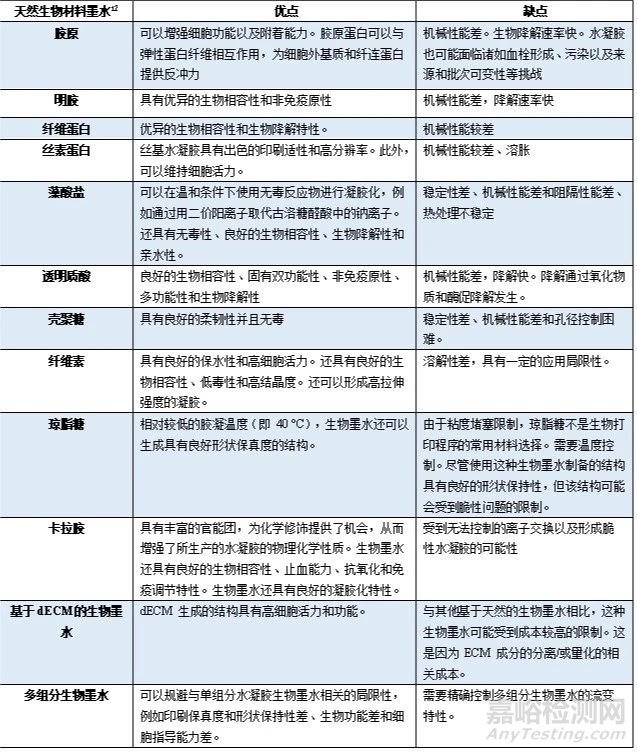
用于生物3D打印的高分子材料可分為合成高分子材料與天然高分子材料���。用于生物3D打印的天然高分子材料有三個(gè)突出特點(diǎn):良好的生物相容性�����、較差的機(jī)械強(qiáng)度和快速的生物降解性���。經(jīng)過幾十年的探索,常用的高分子材料的性質(zhì)總結(jié)如下表:
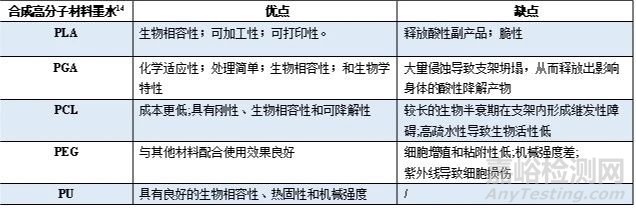
合成高分子網(wǎng)絡(luò)由可重復(fù)的惰性單元組成���。它們通常在機(jī)械性能和免疫原性反應(yīng)方面優(yōu)于天然高分子材料�����。常用的可生物降解合成聚合物包括 PLA���、PGA、PU���、PLGA 和 PCL��。與天然聚合物相比�����,大多數(shù)合成聚合物明顯優(yōu)點(diǎn)包括合成方便�����、資源豐富�����、易加工��、耐壓�����、重量輕��、成本低��。其特點(diǎn)總結(jié)如下表13:
2��、多材料3D打印
材料在體外打印構(gòu)建組織器官時(shí)���,需起到保護(hù)支撐��、維持活性��、誘導(dǎo)分化��、引導(dǎo)新生以及促使功能成熟等多重功能�����。因此�����,任何單一組分的材料都不可能兼具重構(gòu)組織功能所需的所有特性�����。開發(fā)多材料3D打印成為一個(gè)必然的趨勢(shì)��。多材料比單一材料方法更好地復(fù)制其宿主微環(huán)境��。
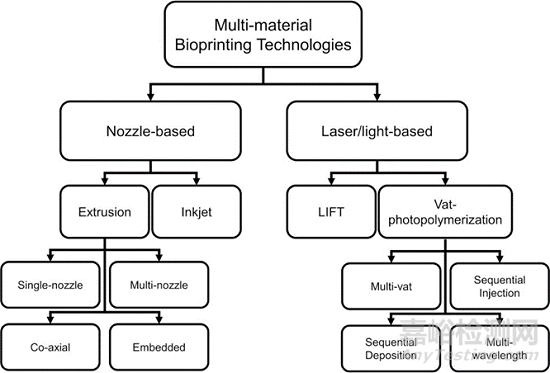
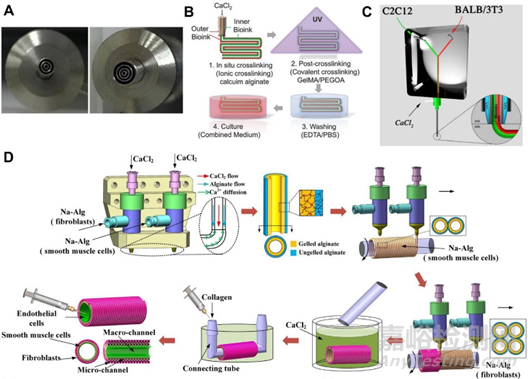
多組分生物墨水是指由兩種或兩種以上不同的生物材料混合而成的單相均質(zhì)生物墨水���。使用多種材料打印��,必須考慮材料界面處的相互作用���。較高的界面粘附力可以提高生物打印結(jié)構(gòu)的韌性和抗疲勞性。但是��,在多材料(生物)打印過程中���,將水凝膠與不同性質(zhì)的材料(尤其是彈性體和熱塑性塑料)結(jié)合起來具有挑戰(zhàn)性15���。用于多材料打印的3D打印技術(shù)如下圖所示:
以下簡(jiǎn)單列舉幾項(xiàng)多材料打印技術(shù):
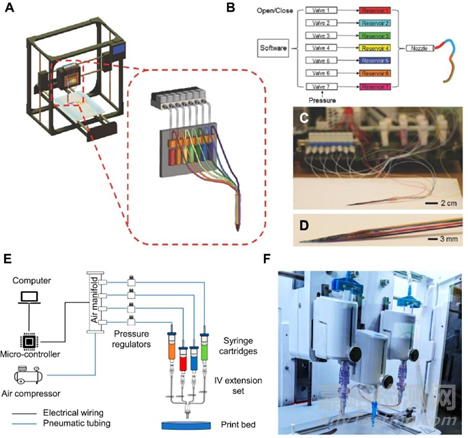
1)單噴嘴生物打印技術(shù)
通過一個(gè)噴嘴擠出不同的生物墨水仍然是多材料生物打印的形式。如下圖所示:多儲(chǔ)液器系統(tǒng)和混合器是兩種最常見的相關(guān)方式��?����;旌掀鞯淖饔檬腔旌蟽煞N或多種不同濃度的生物墨水���,以促進(jìn)多材料打印��,從而促進(jìn)制造具有連續(xù)梯度特性的結(jié)構(gòu)�����。
2)多噴嘴生物打印技術(shù)16
單噴嘴技術(shù)的一個(gè)缺點(diǎn)是(生物)墨水在一個(gè)噴嘴中流動(dòng)時(shí)存在交叉污染的風(fēng)險(xiǎn)���。多噴嘴多材料生物打印機(jī)與單噴嘴生物打印機(jī)相比��,可以以更快的速度和更大的構(gòu)建體積制造更復(fù)雜的特征�����。
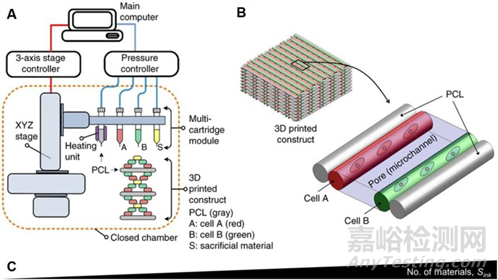
3)同軸生物打印技術(shù)
同軸噴嘴是一種用于生物打印多材料核殼結(jié)構(gòu)的機(jī)制,如血管結(jié)構(gòu)�����、異質(zhì)微纖維和腫瘤模型���。能夠制造具有成分和幾何復(fù)雜性的中空結(jié)構(gòu)���。同軸噴嘴特別適用于與交聯(lián)劑混合后快速交聯(lián)的生物墨水。例如:下圖B中���,CaCl 2用于內(nèi)部噴嘴以離子交聯(lián)生物墨水�����。雙層管狀結(jié)構(gòu)隨后通過紫外線再次交聯(lián)以形成穩(wěn)定的結(jié)構(gòu)���。使用這種設(shè)計(jì)���,可以一步連續(xù)改變形狀、尺寸和層數(shù)���,而無需更換噴嘴�����。這些圓周多層構(gòu)造可用作人體套管組織模型17���。
3、3D打印干細(xì)胞
干細(xì)胞是一類具有自我更新能力�����,并能分化成其他類型細(xì)胞的特殊細(xì)胞��,而人體正常組織的更新和修復(fù)與組織特異性干細(xì)胞密切相關(guān)��,如骨髓干細(xì)胞��、胚胎干細(xì)胞( embryonic stem cells,ESC )���、造血干細(xì)胞���、內(nèi)皮祖細(xì)胞等。隨著技術(shù)進(jìn)步���, 2007 年已實(shí)現(xiàn)人工將人的成年體細(xì)胞經(jīng)過基因重組技術(shù)培養(yǎng)成誘導(dǎo)型多能干細(xì)胞( induced pluripotent stem cells ��, iPSC )18
干細(xì)胞治療特點(diǎn)19:
① 治療適用性強(qiáng):干細(xì)胞可以從單個(gè)細(xì)胞分化成內(nèi)胚層、中胚層和外胚層所有的細(xì)胞��,最終形成機(jī)體的所有組織和器官�����,其成品可以在生物內(nèi)環(huán)境中移植��、存活并保持長(zhǎng)期穩(wěn)定���。因而其治療范圍理論上可涵蓋人體任何組織器官及相關(guān)疾?�。ㄈ缟窠?jīng)系統(tǒng)損傷���、免疫功能障礙�����、器官衰竭���、美容、斷肢等)���,在自體組織器官移植方面有不可替代的作用��;
② 獲取容易:細(xì)胞技術(shù)發(fā)展初期��,細(xì)胞來源往往局限于生物組織甚至體內(nèi)采集�����,不可避免產(chǎn)生創(chuàng)傷及相應(yīng)副作用��,隨著技術(shù)發(fā)展�����,干細(xì)胞已經(jīng)可以通過人工誘導(dǎo)獲取���,是目前免疫治療和基因治療的最佳載體���。
③ 副作用少且效果持久:干細(xì)胞治療是能夠以患者自身的細(xì)胞為基礎(chǔ),制作相應(yīng)的干細(xì)胞并形成適用于疾病的治療手段���,在應(yīng)用時(shí)減少了組織相容性的問題,減低乃至消除了治療�����、移植過程中的排斥反應(yīng)及使用免疫抑制劑所產(chǎn)生的副作用���,且植入細(xì)胞并非快速消耗品,其定植于體內(nèi)后可產(chǎn)生持久的治療效果�����。
目前細(xì)胞打印在生物醫(yī)學(xué)領(lǐng)域可應(yīng)用的打印方案:
① 先打印出具有生物相容性的支架材料�����,再將有活性的細(xì)胞、干細(xì)胞組織種植到材料上形成細(xì)胞 - 材料復(fù)合體��, 然后將細(xì)胞 - 材料復(fù)合體植入組織缺損部位���,支架材料在逐步降解的同時(shí)���,種植的細(xì)胞不斷增殖、生長(zhǎng)���,形成細(xì)胞間連接��,從而達(dá)到修復(fù)組織缺損的目的20���;
② 將細(xì)胞與支架材料直接混合打印,一個(gè)或多個(gè)打印噴頭打印細(xì)胞懸浮液�����,另一個(gè)或多個(gè)噴頭打印細(xì)胞生長(zhǎng)所需的支架(微環(huán)境)�����,其支架材料的主要成分是含水的生物凝膠��,逐層打印, 疊加形成 3D 的多細(xì)胞 - 凝膠支架體系��,最終用于治療或移植�����?����;罴?xì)胞的打印可實(shí)現(xiàn)組織器官結(jié)構(gòu)及部分生物功能的重建��,而由于打印過程是由計(jì)算機(jī)控制細(xì)胞排列���,兩種方案在技術(shù)上均可在生物體內(nèi)進(jìn)行原位打印���,如原位軟骨細(xì)胞打印進(jìn)行骨修復(fù);
③ 新興方案��,將細(xì)胞預(yù)制成細(xì)胞團(tuán)��,打印時(shí)使用臨時(shí)的固定裝置�����,如微型探針等以預(yù)期打印結(jié)構(gòu)為目標(biāo)進(jìn)行結(jié)構(gòu)固定��,讓細(xì)胞團(tuán)生長(zhǎng)融合達(dá)到穩(wěn)定狀態(tài)再去除臨時(shí)固定裝置��,最終形成細(xì)胞自行連接的緊密結(jié)構(gòu)��,從而實(shí)現(xiàn)無支架的細(xì)胞打印21。
參考文獻(xiàn):
[1] Gudapati, H.; Dey, M.; Ozbolat, I. A comprehensive review on droplet-based bioprinting: Past, present and future. Biomaterials.2016, 102, 20–42.
[2] Ricci, J.L.; Clark, E.A.; Murriky, A.; Smay, J.E. Three-dimensional printing of bone repair and replacement materials: Impact on craniofacial surgery. J. Craniofacial Surg. 2012, 23, 304–308.
[3] Billiet, T.; Gevaert, E.; De Schryver, T.; Cornelissen, M.; Dubruel, P. The 3D printing of gelatin methacrylamide cell-laden tissue-engineered constructs with high cell viability. Biomaterials 2014, 35, 49–62.
[4] Turner, B.N.; Strong, R.; Gold, S.A. A review of melt extrusion additive manufacturing processes: Process design and modeling.Rapid Prototyp. J. 2014, 20, 192–204.
[5] Mahdavi, S.S.; Abdekhodaie, M.J.; Kumar, H.; Mashayekhan, S.; Baradaran-Rafii, A.; Kim, K. Stereolithography 3D bioprinting method for fabrication of human corneal stroma equivalent. Ann. Biomed. Eng. 2020, 48, 1955–1970.
[6] Song D, Xu Y, Liu S, Wen L, Wang X. Progress of 3D Bioprinting in Organ Manufacturing. Polymers (Basel). 2021 Sep 18;13(18):3178.
[7] Serpelloni, M.; Cantù, E.; Borghetti, M.; Sardini, E. Printed smart devices on cellulose-based materials by means of aerosol-jet printing and photonic curing. Sensors 2020,20, 841.
[8] Basara, G.; Saeidi-Javash, M.; Ren, X.; Bahcecioglu, G.; Wyatt, B.C.; Anasori, B.; Zhang, Y.; Zorlutuna, P. Electrically conductive 3D printed Ti3C2Tx MXene-PEG composite constructs for cardiac tissue engineering. Acta Biomater. 2020, 19.
[9] Groll, J.; Burdick, J.A.; Cho, D.W.; Derby, B.; Gelinsky, M.; Heilshorn, S.C.; Jüngst, T.; Malda, J.; Mironov, V.A.; Nakayama, K.; et al.A definition of bioinks and their distinction from biomaterial inks. Biofabrication 2018, 11, 013001.
[10] 毛宏理,顧忠偉.生物3D打印高分子材料發(fā)展現(xiàn)狀與趨勢(shì)[J].中國(guó)材料進(jìn)展,2018,37(12):949-969+993.
[11] 朱敏,黃婷,杜曉宇,朱鈺方.生物材料的3D打印研究進(jìn)展[J].上海理工大學(xué)學(xué)報(bào),2017,39(05):473-483+489.
[12] Fatimi A, Okoro OV, Podstawczyk D, Siminska-Stanny J, Shavandi A. Natural Hydrogel-Based Bio-Inks for 3D Bioprinting in Tissue Engineering: A Review. Gels. 2022 Mar 14;8(3):179.
[13] Assad H, Assad A, Kumar A. Recent Developments in 3D Bio-Printing and Its Biomedical Applications. Pharmaceutics. 2023 Jan 11;15(1):255.
[14] Fatimi A, Okoro OV, Podstawczyk D, Siminska-Stanny J, Shavandi A. Natural Hydrogel-Based Bio-Inks for 3D Bioprinting in Tissue Engineering: A Review. Gels. 2022 Mar 14;8(3):179.
[15] Ravanbakhsh H, Karamzadeh V, Bao G, Mongeau L, Juncker D, Zhang YS. Emerging Technologies in Multi-Material Bioprinting. Adv Mater. 2021 Dec;33(49):e2104730.
[16] Kolesky DB, Truby RL, Gladman AS, Busbee TA, Homan KA, Lewis JA, Adv. 2014, 26 , 3124.
[17] Pi Q, Maharjan S, Yan X, Liu X, Singh B, van Genderen AM, Robledo-Padilla F, Parra-Saldivar R, Hu N, Jia W, Xu C, Kang J, Hassan S, Cheng H, Hou X, Khademhosseini A, Zhang YS, Adv. Mater 2018, 30, 1706913.
[18] Takahashi K, Tanabe K, Ohnuki M, et al. Induction of pluripo-tent stem cells from adult human fibroblasts by defined factors [J]. Cell, 2007, 131(5): 861-872.
[19] 莊東林,趙明一,劉南波,何標(biāo)川,黃煥雷,朱平.3D打印技術(shù)在干細(xì)胞再生領(lǐng)域的發(fā)展及應(yīng)用[J].生物醫(yī)學(xué)工程與臨床,2020,24(04):489-495.
[20] Park KM, Shin YM, Kim K, et al. Tissue engineering and regenerative medicine 2017: A year in review [J]. Tissue Eng Part B Rev, 2018, 24(5): 327-344.
[21] Moldovan NI, Hibino N, Nakayama K. Principles of the ken-zan method for robotic cell spheroid -based three -dimensional bioprinting[J]. Tissue Eng Part B Rev, 2017, 23(3): 237-244.