羥丙基甲基纖維素(hydroxypropyl methyl cellulose,HPMC)是一種白色或者近白色纖維狀的粉末或顆粒,具有優(yōu)異的冷水溶性����,且由于其是一種非離子形纖維素醚,在水溶液中不帶電荷���,因此具有較強(qiáng)的穩(wěn)定性�,和其他輔料或API相容性較好���。毒理研究數(shù)據(jù)表明其在體內(nèi)不會被代謝���,體內(nèi)無毒副作用�,是一種更為安全的藥用輔料�。由于其分子量和黏度的不同���,使其具備黏合、增稠�、助懸、乳化���、成膜等特性,因而在制劑中用途廣泛����,在藥物制劑中常被用作粘合劑、分散劑���、增稠劑以及薄膜包衣材料、緩釋骨架材料等���,接下來就這些用途做一些簡單介紹���。
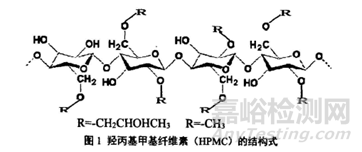

1)在片劑中作為粘合劑和崩解劑
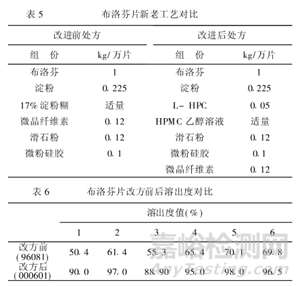
目前市售的HPMC多為陶氏化學(xué)公司的,HPMC根據(jù)甲氧基和羥丙甲基的不同����,可分為E/K/F型號系列,每個(gè)系列下根據(jù)粘度的不同又可劃分為不同的型號�,其中E3/5/6/15/50系列可作為片劑處方中的粘合劑使用�,而E系列,包括E4M/E10M一般用于成膜材料用于包衣;K系列如K100LV/K15M/K100M一般多用作緩釋骨架材料����。用作粘合劑的HPMC是低粘度規(guī)格E3-E50系列的,常用濃度為2-5%的HPMC溶液作粘合劑���,低粘度的HPMC在水溶液中溶解形成澄明且具有粘性的膠體溶液�。HPMC作為粘合劑溶液,可以有效降低藥物的接觸角����,利于藥物的潤濕����,且本身吸水后膨脹系數(shù)可達(dá)數(shù)百倍���,可顯著提高藥物的崩解和溶出釋放速率。例如有文獻(xiàn)研究將布洛芬處方中的原粘合劑淀粉糊替代為HPMC�,可以有效的提高難溶性藥物的溶出,改善片劑的質(zhì)量����。
HPMC可作為粘合劑使用的另外一個(gè)優(yōu)勢作用在于:首先:我們都知道粘合劑的吸濕性和含水量會影響片劑在存放過程中穩(wěn)定性���,吸濕可能會引起制劑結(jié)塊�、潮解����、晶型轉(zhuǎn)變等�,進(jìn)而可能影響制劑的含量和溶出等問題���,且吸濕后的片劑更容易霉變���、氧化、水解等�,因此盡量選用一些吸濕性較低的輔料類型����,有研究表明在生產(chǎn)環(huán)境50%RH及以下條件中,PVP和CMC-Na的平衡含水量大約是重量比的18%和15%���,而纖維素系列如HPMC���、HPC����、EC等一般為5%或者更少���,因此它可作為一個(gè)優(yōu)勢作用;其次�,常用的另外一種粘合劑PVP中含有含量較高的過氧化物,過氧化物會與易被氧化的藥物直接反應(yīng)生成自由基�,從而影響藥物的穩(wěn)定性����,因此,對于該類型藥物而言����,那優(yōu)先選用過氧化物含量較低的纖維素類HPMC�。
2)HPMC可作為薄膜包衣材料
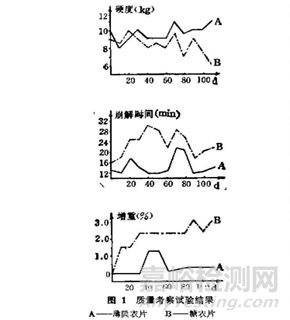
HPMC因其成膜性好����,形成的膜強(qiáng)度適宜����、衣層通透、不易脆裂�,衣膜在光����、熱及一定濕度下較穩(wěn)定,且可溶于有機(jī)溶劑和水�,對片劑的崩解和溶出的不良影響較小���,因此是一種應(yīng)用較廣且薄膜包衣效果較好的一種胃溶性包衣材料。在包衣材料中,HPMC常和色素����、遮光劑以及增塑劑等配成一定比例的復(fù)合物����,使用前將其加溶劑溶解或均勻混懸后用于包衣����。例如早有文獻(xiàn)研究HPMC在慶大霉素包衣片中的應(yīng)用�,因慶大霉素有較強(qiáng)的引濕性����,片劑質(zhì)量不穩(wěn)定,易發(fā)生裂片和變色�,片劑的貯存期限較短,僅一年左右�,而將HPMC用于慶大霉素薄膜包衣后����,可一定程度克服片芯內(nèi)部的變色和裂片行為���,且六個(gè)月的加速實(shí)驗(yàn)結(jié)果證明:HPMC薄膜包衣的各項(xiàng)性能均優(yōu)于其糖衣片����。
3)HPMC在作為膠囊殼材質(zhì)方面的應(yīng)用
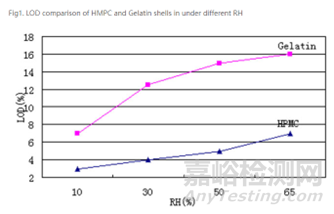
目前,HPMC也常用于制備膠囊殼����,其和明膠膠囊殼材質(zhì)相比���,具有明顯的優(yōu)勢作用,首先可以克服明膠的交聯(lián)作用���,其次是因含水量比明膠材質(zhì)低很多�,HPMC所含水分僅4%~5%����,不像明膠殼材質(zhì)那樣(明膠材質(zhì)含水量一般為12.5~17.5%)����,如果是吸濕性很強(qiáng)的內(nèi)容物會使明膠殼失水從而失去其原有的韌性�,所以使用HPMC膠囊殼更適用于吸濕性較強(qiáng)或者對水分更為敏感的內(nèi)容物,可以有效延長該類產(chǎn)品的保質(zhì)期�。
4)HPMC可作為助懸劑和穩(wěn)定劑
HPMC可以增加液體分散介質(zhì)的粘性,降低固液界面張力����,從而使混懸液保持穩(wěn)定狀態(tài)����,而且可以在不溶性微粒的表面間形成保護(hù)膜����,可以有效阻礙微粒之間的聚集�,延緩微粒的沉降速度,因此常被用于眼科制劑中的助懸劑所使用�,有文獻(xiàn)研究篩選了阿昔洛韋眼用混懸液的助懸劑類型,篩選諸多種類的助懸劑���,結(jié)果發(fā)現(xiàn)處方6(HA/HPMC組合作為助懸劑)的沉降體積比最大�,且粒徑范圍更小,顆粒更加均勻����、細(xì)膩�,因此在該處方中優(yōu)選0.05%HA和0.05%HPMC 4000聯(lián)合作為助懸劑所使用����。
5) HPMC作為親水性骨架材料在緩釋片中的應(yīng)用
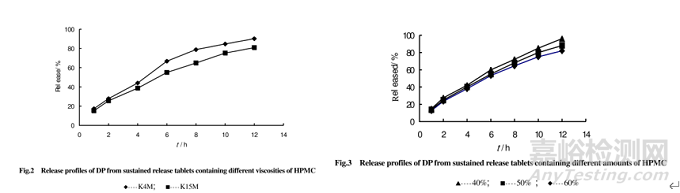
近年來���,隨著給藥系統(tǒng)的研究的不斷深入探索���,人們逐漸發(fā)現(xiàn)高黏度的HPMC常作為一種親水性凝膠骨架材料應(yīng)用于緩釋劑型中���,最常用的就是HPMC K系列,一般來講�,HPMC黏度越大,其遇水后形成的凝膠層黏度也隨之增大����,那水難溶性藥物從骨架中釋放的速度則越慢����。且通常會控制HPMC和藥物的比例,從而控制對藥物的釋放速度����,一般來講����,藥物的釋放速度會隨著HPMC比例的增加而有所下降���,因?yàn)殡S著HPMC用量的增加,凝膠層的厚度也有所增加���,從而導(dǎo)致釋藥速率變慢���。當(dāng)然,也不能一味的增加HPMC的用量來控制藥物釋放速度從而忽略了片重問題�,片重太大的話患者用藥的依從性和可接受程度會較差,例如如果是對于水溶性較強(qiáng)的藥物而言����,僅僅靠調(diào)節(jié)藥物和HPMC的比例問題是很難達(dá)到令人滿意的釋放效果,這種時(shí)候�,可能就需要額外加入一些其他輔料來延緩藥物的釋放速率。例如有文獻(xiàn)研究了雙氯芬酸鉀親水凝膠骨架型緩釋片中不同黏度及用量的HPMC對藥物釋放速率的影響����,結(jié)果表明藥物的釋放速度隨著HPMC黏度和用量的增加而減慢����,最終根據(jù)處方要求選擇了骨架材料HPMC-K4M的用量為40%。
當(dāng)然�,有文獻(xiàn)研究表明在緩釋制劑中�,HPMC并非選擇的黏度越大越好,因?yàn)轲ざ仍酱蟮腍PMC水化速度不快���,會很容易造成前期時(shí)間點(diǎn)突釋�,而后期的藥物釋放量又不足�,(一般來講�,HPMC的水化速度會隨著黏度的增加而有所下降,水化速度快者���,水分滲入后局部膨脹速度較快����,從而快速發(fā)揮控釋作用)����,因此,可以嘗試考慮不同黏度的HPMC搭配使用����,即低黏度的HPMC水化速度快,利于控制前期時(shí)間點(diǎn)的釋放速率�,而高黏度的HPMC水化作用慢,基于控制后期時(shí)間點(diǎn)的釋放速率����。
綜上�,HPMC憑借其良好的理化性質(zhì),在醫(yī)藥行業(yè)得到了廣泛的應(yīng)用�,以上僅列舉其中的幾種應(yīng)用���,它還可以應(yīng)用于固體分散體的載體或者膠體制劑的增稠劑等等�,本文就不做詳細(xì)列舉了,相信隨著HPMC的進(jìn)一步深入研究,會逐漸拓寬它的使用領(lǐng)域�,推動其在多領(lǐng)域的多方位發(fā)展。
參考文獻(xiàn)
[1]單玉華����,羥丙基甲基纖維素(HPMC)在片劑生產(chǎn)中的應(yīng)用[J].齊魯藥事,2004,23(2):56-57
[2]制粒工藝中粘合劑的選擇與應(yīng)用
[3] 周大熙等�,薄膜材料HPMC在慶大霉素片包衣中的應(yīng)用[J].中國醫(yī)藥工業(yè)雜志,1994,25(4):168-169
[4] 上海祺宇生物科技有限公司—膠囊知識專題:羥丙甲基纖維素空心膠囊的特性及應(yīng)用
[5]劉杰等�,阿昔洛韋眼用混懸液的助懸劑篩選[J].食品與藥品,2008,10(11):21-23
[6] 于大海等,雙氯芬酸鉀親水凝膠骨架型緩釋片劑的制備[J].中國藥劑學(xué)雜志,2003,1(4):142-149
[7] 趙麗華���,緩釋骨架材料在制劑中的應(yīng)用[J].醫(yī)藥導(dǎo)報(bào),2008,27(7):827-829