近期���,F(xiàn)DA給iRhythm (Nasdaq: IRTC)的Zio AT移動(dòng)心臟遙測(cè)設(shè)備發(fā)出了警告信���。FDA對(duì)該公司位于美國加州賽普拉斯的工廠進(jìn)行檢查,隨后發(fā)出這封警告信����,警告信稱iRhythm不符合與Zio AT有關(guān)的醫(yī)療器械報(bào)告要求和醫(yī)療器械質(zhì)量體系要求。
iRhythm公司產(chǎn)品收到FDA警告信
近期���,F(xiàn)DA給iRhythm (Nasdaq: IRTC)的Zio AT移動(dòng)心臟遙測(cè)設(shè)備發(fā)出了警告信���。
在2023年5月30日提交給美國證券交易委員會(huì)的8-K表格中����,iRhythm稱公司在5月25日收到了警告信�。FDA對(duì)該公司位于美國加州賽普拉斯的工廠進(jìn)行檢查,檢查于8月2022日結(jié)束���,隨后發(fā)出這封警告信。
根據(jù)iRhythm公司向美國證券交易委員會(huì)提交的文件����,警告信稱iRhythm不符合與Zio AT有關(guān)的醫(yī)療器械報(bào)告要求和醫(yī)療器械質(zhì)量體系要求。
iRhythm說:“公司認(rèn)真對(duì)待相關(guān)問題���,計(jì)劃在規(guī)定的時(shí)間內(nèi)作出回應(yīng)����,并努力工作����,以解決FDA警告信的問題�。”
了解FDA對(duì)iRhythm的警告信
根據(jù)美國證券交易委員會(huì)的文件���,作為對(duì)2022年8月12日收到的FDA 483表("483意見")回應(yīng)的一部分,iRhythm已經(jīng)采取了糾正措施���,旨在解決FDA確定的部分項(xiàng)目���。如今,iRhythm收到了警告信���,公司計(jì)劃采取進(jìn)一步的糾正措施�,以解決FDA的483條意見和警告信中確定的Zio AT系統(tǒng)相關(guān)的其他項(xiàng)目����。
iRhythm公司還表示:“警告信并不直接限制公司任何產(chǎn)品在美國的制造、生產(chǎn)或運(yùn)輸����,也不要求從美國市場撤出任何產(chǎn)品�。目前,公司認(rèn)為�,如果FDA沒有發(fā)起進(jìn)一步不利行動(dòng)����,收到這封警告信不會(huì)對(duì)公司的財(cái)務(wù)業(yè)績產(chǎn)生重大影響。”
與此同時(shí)�,iRhythm表示�,公司可以保證FDA對(duì)其應(yīng)對(duì)措施感到滿意。
警告信報(bào)告是在iRhythm第一季度財(cái)報(bào)發(fā)布后的幾周內(nèi)發(fā)布的���,其中披露了兩年多來聯(lián)邦調(diào)查員發(fā)出的第三張傳票����。
了解公司明星產(chǎn)品
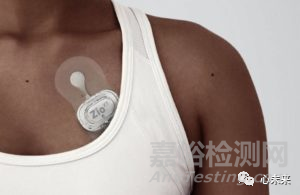
iRhythm Technologies創(chuàng)建了ZIO®Service����,通過將其可穿戴生物傳感技術(shù)與基于云的數(shù)據(jù)分析和機(jī)器學(xué)習(xí)功能相結(jié)合,重新定義心律失常的臨床診斷方法?���;颊吲宕髻N片產(chǎn)品����,可以穿戴長達(dá)14天。后臺(tái)采用專有算法���,從數(shù)百萬的心跳數(shù)據(jù)中提取臨床可用信息�。目前主要產(chǎn)品是Zio XT���,Zio AT和Zio Watch����,適用于不同的患者和場景����。
與傳統(tǒng)的動(dòng)態(tài)心電圖Holter相比,Zio更輕便�,對(duì)正常生活的干擾度低���。Zio不提供無線實(shí)時(shí)數(shù)據(jù)傳輸,而是將用戶動(dòng)態(tài)心電圖的數(shù)據(jù)存儲(chǔ)起來���,數(shù)據(jù)收集完畢后,由用戶通過電腦或其他方式傳回來�,然后由iRhythm的專業(yè)團(tuán)隊(duì)給出心電報(bào)告并傳輸給醫(yī)生���。
關(guān)于iRhythm公司
iRhythm Technologies是一家數(shù)字醫(yī)療保健公司,成立于2006年9月14日�。公司通過將其可穿戴生物傳感技術(shù)與基于云的數(shù)據(jù)分析和機(jī)器學(xué)習(xí)功能相結(jié)合,重新定義心律失常的臨床診斷方法����。