1��、 前言
為了將藥物推向市場����,科學(xué)家們試圖依賴不同類型的臨床前模型來模擬人體生理結(jié)構(gòu)和功能,體外評估藥物的毒性和安全性����。遺憾的是,傳統(tǒng)的臨床前模型(包括二維細胞模型��, 三維球狀細胞和各種實驗動物模型)由于各自的局限性�����,很難真實模擬人類生理結(jié)構(gòu)和功能����,導(dǎo)致在預(yù)測藥物反應(yīng)上受到極大挑戰(zhàn)����。這也是為什么約90%通過臨床前模型評估的藥物在進入人體試驗后失敗的主要原因��。
值得慶幸的是�����,科學(xué)家們開發(fā)了更具模擬人類生理環(huán)境的新一代技術(shù):器官芯片����。有了器官芯片技術(shù)����,研究人員可以在更接近人體生理功能的實驗?zāi)P椭袦y試藥物,可在更短的時間內(nèi)獲得更準確的藥物反應(yīng)數(shù)據(jù)��,輔助篩選出更有競爭力的候選藥物進入臨床試驗����。
2010年,哈佛大學(xué)Wyss研究所Donald E. Ingber院士開發(fā)了世界上第一個成功的器官芯片:肺芯片����,該研究成果發(fā)表于頂級期刊 Science 雜志【1】��。隨后�����,Donald E. Ingber院士作為學(xué)術(shù)創(chuàng)始人��,Emulate公司成立��,將該技術(shù)進行商業(yè)化推廣��。自成立以來�����,Emulate一直在引領(lǐng)行業(yè)發(fā)展�����,將器官芯片技術(shù)引入世界各地的實驗室��。超過100篇同行評議的學(xué)術(shù)論文發(fā)表也證明了此項技術(shù)在提高對人類健康和疾病的理解方面的重要價值����。
本篇將為您系統(tǒng)性介紹器官芯片技術(shù)的基本原理和應(yīng)用價值,尤其是如何利用器官芯片技術(shù)改善疾病研究和藥物開發(fā)全流程以提高效率�����,并推動更多拯救生命的治療方法的開發(fā)��。閱讀后��,您將更好地了解藥物開發(fā)中最普遍的挑戰(zhàn)����,以及什么是器官芯片����,它們能做什么,以及它們可能如何能幫助您解決目前研究中遇到的障礙�����。
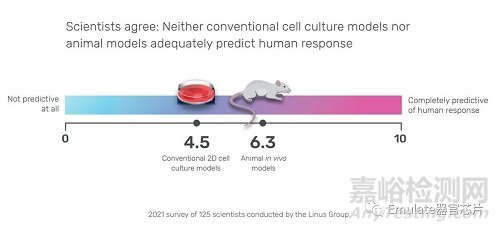
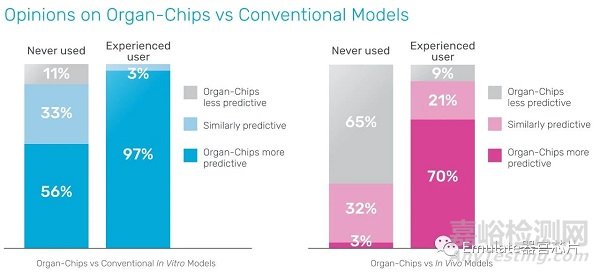
Survey of 125 scientists conducted by the Linus Group on behalf of Emulate (2021)
2�����、傳統(tǒng)實驗?zāi)P偷木窒扌?/span>
為了開發(fā)藥物�����,科學(xué)家們通常依靠小鼠、狗和非人靈長類動物 (non-human primates, NHP) 以及二維細胞系或者三維球狀細胞等實驗?zāi)P蛠眍A(yù)測人類反應(yīng)����。然而,這些傳統(tǒng)的實驗?zāi)P投加懈髯缘奶攸c和局限性�����,一定程度上阻礙藥物開發(fā):
2.1 傳統(tǒng)實驗動物模型的挑戰(zhàn)
1. 冗長的建模和實驗周期:動物實驗需要很長的構(gòu)建周期��,通常需要3-6個月之久��,并且需要大量的倫理審查和監(jiān)管監(jiān)督��。此外每種動物模型都需要專業(yè)化的場地和技術(shù)人員進行飼養(yǎng)和維護����,會進一步增加實驗成本和時間。
2. 缺乏可重復(fù)性:無論科學(xué)家們采取何種措施使動物模型實驗標準化�����,但每只實驗動物都是獨一無二的�����,極易受到科學(xué)家無法預(yù)料的因素影響,從而影響研究結(jié)果�����。事實上�����,Amgen公司的一項研究表明��,在其研發(fā)管線中����,只有約10%的動物實驗可以被內(nèi)部研究小組復(fù)制【2】�����。此外����,不同科學(xué)家處理實驗動物的方式差異等因素也會影響動物在實驗中的反應(yīng)方式。這使得可重復(fù)性這一關(guān)鍵指標在實驗動物模型中難以有效維持��。
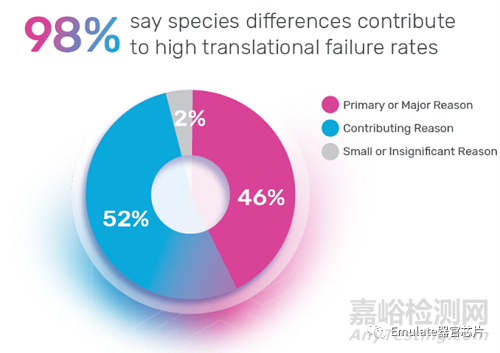
3. 物種轉(zhuǎn)換問題:盡管科學(xué)家們已經(jīng)努力使動物模型人性化,但物種的固有差異將永遠是預(yù)測人類反應(yīng)的一個限制性因素����。事實上,98%的科學(xué)家都認為物種差異導(dǎo)致了高轉(zhuǎn)化失敗率【3】��?�?紤]到目前各大藥企的藥物開發(fā)管線更多轉(zhuǎn)向生物制品����、免疫細胞療法和其他人類特定的治療方法,物種差異帶來的挑戰(zhàn)會越來越大����。
4. 采購實驗動物的困難:由于非人靈長類動物在生理、認知能力�����、神經(jīng)解剖學(xué)�����、社會復(fù)雜性、繁殖和發(fā)育等方面與人類具有高度相似性����。與人類的遺傳物質(zhì)有75%~98.5%的同源性,這種同源性在基礎(chǔ)和轉(zhuǎn)化生物醫(yī)學(xué)研究中發(fā)揮著重要的作用,它們的需求量一直很大�����。然而��,非人靈長類動物進口持續(xù)短缺��,導(dǎo)致不僅價格飆升��,而且購買十分緊俏��,多次面臨諸如“一猴難求”的局面��。造成這種情況的原因有很多����,從監(jiān)管��,到對繁育飼養(yǎng)行為的打擊�����,再到新冠肺炎疫情期間的殘余影響,但目前來看�����,實驗動物的短缺似乎不會很快消失��。
2.2 傳統(tǒng)體外細胞模型的局限性
1. 永生化細胞系的生理相關(guān)性有限:科學(xué)家們經(jīng)常依賴永生細胞系��,因為它們?nèi)菀撰@得�����,并且能夠在實驗室條件下存活并持續(xù)增殖����,采購和維持的難度較低。然而�����,由于遺傳操作而獲得永生化特征的這些細胞系�����,其生理結(jié)構(gòu)和細胞行為已經(jīng)與原代人類細胞差異較大,從而導(dǎo)致對疾病和藥物效果的理解可能會帶來巨大差異��。
2. 缺乏特定器官微環(huán)境:在人類體內(nèi)��,細胞的功能在很大程度上受到其特異性的器官環(huán)境影響��,包括細胞外基質(zhì)(ECM)�����、機械力和液體流動等因素�����。然而��,傳統(tǒng)的2D細胞系往往為單層細胞培養(yǎng)����,缺乏各種細胞外基質(zhì),3D球狀細胞雖然已經(jīng)引入了細胞外基質(zhì)����,并且細胞類型也已經(jīng)有進一步提升。但是它們?nèi)匀欢寂囵B(yǎng)在靜止的體系中����,意味著缺乏液體流動和物理機械力。而我們?nèi)梭w處于動態(tài)的環(huán)境��,尤其是如我們的肺部需要有節(jié)律的呼吸運動�����,我們的腸道也一直在經(jīng)受液體的流動和蠕動�����,因此�����,缺乏這些器官特異性的動態(tài)微環(huán)境��,很難真實模擬人體生理結(jié)構(gòu)和功能����。
3. 缺乏體內(nèi)的復(fù)雜性:在人體中,細胞相互之間存在持續(xù)不斷的交互�����,是器官行使正常功能所不可或缺的。然而����,傳統(tǒng)2D細胞系往往只包括單一的細胞類型,導(dǎo)致它們對藥物的反應(yīng)方式不能反映體內(nèi)的功能����。傳統(tǒng)的3D球狀細胞在一定程度上提升了細胞之間的類型和交互復(fù)雜性,但是仍然存在一些短板�����,比如球體中央的細胞大部分經(jīng)受缺氧環(huán)境��,甚至中間的細胞已經(jīng)死亡��,細胞交互實際會產(chǎn)生問題�����。此外人體器官大多數(shù)伴隨著各種共生微生物菌群��,以及各種血管內(nèi)的免疫細胞�����,而傳統(tǒng)模型難以有效引入這些復(fù)雜度。
4. 缺乏血管系統(tǒng):人體每一個器官幾乎都需要血管系統(tǒng)來維持營養(yǎng)和正常的代謝�����,因此��,非常有必要在體外模型中引入血管系統(tǒng)�����。但傳統(tǒng)2D或者3D類器官球難以構(gòu)建具備生理功能的血管系統(tǒng)����,使得組織與血液系統(tǒng)的的交互�����,代謝物的有效排出都受到挑戰(zhàn)��。
5 藥物灌注困難:傳統(tǒng)靜態(tài)培養(yǎng)的3D類器官球體中央致密�����,細胞高度缺氧��,導(dǎo)致藥物難以滲透到球體中央的細胞,帶來模型對藥物的反應(yīng)難以真實呈現(xiàn)��。加之本身缺乏血管系統(tǒng)��,進一步阻礙了藥物通過血管系統(tǒng)遞送的可能性��。
6 培養(yǎng)的標準化和可重復(fù)性:傳統(tǒng)靜態(tài)培養(yǎng)的3D類器官球模型在制備時��,類器官球在培養(yǎng)環(huán)境中處于無序控制狀態(tài)��,導(dǎo)致培養(yǎng)出的類器官球體大小不一����,均勻度差,同一個孔中的不同類器官球的形態(tài)都千差萬別�����。加上缺乏有效的和標準的培養(yǎng)方案��,同時由于不同實驗室之間實驗人員的差異�����,培養(yǎng)所用材料和方案的差異�����,導(dǎo)致傳統(tǒng)3D靜態(tài)類器官球模型的重復(fù)性較差。
Survey of 125 scientists conducted by the Linus Group on behalf of Emulate (2021)
值得慶幸的是�����,上述提到的這些挑戰(zhàn)可以通過最新的器官技術(shù)來克服��!
3����、器官芯片技術(shù)基本概念����、工作原理和價值
3.1 器官芯片技術(shù)概念和工作原理
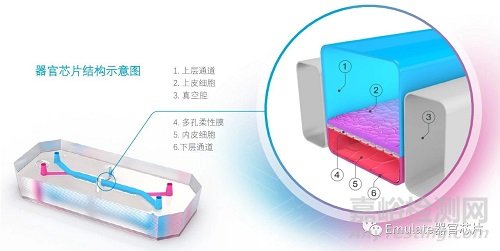
器官芯片技術(shù)使研究人員能夠利用活細胞和器官特異性動態(tài)微環(huán)境在體外創(chuàng)建一個器官的功能單元,為了解人類生物學(xué)的內(nèi)部機理提供了一個模型基礎(chǔ)�����。器官芯片是一種微流控的小型化靈活裝置��,其通常包含兩個上下平行的通道��。不同類型的人類相關(guān)細胞均可接種到這些通道中��,包括原始細胞、iPSCs����、類器官球和免疫細胞。上下通道被一層薄薄的多孔膜隔開��,使其形成了一個組織與血管的界面��,更好地用于細胞與細胞之間的交互��。膜上包被有組織特定的細胞外基質(zhì)��,有助于進一步促使對應(yīng)組織的成熟�����,形成高度與人類生理結(jié)構(gòu)相似的組織界面����。
器官芯片的一個重要指標和關(guān)鍵特征為,研究人員可以很容易地控制和微調(diào)細胞所經(jīng)歷的機械力��,為組織在體外施加器官特異性的動態(tài)微環(huán)境�����。當器官芯片被置于液體流動和循環(huán)機械應(yīng)力作用下時,細胞會經(jīng)歷類似于它們在體內(nèi)的機械環(huán)境����,如腸道的蠕動、肺部的呼吸和血管中的血液流動����。器官芯片還能給予更復(fù)雜的結(jié)構(gòu)特征,包括多細胞的復(fù)雜性��、細胞與細胞之間的相互作用����、組織特定的ECM和機械力�����,造就了器官芯片的獨特優(yōu)勢�����。相比于傳統(tǒng)細胞培養(yǎng)方法����,器官芯片無論在結(jié)構(gòu)����、形態(tài)����、基因表達譜還是在體外對應(yīng)器官所呈現(xiàn)出的功能,都與人類更為接近�����。
器官芯片的示意圖�����。器官芯片由兩個平行的微流體通道組成��,分為上層通道(1)和下層通道(2)��。上皮細胞(2)或組織的實質(zhì)細胞通常接種于上層通道����,而下層通道往往接種血管內(nèi)皮細胞(5)以形成管腔狀的血管系統(tǒng)。上下兩個通道中間由一張多孔柔性膜(4)隔開�����,既保證細胞的相互獨立,又可使上下通道間的物質(zhì)和信號交互����,以及觀測細胞遷移成為可能。微流體通道旁邊的真空腔(3)提供了可調(diào)節(jié)的機械拉伸����,更好的模擬器官運動(如肺部呼吸和腸道蠕動)。
3.2 器官芯片在藥物開發(fā)中的價值
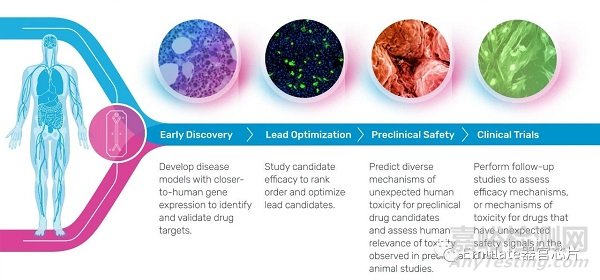
究竟器官芯片如何在藥物開發(fā)工作流程中的發(fā)揮效用�����,它們?nèi)绾翁岣吣愕呐R床成功率��?當我們審視器官芯片的應(yīng)用時����,我們看到器官芯片對于藥物開發(fā)管線的全流程都有益處�����。
一����、早期發(fā)現(xiàn):在藥物發(fā)現(xiàn)的早期階段����,器官芯片可用于開發(fā)具有更接近人類基因表達和生理結(jié)構(gòu)和功能的疾病模型��,以確定和驗證藥物反應(yīng)��。器官芯片已被用于生成多個器官和疾病的人類相關(guān)模型����,包括骨癌轉(zhuǎn)移、細菌性陰道炎�����、環(huán)境性腸功能紊亂和COVID-19新冠肺炎等����。這些模型使研究人員能夠更好地了解潛在的疾病機制并開發(fā)更有競爭力的治療方法。
二�����、先導(dǎo)物優(yōu)化:在先導(dǎo)物優(yōu)化階段�����,器官芯片提供與人類相關(guān)的反應(yīng)數(shù)據(jù),對顯示出最有效和最小毒性的候選先導(dǎo)物進行排序和優(yōu)化��。通過將器官芯片研究納入藥物開發(fā)的這一階段��,在人體器官芯片中產(chǎn)生毒性信號的化合物可以在早期體內(nèi)研究中被取消優(yōu)先級��,盡早淘汰�����,從而減少動物試驗��,確保推動更安全的候選藥物進入到后續(xù)開發(fā)流程�����。
三����、臨床前評估:在臨床前安全評估階段�����,器官芯片可以作為篩選工具來預(yù)測毒性的各種機制【4】。在這個階段�����,它們還可以用來評估在臨床前動物研究中可能觀察到的毒性與人類的相關(guān)性【5】��。器官芯片在這一階段特別有利于評估越來越針對人類的新型藥物����,如生物制劑和免疫療法。
四����、臨床試驗:最后,器官芯片甚至可以對藥物開發(fā)的臨床試驗階段受益�����。對于在臨床上產(chǎn)生意料之外的毒性信號的候選藥物����,器官芯片可以用來進行后續(xù)回溯性研究,以評估毒性機制����,研究人員可以利用這些信息來指導(dǎo)備用候選藥物的優(yōu)先次序�����。
器官芯片用戶案例:Emulate公司的研究人員與Janssen公司合作����,通過在人類肝臟芯片上測試Atabecestat的肝臟毒性����,該化合物是Janssen公司開發(fā)的BACE抑制劑,在臨床試驗中引起藥物性肝損傷(DILI)�����。通過這項研究�����,他們確認了該化合物的肝臟毒性����,確定了與治療相關(guān)的機制和損傷生物標志物,并確認其作用機制是氧化應(yīng)激引發(fā)炎癥體反應(yīng)��。最終�����,這些結(jié)果能夠幫助Janssen公司篩選更安全的備用化合物����。
如您所見,器官芯片可以對藥物開發(fā)的全流程都有益處����。下一節(jié)將進一步討論器官芯片系統(tǒng)豐富的實驗方式及豐富應(yīng)用。
4�����、器官芯片豐富的實驗分析方式
每個器官芯片使研究人員能夠收集和分析多樣的數(shù)據(jù)����。并且與傳統(tǒng)細胞培養(yǎng)或臨床中使用的終點檢測相互兼容。
一��、流出物分析:單向的流路設(shè)計�����,使得研究人員能夠?qū)γ總€細胞通道的流出物進行獨立采樣����。對流出物進行定性或者定量分析����,可獲得功能相關(guān)的數(shù)據(jù)����,如組織健康和損傷的功能生物標志物、表觀滲透率(Papp)��、細胞因子釋放��、代謝物和外泌體分泌等����。
二、成像分析:這也是器官芯片平臺最重要的分析手段����。研究人員能夠通過各種實驗室成像設(shè)備評估細胞形態(tài)、標志物表達和細胞遷移等行為����。器官芯片可進行原位免疫熒光,無需繁瑣的切片制片過程,可直接將熒光抗體和標記物在芯片中與細胞孵育����,節(jié)省大量的實驗周期和資源投入。與目前各種實驗室主流成像技術(shù)相兼容����,包括相差顯微鏡�����、寬視場熒光��、共聚焦����、多光子和掃描電子顯微鏡。還可以進行高內(nèi)涵成像��,捕捉整個芯片通道的培養(yǎng)區(qū)域��,結(jié)合AI智能分析芯片中特定細胞的表達特征和行為特征�����,并進行海量數(shù)據(jù)的定量分析,做到無偏好性的數(shù)據(jù)輸出�����。
三�����、組學(xué)分析:組學(xué)分析手段可解析器官芯片與人體組織的相似性�����,或健康和病變組織之間的遺傳差異��,使研究人員能夠確定相關(guān)的疾病分子機制����,闡明其下游信號通路和主要調(diào)控因子。目前已經(jīng)有成熟的轉(zhuǎn)錄組����、基因組、單細胞組學(xué)以及蛋白組學(xué)等分析方案可供參考�����。
器官芯片的數(shù)據(jù)讀取形式豐富多樣,可更好地了解人類的生理和疾病機制��。通過詳盡的終點分析����,Emulate可以更好地指導(dǎo)研究人員進行整個器官芯片的分析。
5�����、器官芯片應(yīng)用場景
本節(jié)我們著重展示器官芯片為人類疾病機制解析和助力候選藥物開發(fā)的幾種方式�����。
5.1 細胞與基因治療
基因療法在治療遺傳性和獲得性遺傳疾病方面有著巨大的前景����,但開發(fā)這些療法的進展仍然緩慢����。以基于腺相關(guān)病毒(Adeno-Associated Virus, AAV)的基因療法為例:雖然到目前為止已經(jīng)有超過136項基于AAV的療法的臨床試驗,但目前只有兩種被批準上市��。此外�����,由于傳統(tǒng)的臨床前實驗?zāi)P蜔o法準確預(yù)測毒性,這些試驗中有35%出現(xiàn)了嚴重的不良安全事件��。
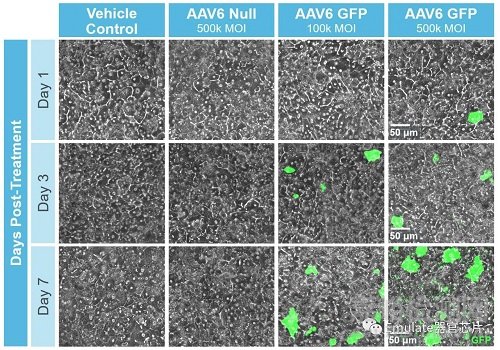
幸運的是�����,我們可以基于肝臟器官芯片芯片開發(fā)AAV轉(zhuǎn)導(dǎo)應(yīng)用�����。研究人員可以在與人類高度相似的肝臟器官芯片中快速迭代AAV設(shè)計����,在臨床試驗前加速載體優(yōu)化篩選。用戶可以在上皮通道中施加待測的AAV載體����,可持續(xù)監(jiān)測其轉(zhuǎn)導(dǎo)效率和毒性信號,使研究人員能夠以時間和劑量依賴的方式評估轉(zhuǎn)導(dǎo)和毒性反應(yīng)����。轉(zhuǎn)導(dǎo)效率可以通過GFP在肝細胞中的表達進行量化,而AAV載體的潛在毒性可以通過白蛋白分泌和ALT釋放水平等功能性生物標志物進行測量����。
AAV轉(zhuǎn)導(dǎo)效率只是基因治療中器官芯片可以應(yīng)用的一個領(lǐng)域�����。除了改善基于AAV的療法的開發(fā)外����,這一工作流程還可適用于評估AAV以外的載體����,包括病毒和非病毒載體。這項技術(shù)的靈活性和敏捷性可縮短為患者提供有效和安全的基因療法開發(fā)周期����。通過讓研究人員在短短幾周內(nèi)產(chǎn)生與人類相關(guān)的數(shù)據(jù)(而在非人類靈長類動物身上則需要幾個月)����,器官芯片可以促進載體設(shè)計的快速迭代,以確保最有前景的候選載體進入臨床試驗�����。
圖注:在血友病研究中��,AAV6是治療性研究的主要載體之一。為了評估Emulate肝臟芯片在預(yù)測AAV轉(zhuǎn)導(dǎo)和肝臟毒性風(fēng)險方面的作用��,用編碼綠色熒光蛋白(GFP)的AAV6載體處理肝臟芯片����。AAV6表現(xiàn)出時間和濃度依賴性的轉(zhuǎn)導(dǎo)表型,而肝實質(zhì)細胞和肝竇內(nèi)皮細胞保持健康的形態(tài)�����,沒有毒性信號存在��。
5.2 免疫與炎癥
炎癥在許多疾病中起著作用�����,慢性炎癥性疾病在全世界造成了五分之三的死亡【6】����。然而,由于在體外建立復(fù)雜的免疫反應(yīng)模型難度極大��,加上常用的動物模型與人類免疫系統(tǒng)的差異巨大����,我們目前對炎癥的機制仍然知之甚少�����。
器官芯片技術(shù)可用于建立更多與人類相關(guān)的炎癥模型��,使研究人員能夠?qū)Ⅲw內(nèi)看到的細胞多樣性納入到這種體外模型中��。器官芯片模型的靈活性使研究人員能夠精確控制和研究炎癥過程中各種因素的單獨或聯(lián)合貢獻����,包括常駐和循環(huán)免疫細胞��、炎癥細胞因子����、細胞-細胞相互作用和組織相關(guān)的機械力,更好地了解疾病病理和藥物效應(yīng)����。
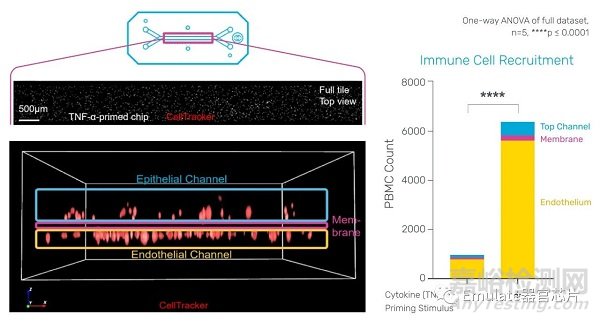
以炎癥性腸?�。↖nflammatory Bowel Disease, IBD)為例����。結(jié)腸器官芯片可以準確模擬失調(diào)的免疫細胞招募����,這是IBD發(fā)病機制的主要因素�����。當免疫細胞在促炎癥因子的刺激下流經(jīng)芯片的血管通道時�����,它們經(jīng)歷了免疫細胞招募的整個過程:從附著到遷移��,再到下游效應(yīng)器功能和屏障損傷����。這是迄今為止唯一一個以組織和炎癥特異性方式捕捉這一完整過程的模型,使我們能夠更完整地了解IBD的發(fā)病機制�����。該模型評估了四種具有不同作用機制的臨床相關(guān)IBD治療藥物�����,表明器官芯片可用于評估藥物療效和對候選藥物進行排序��。
圖注:復(fù)雜的免疫反應(yīng),包括免疫細胞的招募�����,都可以被模擬出來����。這里顯示的是PBMC(紅色CellTracker 預(yù)染)免疫細胞從血管通道招募到上皮通道的過程,IBD發(fā)病機制的關(guān)鍵步驟�����。
5.3 毒理研究
如何評估藥物對人體的毒性是目前生物制藥公司在開發(fā)安全有效藥物時面臨的巨大挑戰(zhàn)����。大約30%的藥物在臨床試驗中因毒性而失敗--盡管已經(jīng)通過了動物的臨床前安全篩選【7】。換言之�����,傳統(tǒng)的模型缺乏預(yù)測毒性的價值�����,無法高效地將有競爭力的候選藥物推向臨床�����。
器官芯片使研究人員能夠在藥物開發(fā)的早期預(yù)測藥物對人類的反應(yīng)����,從而有信心將其轉(zhuǎn)化為到臨床試驗階段。為了衡量器官芯片能在多大程度上改善病人的安全����,研究人員根據(jù)IQ MPS聯(lián)盟(國際藥品開發(fā)創(chuàng)新和質(zhì)量聯(lián)盟的一個附屬機構(gòu))規(guī)定的指南標準,對Emulate人體肝芯片進行了鑒定�����。該研究表明�����,肝臟芯片能夠正確識別87%的導(dǎo)致患者藥物性肝損傷(Drug-Induced Liver Injury, DILI)的測試藥物����,而這些藥物,之前都能順利地通過了動物評估����,但在臨床試驗中因為毒性造成受試者的死亡而終止����。同時����,Emulate人類肝臟芯片沒有錯誤地識別任何無毒的藥物,特異性達到100%��,這種完美的特異性為器官芯片在毒理學(xué)篩選工作流程中的應(yīng)用奠定基礎(chǔ)【4】�����。
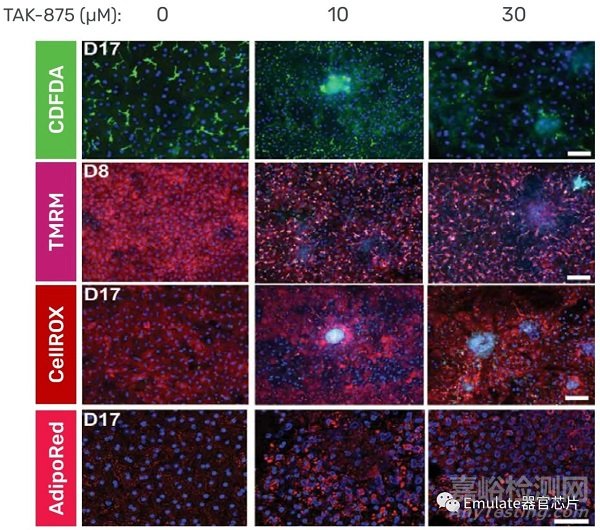
為了證明在臨床前評估中使用器官芯片如何能改善臨床試驗的結(jié)果��,請看如下的這個使用案例:TAK-875是一個候選藥物��,它由于DILI而在III期試驗中被中止了����。當在肝臟芯片上對該化合物進行回顧性研究時,結(jié)果顯示�����,長期接觸該化合物會導(dǎo)致線粒體功能障礙、氧化應(yīng)激�����、脂滴形成和先天免疫反應(yīng)�����,這些都是易感患者DILI的預(yù)兆【8】��。如果在臨床試驗之前進行肝臟芯片研究�����,研究人員可以更早地發(fā)現(xiàn)人類特有的毒性問題����,取消TAK-875作為候選藥物的優(yōu)先級��,并將更安全的候選藥物向前推進����。
圖注:識別特異性DILI的風(fēng)險。每天用TAK-875處理人類肝臟芯片�����,劑量相當于人類的Cmax(10μM),以確定它們是否能檢測DILI����。對 MRP2底物CDFDA(綠色)的膽汁外流進行共聚焦顯微鏡分析顯示,TAK-875導(dǎo)致MRP2活性的劑量依賴性下降��。同時�����,通過測量TMRM的劑量相關(guān)和時間依賴的重新分布��、脂滴積累和活性氧(ROS)的形成����,證實TAK-875的治療對線粒體膜電位有影響。這些結(jié)果與TAK-875治療的臨床結(jié)果一致����,表明肝臟器官芯片可用于評估特異性DILI。
6��、用戶反饋結(jié)果:器官芯片優(yōu)于傳統(tǒng)的臨床前模型
器官芯片是如此強大的技術(shù)����,可以幫助科學(xué)家在整個藥物研發(fā)過程中更早地預(yù)測藥物對人體的反應(yīng)�����。調(diào)查中��,97%的器官芯片用戶同意,器官芯片比傳統(tǒng)的體外模型更具預(yù)測性�����。此外����,更令人驚訝的發(fā)現(xiàn)是,70%器官芯片用戶認為該技術(shù)比體內(nèi)模型更具預(yù)測性��,另有21%的用戶認為該技術(shù)具有類似的預(yù)測性【3】�����。這些調(diào)查結(jié)果直接說明了采用器官芯片技術(shù)可以對延誤研究項目產(chǎn)生影響�����。
7、總結(jié)
正如本文所討論的����,器官芯片技術(shù)可以幫助研究人員克服與傳統(tǒng)體外和體內(nèi)模型相關(guān)的一些挑戰(zhàn)。下表總結(jié)了一些最常見的挑戰(zhàn)以及器官芯片可以帶來什么樣的幫助�����。
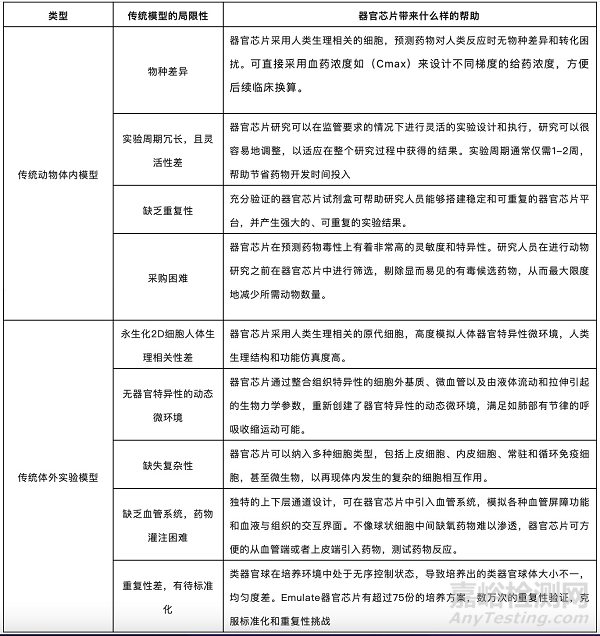
為了使廣大科研工作者能快速掌握器官芯片技術(shù)����,Emulate開發(fā)了商業(yè)化的器官芯片系統(tǒng)Human Emulation System ®。加上積累的超過75種的標準化解決方案����,科研人員使用該系統(tǒng)將非常容易在體外構(gòu)建多種器官模型,為各自的研究添磚加瓦��。
參考文獻
1. Huh D, Matthews BD, Mammoto A, Montoya-Zavala M, Hsin HY, Ingber DE. Reconstituting organ-level lung functions on a chip. Science. 2010 Jun 25;328(5986):1662-8. https://doi: 10.1126/science.1188302.
2. Begley, C. G., & Ellis, L. M. (2012, March 28). Raise standards for preclinical cancer research - Nature. Nature. https://doi.org/10.1038/483531a
3. Survey of 125 scientists conducted by the Linus Group on behalf of Emulate (2021)
4. Ewart, L., Apostolou, A., Briggs, S. A., Carman, C. V., Chaff, J. T., Heng, A. R., Jadalannagari, S., Janardhanan, J., Jang, K. J., Joshipura, S. R., Kadam, M. M., Kanellias, M., Kujala, V. J., Kulkarni, G., Le, C. Y., Lucchesi, C., Manatakis, D. V., Maniar, K. K., Quinn, M. E., . . . Levner, D. (2022, December 6). Performance assessment and economic analysis of a human Liver-Chip for predictive toxicology - Communications Medicine. Nature. https://doi.org/10.1038/s43856-022-00209-1
5. Jang, Kyung-Jin, et al. “Reproducing Human and Cross-Species Drug Toxicities Using a Liver-Chip.” Science Translational Medicine, vol. 11, no. 517, 6 Nov. 2019, p. eaax5516, stm.sciencemag.org/content/scitransmed/11/517/eaax5516.full.pdf, https://doi.org/10.1126/scitranslmed.aax5516.
6. Pahwa, R., Goyal, A., & Jialal, I. (2022, August 8). Chronic Inflammation - StatPearls - NCBI Bookshelf. Chronic Inflammation - StatPearls - NCBI Bookshelf. https://www.ncbi.nlm.nih.gov/books/NBK493173/#_article-19530
7. The NIH microphysiological systems program: developing in vitro tools for safety and efficacy in drug development - PubMed. (2019, October 1). PubMed. https://doi.org/10.1016/j.coph.2019.09.007
8. Liver Safety of Fasiglifam (TAK-875) in Patients with Type 2 Diabetes: Review of the Global Clinical Trial Experience - PubMed. (2018, June 1). PubMed. https://doi.org/10.1007/s40264-018-0642-6