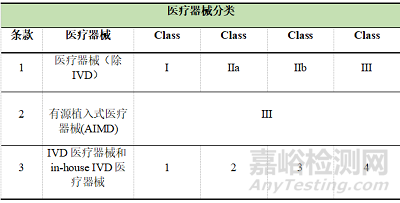
TGA對(duì)醫(yī)療器械監(jiān)管的分類同樣是依據(jù)產(chǎn)品的風(fēng)險(xiǎn)程度���,產(chǎn)品的分類等級(jí)隨著其風(fēng)險(xiǎn)的升高而遞增���。
二、醫(yī)療器械注冊(cè)費(fèi)用
計(jì)劃將醫(yī)療器械產(chǎn)品投放TGA市場(chǎng)的制造商���,都需要向TGA申請(qǐng)將產(chǎn)品納入ARTG注冊(cè)庫中。在將產(chǎn)品納入ARTG注冊(cè)庫過程中會(huì)涉及到注冊(cè)費(fèi)用和體系審核費(fèi)用等���。此外���,與FDA類似,申辦者還需要每年向TGA繳納年費(fèi)以維持產(chǎn)品在澳大利亞的合法銷售���。澳大利亞的財(cái)政年度是從當(dāng)年的7月1日到第二年的6月30日���。
已有產(chǎn)品在澳大利亞銷售的制造商及申辦者應(yīng)在每個(gè)財(cái)年結(jié)束前確定需要繼續(xù)在澳大利亞銷售的產(chǎn)品并及時(shí)繳納年費(fèi),不想繼續(xù)在澳大利亞銷售的產(chǎn)品則需要及時(shí)向TGA申請(qǐng)撤銷���,以免產(chǎn)生新的年費(fèi)���。
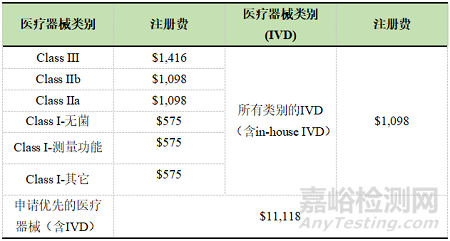
1. 申請(qǐng)ARTG的注冊(cè)費(fèi)用
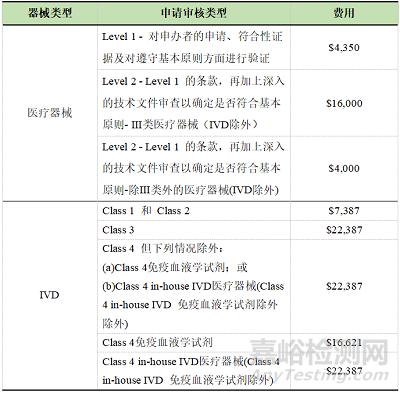
2. 醫(yī)療器械注冊(cè)的體系審核費(fèi)用
TGA的體系審核分三種情況:強(qiáng)制���、豁免,自行選擇���。
強(qiáng)制審核的情況有:
★在性交時(shí)陰莖插入過程中作為避孕或預(yù)防疾病傳播的屏障的器械(避孕套除外)���;
★植入式避孕的器械;
★脊柱融合植入式器械���;
★專門用于為另一醫(yī)療器械消毒的器械���;
★可植入的人工晶狀體醫(yī)療器械;
★一種眼內(nèi)粘彈性流體的醫(yī)療器械���;
★未根據(jù)EC互認(rèn)協(xié)議或EFTA互認(rèn)協(xié)議進(jìn)行評(píng)估的第3類醫(yī)療器械���;
★用于監(jiān)測(cè)第4類IVD醫(yī)療器械的非測(cè)定專用質(zhì)量控制材料;
★用于自檢的IVD醫(yī)療器械���;
★用于護(hù)理點(diǎn)檢測(cè)的IVD醫(yī)療器械���;
★用于檢測(cè)性傳播因子存在或暴露于性傳播因子的第3類IVD醫(yī)療器械���;
★擬在藥品福利計(jì)劃下提供使用的IVD醫(yī)療器械;
★擬供國家篩選項(xiàng)目使用的IVD醫(yī)療器械;
★第4類IVD醫(yī)療器械;
★第4類in-house IVD醫(yī)療器械���;
★伴隨診斷醫(yī)療器械���。
豁免審核的情況有:
★獲得TGA合格評(píng)定證書;
★持有未被暫?��;虺蜂N的MDR或IVDR證書;
★被納入ARTG作為僅限出口的醫(yī)療器械或IVD���。
自行選擇的情況指的是沒有在強(qiáng)制審核列表中的醫(yī)療器械產(chǎn)品���,申辦者可以自行選擇是否要求體系審核,并且無需支付審核費(fèi)用���。
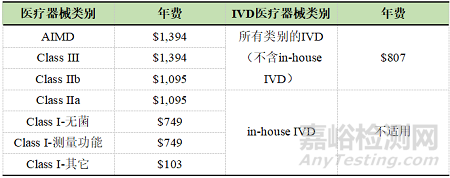
3. 醫(yī)療器械年費(fèi)
TGA每年都會(huì)更新醫(yī)療器械年費(fèi)���,因此每年的年費(fèi)會(huì)發(fā)生變化���。下表是2023財(cái)政年度的年費(fèi)。