隨著過程分析技術(shù)( process analysis technology�,PAT) 在制藥行業(yè)越來越受到重視,美國食品藥品監(jiān)督管理局( FDA) 等官方機(jī)構(gòu)正在積極推動應(yīng)用PAT 技術(shù)�����,力圖從過程�、工藝上保證產(chǎn)品的質(zhì)量,改變目前主要依靠認(rèn)證認(rèn)可檢查的現(xiàn)狀���。本文綜述了制藥行業(yè)中的PAT 相關(guān)法規(guī)/指導(dǎo)原則發(fā)展進(jìn)程以及常用的PAT 工具和相關(guān)應(yīng)用進(jìn)展���,為加強(qiáng)我國制藥行業(yè)對PAT 的理解提供一定參考�����,推動制藥企業(yè)將其融入生產(chǎn)過程�,從藥品質(zhì)量的源頭抓起�����,提高藥品質(zhì)量���。
過程分析技術(shù)( process analytical technology�����,PAT) 是主要指以保證產(chǎn)品最終質(zhì)量為目的�,通過對藥品制造過程中有關(guān)原料�、輔料等物料以及工藝的關(guān)鍵參數(shù)及指標(biāo)進(jìn)行實時測定的過程,是實現(xiàn)質(zhì)量源于設(shè)計( QbD) 理念的有效工具�。采用PAT 用于優(yōu)化制藥工藝和質(zhì)量控制,實現(xiàn)藥品從研發(fā)到生產(chǎn)的技術(shù)銜接和產(chǎn)品質(zhì)量一致性�,從而實現(xiàn)制藥工程項目的全生命周期管理�����。本文綜述了PAT 在制藥行業(yè)中的相關(guān)法規(guī)�����、工具及應(yīng)用等現(xiàn)狀,以期對我國制藥行業(yè)發(fā)展有所啟發(fā)�。
1�����、制藥行業(yè)中的PAT相關(guān)法規(guī)/指導(dǎo)原則
PAT 理念最早源于1993 年美國分析化學(xué)家協(xié)會(AOAC) 發(fā)起的一次論壇�,后于2004 年由美國食品藥品監(jiān)督管理局(FDA) 正式發(fā)布了關(guān)于PAT 的制藥工業(yè)指導(dǎo)原則[1-2]。同時也是制藥工業(yè)的第一個正式的法規(guī)性指導(dǎo)原則���。該指導(dǎo)原則的發(fā)布�,使得越來越多的制藥企業(yè)開始重視QbD 理念,并開始引入PAT 以實現(xiàn)藥品生產(chǎn)過程的全程監(jiān)控���,以更好的保證藥品的質(zhì)量。
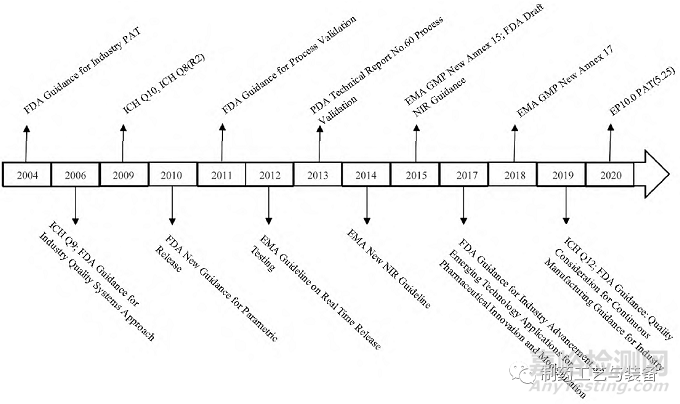
為了推行科學(xué)監(jiān)管理念�,鼓勵制藥企業(yè)不斷創(chuàng)新與發(fā)展,各國監(jiān)管部門和組織均對PAT 的相關(guān)指南�、標(biāo)準(zhǔn)或應(yīng)用作了極大的努力(圖1) [3-5]�。如FDA 于2006 年發(fā)布了動態(tài)藥品生產(chǎn)管理規(guī)范(CGMP) 工業(yè)指南, 2011 年發(fā)布了改版的工藝驗證指南���, 2013 年美國注射劑協(xié)會發(fā)布的第60 號技術(shù)報告中,均在相關(guān)章節(jié)闡述了PAT 技術(shù)的重要性�,以及相關(guān)技術(shù)規(guī)范及要求�����。2015 年FDA 又發(fā)布了工業(yè)界開發(fā)和申報近紅外分析方法指導(dǎo)原則草案���。同時人用藥品注冊技術(shù)規(guī)定國際協(xié)調(diào)會(ICH) 也發(fā)布了多個相關(guān)文件�, ICH Q8、ICHQ9�����、ICH Q10 和ICH Q12 等���,來表達(dá)產(chǎn)品開發(fā)���、技術(shù)轉(zhuǎn)移、商業(yè)化生產(chǎn)等行為中QbD 和PAT 理念的重要性���,從而細(xì)化了PAT 在生產(chǎn)過程中需深刻理解的具體范圍和要求,是實施PAT 所需的理論基礎(chǔ)之一�。
圖1 歐美制藥工業(yè)中過程分析技術(shù)( PAT) 相關(guān)指導(dǎo)原則概覽
同時歐美制藥發(fā)達(dá)國家的藥典為協(xié)助或推進(jìn)實行PAT技術(shù)�����,作了大量的工作�����,其中美國藥典(USP) 兩項最主要的工作是: 在其PAT 主要分析技術(shù)手段近紅外光譜< 1119 >和拉曼光譜< 1120 > 章節(jié)中對二者作為PAT 應(yīng)用工具的應(yīng)用范圍、技術(shù)要求、儀器設(shè)備性能確認(rèn)等作了詳細(xì)的說明和規(guī)定。歐洲藥典(EP) 作為歐洲地區(qū)唯一的藥品質(zhì)量標(biāo)準(zhǔn)指導(dǎo)性文獻(xiàn)���,由歐洲藥品質(zhì)量管理局(EDQM) 出版發(fā)行,其在EP10. 0 最新版本中增加了目前全球唯一的專門性PAT藥典指導(dǎo)原則: PAT(5. 25) 。其在具體內(nèi)容中著重于描述分析技術(shù)與制造過程的銜接���,以此作為加強(qiáng)過程控制和提高過程理解的手段���。并同時還新增或修訂了PAT 相關(guān)的多個技術(shù)章節(jié),包括近紅外光譜(2. 2. 40) 、拉曼光譜(2. 2. 48) 、化學(xué)成像(5. 24) 、化學(xué)計量學(xué)方法用于分析數(shù)據(jù)(5. 21) 等。
由上述歐美國家制藥領(lǐng)域PAT 相關(guān)法規(guī)�����、指南及指導(dǎo)原則可知,PAT 技術(shù)于2004 年FDA 首次在制藥工業(yè)提出至今�,隨著各類儀器技術(shù)的發(fā)展,以及連續(xù)制造(CM) �、智慧制造等理念的發(fā)展,PAT 技術(shù)已逐步從構(gòu)思���、實驗室階段逐漸向制藥工業(yè)應(yīng)用化發(fā)展���,并對各國的藥監(jiān)部門如何監(jiān)管審批提出了新的挑戰(zhàn)���。
2、制藥行業(yè)中的PAT工具
PAT 中的分析是涉及多學(xué)科的綜合分析�,PAT 中的過程是貫穿于整個藥品生產(chǎn)的過程。FDA 提出的PAT 測量包括3 種類型,即: 近線檢測(at-line)�、在線檢測(on-line)�����、線內(nèi)檢測(in-line)�����。近線測量涉及將樣品從工藝流程轉(zhuǎn)移到分析設(shè)備���,分析設(shè)備與工藝流程相互脫離���,但又靠近工藝流程,使檢測過程延遲小�����,因此可以根據(jù)測量的結(jié)果進(jìn)行工藝調(diào)整�。在線檢測是將生產(chǎn)過程中的樣品從生產(chǎn)裝備中引出后自動引入分析儀器進(jìn)行監(jiān)測并根據(jù)試驗性質(zhì)決定轉(zhuǎn)移的部分可否返回工藝流; 在線分析方式中,PAT 工具與生產(chǎn)流程分別作為側(cè)線與主線組合在一起�����。線內(nèi)檢測通過在生產(chǎn)設(shè)備或流程內(nèi)部需要檢測質(zhì)量的部位安裝傳感器或者測量探頭進(jìn)行分析工作���,PAT 工具與生產(chǎn)設(shè)備往往可視作一體式�����。在線與線內(nèi)2種檢測方式將分析技術(shù)轉(zhuǎn)移到過程流中�,通常支持快速和自動化的過程調(diào)整。
相比傳統(tǒng)的分析技術(shù)�,PAT 具有以下優(yōu)勢: 促進(jìn)參數(shù)的快速測試而不破壞樣品; 可以立即做出關(guān)鍵決策和流程調(diào)整; 提高自動化程度,保證操作人員的安全性; 能夠確定和解釋所有的變異的關(guān)鍵來源; 使用的材料所建立的設(shè)計空間�、工藝參數(shù)、制造�、環(huán)境和其他條可以準(zhǔn)確可靠地預(yù)測產(chǎn)品質(zhì)量屬性[6]。
目前���,PAT 研究的分析工具包括光譜技術(shù)���、光學(xué)成像技術(shù),動態(tài)光散射�、氣相色譜(GC) 、質(zhì)譜(MS) ���、核磁共振(NMR) �����、紅外光譜(IR) �����、紫外-可見光譜(UV-Vis) 及X 射線熒光(XRF) 等�。其中制藥行業(yè)研究最多�,且應(yīng)用最廣的是光譜技術(shù)主要是: 近紅外光譜(NIR) 技術(shù)、拉曼(Raman) 光譜技術(shù)[7]���。
2.1近紅外光譜
由于NIR是PAT最常用的分析工具之一�����,各國藥典都有相關(guān)章節(jié)的收載���。同時歐洲藥品管理局(EMA) 和FDA都要相關(guān)的重要指導(dǎo)原則。2015 年FDA發(fā)布了工業(yè)界開發(fā)和申報近紅外分析方法指導(dǎo)原則草案(< Development and submission of near infrared analytical procedures���,Guidance for industry���,Draft guidance >),該指導(dǎo)原則明確了制藥工業(yè)在新藥申請及申請主文件中采用NIR方法的開發(fā)�����、驗證、變更需考慮的關(guān)注點以及需提交的文件資料���。NIR光譜具有快速�����、無損和同時測定多種性質(zhì)的優(yōu)勢���,已逐步應(yīng)用于藥品生產(chǎn)的多個環(huán)節(jié),如混合�、干燥、壓片�����、包衣���、預(yù)處理�、包裝等�����,為生產(chǎn)過程提供在線、實時的質(zhì)量信息[8]���。
現(xiàn)代NIR技術(shù)由NIR儀�����、化學(xué)計量學(xué)軟件技術(shù)和統(tǒng)計校正模型3個部分組成。一般操作流程是���,根據(jù)樣品的NIR譜圖特性�����,采用適合的化學(xué)計量學(xué)方法�����,建立校正模型�����,實現(xiàn)定性�、定量分析或者在線過程分析���。此外���,硬件部分�����,干涉儀的發(fā)展和應(yīng)用促使傅里葉變換型光譜儀的抗震能力大大增強(qiáng)���,可實現(xiàn)便攜、車載的功能�����,大大增強(qiáng)了其應(yīng)用于生產(chǎn)過程環(huán)境的適用性�����。
2.2拉曼光譜
盡管近紅外光譜技術(shù)在制藥行業(yè)仍占主導(dǎo)地位���,但Raman光譜技術(shù)的利用正變得越來越廣泛�����。Raman 光譜是一種非彈性散射光譜�����,因為其與入射光頻率不同的散射光譜進(jìn)行分析以得到分子振動���、轉(zhuǎn)動方面信息�����,并應(yīng)用于分子結(jié)構(gòu)研究的一種分析方法�����。
藥物的生產(chǎn)過程很容易導(dǎo)致晶型轉(zhuǎn)化,特別是當(dāng)亞穩(wěn)態(tài)的晶型作為主藥的時候���。藥品開發(fā)過程中�����,最佳的劑型設(shè)計���,輔料的正確選擇,生產(chǎn)方式的制定�����,與溶出試驗的監(jiān)控是一套完整的流程。而Raman 光譜是唯一1個能夠從藥品分子的層次�,適用于上述整個流程中每一環(huán)節(jié)的藥品晶型實時監(jiān)測的儀器[9]。
2020年版《中國藥典》���、USP�、EP都提到了一種最新的拉曼光譜技術(shù)———空間位移拉曼光譜(SORS) �,SORS 可分析數(shù)毫米厚的樣品,也可以對不透明包裝內(nèi)的材料進(jìn)行化學(xué)分析�����。例如�����,乙醇是常用的醫(yī)療用品和有機(jī)溶劑���,當(dāng)其被裝在透明聚對苯二甲酸乙二醇酯(PET) 塑料中���。用傳統(tǒng)Raman僅得到包裝的光譜信息,而通過SORS 甚至能夠獲得21 mm厚度的PET 瓶內(nèi)的乙醇譜圖[10]���。因此�����,SORS 能夠輕松實現(xiàn)原輔料鑒別�����,減少物料開包檢測帶來的污染風(fēng)險�����,更好地滿足日益嚴(yán)格的法規(guī)要求�����。
2.3其他
除了上述提到的幾種傳統(tǒng)的PAT 工具�����,目前有越來越多的新型分析方法加入進(jìn)來�����。激光誘導(dǎo)熒光技術(shù)(LIF) 是在藥物制劑中進(jìn)行熒光材料的選擇(通常有效成分) �����。LIF 技術(shù)是一種非破壞性的PAT 分析工具�,用來分析攪拌動力學(xué)和混合一致性,以及藥片有效成分的含量�����。LIF 在制藥行業(yè)有非常大的用處���,因為近兩百種的活性成分中60%有發(fā)熒光的特性�。在線LIF 的好處是獲得實時混合動力學(xué)的結(jié)果和減少由于取樣所導(dǎo)致的錯誤和時間浪費[11]���。
聚焦光束反射測量技術(shù)(FBRM) 可以在原位條件下�����,實時追蹤顆粒和液滴的變化情況�。最初是作為實時在線顆粒表征技術(shù)而發(fā)明的�����,經(jīng)不斷研究與完善,現(xiàn)能對高濃度的漿料和顆粒體系進(jìn)行實時測量���。FBRM 獨特的設(shè)計結(jié)構(gòu)確保即使在高濃度及不透明的溶液體系下�,依然能對顆粒粒徑和相對顆粒數(shù)進(jìn)行高重復(fù)性和高重現(xiàn)性的測量[12]�����。
激光誘導(dǎo)擊穿光譜(LIBS) 技術(shù)通過超短脈沖激光聚焦樣品表面形成等離子體�,進(jìn)而對等離子體發(fā)射光譜進(jìn)行分析以確定樣品的物質(zhì)成分及含量。超短脈沖激光聚焦后能量密度較高�,可以將任何物態(tài)的樣品激發(fā)形成等離子體,LIBS(原則上) 可以分析任何物態(tài)的樣品���。LIBS 以其可原位�����、在線�、同時分析多種元素成分的優(yōu)點�����,成為流程工業(yè)現(xiàn)場檢測關(guān)注的重要技術(shù)[13]���。
2.4模型建立方法
在將PAT 工具用于制藥過程監(jiān)測時�����,由于物料體系復(fù)雜���,待測關(guān)鍵工藝參數(shù)(CPAs) 或關(guān)鍵質(zhì)量屬性(CQAs) 的譜圖信息可能相互重疊或被其他干擾信息掩蓋,無法從中直接獲取所需信息�����,且采集過程中存在因儀器或環(huán)境而引入的噪聲�。因此,通常需要使用化學(xué)計量學(xué)方法提取有用信息���,并選擇合適的算法建立多元定性或定量分析模型�,以實現(xiàn)分析目的���。解決定性分析問題需要用到化學(xué)計量學(xué)中的模式識別方法�。模式識別方法根據(jù)學(xué)習(xí)過程可分為有監(jiān)督模式識別方法和無監(jiān)督模式識別方法���。常用的有監(jiān)督模式識別方法有: 距離判別(如馬氏距離���、歐式距離) �����、K-最鄰近(KNN) �、線性判別分析(LDA) 等; 而無監(jiān)督模式識別中則是主成分分析�、聚類分析等方法最為常用。常用的定量分析方法有主成分分析(PCA) ���、偏最小二乘(PLS)�����、人工神經(jīng)網(wǎng)絡(luò)(ANN) 以及支持向量機(jī)(SVM) 和最小二乘支持向量機(jī)(LS-SVM) 等[14]�。此外�,PLS、SVM���、LS-SVM 也被用于定性分析���。
PCA 是一種無監(jiān)督的技術(shù),通常用于減少數(shù)據(jù)的維數(shù)和對高光譜圖像中的信息進(jìn)行分類���。PCA 的核心是數(shù)據(jù)降維�����,從而消除原變量中的重疊信息�����。所得新變量為原變量的線性組合���,新變量具有數(shù)目少、相互正交�����、能較好地表征原變量數(shù)據(jù)結(jié)構(gòu)特征等優(yōu)點���。PCA 用于分析NIR���,F(xiàn)TIR 和LIBS 光譜等[15]。
PCA 算法通過選擇主成分?jǐn)?shù)可有效濾除無效信息���,同時解決了共線性問題�����,適用于復(fù)雜分析體系�。不足之處在于PCA 僅對自變量矩陣進(jìn)行分解降維,并沒有將因變量矩陣的噪音考慮在內(nèi)�����,無法保證參與回歸的主成分與被測組分或性質(zhì)相關(guān)�。基于上述思想�����,PLS 算法同時分解自變量矩陣和因變量矩陣�,然后將獲得的自變量和因變量的得分矩陣進(jìn)行多元線性回歸,既達(dá)到了降維的目的���,又具有模型簡單穩(wěn)健���、預(yù)測精度高、計算量小等優(yōu)點���,已成為目前過程分析領(lǐng)域應(yīng)用最為廣泛的分析算法[16]�����。
ANN 是解釋因素和響應(yīng)變量之間的非線性數(shù)據(jù)的強(qiáng)大工具�����,其原理是給網(wǎng)絡(luò)各種訓(xùn)練樣本�,然后根據(jù)網(wǎng)絡(luò)實際輸出和正確目標(biāo)值之間的偏差修改各神經(jīng)元間的連接權(quán)重�����,網(wǎng)絡(luò)不斷朝誤差減小的方向進(jìn)行變化�,直到實際輸出值與正確目標(biāo)值的偏差滿足所需精度。人工神經(jīng)網(wǎng)絡(luò)由1個輸入層和1個輸出層組成�����,其中輸入層從外部源( 數(shù)據(jù)文件���,圖像���,硬件傳感器等) 接收數(shù)據(jù),1個或多個隱藏層處理數(shù)據(jù)�,輸出層基于網(wǎng)絡(luò)功能提供1個或多個數(shù)據(jù)點[17]���。
PAT是以確保成品質(zhì)量為目標(biāo)設(shè)計、分析與控制制造的一體化系統(tǒng)�。樣品數(shù)據(jù)被采集后,經(jīng)處理系統(tǒng)篩選���、校正���、驗證后,將得到的結(jié)果重新反饋于工藝流程�����,并對工藝流程進(jìn)行調(diào)控�����,從而實現(xiàn)自動化生產(chǎn)�����。
3�、PAT在制藥行業(yè)中的應(yīng)用
目前禮來、強(qiáng)生�����、輝瑞等公司已運用PAT 實現(xiàn)了藥品的連續(xù)制造,并獲得了FDA 的批文���。諾華���、葛蘭素史克�����、龍沙以及天津天士力���、華潤江中等藥企也通過PAT 實現(xiàn)了產(chǎn)品的中控放行���。PAT 在醫(yī)藥行業(yè)的應(yīng)用也受到了國內(nèi)外許多專家和學(xué)者的關(guān)注[18]。
3.1在化學(xué)藥品生產(chǎn)過程中的應(yīng)用
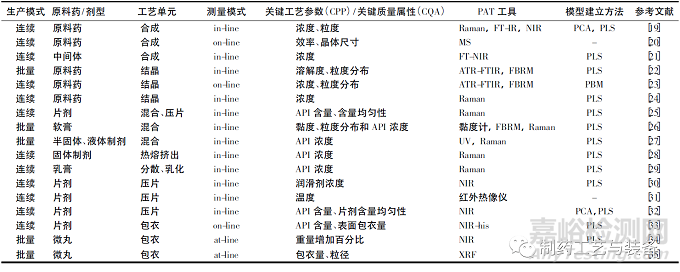
化學(xué)藥品智能化生產(chǎn)隨著數(shù)據(jù)化管理逐漸進(jìn)步�,而質(zhì)量控制依賴人工手段滯后于生產(chǎn)過程。部分大型制藥企業(yè)研究的在線分析技術(shù)在化學(xué)藥品合成�����、混合���、干燥�����、壓片���、結(jié)晶�、包衣�����、包裝等生產(chǎn)過程已發(fā)揮作用���。近5 年部分相關(guān)文獻(xiàn)匯總���,見表1。
表1 近5年過程分析(PAT) 在化學(xué)藥品生產(chǎn)中部分應(yīng)用實例文獻(xiàn)列表
原料藥(API) 合成是藥品生產(chǎn)的起始步驟�����,也是決定藥品安全有效的關(guān)鍵步驟�����。PAT 工具可實時監(jiān)測合成過程變化趨勢,判斷合成終點����,實現(xiàn)智能化控制合成過程。Loren等[20]報道了一種苯海拉明連續(xù)合成的高度集成方法�����。質(zhì)譜(MS) 在整個系統(tǒng)中用于在線反應(yīng)監(jiān)控��、離線產(chǎn)量定量����,并作為反應(yīng)篩選模塊�����,利用帶電微滴中的反應(yīng)加速進(jìn)行高通量路線篩選��,針對反應(yīng)效率進(jìn)行了優(yōu)化�����。Mitic 等[21]在管層流反應(yīng)器進(jìn)行9-烯丙基-2-氯硫雜蒽-9-醇的脫水反應(yīng),研究者設(shè)計線內(nèi)FT-NIR 裝置實時監(jiān)測該化合物反應(yīng)過程并建立PLS模型����,在線分析結(jié)果通過了近線NIR 結(jié)果及離線的HPLC 結(jié)果驗證并具有較高的預(yù)測準(zhǔn)確率。此外����,利用在線分析所得數(shù)據(jù)建立反應(yīng)的動力學(xué)模型更精確地反映生產(chǎn)過程。
結(jié)晶是制藥工業(yè)生產(chǎn)API 中最常見的分離純化操作��。近年來�����,應(yīng)用PAT 工具對結(jié)晶過程進(jìn)行實時監(jiān)測��,促進(jìn)了研究人員對結(jié)晶過程機(jī)理的進(jìn)一步理解����。同時,將PAT 工具應(yīng)用于結(jié)晶過程的開發(fā)����、優(yōu)化、設(shè)計����、分析和調(diào)控����,有助于確保API��、工藝參數(shù)和最終產(chǎn)品的關(guān)鍵質(zhì)量屬性達(dá)到設(shè)計指標(biāo)�����,從而最終實現(xiàn)QBD 的理念����。最常用的技術(shù)包括用于溶液濃度測量的衰減全反射傅里葉變換紅外光譜(ATR-FTIR) 和用于監(jiān)測顆粒數(shù)量及其尺寸分布變化的FBRM[22-23]、用于顆粒直接可視化的顆粒視覺和測量以及用于監(jiān)測多晶型轉(zhuǎn)變的拉曼光譜[24]��。
物料混合過程是制劑生產(chǎn)過程中的關(guān)鍵環(huán)節(jié)����,混合不充分將使藥品質(zhì)量不均一而混合過久則極大地浪費資源����。傳統(tǒng)監(jiān)控物料混合過程的方法分析時間長、破壞樣品�����、多次取樣藥品污染風(fēng)險增加等弊端。因此��,將NIR�����、Raman 等方法應(yīng)用于實時監(jiān)測藥物的原輔料混合過程與FDA 提出的PAT的宗旨一致�����,對于確保最終產(chǎn)品的質(zhì)量(例如片劑的含量均勻性) 至關(guān)重要����。Nagy 等[25]運用線內(nèi)拉曼光譜監(jiān)測3組分(咖啡因、葡萄糖��、硬脂酸鎂) 模型藥物系統(tǒng)的連續(xù)混合和壓片過程�����。使用PLS 定量方法對API 含量����,混合均勻性和片劑含量均勻性進(jìn)行實時分析��。在線拉曼光譜監(jiān)測表明�����,連續(xù)式攪拌機(jī)能夠生產(chǎn)出具有高均質(zhì)性的共混物�����。還建立了基于拉曼光譜的API 進(jìn)料器反饋控制����,從而創(chuàng)建了一種“過程分析控制技術(shù)”(PACT) �����,保證了所生產(chǎn)混合物中所需的API含量����。
壓片通常是獲得片劑最終形式的最后一步。在工業(yè)規(guī)模上��,PAT 的應(yīng)用可以快速分析可以測量更多的樣品����,從而提高了質(zhì)量保證的統(tǒng)計意義。Sasakura 等[30]和Pauli 等[32]均研究了采用線內(nèi)NIR 定量監(jiān)測壓片設(shè)備進(jìn)料管中API 或輔料濃度變化的可行性����。Lee 等[31]的研究結(jié)果顯示了線內(nèi)紅外熱成像技術(shù)在相同壓制力下生產(chǎn)的相同配方片劑之間進(jìn)行區(qū)分的潛在能力。
在制藥工業(yè)中�����,為了實現(xiàn)藥物的持續(xù)釋放或控制釋放����,通常對多顆粒制劑如微丸進(jìn)行包衣。Nishii 等[33] 和Naidu等[34]分別采用NIR 在線檢測和近線檢測方式監(jiān)測包衣過程的均勻性�����,Nakano 等[35]證明了近線XRF 可用作監(jiān)測顆粒包衣過程的PAT����,并成為制藥生產(chǎn)中的強(qiáng)大工具。
3.2在生物藥中的應(yīng)用
生物制藥過程比傳統(tǒng)的化學(xué)藥制藥過程更為復(fù)雜��。生物制藥過程所用原料較復(fù)雜��,批次間存在質(zhì)量差異��,且生物技術(shù)藥物對生產(chǎn)過程極為敏感。因此�����,固定的工藝操作條件無法滿足質(zhì)量控制需求����,需要將PAT 用于生物制藥過程監(jiān)測,保證生物技術(shù)藥物產(chǎn)品質(zhì)量����。
以發(fā)酵或細(xì)胞培養(yǎng)為代表的生物制藥上游環(huán)節(jié),是整個生物制藥的最關(guān)鍵環(huán)節(jié)之一��。通過檢測和控制CQAs�����,藥品質(zhì)量的提高和生產(chǎn)成本的降低均存在較大空間��。發(fā)酵液和細(xì)胞培養(yǎng)液的特點是組成復(fù)雜����,通常氣、固、液三相共存����,其組分和含量不斷變化����。因此將PAT 用于生物制藥過程監(jiān)測,也具有較大挑戰(zhàn)����。已有研究中使用光譜技術(shù)監(jiān)測的指標(biāo)多為與發(fā)酵/培養(yǎng)“環(huán)境”、細(xì)胞生長和產(chǎn)品質(zhì)量相關(guān)的指標(biāo)�����。Sun 等[36]利用微型近紅外光譜儀線內(nèi)監(jiān)測發(fā)酵過程中氨基葡萄糖含量��,控制發(fā)酵過程��,這種便攜式儀器的實施能夠減少時間和分析成本�����。Eamonde-White 等[37]報道��,利用表面增強(qiáng)拉曼光譜技術(shù)(SERS) 以及拉曼光譜聯(lián)合非線性模型預(yù)測控制器(NMPC) ����,對中國倉鼠卵巢(CHO) 細(xì)胞培養(yǎng)中營養(yǎng)物濃度等參數(shù)進(jìn)行在線監(jiān)控�����,正在從實驗研究往GMP 生產(chǎn)應(yīng)用上發(fā)展��。
生物技術(shù)產(chǎn)品下游加工常用的純化操作包括復(fù)性�����、層析����、過濾和制備色譜等����,整個處理過程由若干個目的明確的操作單元組成,相互影響�����。常用的PAT 方法是通過在線液相色譜分析技術(shù)����、NIR 分析技術(shù)檢測目標(biāo)生物藥物純度變化�����,建立純化終點判斷方法,優(yōu)化藥物純化工藝����,提高生物藥的得率,減少純化過程中生物藥的活性破壞�����。West 等[38]展示了新型的PAT 方法�����,可在超濾和滲濾工藝操作過程中同時監(jiān)控多個質(zhì)量屬性����。并開發(fā)了體積排阻色譜(SEC) 方法,對在線PAT 模式下賦形劑精氨酸����,組氨酸和高分子量物質(zhì)的測量。Lofgren 等[39]介紹了使用線內(nèi)弱陰離子交換柱(捕獲步驟) 捕獲澄清的上清液,然后進(jìn)行病毒滅活步驟和拋光步驟����,實現(xiàn)CHO 細(xì)胞系產(chǎn)生的重組蛋白的純化,集成的連續(xù)過程大大提高了產(chǎn)率及生產(chǎn)率�����。
藥品制備步驟中��,將輔料和活性藥物等配制起來��,制成最終的配方����。為增加生物制品穩(wěn)定性,最后一步往往通過凍干流程實現(xiàn)�����。1 個良好的凍干工藝����,應(yīng)具有產(chǎn)品質(zhì)量穩(wěn)定、時間短�����、能耗低、凍干周期可控�����、可驗證的特征��。在藥品凍干過程中�����,監(jiān)控溫度以及準(zhǔn)確判斷一次升華干燥和解析干燥結(jié)束點是凍干工藝中需要控制的關(guān)鍵��。Ten Have 等[40]利用線內(nèi)真空閥開閉頻率監(jiān)測卡介苗(BCG) 的中試和生產(chǎn)規(guī)模的凍干過程����,以確定生產(chǎn)規(guī)模初次干燥的終點��。Vam 等[41]開發(fā)了一種近紅外光譜方法在線監(jiān)測生物制藥的旋轉(zhuǎn)冷凍小瓶的干燥行為�����,這種方法可以使凍干過程可視化��,并可以確定初次和二次干燥的終點。
3.3在生物藥中的應(yīng)用
中成藥生產(chǎn)方式較為傳統(tǒng)�����,產(chǎn)品研發(fā)時對工藝?yán)斫獠蛔?�,?dǎo)致目前中藥質(zhì)量控制主要依靠生產(chǎn)經(jīng)驗和終產(chǎn)品檢測�����,缺乏調(diào)控方法����,不能有效應(yīng)對藥材質(zhì)量波動和工藝參數(shù)波動對產(chǎn)品質(zhì)量的影響。中藥制藥過程中間體和終產(chǎn)品大多成分復(fù)雜����。對于部分中藥品種,其制藥中間體和終產(chǎn)品缺乏物質(zhì)基礎(chǔ)及分析方法研究�����,無法明確影響PAT 實現(xiàn)的干擾因素����。
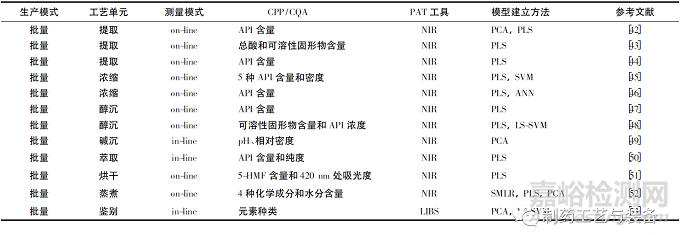
傳統(tǒng)的中成藥制藥過程包括提取��、濃縮����、水/醇沉��、過濾�����、配液等����。從藥材炮制到制藥過程��,再到終產(chǎn)品檢測����,PAT 均已在中成藥制藥過程監(jiān)測中發(fā)揮了重要作用,為增加過程了解和提高質(zhì)控水平提供了依據(jù)�����。PAT 在中成藥制藥過程監(jiān)測中的部分應(yīng)用見表2��。
表2 近10年P(guān)AT在中成藥生產(chǎn)中部分應(yīng)用實例文獻(xiàn)列表
提取過程是對傳統(tǒng)中藥制備過程中的一個重要步驟?����;钚猿煞痔崛∵^程的本質(zhì)是溶質(zhì)溶解在溶劑中的傳質(zhì)過程��。為了提高生產(chǎn)效率和確保最終產(chǎn)品的質(zhì)量��,采用快速��,可靠��,無損在線實時測量方法在中藥制藥中具有重要的價值�����。Gao等[42]利用水作為監(jiān)測中藥提取過程的探針����,NIR 用于在線監(jiān)測藥物提取過程,提出了一種利用水譜來了解整個提取過程并快速確定丹酚酸B( 中藥丹參的主要活性藥物成分) 含量的方法��。Yang 等[43]同樣用NIR 光譜技術(shù)����,在線監(jiān)測金銀花提取過程��。并建立了4 種不同的PLS 模型��,比較了它們在預(yù)測2個質(zhì)量參數(shù)( 總酸和可溶性固形物) 方面的性能�����。
濃縮過程是影響中成藥生產(chǎn)的必不可少的單元操作�����。濃縮過程的目的是除去存在于先前連接中間的溶劑(例如水�����,乙醇等) ����。傳統(tǒng)上�����,濃縮過程的終點是由濃縮物的密度決定的�����,濃縮物的密度可能無法反映活性成分含量的變化并無法準(zhǔn)確地判斷終點��。因此����,有必要確定有效成分的含量以監(jiān)測濃縮過程。例如��,NIR 光譜技術(shù)被Liu 等[45]用于在線監(jiān)測中藥靈芝靈口服液濃縮過程中的多個物理及化學(xué)參數(shù)�����。Xue等[46]采用相同的PAT 工具建立了葛根滲濾濃縮過程中葛根素的快速測定方法��,以高效液相色譜分析值為參考��,通過PLS 回歸和ANN 生成校正模型��。這些研究都證明了NIR 模型可用于濃縮過程中的在線質(zhì)量控制��。
水/醇沉是中藥生產(chǎn)中最常用的純化方法之一��。在此過程中��,去除了大量雜質(zhì),包括蛋白質(zhì)����,多糖,鹽�����,單寧和色素����。提取物的初始組成,乙醇的濃度�����,乙醇的體積和沉淀溫度����,所有這些變量都可能相互影響,并影響最終產(chǎn)品的質(zhì)量屬性�����。因此����,至關(guān)重要的是監(jiān)視和控制這些變量并了解它們的復(fù)雜關(guān)系,以最大程度地減少沉淀過程中批次間的差異��,從而確保一致的輸出����。Jin 等[48]研究了NIR 光譜在丹紅注射液生產(chǎn)過程中醇沉工藝在線定量監(jiān)測中的應(yīng)用。分析關(guān)鍵的中間質(zhì)量屬性: 可溶性固形物( SSC) 和丹參素的濃度( DSS) 等�����。而Li 等[49]以復(fù)方阿膠口服液的堿沉法為例�����,對線內(nèi)收集的NIR 光譜進(jìn)行多路主成分分析��。結(jié)果表明��,基于近紅外光譜的多變量工藝軌跡可以有效反映批次間的重現(xiàn)性��,也有助于中藥生產(chǎn)中故障批次的診斷�����。
從表2可以看出,在中藥制藥過程監(jiān)測中����,NIR 光譜技術(shù)是應(yīng)用最廣泛的PAT 工具,PLS 算法是使用最廣泛的建模方法����。除了以上介紹的幾個中成藥生產(chǎn)的重要步驟,PAT 工具在其他工藝過程中也有應(yīng)用�����。例如����,Xiong 等[50]以液-液萃取為典型實例,以探索線內(nèi)NIR 光譜結(jié)合多變量分析在中藥分批生產(chǎn)過程監(jiān)控中的潛力��。Li 等[51]以檳榔����,麥芽和山楂3 種中藥材的烘干過程為實例,使用NIR 建立了5-( 羥甲基)糠醛( 5-HMF) 含量和420 nm 吸光度的兩種模型�����,該模型對于在線分析和質(zhì)量控制具有魯棒性,準(zhǔn)確性和可重復(fù)性����。Zhou 等[52]探索了NIR 光譜技術(shù)用于在線監(jiān)測天麻根莖蒸制過程的潛在用途��,以確定在蒸煮過程中4 種化學(xué)成分和水分變化����。在上面的基礎(chǔ)上��,NIR 可以有效地實時監(jiān)視產(chǎn)品質(zhì)量�����,從而獲得最佳質(zhì)量的產(chǎn)品�����。
4��、結(jié)論及展望
隨著智能制造��、連續(xù)制造在制藥業(yè)的應(yīng)用日益廣泛�����,PAT的應(yīng)用也愈發(fā)廣泛。PAT 工具與化學(xué)計量學(xué)相結(jié)合��,可以成為強(qiáng)大的實時監(jiān)控系統(tǒng)��,并通過防止過程中的危險故障而提供安全的過程操作����。采用PAT 替代傳統(tǒng)的質(zhì)量控制實驗室檢測,不僅可以提高生產(chǎn)效率�����,降低質(zhì)量控制實驗室檢測費用�����,減少廢液的產(chǎn)生����,實現(xiàn)綠色生產(chǎn); 還可以提升產(chǎn)品批次間的一致性��。目前各國監(jiān)管機(jī)構(gòu)也都鼓勵制藥企業(yè)在生產(chǎn)過程中采用PAT��。
PAT 在國內(nèi)藥品生產(chǎn)領(lǐng)域的研究仍處于起始階段�����。我國醫(yī)藥生產(chǎn)長期以來采用傳統(tǒng)的生產(chǎn)方式��,大多數(shù)企業(yè)的制藥過程自動化程度不高��,控制方案簡單����,控制效果不盡人意��。許多制藥企業(yè)規(guī)模小�����、經(jīng)濟(jì)實力比較弱��,而實現(xiàn)PAT 的成本相對較高����。制藥行業(yè)更傾向于將資金投入新產(chǎn)品開發(fā)中,對于提高產(chǎn)品質(zhì)量����、節(jié)約成本的新技術(shù)投入認(rèn)識不足����。這是很多制藥企業(yè)的價值觀念����。但近幾年來隨著科學(xué)技術(shù)的不斷發(fā)展,國內(nèi)在藥物生產(chǎn)過程研究的PAT 也逐漸取得很大觀念突破����,明白生產(chǎn)質(zhì)量一致性與高效率的重要性。未來配合藥品監(jiān)管系統(tǒng)與法規(guī)對QbD /PAT 的逐漸認(rèn)可�����,PAT 將會成為藥品生產(chǎn)過程智能化監(jiān)測的必然方法�����。
參考文獻(xiàn)
[1] DZIKI W��,JIANG Z��,RADSPINNER D A����,et al. The FDA process analytical technology( PAT) initiative - an alternative pharmaceutical manufacturing practice( aPMP) [J]. Pharmacop Forum����,2004��,30( 6): 2254-2262.
[2] WANG P��,ZANG H C�����,ZENG Y Z. Causes and control of quality risks in drug production process[J]. Chin Pharm J (中國藥學(xué)雜志) ��,2011��,46( 13) : 969-972.
[3] CHEW W����,SHARRATT P. Trends in process analytical technology[J]. Anal Methods��,2010��,2( 10) : 1412-1438.
[4] LEE S L,O’CONNOR T F�����,YANG X C����,et al. Modernizing pharmaceutical manufacturing: from batch to continuous production[J]. J Pharm Innov,2015��,10( 3) : 191-199.
[5] KOMECKI M��,SCHMIDT A�����,STRUBE J. PAT as key-enabling technology for QbD in pharmaceutical manufacturing-A conceptual review on upstream and downstream processing[J]. Chim Oggi��,2018��,36( 6) : 44-48.
[6] SHENG P P�����,LUO S Q,YIN L H. Application of process analysis technology in pharmaceutical production process[J]. Chin J Pharm Anal ( 藥物分析雜志) �����,2018��,38( 5) : 748-757.
[7] KIM E J�����,KIM J H��,KIM M S��,et al. Process analytical technology tools for monitoring pharmaceutical unit pperations: a control strategy for continuous process verification[J]. Pharmaceutics����,2021�����,13( 6) : 919-967.
[8] ZHOU Z L. Quality control of traditional Chinese medicine using near infrared spectroscopy[D]. Guangzhou: South China University of Technology����,2017.
[9] NAGY B,F(xiàn)ARKAS A,BORBAS E����,et al. Raman spectroscopy for process analytical technologies of pharmaceutical secondary manufacturing[J]. AAPS Pharmscitech,2019�����,20( 1): 1-16.
[10] NICOLSON F����,JAMIESON L E,MABBOTT S����,et al. Through barrier detection of ethanol using handheld Raman spectroscopyconventional Raman versus spatially offset Raman spectroscopy(SORS) [J]. J Raman Spectrosc,2017��,48( 12) : 1828-1838.
[11] BUTTE P��,LAPCHAK P. Continuous laser induced fluorescence spectroscopy( CLIFS) technique for screening drugs by assessing the metabolic effects in real-time[J]. Neurology�����,2013�����,80( Suppl 7) : 65.
[12] WERNER P�����,MUNZBERG M����,HASS R,et al. Process analytical approaches for the coil-to-globule transition of poly( N-isopropylacrylamide)in a concentrated aqueous suspension[J]. Anal Bioanal Chem����,2017,409( 3) : 807-819.
[13] SHAH S K H��,IQBAL J����,AHMAD P,et al. Laser induced breakdown spectroscopy methods and applications: a comprehensive review[J]. Radiat Phys Chem��,2020��,170( 1) : 1-23.
[14] YAN X. Studies on the application of machine learning in pharmaceutical process analysis[D]. Hangzhou: Zhejiang University����,2020.
[15] BEATTIE J R,ESMONDE-WHITE F W L. Exploration of principal component analysis: deriving principal component analysis visually using spectra[J]. Appl Spectrosc��,2021��,75( 4) : 361-375.
[16] BIANCOLILLO A����,MARINI F. Chemometric methods for spectroscopybased pharmaceutical analysis[J]. Front Chem,2018����,6(1) : 1-14.
[17] ZHANG C,GUO Y�����,LI M. Review of development and application of artificial neural network models[J]. Comput Eng Appl( 計算機(jī)工程與應(yīng)用) �����,2021�����,57( 11) : 57-69.
[18] DONG Q,ZANG H C�����,LIU A H�����,et al. Application of process analysis technology in pharmaceutical field and its enlightenment to China's pharmaceutical industry[J]. Chin Pharm J ( 中國藥學(xué)雜志) ����,2010,45( 12) : 881-884.
[19] GUOVEIA F F����,RAHBEK J P,MORTENSEN A R��,et al. Using PAT to accelerate the transition to continuous API manufacturing[J]. Anal Bioanal Chem��,2017��,409( 3) : 821-832.
[20] LOREN B P��,WLEKLINSKI M�����,KOSWARA A�����,et al. Mass spectrometric directed system for the continuous-flow synthesis and purification of diphenhydramine[J]. Chem Sci����,2017,8 ( 6 ) :4363-4370.
[21] MITIC A�����,CEVERA-PADRELL A E�����,MORTENSEN A R�����,et al.Implementation of near-infrared spectroscopy for in-line monitoring of a dehydration reaction in a tubular laminar reactor[J]. Org Process Res Dev��,2016����,20( 2) : 395-402.
[22] MCDONALD M A�����,MARSHALL G D�����,BOMMARIUS A S�����,et al.Crystallization kinetics of cephalexin monohydrate in the presence of cephalexin precursors[J]. Cryst Growth Des����,2019�����,19 ( 9):5056-5074.
[23] TRAMPUZ M��,TESLIC D�����,LIKOZAR B,et al. Process analytical technology-based( PAT) model simulations of a combined cooling��,seeded and antisolvent crystallization of an active pharmaceutical ingredient ( API) [J]. Powder Technol�����,2020�����,366 ( 1 ) :873-890.
[24] ACEVEDO D�����,YANG X C��,MOHAMMAD A��,et al. Raman spectroscopy for monitoring the continuous crystallization of carbamazepine[J]. Org Process Res Dev��,2018����,22( 2) : 156-165.
[25] NAGY B����,F(xiàn)ARKAS A����,GYURKES M�����,et al. In-line Raman spectroscopic monitoring and feedback control of a continuous twinscrew pharmaceutical powder blending and tableting process[J].Int J Pharm�����,2017�����,530( 1-2) : 21-29.
[26] BOSTJIN N�����,DHONDT W�����,VERVAET C,et al. PAT-based batch statistical process control of a manufacturing process for a pharmaceutical ointment[J]. Eur J Pharm Sci�����,2019��,136( 1) : 1-9.
[27] BOSTJIN N��,HELLINGS M��,VAN DER VEEN M����,et al. In-line UV spectroscopy for the quantification of low-dose active ingredients during the manufacturing of pharmaceutical semi-solid and liquid formulations[J]. Anal Chim Acta�����,2018����,1013( 1) : 54-62.
[28] NETCHACOVITCH L,THIRY J�����,DE BLEYE C,et al. Global approach for the validation of an in-line Raman spectroscopic method to determine the API content in real-time during a hotmelt extrusion process[J]. Talanta��,2017����,171( 1) : 45-52.
[29] BOSTJIN N,VAN RENTERGHEM J��,VANBILLEMONT B�����,et al. Continuous manufacturing of a pharmaceutical cream: investigating continuous powder dispersing and residence time distribution(RTD) [J]. Eur J Pharm Sci����,2019,132( 1) : 106-117.
[30] SASAKURA D��,NAKAYAMA K�����,CHIKUMA T. Application of the quantitative detection of a change in concentration of magnesium stearate in a feeder tube of tableting manufacture by real-time near-infrared spectroscopy[J]. Pharmazie��,2015����,70 ( 10): 636-639.
[31] LEE H P�����,GULAK Y��,CUITINO A M. Transient temperature monitoring of pharmaceutical tablets during compaction using infrared thermography[J]. AAPS Pharmscitech��,2018����,19 ( 5 ) : 2426-2433.
[32] PAULI V��,ROGGO Y��,PELLEGATTI L�����,et al. Process analytical technology for continuous manufacturing tableting processing:A case study[J]. J Pharm Biomed Anal�����,2019��,162(1) : 101-111.
[33] NISHII T�����,MATSUZAKI K��,MORITA S. Real-time determination and visualization of two independent quantities during a manufacturing process of pharmaceutical tablets by near-infrared hyperspectral imaging combined with multivariate analysis[J]. Int J Pharm����,2020,590(1) : 1-7.
[34] NAIDU V R�����,DESHPANDE R S��,SYED M R����,et al. PAT-based control of fluid bed coating process using NIR spectroscopy to monitor the cellulose coating on pharmaceutical pellets[J]. AAPS Pharmscitech, 2017����,18(6) : 2045-2054.
[35] NAKANO Y,KATAKUSE Y��,AZECHI Y. An application of XRay fluorescence as process analytical technology( PAT) to monitor particle coating processes[J]. Chem Pharm Bull,2018��,66(6) : 596-601.
[36] SUN Z Y�����,LI C��,LI L�����,et al. Study on feasibility of determination of glucosamine content of fermentation process using a micro NIR spectrometer[J]. Spectrochim Acta Part A��,2018��,201( 1) : 153-160.
[37] EAMONDE-WHITE K A�����,CUELLAR M��,UERPMANN C��,et al.Raman spectroscopy as a process analytical technology for pharmaceutical manufacturing and bioprocessing [J]. Anal Bioanal Chem�����,2017�����,409(3) : 637-649.
[38] WEST J M��,F(xiàn)EROZ H��,XU X�����,et al. Process analytical technology for on-line monitoring of quality attributes during single-use ultrafiltration/diafiltration[J]. Biotechnol Bioeng�����,2021����,118(6):2293-2300.
[39] LOFGREN A,GOMIS-FONS J����,ANDERSSON N����,et al. An integrated continuous downstream process with real-time control: A case study with periodic countercurrent chromatography and continuous virus inactivation[J]. Biotechnol Bioeng��,2021�����,118(4) : 1664-1676.
[40] TEN HAVE R����,REUBSAET K,VAN HERPEN P�����,et al. Demonstrating functional equivalence of pilot and production scale freezedrying of BCG[J]. Plos One�����,2016����,11( 3) : 1-13.
[41] VAN BOCKSTAL P J����,DE MEYER L�����,CORVER J����,et al. Noncontact infrared-mediated heat transfer during continuous freezedrying of unit doses[J]. J Pharm Sci����,2017,106( 1) : 71-82.
[42] GAO L L��,ZHONG L����,ZHANG J,et al. Water as a probe to understand the traditional Chinese medicine extraction process with near infrared spectroscopy: A case of Danshen( Salvia miltiorrhizaBge)extraction process[J]. Spectrochim Acta Part A��,2021�����,244(1): 1-11.
[43] YANG Y��,WANG L,WU Y J�����,et al. On-line monitoring of extraction process of Flos Lonicerae Japonicae using near infrared spectroscopy combined with synergy interval PLS and genetic algorithm[J]. Spectrochim Acta Part A�����,2017�����,182( 1) : 73-80.
[44] LI Y�����,SHI X��,WU Z����,et al. Near-infrared for on-line determination of quality parameter of Sophora japonica L. ( formula particles): From lab investigation to pilot-scale extraction process[J].Pharmacogn Mag,2015��,11( 41) : 8-13.
[45] LIU R H,SUN Q F�����,HU T��,et al. Multi-parameters monitoring during traditional Chinese medicine concentration process with near infrared spectroscopy and chemometrics[J]. Spectrochim Acta Part A��,2018�����,192( 1) : 75-81.
[46] XUE J T�����,YANG Q W�����,JING Y����,et al. Rapid determination of puerarin by near-infrared spectroscopy during percolation and concentration process of puerariaelobatae radix[J]. Pharmacogn Mag��,2016,12( 47) : 188-192.
[47] WU Z S�����,XU B�����,DU M��,et al. Validation of a NIR quantification method for the determination of chlorogenic acid in Lonicera japonica solution in ethanol precipitation process[J]. J Pharm Biomed����,2012,62( 1) : 1-6.
[48] JIN Y��,WU Z Z����,LIU X S,et al. Near infrared spectroscopy in combination with chemometrics as a process analytical technology(PAT) tool for on-line quantitative monitoring of alcohol precipitation[J]. J Pharm Biomed�����,2013�����,77( 1) : 32-39.
[49] LI W L,HAN H F����,CHENG Z W��,et al. A feasibility research on the monitoring of traditional Chinese medicine production process using NIR-based multivariate process trajectories[J].Sensor Actuat B Chem����,2016,231( 1) : 313-323.
[50] XIONG H S�����,GONG X C��,QU H B. Monitoring batch-to-batch reproducibility of liquid-liquid extraction process using in-line near-infrared spectroscopy combined with multivariate analysis[J]. J Pharm Biomed��,2012����,70( 1) : 178-187.
[51] LI K Y,WANG W Y��,LIU Y P,et al. Near-infrared spectroscopy as a process analytical technology tool for monitoring the parching process of traditional Chinese medicine based on two kinds of chemical indicators[J]. Pharmacogn Mag����,2017,13( 50) : 332-337.
[52] ZHOU Y M��,YANG J����,LI C,et al. Near-infrared spectroscopy as a process analytical technology tool for monitoring the steaming process of gastrodiaerhizoma with multiparameters and chemometrics[J]. J Anal Methods Chem����,2020,2020( 1) : 1-12.
[53] LIU X N��,CHE X Q����,LI K Y,et al. Geographical authenticity evaluation of Mentha haplocalyx by LIBS coupled with multivariate analyzes[J]. Plasma Sci Technol����,2020,22( 7) : 1-7.
本文作者謝升谷�����、黃艷、孫逍�����、鄭金琪����、陶巧鳳��,浙江省食品藥品檢驗研究院����、國家藥品監(jiān)督管理局仿制藥評價關(guān)鍵技術(shù)重點實驗室、浙江省藥品接觸材料質(zhì)量控制研究重點實驗室��、浙江工業(yè)大學(xué)��。