MDSAP英文全稱是“Medical Device Single Audit Program”��,中文全稱是醫(yī)療器械單一審核程序��,是由國(guó)際醫(yī)療器械法規(guī)論壇(IMDRF)發(fā)起��,以ISO13485為基礎(chǔ)��,結(jié)合五個(gè)參與國(guó)(美國(guó)��、加拿大�、巴西��、澳大利亞和日本)的法規(guī)要求��,來實(shí)現(xiàn)各成員國(guó)對(duì)醫(yī)療器械生產(chǎn)企業(yè)質(zhì)量管理體系檢查結(jié)果的互認(rèn),以減少監(jiān)管機(jī)構(gòu)的重復(fù)檢查對(duì)有限檢查資源的浪費(fèi)和企業(yè)的負(fù)擔(dān)�。
目前,MDSAP的成員是:澳大利亞治療品管理局 TGA/巴西衛(wèi)生局 ANVISA/加拿大衛(wèi)生部 HC/日本厚生勞動(dòng)省以及醫(yī)藥醫(yī)療器械管理局 MHLW�、PMDA以及美國(guó)食藥品監(jiān)督管理局 FDA。此外歐盟/ 英國(guó)藥品和保健產(chǎn)品監(jiān)管局MHRA和世衛(wèi)組織也擔(dān)任官方觀察員��。
2. 實(shí)施MDSAP的目的和涉及的法規(guī)有哪些����?
2.1 實(shí)施MDSAP對(duì)制造商有以下好處:
對(duì)醫(yī)療器械制造商的質(zhì)量管理體系進(jìn)行適當(dāng)?shù)谋O(jiān)管監(jiān)督,同時(shí)最大限度地減少行業(yè)的監(jiān)管負(fù)擔(dān)����;
通過監(jiān)管機(jī)構(gòu)之間的工作共享和相互接受,在尊重每個(gè)機(jī)構(gòu)主權(quán)的同時(shí),促進(jìn)監(jiān)管資源的更高效和靈活使用��;
從長(zhǎng)遠(yuǎn)來看����,在全球范圍內(nèi),基于國(guó)際標(biāo)準(zhǔn)和最佳實(shí)踐,促進(jìn)監(jiān)管方法和技術(shù)要求的更大一致性;
通過標(biāo)準(zhǔn)化促進(jìn)監(jiān)管計(jì)劃的一致性,可預(yù)測(cè)性和透明度����;
參與監(jiān)管機(jī)構(gòu)監(jiān)督第三方審核機(jī)構(gòu)的做法和程序,以及參與第三方審核機(jī)構(gòu)的做法和程序。
2.2 MDSAP涉及的法規(guī)
Australia
Therapeutic Goods (Medical Devices) Regulations 2002 Schedule 3
Canada
Medical Device Regulations SOR/98-282
Brazil
RDC ANVISA n.665/2022
RDC ANVISA n.551/2021
RDC ANVISA n.67/2009
FDA
21 CFR Part 803
21 CFR Part 806
21 CFR Part 807
21 CFR Part 820
Japan
MHLW Ministerial Ordinance No.169
3. MDSAP怎么審��?誰(shuí)來審��?
3.1 審核流程
MDSAP的審核借鑒了FDA QSIT審核思路和模式����,將質(zhì)量管理體系分為七大流程,主要分為:
·管理(Management)
·器械批準(zhǔn)和工廠登記(Device marketing authorization and facility registration)
·測(cè)量�、分析和改進(jìn)(Measurement, analysis and improvement)
·不良事件報(bào)告和忠告性通知(Medical device adverse events and advisory notices reporting)
·設(shè)計(jì)開發(fā)(Design and development)
·生產(chǎn)和服務(wù)控制(Production and service controls)
·采購(gòu)(Purchasing)
每個(gè)流程包括不同的審核任務(wù)(Task)。其中管理流程��、測(cè)量分析改進(jìn)流程、設(shè)計(jì)開發(fā)流程和生產(chǎn)服務(wù)控制流程是主流程�,其它三個(gè)流程為支持性流程。
3.2 審核周期
MDSAP的審核周期和ISO 13485一樣��,也是3年一個(gè)循環(huán)�,包括初次的正式審核、正式審核之后的第一年和第二年為監(jiān)督審核����、第三年為再認(rèn)證審核��。初次的正式審核包括第一階段和第二階段����,第二階段會(huì)對(duì)醫(yī)療器械制造商的質(zhì)量管理體系(QMS)進(jìn)行完整的審核。和ISO13485不同的是審核時(shí)間的計(jì)算����,ISO 13485的審核以企業(yè)的員工人數(shù)計(jì)算人天,而MDSAP以審核的任務(wù)(Task)來計(jì)算人天����。申請(qǐng)企業(yè)因?yàn)樾枰獫M足的法規(guī)、產(chǎn)品��、體系的流程和任務(wù)不同��,人天會(huì)有差異。
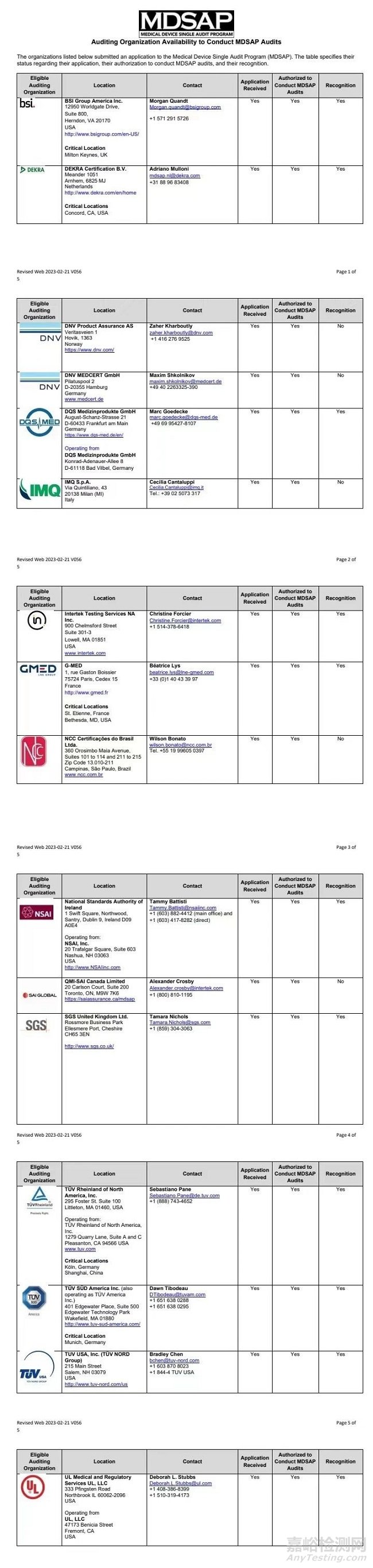
3.3 審核機(jī)構(gòu)
和CE-MDR/IVDR認(rèn)證類似��,五個(gè)參與國(guó)按照流程認(rèn)可了一些審核機(jī)構(gòu)(AO)的資格����,由AO機(jī)構(gòu)來進(jìn)行審核。截至目前��,已有以下幾家第三方機(jī)構(gòu)獲得資質(zhì)�,F(xiàn)DA官網(wǎng)7月份的最新信息哈,大家可以看看��,可以參考下問問這些中國(guó)區(qū)第三方機(jī)構(gòu)的sales
3.4 MDSAP必須申請(qǐng)5個(gè)國(guó)家嗎�?
MDSAP認(rèn)證的法規(guī)的選擇可以根據(jù)目標(biāo)市場(chǎng)而確定,如果已經(jīng)在該國(guó)市場(chǎng)銷售了醫(yī)療器械產(chǎn)品�,就應(yīng)該在MDSAP的認(rèn)證中包括該國(guó)適用的法規(guī)要求,如果沒有在該國(guó)銷售產(chǎn)品��,制造商可以根據(jù)自身的情況確定是否要包括該國(guó)的法規(guī)要求�。初次認(rèn)證審核沒有包括的國(guó)家和法規(guī),可以再后續(xù)的審核中進(jìn)行擴(kuò)證��。