摘要
目的 篩選碳酸司維拉姆分散片的最優(yōu)處方��,制備成分散片��,解決該藥品普通片造成患者吞咽困難以及食道異常等方面的問題����。
方法 根據(jù)輔料特性選擇交聯(lián)聚乙烯吡咯烷酮(crosslinked polyvinylpyrrolidone,PVPP)為崩解劑����,微晶纖維素為賦形劑,聚維酮K-30 為黏合劑�,硬脂酸鎂為潤滑劑,阿斯巴甜和檸檬香精為矯味劑的分散片處方����;通過DOE 設計對處方進行篩選,以分散均勻性和溶出度作為指標考察����。
結果 篩選得到原料粒徑(D90)為15.0 μm,PVPP 占比45.0%�,硬脂酸鎂占比0.6%組成最優(yōu)處方。結論 研制的碳酸司維拉姆分散片處方合理����、工藝可行,藥品符合質(zhì)量標準要求��。
關鍵詞
碳酸司維拉姆;分散片��;DOE 設計����;處方工藝
碳酸司維拉姆是一種適用于正在接受透析治療的慢性腎臟病[1-2]成人患者高磷血癥的新型藥物。目前該藥物在市場上主要為普通片��,規(guī)格為每片0.8 g�,根據(jù)說明書中記載因其單片規(guī)格大和藥物本身吸附作用的特性,易造成患者吞咽困難�、吞咽障礙、重度胃腸功能紊亂�,以及對胃輕癱、胃內(nèi)容物滯留或腸道運動異常的患者造成不良影響����。為解決原有劑型給患者造成的不良反應��,并結合碳酸司維拉姆幾乎不溶于水��、不溶于酸堿和有機溶劑[3]的特點����,特將其設計制成分散片[4],利用分散片服用前遇水形成混懸液方便患者服用,可解決患者吞咽困難��、食道藥片滯留的問題����,而且混懸液更易通過胃腸道,可解決普通片在胃中膨脹滯留��、造成腸梗阻等方面的問題����。
1、儀器與試劑
1.1 儀器
HLSG50 濕法混合制粒機(明天機械)��;Pilotlab LBosch 流化床[博世包裝技術(杭州)有限公司]��;SYH120L 三維混合機(南京健牌干燥設備廠)�;ZPT-26 旋轉式壓片機(北京翰林科技有限公司);FM-29-01 電子天平(上海精科天平廠)�;CJY-300B片劑脆碎度測定儀(上海黃海藥檢儀器有限公司);SNTR-8400A 型智能藥物溶出儀(島津科技) �;TBH125 型片劑硬度測試儀(德國ERWEKA);Agilent1260 高效液相色譜儀(美國Agilent)��。
1.2 藥品與試劑
碳酸司維拉姆(浙江金華康恩貝生物制藥有限公司�,批號:180604)�;碳酸司維拉姆對照品[高拓耀業(yè)(北京)科技有限公司�,批號:1803002;純度:98.6%]��;聚維酮K30(湖州展望藥業(yè)有限公司�,批號:20180101);交聯(lián)聚乙烯吡咯烷酮(crosslinkedpolyvinylpyrrolidone��,PVPP����,美國國際特品公司肯塔基州工廠,批號:0002127497)�;微晶纖維素(microcrystalline cellulose,MCC����,湖州展望藥業(yè)有限公司,批號:20180346)��;阿斯巴甜(湖南爾康制藥股份有限公司��,批號:103420180701)����;檸檬香精(上海德欣香料有限公司,批號:20180912-1)��;硬脂酸鎂( 湖州展望藥業(yè)有限公司����, 批號:20180514)。
內(nèi)容由凡默谷小編查閱文獻選取�,排版與編輯為原創(chuàng)。如轉載��,請尊重勞動成果�,注明來源于凡默谷公眾號。
2�、碳酸司維拉姆分散片工藝
本次處方工藝篩選遵循QbD 理念[5-6],試驗分散片的制備規(guī)格與市售碳酸司維拉姆普通片規(guī)格(每片0.8 g)一致�,藥品制成片重為每片1.7~1.9 g。處方暫定為碳酸司維拉姆��、MCC��、PVPP��、阿斯巴甜����、檸檬香精��、硬脂酸鎂和聚維酮K30 乙醇溶液��。
2.1 輔料選擇
2.1.1 賦形劑的選擇
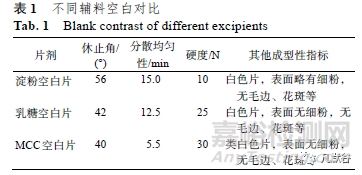
片劑常用的賦形劑有乳糖�、淀粉及MCC����。選用10%聚維酮做黏合劑,試制上述輔料的空白片��,控制片重統(tǒng)一為1.8 g 左右�,考察各輔料空白片的成型性指標,最終結合碳酸司維拉姆原料的性質(zhì)����,選用MCC 作為賦形劑,檢測結果見表1�。
2.1.2 黏合劑濃度的選擇
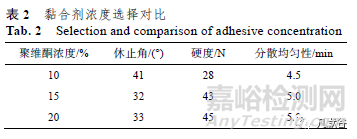
分散片常采用聚維酮作為黏合劑,采用聚維酮制成的顆粒�,表面具親水性,壓片后水分易潤濕��、滲入��,片劑易崩解�,有利于藥物的溶出。黏合劑濃度選擇10%�,15%,20%����,按“2.1.1”項下MCC 空白片處方進行制粒,對制得顆粒以及片劑的硬度進行休止角和分散均勻性檢測����,結果見表2。10%濃度制得的顆粒與后兩者制得的顆粒休止角�、硬度差異較大,15%與20%濃度制得的顆粒差異不大����;在分散均勻性方面3 個濃度制得的顆粒差異不大,因此采用15%聚維酮乙醇溶液作為黏合劑�。
2.1.3 崩解劑的選擇
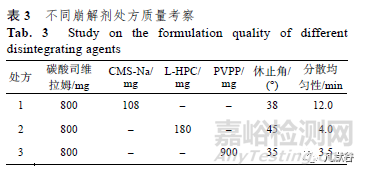
分散片常用崩解劑[7]有羧甲基淀粉鈉(carboxymethyl starch sodium ,CMS-Na) ����、低取代羥丙纖維素(low-substitutedhydroxypropyl cellulose , L-HPC) ��、PVPP 等����。CMS-Na 推薦用量為3%~6%����,L-HPC 推薦用量為2%~10%����,PVPP 推薦用量5%~50%。按“2.1.1”項下MCC 空白片處方試驗��,采用15%聚維酮乙醇溶液作黏合劑��,選用上述崩解劑進行制粒壓片����,控制片重為1.8 g 左右。崩解劑用量為各自適宜的最大用量:CMS-Na 6%����,L-HPC 10%,PVPP 50%����,測得相關指標結果見表3,從處方選擇確定選用PVPP 作為崩解劑。
2.1.4 潤滑劑的選擇
常用潤滑劑為滑石粉[8]和硬脂酸鎂�,滑石粉為一種親水性潤滑劑,比重大����、不易黏附��、易分層�。硬脂酸鎂[9]黏附性能強、潤滑性好����,在片劑中應用比較廣泛,常用量為0.5%~2%����,本試驗處方選用硬脂酸鎂作為潤滑劑。
2.1.5 矯味劑的選擇
分散片口感不良�,為使得水中分散后服用時口感好,考慮添加適當?shù)某C味劑�。試驗選用甜度大、口味清爽��、穩(wěn)定性好的甜味劑阿斯巴甜��,同時添加香味較能被大眾接受的檸檬香精作為矯味劑。
2.2 DOE 設計
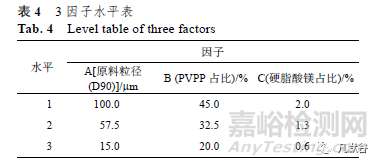
經(jīng)過上述輔料確定以及結合分散片的特點,確定3 因子:原料粒徑(A)��、PVPP 占比(B)以及硬脂酸鎂占比(C)對產(chǎn)品溶出度�、分散均勻性影響較大����。通過Minitab 軟件中“DOE 設計”對“3 因子3 個中心點重復方法”進行選擇,3 因子水平見表4��,11 組試驗結果見表5����。
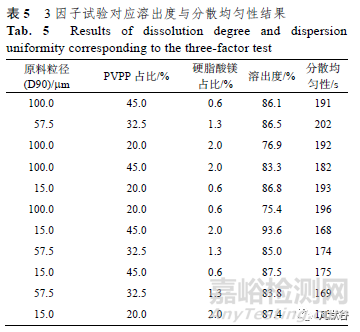
通過軟件進行分析, 得出原料粒徑(D90)15.0 μm����、PVPP 占比45.0%與產(chǎn)品的溶出度關系顯著,與硬脂酸鎂占比關系不顯著��;且所有產(chǎn)品分散均勻性結果在168~202 s����,無顯著差異����;經(jīng)評估硬脂酸鎂用量選擇占比0.6%��。根據(jù)Minitab 軟件中“響應優(yōu)化器”功能得到三因子在原料粒徑(D90)15 μm�、PVPP 占比45%��、硬脂酸鎂占比0.6%水平條件下����,溶出度擬合值91%,95%置信區(qū)間在88.91%~95.00%��,表明該處方組合為最優(yōu)��。
2.3 最優(yōu)處方驗證
根據(jù)“2.2”項下得到的組合進行平行試驗3次�,測得溶出度分別為92%,93%��,91%��,平均值為92%;分散均勻性分別為162�,168,163 s����,基本與DOE 試驗持平,表明該處方組合為最優(yōu)處方組合�。
3、碳酸司維拉姆分散片工藝研究
經(jīng)最優(yōu)處方確認分散均勻性結果在3 min 邊緣��,接近標準規(guī)定:3 min 內(nèi)應全部崩解并通過篩網(wǎng)�。需對原處方工藝進行優(yōu)化,縮短分散均勻性����。
3.1 崩解劑內(nèi)外加比例的選擇
PVPP 作為強效崩解劑,內(nèi)加����、外加比例影響分散均勻性時間。取原處方PVPP 20%和40%外加分別進行試驗�,測得分散均勻性結果:20%外加分散均勻性為126,119�,124 s;40%外加分散均勻性為117�,121��,120 s�。取部分PVPP 外加后����,分散均勻性明顯縮短,但20%和40%差異不顯著��,選擇20%作為外加比例����。
3.2 最優(yōu)處方工藝驗證
根據(jù)“3.1”項下得到最優(yōu)處方工藝平行試驗3 次,分散均勻性分別為123�,127����,116 s,平均值為122 s��,基本與“3.1”項試驗持平��,表明該比例適用��。
4�、碳酸司維拉姆分散片的制備
4.1 分散片處方
通過上述試驗得該分散片最優(yōu)處方每片含:碳酸司維拉姆800 mg��、MCC 154 mg��、阿斯巴甜9.8 mg�、檸檬香精11 mg、PVPP 833 mg����、聚維酮K-30 30.2 mg、硬脂酸鎂11 mg��。
4.2 分散片制備
按“4.1”項下處方制備3 批碳酸司維拉姆分散片�,將處方量的碳酸司維拉姆、MCC��、阿司巴甜����、PVPP(內(nèi)加),混合均勻��,加入15%聚維酮K-30乙醇溶液����,制軟材����,過12 目篩�,設定干燥溫度85 ℃,干燥30 min����,過16 目篩整粒。將制好的顆粒與檸檬香精�、PVPP(外加)以及處方量的潤滑劑硬脂酸鎂混合后壓片, 控制片子的硬度在40~70 N��。
5����、碳酸司維拉姆分散片的質(zhì)量評價
5.1 溶出度檢測方法
本品溶出度檢測方法采用中國藥典第二法漿法,轉速為75 r×min?1��、以pH 6.8 磷酸鹽緩沖液(取0.5 g 十二烷基硫酸鈉����、2.4 g 磷酸二氫鈉和0.3 g氫氧化鈉�,加1 L 水溶解)1 L 為溶出介質(zhì)、溶出液溫度37 ℃��。經(jīng)30 min 時取樣;取碳酸司維拉姆對照品用緩沖液溶解����,進行HPLC 檢測,按外標法以峰面積計算每片的溶出量����。檢測條件:色譜柱十八烷基硅烷鍵合硅膠(55 mm× 4.0 mm,3 μm)��;流動相乙腈∶水=40∶60�;流速1.0 mL·mL?1;等度洗脫�;進樣量10 μL;檢測波長250 nm����;柱溫40 ℃;樣品溫度N/A�;運行時間10 min。
5.2 檢測結果
3 批樣品檢測結果分別為溶出度95%����,93%,96%��,硬度47,63��,59 N��,分散均勻性120�,127,116 s����,結果符合質(zhì)量標準。
6��、討 論
由于碳酸司維拉姆幾乎不溶于水����,將其制成分散片原料粒徑對溶出度影響極為重要,本試驗重點對粒徑選擇進行研究����,須將粒徑控制在合理范圍內(nèi),才能保證產(chǎn)品的溶出度>90%��。黏合劑制備宜選用乙醇而非水作為溶劑�,乙醇作為溶劑制得的顆粒較為松散�,能達到快速崩解的目的��,符合分散片的要求����。矯味劑選用阿斯巴甜����,因其口感好、其甜度比蔗糖高150~200 倍�,且無后苦味,不易導致齲齒��,還可有效降低熱量��,較適用于糖尿病和肥胖癥患者[10]��。本試驗制得的產(chǎn)品服用方便����,并能有效解決碳酸司維拉姆普通片造成的患者吞咽困難以及胃腸道等方面問題,具有良好的市場開發(fā)前景����。