今日頭條
盟科抗菌藥上糖尿病足感染III期臨床�����。上海盟科藥業(yè)自主研發(fā)的抗革蘭氏陽(yáng)性耐藥菌新藥注射用MRX-4序貫口服康替唑胺片治療糖尿病足感染的國(guó)際Ⅲ期臨床中國(guó)部分在四川大學(xué)華西醫(yī)院入組首例受試者�����。中國(guó)各分中心由四川大學(xué)華西醫(yī)院糖尿病足診治中心主任冉興無教授牽頭�����,擔(dān)任主要研究者。早在2022年�����,盟科藥業(yè)已正式開啟全球Ⅲ期臨床的入組工作�����,計(jì)劃在中國(guó)�����、美國(guó)和歐洲同步開展臨床研究�����。
國(guó)內(nèi)藥訊
1.博瑞GLP-1R/GIPR激動(dòng)劑獲批II期臨床�����。博瑞醫(yī)藥GLP-1R/GIPR激動(dòng)劑BGM0504用于治療2型糖尿病和肥胖的II期臨床研究方案通過牽頭醫(yī)院中南大學(xué)湘雅三醫(yī)院倫理委員會(huì)批準(zhǔn)�����。在Ia期臨床中�����,BGM0504能夠劑量依賴性降低受試者體重,受試者平均體重較基線降幅為3.24%~8.30%�����;在2.5-15mg劑量遞增范圍內(nèi)�����,所有不良反應(yīng)均為1~2級(jí)�����,未觀察到3級(jí)及以上不良反應(yīng)�����。
2.南京諾惟溶瘤病毒獲批實(shí)體瘤臨床�����。南京諾惟生物1類生物制品“重組NV-A01腺病毒注射液”獲國(guó)家藥監(jiān)局臨床試驗(yàn)?zāi)驹S可�����,擬開展針對(duì)晚期惡性實(shí)體瘤的臨床試驗(yàn)�����。諾惟生物依托南京大學(xué)醫(yī)學(xué)院�����,已完成重組溶瘤腺病毒和痘苗病毒等多個(gè)開發(fā)平臺(tái)建設(shè)�����。NV-A01腺病毒旨在改善治理腫瘤微環(huán)境�����,在控制腫瘤侵襲轉(zhuǎn)移的同時(shí)�����,重建免疫監(jiān)控�����,最大程度的保證患者的安全�����,延長(zhǎng)生存時(shí)間。
3.邦耀新一代通用型CAR-T獲批臨床�����。上海邦耀生物1類生物制品“靶向CD19基因修飾的異體嵌合抗原受體T細(xì)胞注射液”(BRL-301)獲國(guó)家藥監(jiān)局臨床批準(zhǔn)�����,擬用于治療18-70周歲�����、復(fù)發(fā)或難治性B細(xì)胞急性淋巴細(xì)胞白血病患者�����。這是邦耀生物專有通用型細(xì)胞平臺(tái)(TyUCell®)開發(fā)的全新一代UCAR-T產(chǎn)品�����,能有效避免異體細(xì)胞移植中可能存在的移植物抗宿主?����。℅VHD)風(fēng)險(xiǎn)�����,針對(duì)的適應(yīng)癥分別為B細(xì)胞惡性腫瘤�����、自身免疫系統(tǒng)疾病�����。
4.默沙東CYP11A1抑制劑中國(guó)報(bào)IND�����。默沙東與Orion公司合作開發(fā)的1類化藥MK-5684片(ODM-208)臨床試驗(yàn)申請(qǐng)獲CDE受理�����。ODM-208是一款口服非類固醇CYP11A1抑制劑�����,旨在通過抑制CYP11A1酶的活性,抑制所有類固醇激素和可能激活雄激素受體(AR)信號(hào)通路的激素前體的產(chǎn)生�����。目前�����,ODM-208正在Ⅱ期臨床中評(píng)估用于治療轉(zhuǎn)移性去勢(shì)抵抗性前列腺癌(mCRPC)的潛力�����。
5.江蘇瑞科帶狀皰疹疫苗國(guó)內(nèi)報(bào)IND�����。江蘇瑞科生物3.3類生物制品“重組帶狀皰疹疫苗(CHO細(xì)胞)”(REC610)的臨床試驗(yàn)申請(qǐng)獲CDE受理�����。這是一項(xiàng)I期臨床�����,擬在國(guó)內(nèi)招募180例40歲及以上健康受試者評(píng)估REC610的安全性�����、耐受性和免疫原性�����,Shingrix®(葛蘭素史克)為陽(yáng)性對(duì)照藥物�����。今年2月�����,該疫苗已在菲律賓開展首次人體試驗(yàn)�����,目前所有受試者已完成兩劑疫苗接種后30天隨訪�����,藥物總體耐受性良好�����。
6.宜明昂科CD24單抗報(bào)IND。宜明昂科1類生物制品IMM47注射液的臨床試驗(yàn)申請(qǐng)獲CDE受理�����。IMM47是一款人源化IgG1 CD24單克隆抗體�����,能夠阻斷從CD24/Siglec-10通路傳遞至巨噬細(xì)胞�����、自然殺傷細(xì)胞(NK)和T細(xì)胞的免疫抑制信號(hào)�����。在臨床前研究中�����,IMM47單藥或者與免疫檢查點(diǎn)藥物聯(lián)用均顯示出強(qiáng)大的抗腫瘤療效�����。國(guó)內(nèi)同靶點(diǎn)藥物開發(fā)還包括德琪醫(yī)藥�����、百奧賽圖和昂科免疫。
國(guó)際藥訊
1.依庫(kù)珠單抗治療兒童重癥肌無力新適應(yīng)癥獲歐盟批準(zhǔn)�����。阿斯利康補(bǔ)體C5抑制劑依庫(kù)珠單抗(Soliris)獲歐盟(EU)批準(zhǔn)擴(kuò)大應(yīng)用范圍�����,可用于治療抗乙酰膽堿受體(AChR)抗體陽(yáng)性(Ab+)的6歲-17歲兒童和青少年的難治性全身性肌無力(gMG)�����。依庫(kù)珠單抗通過抑制補(bǔ)體級(jí)聯(lián)反應(yīng)終端的C5蛋白�����,降低炎癥反應(yīng)�����。2017年�����,依庫(kù)珠單抗已在歐盟獲批用于治療成人gMG�����。
2.艾伯維IL-23單抗銀屑?����、羝谂R床積極�����。艾伯維IL-23抑制劑Skyrizi(risankizumab)治療中度斑塊狀銀屑病的Ⅳ期臨床IMMpulse積極結(jié)果發(fā)布于British Journal of Dermatology期刊上�����。與阿普米司特相比�����,Skyrizi治療組第16周時(shí)達(dá)到銀屑病面積與嚴(yán)重程度指數(shù)改善至少90%的患者比例更高(55.9%vs5.1%�����,P<0.001)�����,達(dá)到靜態(tài)醫(yī)生總體評(píng)估(sPGA)0/1的比例更高(75.4%vs18.4%)。該項(xiàng)研究達(dá)到主要和次要終點(diǎn)�����,未發(fā)現(xiàn)新的安全信號(hào)�����。
3.默沙東個(gè)體化癌癥疫苗上III期臨床�����。默沙東與Moderna開發(fā)的癌癥疫苗mRNA-4157 (V940)聯(lián)合PD-1抑制劑Keytruda一線治療經(jīng)手術(shù)切除高風(fēng)險(xiǎn)黑色素瘤(IIB-IV期)患者的Ⅲ期臨床(V940-001)首批患者目前正在澳大利亞入組�����。mRNA-4157是包含編碼最多34種新抗原的單一合成mRNA分子�����,該疫苗是根據(jù)每例患者獨(dú)特腫瘤突變通過算法設(shè)計(jì)而成�����。在IIb期臨床中�����,mRNA-4157聯(lián)合輔助治療較Keytruda使腫瘤產(chǎn)生遠(yuǎn)處轉(zhuǎn)移或死亡的風(fēng)險(xiǎn)降低65%�����。
4.FIC腸-腦軸口服療法AD早期臨床積極�����。Viage Therapeutics公司擬開發(fā)用于改善阿爾茨海默病或帕金森病導(dǎo)致輕中度認(rèn)知障礙的靶向腸-腦軸AVPR1A受體的潛在“first-in-class”口服療法DGX-001�����,在健康志愿者中開展的Ⅰ期臨床獲積極結(jié)果�����。DGX-001旨在通過與腸道內(nèi)分泌細(xì)胞上的特異性受體相互作用來調(diào)節(jié)迷走神經(jīng)�����,從而調(diào)節(jié)腦細(xì)胞活性�����。結(jié)果顯示DGX-001具有良好的安全性和耐受性;定量腦電圖(qEEG)測(cè)量的腦活動(dòng)變化也顯示DGX-001具有改善認(rèn)知和執(zhí)行功能的潛力�����。
5.不可成藥靶點(diǎn)藥物研發(fā)公司完成A輪融資�����。Nexo公司宣布完成6000萬美元A輪融資�����,以用于支持其CODON(共價(jià)發(fā)現(xiàn)和優(yōu)化平臺(tái))技術(shù)平臺(tái)�����,針對(duì)不可成藥靶點(diǎn)開發(fā)創(chuàng)新癌癥療法管線�����。CODON結(jié)合一個(gè)專有的文庫(kù)�����,并利用化學(xué)多樣性和創(chuàng)新的共價(jià)化學(xué)與可擴(kuò)展的生物化學(xué)和細(xì)胞內(nèi)蛋白組學(xué)�����,旨在識(shí)別有希望的苗頭化合物并進(jìn)行快速優(yōu)化以生產(chǎn)用于體內(nèi)研究的化合物�����。此前�����,Nexo公司已與MD安德森癌癥中心達(dá)成合作�����,針對(duì)不可成藥靶點(diǎn)開發(fā)創(chuàng)新小分子療法�����。
6.渤健2023年Q2營(yíng)收24.56億美元�����。Biogen發(fā)布2023第二季度業(yè)績(jī)報(bào)告,總營(yíng)收24.56億美元�����,同比下降5%�����,凈利潤(rùn)為9.81億美元�����,同比下滑23.2%�����,研發(fā)投入11.55億美元�����,同比增長(zhǎng)6.9%�����。其中用于治療脊髓性肌萎縮癥的ASO藥物Spinraza2023年Q2營(yíng)收4.37億美元�����,同比增長(zhǎng)1.4%�����;2023H1營(yíng)收8.8億美元�����,同比下降2.6%�����。據(jù)美國(guó)國(guó)家生物信息中心官網(wǎng)顯示�����,Spinraza每次注射為11.8萬美元�����。
醫(yī)藥熱點(diǎn)
1.北京積水潭醫(yī)院健康管理中心啟用�����。7月25日,北京積水潭醫(yī)院健康管理中心在新龍澤院區(qū)正式啟用�����。該中心以綜合三甲醫(yī)院的醫(yī)療資源為依托�����,打造“體檢+健康管理”為一體的高質(zhì)量健康管理中心�����。中心所有醫(yī)護(hù)來源于臨床各崗位�����,其中檢驗(yàn)�����、影像等操作均由本院在職或退休醫(yī)生完成�����,且與臨床檢查在同一個(gè)實(shí)驗(yàn)室完成�����,保證了體檢的質(zhì)量與準(zhǔn)確性�����。體檢報(bào)告可實(shí)現(xiàn)三甲醫(yī)院互認(rèn)�����,解決了受檢者需要到臨床就診進(jìn)行二次復(fù)查帶來的麻煩�����。
2.國(guó)家疾控局印發(fā)猴痘防控方案�����。為進(jìn)一步做好猴痘防控工作�����,及時(shí)有效應(yīng)對(duì)猴痘疫情�����,提升猴痘防控工作的科學(xué)性、精準(zhǔn)性和有效性�����,切實(shí)維護(hù)人民群眾生命安全和身體健康�����,國(guó)家疾控局會(huì)同國(guó)家衛(wèi)生健康委制定了《猴痘防控方案》�����。該方案要求�����,各級(jí)各類醫(yī)療機(jī)構(gòu)開展猴痘樣癥狀監(jiān)測(cè)�����,對(duì)猴痘密切接觸者實(shí)施21天自我健康監(jiān)測(cè)�����。
3.海吉亞醫(yī)療公告收購(gòu)西安長(zhǎng)安醫(yī)院�����。7月25日�����,海吉亞醫(yī)療公告收購(gòu)西安長(zhǎng)安醫(yī)院100%股權(quán)�����,合計(jì)人民幣16.6億元�����。長(zhǎng)安醫(yī)院是一家有著二十多年運(yùn)營(yíng)經(jīng)驗(yàn)積淀的三級(jí)甲等綜合醫(yī)院�����,注冊(cè)床位1,000張�����,醫(yī)院擁有一支經(jīng)驗(yàn)豐富�����、技術(shù)精湛的醫(yī)療團(tuán)隊(duì),2022年獲評(píng)艾力彼社會(huì)辦醫(yī)單體醫(yī)院100強(qiáng)第13名�����。收購(gòu)事項(xiàng)將進(jìn)一步擴(kuò)展海吉亞醫(yī)療集團(tuán)的腫瘤醫(yī)療服務(wù)網(wǎng)絡(luò)�����,為該集團(tuán)在西北地區(qū)進(jìn)一步擴(kuò)張并建立三級(jí)診療網(wǎng)絡(luò)打下堅(jiān)實(shí)基礎(chǔ)�����。
評(píng)審動(dòng)態(tài)
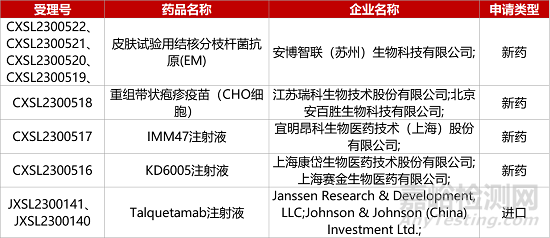
1. CDE新藥受理情況(07月27日)
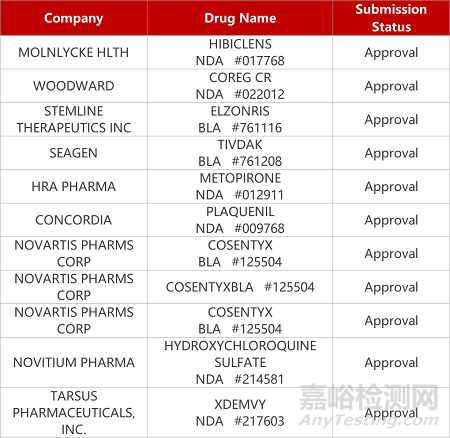
2. FDA新藥獲批情況(北美07月26日)