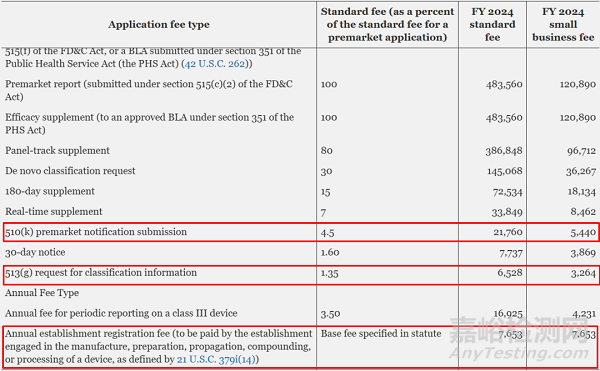
當(dāng)?shù)貢r(shí)間2023年7月28日���,F(xiàn)DA公布了2024財(cái)年醫(yī)療器械使用費(fèi)的收費(fèi)標(biāo)準(zhǔn)�,2024財(cái)年的收費(fèi)標(biāo)準(zhǔn)適用于2023年10月1日至2024年9月30日�。
與2023財(cái)年相比,2024財(cái)年的各項(xiàng)醫(yī)療器械使用費(fèi)大都有所增長(zhǎng)�,如2024年度場(chǎng)地注冊(cè)費(fèi)為$7653,較去年上漲了$1160���;小型企業(yè)減免后的FDA 510(k)注冊(cè)費(fèi)用也從去年的$4967增長(zhǎng)至$5440���。
小型企業(yè)優(yōu)惠政策
豁免:獲得批準(zhǔn)的小型企業(yè)決定(SBD)且總收入或銷售額為3000萬(wàn)美元或以下的小型企業(yè)有資格在其首次上市前批準(zhǔn)申請(qǐng)(PMA),產(chǎn)品開(kāi)發(fā)協(xié)議(PDP)�,上市前報(bào)告(PMR)或生物制劑許可證申請(qǐng)(BLA)中免除費(fèi)用。
如果您想申請(qǐng)支付小型企業(yè)費(fèi)率���,或者獲得首次上市前申請(qǐng)或上市前通知的費(fèi)用豁免�����,您應(yīng)在向FDA提交材料前的至少60天前提交小型企業(yè)認(rèn)證請(qǐng)求和證明您有資格成為小型企業(yè)的證明材料�����。
如果您的企業(yè)符合2023財(cái)年的小型企業(yè)資格�����,您的小型企業(yè)資格將在2023年9月30日到期�����。您必須重新獲得2024財(cái)年的小型企業(yè)資格�,才能在2024財(cái)年支付小型企業(yè)費(fèi)用�����。
值得注意的是���,所有企業(yè)機(jī)構(gòu)必須支付場(chǎng)地注冊(cè)費(fèi)���,對(duì)于小微企業(yè)或團(tuán)體�����,沒(méi)有豁免或減少�����。