2016年03月國家藥品監(jiān)督管理局藥品審評中心發(fā)布的《以藥動學(xué)參數(shù)為終點評價指標(biāo)的化學(xué)藥物仿制藥人體生物等效性研究技術(shù)指導(dǎo)原則》指導(dǎo)原則指出“調(diào)釋制劑若以下條件全部滿足�����,則可以認(rèn)為調(diào)釋制劑的其他規(guī)格與相應(yīng)規(guī)格的參比制劑具有生物等效性:1)其他規(guī)格制劑的活性和非活性組分組成比例與試驗規(guī)格的受試制劑相似�����;2)其他規(guī)格制劑的釋藥原理與試驗規(guī)格的受試制劑相同��;3)各規(guī)格制劑體外溶出試驗結(jié)果相似�����。建議至少在3種不同pH溶媒(例如pH1.2��,4.5和6.8)中通過f2值判斷其他規(guī)格的溶出曲線與生物等效性研究中受試制劑溶出曲線的相似性��。”而本指導(dǎo)原則中指出的“其他規(guī)格制劑的活性和非活性組分組成比例與試驗規(guī)格的受試制劑相似”在2022年02月國家藥品監(jiān)督管理局藥品審評中心發(fā)布的《對我國《以藥動學(xué)參數(shù)為終點評價指標(biāo)的化學(xué)藥物仿制藥人體生物等效性研究技術(shù)指導(dǎo)原則》中關(guān)于多規(guī)格豁免BE藥學(xué)評價標(biāo)準(zhǔn)“處方比例相似性”相關(guān)問題的問答(試行)》中有明確的解答��。
對我國《以藥動學(xué)參數(shù)為終點評價指標(biāo)的化學(xué)藥物仿制藥人體生物等效性研究技術(shù)指導(dǎo)原則》中關(guān)于多規(guī)格豁免BE藥學(xué)評價標(biāo)準(zhǔn)“處方比例相似性”相關(guān)問題的問答(試行)中指出“對于調(diào)釋制劑:“組成比例相似”包括以下情況:①不同規(guī)格之間所有非活性成分與活性成份的比例完全相同�����;②不同規(guī)格之間非活性成分與活性成分的比例不完全相同����,如申請人申請豁免,應(yīng)證明比例是合理的��,且與產(chǎn)品的藥物釋放機制相適應(yīng)��。審評期間基于整體資料進(jìn)行綜合評估�����。”說明對于調(diào)釋制劑,如果大規(guī)格制劑已通過BE試驗�����,而小規(guī)格制劑想要豁免BE����,則必須滿足上述的三點要求,其中一點是必須滿足不同規(guī)格之間所有非活性成分與活性成份的比例完全相同����。
我們在做藥品多規(guī)格膜控型調(diào)釋制劑研發(fā)時常常遇到這樣的問題,大規(guī)格制劑已通過BE試驗�����,新增小規(guī)格制劑可申請BE豁免��,小規(guī)格制劑的處方與大規(guī)格制劑保持一致��,處方量是在大規(guī)格制劑處方基礎(chǔ)上進(jìn)行等比例遞減得到�����。但是小規(guī)格制劑的溶出度比大規(guī)格制劑快��,致使小規(guī)格制劑與BE規(guī)格制劑在各介質(zhì)中溶出曲線不相似����。發(fā)生這種情況有2種原因。1����、出現(xiàn)這種情況是由于原料藥屬于BCSⅡ,在各介質(zhì)中呈pH依賴性����,在某些介質(zhì)中溶解度較小,大規(guī)格制劑進(jìn)行溶出時沒有達(dá)到漏槽條件����,而小規(guī)格制劑則達(dá)到或接近漏槽條件,從而造成小規(guī)格制劑在某些介質(zhì)中的溶出較大規(guī)格制劑快����。根據(jù)“GUIDELINE ON THE INVESTIGATION OF BIOEQUIVALENCE中At pH values where sink conditions may not be achievable for all strengths in vitro dissolution may differ between different strengths. However, the comparison with the respective strength of the reference medicinal product should then confirm that this finding is drug substance rather than formulation related. In addition, the applicant could show similar profiles at the same dose (e.g. as a possibility two tablets of 5 mg versus one tablet of 10 mg could be compared)”(在不可能對所有規(guī)格都達(dá)到漏槽條件的pH值下,不同規(guī)格制劑的體外溶出可能不同�����。然而,與參比制劑的各規(guī)格制劑進(jìn)行比較應(yīng)確認(rèn)這一情況與原料藥有關(guān)�����,而與制劑無關(guān)����。此外,申請人可以在相同劑量下表明類似的情況(例如����,可以比較兩片5mg片和一片10mg片的可能性))的描述。則在溶出偏快的介質(zhì)中投入兩片小規(guī)格制劑��,若此時溶出趨勢和大規(guī)格制劑一致��,則不需進(jìn)行處方調(diào)整�����,因其是原料藥自身性質(zhì)造成的����。2、在排除了是原料藥自身溶解度的因素后�����,造成小規(guī)格制劑溶出度大的原因就是制劑因素�����。片子由原來的大片子變成了小片子����,同樣批量的小片子的比表面積增加,而大規(guī)格制劑和小規(guī)格制劑的包衣液在處方中的比例卻保持不變����,故小規(guī)格制劑每片的包衣厚度變薄了,導(dǎo)致溶出變快����,用下表格中3個規(guī)格制劑舉例:
表1:3個不同規(guī)格處方組成
上表中200mg規(guī)格為BE規(guī)格。擬申請豁免50mg��、150mg規(guī)格與BE規(guī)格的所有活性和非活性組分組成比例完全相同����,屬于調(diào)釋制劑“不同規(guī)格之間所有活性和非活性組分組成比例完全相同”,結(jié)合BE規(guī)格制劑符合生物等效性要求����,兩個規(guī)格制劑與BE制劑釋藥原理相同����,且兩個規(guī)格與BE規(guī)格仿制藥在三種pH介質(zhì)中體外溶出曲線相似的前提條件����,可以豁免50mg、150mg規(guī)格的BE試驗����。
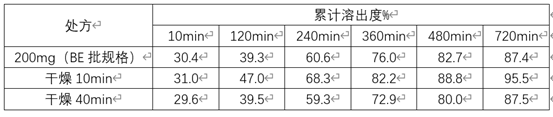
解決此問題已經(jīng)不能從處方上調(diào)整,只能從工藝入手使小規(guī)格制劑的溶出減慢����,可以分兩三步來控制,1�����、在設(shè)計片子大小時����,盡量使用直徑比較大的模具進(jìn)行壓片,以減少因比表面積的因素造成的溶出變快�����。2、在素片階段控制����,若制粒工藝為濕法制粒�����,則在制粒步驟中可以考察攪拌槳轉(zhuǎn)速��、制粒刀轉(zhuǎn)速及制粒時間對溶出的影響����,根據(jù)結(jié)果選擇合適的參數(shù)作為最終制粒參數(shù);在壓片步驟考察不同硬度對溶出的影響����,根據(jù)結(jié)果選擇合適的硬度作為最終的硬度進(jìn)行控制。3����、在膜控階段進(jìn)行控制,對于緩控釋制劑來說�����,包衣材料需要達(dá)到最低成膜溫度,在薄膜形成過程中����,衣膜逐漸融合直至薄膜的孔隙消除后達(dá)到終點,才能在片劑或者微丸表面鋪展和相互結(jié)合����,發(fā)揮其緩控釋作用。衣膜融合可通過包衣過程完成��,也可在包衣結(jié)束后通過短暫的老化過程完成��,因此在對素片進(jìn)行包衣階段��,可延長干燥時間����,使包衣處方能得到完整且進(jìn)一步的衣膜融合,以達(dá)到減慢溶出的目的�����。下表是50mg規(guī)格包衣后不同干燥時間與200mg規(guī)格(BE規(guī)格)的溶出對比:
表2: 50mg規(guī)格包衣后不同干燥時間與200mg規(guī)格(BE規(guī)格)的溶出對比
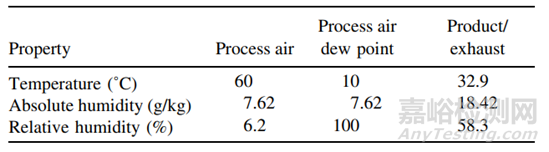
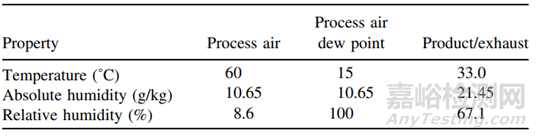
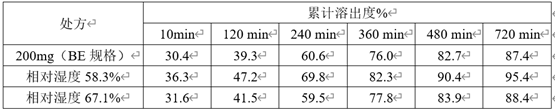
從上表中可以看出��,干燥時間越久,溶出越慢����,與大規(guī)格制劑BE批越相似。4��、在包衣階段��,通過調(diào)整各包衣參數(shù)�����,使包衣過程中相對濕度升高�����,這樣會使包衣膜更致密�����,從而使溶出減慢�����。下表3����、表4是50mg規(guī)格包衣過程中不同相對濕度的包衣具體參數(shù),表5是50mg規(guī)格包衣過程中不同相對濕度與200mg規(guī)格(BE規(guī)格)的溶出對比:
表3: 低的包衣相對濕度的包衣具體參數(shù)
表4 :高的包衣相對濕度的包衣具體參數(shù)
表5 :50mg規(guī)格包衣過程中不同相對濕度與200mg規(guī)格(BE規(guī)格)的溶出對比
從上表中可以看出����,包衣相對濕度越高,溶出越慢����,與大規(guī)格制劑BE批越相似。