啟明醫(yī)療宣布其自主研發(fā)的經(jīng)導(dǎo)管人工肺動(dòng)脈瓣膜置換(TPVR)系統(tǒng)VenusP-Valve獲得FDA批準(zhǔn)進(jìn)行研究性器械豁免(Investigational Device Exemption��,IDE)申請(qǐng)�����,此次批準(zhǔn)為不帶附加條件的完全批準(zhǔn)(Full Approval)���。VenusP-Valve成為首個(gè)獲得美國(guó)FDA批準(zhǔn)進(jìn)行臨床研究的中國(guó)產(chǎn)人工心臟瓣膜,創(chuàng)出中國(guó)瓣膜出海的新紀(jì)錄��。
本次臨床研究將在美國(guó)的10個(gè)醫(yī)療中心與日本的5個(gè)醫(yī)療中心同步開(kāi)展��,預(yù)計(jì)共入組60例患者��。根據(jù)計(jì)劃����,VenusP-Valve將于今年下半年在美國(guó)入組患者,2024年初開(kāi)始在日本入組患者�����,預(yù)計(jì)可于2026年左右在美國(guó)及日本同步獲批上市。
如果按照計(jì)劃正常上市����,也創(chuàng)造國(guó)產(chǎn)心血管介入產(chǎn)品新歷史。在高風(fēng)險(xiǎn)的心血管介入產(chǎn)品�,一般都認(rèn)為外國(guó)月亮比較圓。在現(xiàn)實(shí)中我們可以在國(guó)內(nèi)看到美敦力�、強(qiáng)生、波科����、雅培等公司先進(jìn)且高風(fēng)險(xiǎn)產(chǎn)品橫行無(wú)阻。但是很少有同類國(guó)產(chǎn)產(chǎn)品能夠出現(xiàn)在美國(guó)市場(chǎng)上����,對(duì)國(guó)產(chǎn)產(chǎn)品一句話概況“內(nèi)戰(zhàn)內(nèi)行�����、外戰(zhàn)外行”�����。國(guó)內(nèi)市場(chǎng)極度內(nèi)卷���,卻無(wú)法將內(nèi)卷帶到美利堅(jiān)���。這說(shuō)明國(guó)產(chǎn)產(chǎn)品沒(méi)有底氣(沒(méi)有知識(shí)產(chǎn)權(quán)和無(wú)法面對(duì)最嚴(yán)格監(jiān)管)���,只能在國(guó)內(nèi)橫。
當(dāng)然隨著國(guó)內(nèi)工業(yè)水平不斷進(jìn)步�����,醫(yī)療器械也將像其它工業(yè)產(chǎn)品領(lǐng)域一樣����,最終將國(guó)內(nèi)內(nèi)卷模式漂洋過(guò)海帶到美利堅(jiān)。但是這需要更多能夠吃螃蟹的企業(yè)��,在全球?qū)χR(shí)產(chǎn)權(quán)��、醫(yī)療法規(guī)監(jiān)管最嚴(yán)地方立足����,直面美敦力、愛(ài)德華等公司競(jìng)爭(zhēng)�����。從而才能促使國(guó)內(nèi)醫(yī)療企業(yè)成長(zhǎng)并誕生像華為一樣牛逼企業(yè)。除了美國(guó)政府��,沒(méi)有其它因素能夠干擾國(guó)內(nèi)高端醫(yī)療器械產(chǎn)品在美國(guó)橫行無(wú)阻�����,贏得同行重遵����。
VenusP-Valve
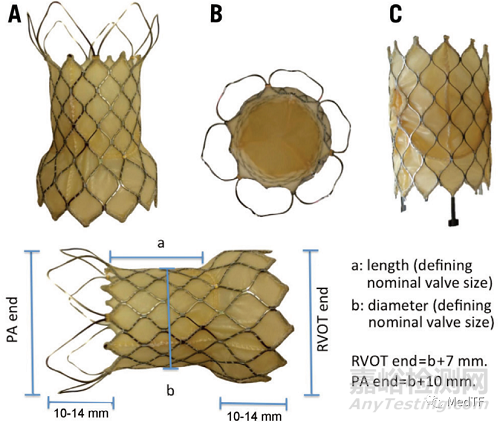
VenusP-Valve是由豬心包和鎳鈦合金支架資本的自膨脹式TPVR產(chǎn)品,其獨(dú)特的雙喇叭口設(shè)計(jì)��,錨定穩(wěn)定���,釋放簡(jiǎn)便���,植入前無(wú)需預(yù)先放置固定支架。
VenusP-Valve支架具有近端和遠(yuǎn)端喇叭口���,以將瓣膜錨定在 RVOT 和肺動(dòng)脈分叉處。近端耀斑被心包組織覆蓋��,而遠(yuǎn)端耀斑是開(kāi)放式細(xì)胞線框架��,以避免阻塞肺動(dòng)脈分支。中間部分也被心包和瓣膜完全覆蓋��。在近端耀斑處有三個(gè)不透射線的鉑標(biāo)記�����,用于識(shí)別瓣膜位置����。中間部分的直徑范圍為 18 至 34 mm,增量為 2 mm����,長(zhǎng)度范圍為 20 至 35 mm,增量為 5 mm����。近端和遠(yuǎn)端擴(kuò)口直徑比中間段大 10 毫米。瓣膜近端有兩個(gè)小鉤子�����,用于連接輸送系統(tǒng)��,輸送系統(tǒng)由一個(gè) 16 Fr、100 厘米長(zhǎng)的軸導(dǎo)管���、一個(gè) 20-22 Fr 的膠囊和一個(gè)用于控制瓣膜展開(kāi)的手柄旋轉(zhuǎn)機(jī)構(gòu)組成���,輸送系統(tǒng)由一個(gè) 16 Fr、100 厘米長(zhǎng)的軸導(dǎo)管�����、一個(gè) 20-22 Fr 的膠囊和一個(gè)用于控制瓣膜展開(kāi)的手柄旋轉(zhuǎn)機(jī)構(gòu)組成�����。
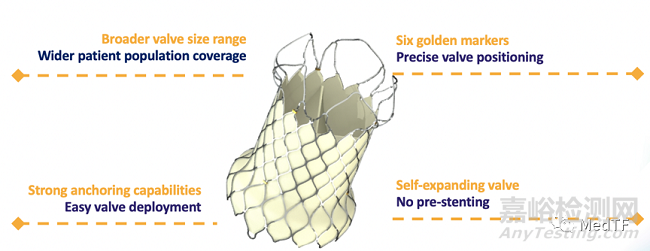
VenusP-Valve瓣膜尺寸規(guī)格多����,適用范圍廣
6個(gè)黃金顯影點(diǎn),確保瓣膜精準(zhǔn)釋放
多位錨定設(shè)計(jì)�����,錨定穩(wěn)固
自膨式瓣膜����,無(wú)需預(yù)先放置固定支架
VenusP-Valve已經(jīng)獲得NMPA和CE批準(zhǔn)上市,在國(guó)內(nèi)和歐洲已經(jīng)驗(yàn)證其安全性和有效性�����。根據(jù)啟明醫(yī)療公布在歐洲三年期隨訪數(shù)據(jù)顯示���,64名接受TPVR手術(shù)的患者(尚有部分患者由于新冠疫情未能計(jì)入)手術(shù)成功率為100%�����,全因死亡率及手術(shù)再干預(yù)率均為0����,所有患者均未出現(xiàn)中度或重度肺動(dòng)脈瓣反流��;96.87%受試者的瓣周漏及三尖瓣反流在輕度以內(nèi)����。
啟明醫(yī)療
啟明醫(yī)療是中國(guó)最領(lǐng)先的經(jīng)導(dǎo)管心臟瓣膜治療領(lǐng)域龍頭企業(yè),自2009年在杭州落戶以來(lái)���,公司在創(chuàng)新產(chǎn)品開(kāi)發(fā)方面的亮眼記錄為公司帶來(lái)顯著的先發(fā)優(yōu)勢(shì)��,重點(diǎn)產(chǎn)品VenusA-Valve和VenusA-Plus為全球第一個(gè)獲得NMPA批準(zhǔn)并在中國(guó)上市的第一��、第二代TAVR產(chǎn)品����。目前,啟明醫(yī)療已建立了一個(gè)全面的結(jié)構(gòu)性心臟病整體解決方案��,覆蓋主動(dòng)脈瓣���、肺動(dòng)脈瓣����、二尖瓣���、三尖瓣等心臟瓣膜疾病�,肥厚性心肌病����,高血壓腎動(dòng)脈去交感神經(jīng)消融術(shù)以及手術(shù)配套產(chǎn)品等完整管線。