近期��,清華大學(xué)溫鵬����,北京大學(xué)鄭玉峰����,北醫(yī)三院田耘在科愛創(chuàng)辦的期刊Bioactive Materials上聯(lián)合發(fā)表研究論文:高溫氧化處理3D 打印鎂合金骨內(nèi)植入體結(jié)構(gòu)優(yōu)化及體內(nèi)外生物降解行為�。利用高溫氧化處理工藝,形成的表面氧化層和遷移層減緩了3D 打印鎂合金的降解速率�。研究團(tuán)隊制備出孔徑分別為 500、800 和 1400 微米(P500����,P800 和 P1400)的鎂支架多孔支架,對力學(xué)性能�,生物相容性、降解行為和成骨能力進(jìn)行體內(nèi)外表征�,其中P500結(jié)構(gòu)性能表現(xiàn)良好。由此啟發(fā)我們通過結(jié)構(gòu)優(yōu)化設(shè)計來調(diào)控其力學(xué)性能及降解速率�,進(jìn)而實現(xiàn)骨缺損重建。
1����、研究內(nèi)容簡介
圍關(guān)節(jié)區(qū)骨缺損是常見而復(fù)雜的臨床疾患,需要植骨材料在應(yīng)力下完成對關(guān)節(jié)面均衡持久的整體支撐��,并于降解過程形成有利于成骨環(huán)境,實現(xiàn)缺損區(qū)修復(fù)與關(guān)節(jié)面的穩(wěn)定��,這對植骨材料及結(jié)構(gòu)的研發(fā)提出了挑戰(zhàn)�。增材制造技術(shù)為精準(zhǔn)修復(fù)骨缺損帶來技術(shù)革命,將生物可降解鎂金屬與增材制造相結(jié)合����,制備“生物活性可降解”及“定制化結(jié)構(gòu)”的個性化骨植入物成為骨缺損治療的發(fā)展前沿。增材制造在實現(xiàn)多孔結(jié)構(gòu)的同時����,也增大了比表面積,在與體液接觸過程中降解加速��。因此�,如何在實現(xiàn)多孔結(jié)構(gòu)的同時控制鎂合金修復(fù)體的吸收速率,是研究者廣為關(guān)注的問題��。
圖1為本文的研究概要圖�,利用激光粉末床熔融增材制造工藝 (LPBF)和高溫氧化處理工藝制備了具有定制化宏微觀結(jié)構(gòu)的WE43生物可降解鎂合金多孔支架,針對三種不同孔徑的鎂支架多孔支架的體內(nèi)外力學(xué)性能�,生物相容性�、降解行為和成骨能力進(jìn)行研究,旨在為激光增材制造生物可降解鎂合金的臨床應(yīng)用奠定基礎(chǔ)����,解決骨缺損精準(zhǔn)治療面臨的臨床難題��。
圖1:本文的研究概要
一�、WE43鎂合金多孔支架的顯微組織分析及力學(xué)性能
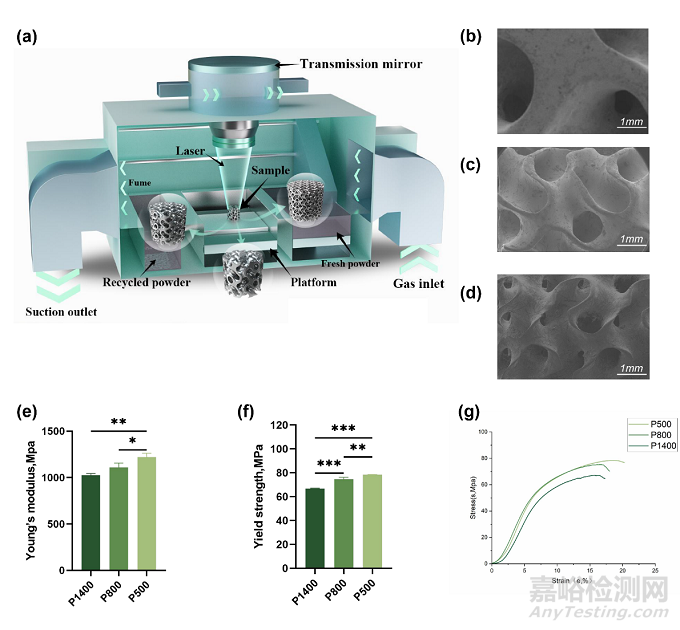
研究團(tuán)隊針對WE43鎂合金多孔支架在生物體內(nèi)降解過快的難題 ����, 開 發(fā) 了 抑 制 其 降 解 的 高 溫 氧 化 處 理 工 藝,形成的表面氧化層 (圖2b)��。根據(jù) EDS 分析(圖2c) �,高 溫 氧 化 處 理 后,在支架表面形成含Y�,Nd,Gd����,Zr 和 O等元素的氧化物層,它能將鎂合金基體與體液隔絕開����,因此減緩了鎂合金支架的降解速率。
研究團(tuán)隊制備了孔徑分別為 500����、800 和 1400 微米(P500����,P800 和 P1400)的鎂合金支架��。不同孔徑的鎂合金支架表面形貌類似����,均無明顯缺陷(圖3b-d)。然而����,不同孔徑的鎂合金支架的體外力學(xué)行為存在明顯差異,其中P500結(jié)構(gòu)性能表現(xiàn)良好����。(圖3e-g)
圖2:鎂合金支架高溫氧化處理前后橫截面上的 SEM 形貌(a-b)和 EDS 分析(c)
圖3:不同孔徑的鎂合金支架SEM 形貌(b-d)和 體外力學(xué)測試(c)
二、體外生物相容性及促成骨能力
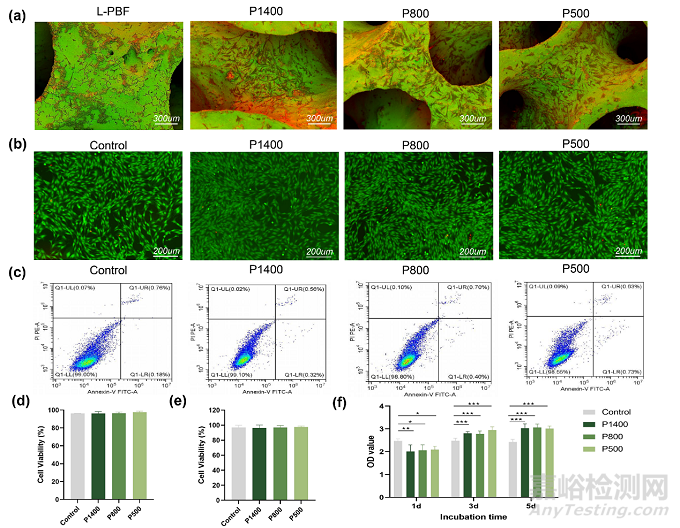
為了測試鎂合金支架的生物相容性�,將骨髓間充質(zhì)干細(xì)胞直接接種在 P500,P800和 P1400組的鎂合金支架上�,骨髓間充質(zhì)干細(xì)胞能夠很好地黏附于 P500、 P800和 P1400組的支架表面(圖4a)��。研究團(tuán)隊使用間接接觸法測試鎂合金支架體外生物相容性�。活/死染色細(xì)胞����、細(xì)胞凋亡測試和CCK-8細(xì)胞毒性試驗均顯示所有組別細(xì)胞相容性良好,各組別之間沒有統(tǒng)計顯著性差異(圖4b-d)��。
之后為了測試鎂合金支架的體外成骨性能�,在浸提液中加入地塞米松,L-抗壞血酸����,β-甘油磷酸鈉進(jìn)行成骨誘導(dǎo)。如圖5a-d所示����,鎂合金支架組的堿性磷酸酶活性和細(xì)胞外基質(zhì)的礦化水平均較對照組高,其中P500組骨髓間充質(zhì)干細(xì)胞的成骨性能最為顯著����。之后使用蛋白質(zhì)免疫印跡實驗對成骨相關(guān)分子蛋白表達(dá)量進(jìn)行定量,P500組的成骨相關(guān)分子蛋白表達(dá)量均較其他組高(圖5e-h)��。
圖4:不同孔徑的鎂合金支架組的體外細(xì)胞黏附性(a)和生物相容性測試(b-f)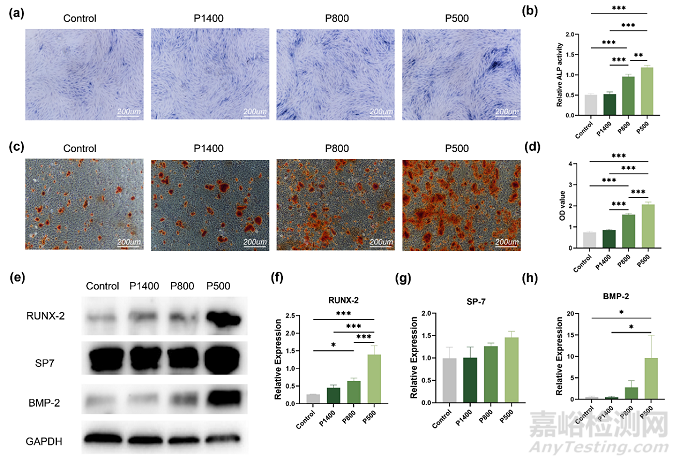
圖5:不同孔徑的鎂合金支架組體外促成骨能力測試:(a)堿性磷酸酶染色和(b) 堿性磷酸酶活性測試����,(c-d)茜素紅染色及其半定量分析,(e-h) 成骨相關(guān)分子蛋白半定量分析結(jié)果
三�、體內(nèi)生物降解行為及促成骨能力
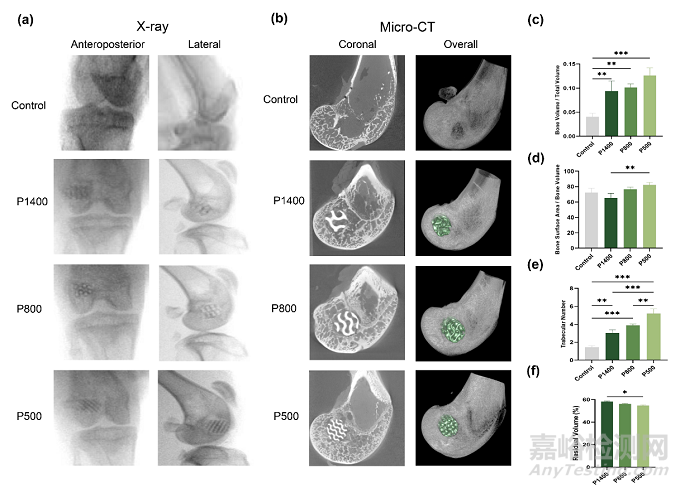
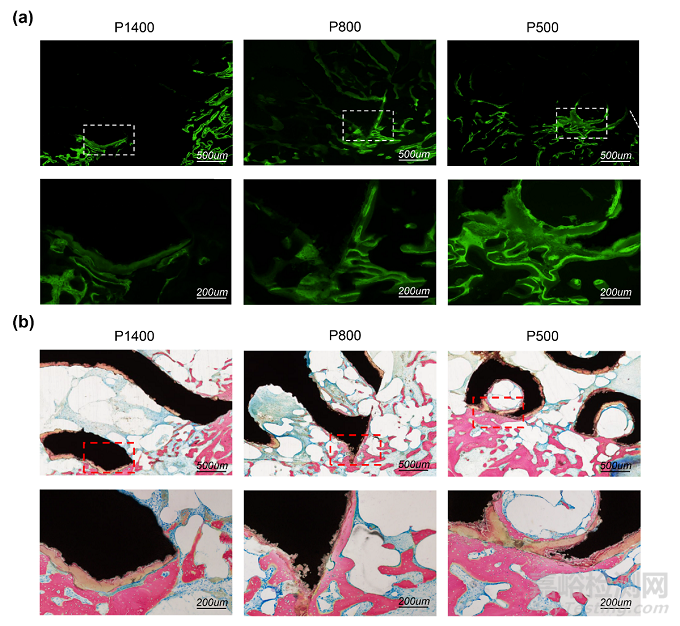
為了研究不同孔徑的鎂合金支架體內(nèi)生物降解行為及促成骨能力��,研究團(tuán)隊進(jìn)一步建立了兔股骨髁缺損模型�,硫酸鈣骨水泥作為對照�。WE43多孔支架結(jié)構(gòu)在手術(shù)后4周仍然清晰可見,表明支架沒有明顯降解�,具有良好的結(jié)構(gòu)完整性。在骨水泥組�,硫酸鈣骨水泥完全降解(圖6a)。Micro-CT 結(jié)果顯示鎂合金支架組新骨形成量明顯高于對照組����,并且P500組的 BV/TV,BSA/BV 和 Tb.N 值顯著高于 P800和 P1400組(圖6b-e) �,表明 P500支架成骨性能優(yōu)越,較為持久的整理力學(xué)支撐有利于圍關(guān)節(jié)骨缺損的修復(fù)�,具有作為骨科植入物的潛力。對缺損部位進(jìn)行硬組織切片的結(jié)果也與Micro-CT 結(jié)果相吻合(圖7)�。
圖6:不同孔徑的鎂合金支架組在4周時X 射線和micro- CT 結(jié)果
圖7:不同孔徑的鎂合金支架在4周時鈣黃綠素?zé)晒夂蛠喖谆{(lán)/酸性品紅溶液染色結(jié)果
2、原文信息
Chaoxin Wang, Jinge Liu, Shuyuan Min, Yu Liu, Bingchuan Liu, Yuanyu Hu, Zhengguang Wang, Fengbiao Mao, Caimei Wang, Xiaolin Ma, Peng Wen*, Yufeng Zheng*, and Yun Tian*.
The effect of pore size on the mechanical properties, biodegradation and osteogenic effects of additively manufactured magnesium scaffolds after high temperature oxidation: An in vitro and in vivo study.
Bioactive Materials, 28 (2023) 537-548.