多肽偶聯(lián)藥物(PDC)介紹
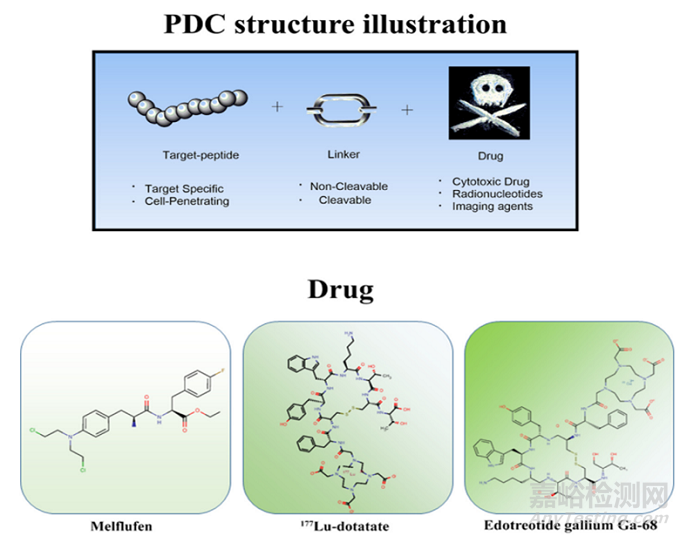
多肽偶聯(lián)藥物(PDC)是一種新興的靶向治療方法�,可提高腫瘤的穿透性和選擇性�。PDC主要由三部分組成——多肽(peptide)�、連接子(linker)以及具有細(xì)胞毒性的有效載荷(cytotoxicity payload)[1]。
圖1多肽-藥物偶聯(lián)結(jié)構(gòu)示意圖���,由不同有效載荷的靶肽���、連接體和藥物組成
與非靶向抗癌藥物相比,PDC可顯著延長血液循環(huán)時(shí)間�����、增加最大耐受劑量�、增強(qiáng)腫瘤積聚和提高抗癌生物活性。因?yàn)檎<?xì)胞缺乏靶向受體不能與腫瘤靶向肽結(jié)合���,化合物會(huì)在受體陽性腫瘤細(xì)胞中富集�����,可以降低給藥劑量�,減少毒副作用。另外���,PDC還可以依靠多肽的特性來提高藥物的溶解性���、滲透性和選擇性[1]。
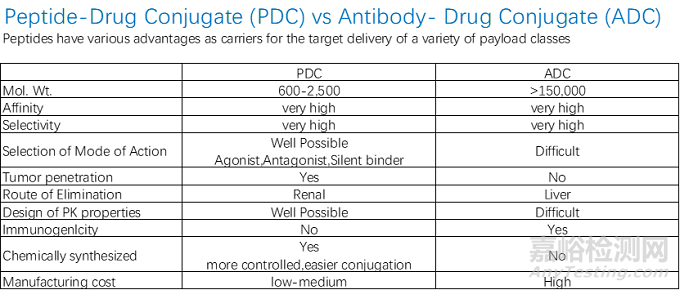
與ADC藥物相比�����,PDC藥物具有諸多優(yōu)勢:分子量小���,腫瘤穿透性強(qiáng)�����,對(duì)實(shí)體瘤抑瘤效果好�,且由于體積小,也容易合成單一同質(zhì)物質(zhì)���;免疫原性低;細(xì)胞毒性藥物選擇面廣���,由于較強(qiáng)的腫瘤組織滲透性,PDC能夠在靶標(biāo)處累積達(dá)到高濃度�,因此可以選擇阿霉素、紫杉醇等毒性相對(duì)較低且普遍應(yīng)用于臨床的化療藥物���;另外由于可原核表達(dá)或化學(xué)合成���,PDC生產(chǎn)過程簡單且易于規(guī)模放大,生產(chǎn)成本較低���。因此,PDC有望成為繼小分子藥物�����、單抗���、ADC藥物之后新一代抗腫瘤藥[6]�。目前,全球已上市2款PDC藥物���。
圖2 PDC與ADC藥物對(duì)比
多肽偶聯(lián)藥物作用機(jī)制
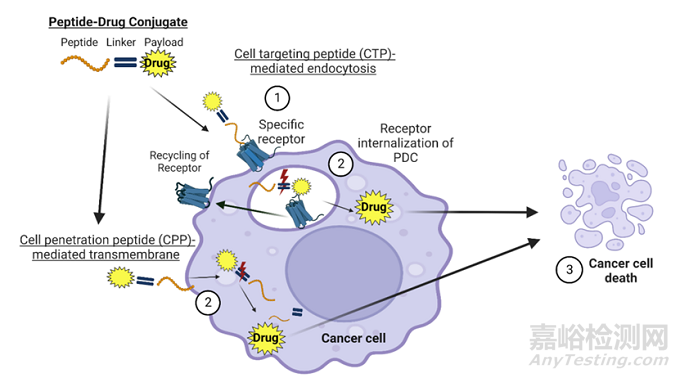
PDC的作用機(jī)制與ADC類似���,通過連接子將靶向多肽和細(xì)胞毒素共價(jià)連接,精準(zhǔn)靶向腫瘤細(xì)胞特定受體�����,可控釋放細(xì)胞毒素�����,從而殺傷腫瘤細(xì)胞[2]�。在早期研發(fā)中���,除了PDC整體的藥理/藥效作用外���,還需要對(duì)其各個(gè)組成部分的藥理作用進(jìn)行研究���。
圖3 PDC藥物的腫瘤細(xì)胞內(nèi)化步驟及作用機(jī)制
1、PDC中的多肽
多肽作為PDC的重要組成部分���,是實(shí)現(xiàn)PDC多種功能的基礎(chǔ)���。PDC通過連接水溶性多肽或多肽組合可以增加疏水性藥物的溶解度和成藥性。肽可根據(jù)其功能分為:細(xì)胞穿透肽 (CPP)�����、細(xì)胞靶向肽 (CTP)和反應(yīng)肽[5]���。細(xì)胞穿透肽 (CPP)是指能進(jìn)入細(xì)胞而不破壞其膜完整性的小分子���、短分子多肽,一般由5-30個(gè)氨基酸組成���。細(xì)胞穿透肽 (CPP)在生理環(huán)境下具有帶正電荷和兩親性兩種共同特征���,在藥物遞送系統(tǒng)中得到了廣泛的應(yīng)用。
細(xì)胞靶向肽 (CTP)有被動(dòng)靶向和主動(dòng)靶向兩大類�����。被動(dòng)靶向是指由于給藥系統(tǒng)本身的性質(zhì)或靶組織的特性,藥物與血液循環(huán)一起被動(dòng)地聚集在病灶組織中���。主動(dòng)靶向是通過識(shí)別靶組織中特異性表達(dá)的受體或蛋白���,將藥物主動(dòng)遞送至病灶組織來實(shí)現(xiàn)的。大多數(shù)基于細(xì)胞靶向肽 (CTP)的PDC是通過主動(dòng)靶向機(jī)制遞送的�����。反應(yīng)肽是在外界刺激下發(fā)生結(jié)構(gòu)變化的肽�,這種變化發(fā)生在結(jié)構(gòu)水平上�,而不是簡單的連接子斷裂。通常�����,外界環(huán)境刺激包括溫度���、pH���、酶等�����,腫瘤微環(huán)境的弱酸性也成為靶向腫瘤的新途徑[5]���。
2�����、PDC中的連接子
作為 PDC中藥物與多肽之間的連接橋梁���,連接子決定了 PDC在體內(nèi)的循環(huán)時(shí)間和穩(wěn)定性���。理想的連接子應(yīng)在循環(huán)中保持穩(wěn)定�����,以避免藥物過早釋放���,同時(shí)一旦到達(dá)病灶組織�,能夠快速有效地釋放藥物。同時(shí)�,連接子不應(yīng)影響肽與其受體的親和力和藥物的活性[4]���。此外,帶有多肽和藥物的連接子的合成工藝應(yīng)盡可能簡單�����,并在整個(gè)合成過程中保持穩(wěn)定。連接子的疏水性不應(yīng)過強(qiáng)���,以防止 PDC因疏水性而聚集,導(dǎo)致體內(nèi)穩(wěn)定性差和藥效降低���,以及較強(qiáng)的全身毒性和免疫副作用���。根據(jù)藥物釋放機(jī)制和連接物的裂解行為,連接物主要分為不可裂解連接子和可裂解連接子[5]���。
2.1 不可裂解連接子
不可裂解連接子是指相對(duì)穩(wěn)定���,在血液循環(huán)過程中不斷裂的連接子。與可裂解連接子相比�����,不可裂解連接子的最大優(yōu)點(diǎn)是血漿穩(wěn)定性好、較低的脫靶毒性���、較大的治療窗和較好的耐藥性���。不可斷裂的連接子一般對(duì)外界刺激無反應(yīng),而是在肽代謝后釋放藥物�。因此�����,在到達(dá)靶部位之前�����,不可斷裂連接子可以在血液循環(huán)中保持穩(wěn)定[4]���。
2.2 可裂解連接子
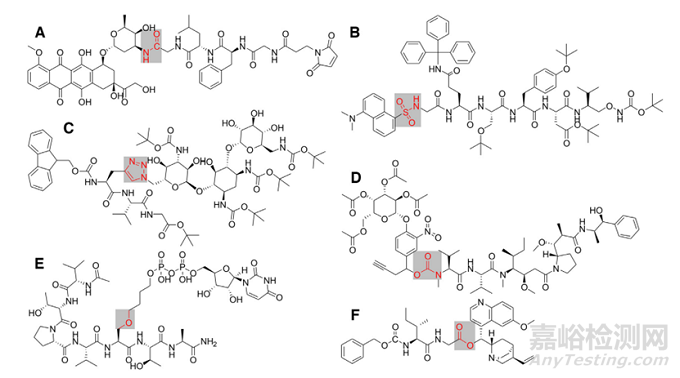
可裂解連接子是 PDC 構(gòu)建中最常用的連接子�����,可在機(jī)體生理環(huán)境或酶存在的情況下裂解釋放藥物�,包括蛋白酶敏感類�、PH敏感類���、氧化還原敏感類等類型(如圖4 )�。與不可裂解的連接子相比,這些 PDC最大的優(yōu)點(diǎn)是可以在靶組織中特異性斷裂�,快速釋放藥物達(dá)到治療濃度,降低了對(duì)其他組織或器官的毒副作用從而真正實(shí)現(xiàn)了智能給藥的概念[4]�����。
圖4. 不同可裂解連接子的連接化學(xué)鍵
3、PDC中的有效載荷
PDC的有效載荷是發(fā)揮細(xì)胞毒性或治療作用的藥物,這些藥物大多存在水溶性低�����、選擇性差、半衰期短和穩(wěn)定性差等缺點(diǎn)�,限制了其臨床應(yīng)用[1]??梢允褂?PDC策略遞送的藥物需要有可行的連接位點(diǎn)。此外�����,藥物應(yīng)以結(jié)合形式不具有藥理活性���,當(dāng)在病灶組織中釋放時(shí)�����,應(yīng)繼續(xù)發(fā)揮具有明確作用機(jī)制和較強(qiáng)藥理活性的治療作用[2]�����。與多肽偶聯(lián)后���,可增強(qiáng)藥物的溶解度,促進(jìn)藥物選擇性,延長體內(nèi)循環(huán)時(shí)間�,優(yōu)化生物利用度,防止藥物對(duì)其他組織的副作用和毒性[3]���。
PDC方法開發(fā)與案例分享
1���、PDC方法開發(fā)的挑戰(zhàn)
PDC的偶聯(lián)結(jié)構(gòu)特性,導(dǎo)致其體內(nèi)過程多樣�����,因此�,生物分析方法具有一定的復(fù)雜性。藥代動(dòng)力學(xué) (PK) 和毒代動(dòng)力學(xué) (TK) 的研究中主要檢測PDC全藥�、多肽及游離小分子化合物。PDC的毒性作用與多肽�����、小分子化合物以及連接子的特性密切相關(guān)�,隨著多肽、小分子化合物和連接子的變換�����,其毒性反應(yīng)特征也會(huì)產(chǎn)生變化。非臨床安全性研究中�,應(yīng)關(guān)注藥物組成結(jié)構(gòu)、藥代特征對(duì)毒性作用的影響�����,綜合分析試驗(yàn)結(jié)果���。
PDC藥物的特殊結(jié)構(gòu)和作用機(jī)制,使其在基質(zhì)中的穩(wěn)定性增加了不確定因素�,需要考慮到多肽、連接子以及具有細(xì)胞毒性的有效載荷的各自穩(wěn)定性�,可添加酶抑制劑、調(diào)整PH值���、添加氧化還原劑和控制實(shí)驗(yàn)環(huán)境等解決穩(wěn)定性問題�;PDC在LC-MS/MS中會(huì)有不同m/z的多電荷離子對(duì)產(chǎn)生�,可通過調(diào)整流動(dòng)相的PH值,改變電荷分布���,優(yōu)化儀器參數(shù)和液相條件等���,使靈敏度滿足分析需求���;保證PDC在基質(zhì)中的提取回收率也是至關(guān)重要的,應(yīng)避免前處理時(shí)破壞PDC的結(jié)構(gòu)���;非特異性吸附和系統(tǒng)殘留也是PDC生物分析中常遇到的問題�。
2���、案例分享
待分析的PDC藥物分子量大于4500 g/mol�,多肽與細(xì)胞毒性化合物通過可裂解連接子連接�。為了檢測大鼠給藥后的血藥濃度變化,需要開發(fā)一種可靠的生物分析方法來準(zhǔn)確定量大鼠血漿中PDC全藥的濃度�����,多肽和游離小分子化合物的生物分析策略與挑戰(zhàn)會(huì)在后續(xù)研究中繼續(xù)分享�。
方法開發(fā)中,我們成功克服該P(yáng)DC藥物在血漿中的穩(wěn)定性和非特異性吸附問題���、多電荷的靈敏度問題���、回收率和系統(tǒng)殘留問題,用蛋白沉淀法成功建立了檢測大鼠血漿(含穩(wěn)定劑)中PDC藥物濃度的LC-MS/MS 分析方法���,其檢測線性范圍是 5.00 ~ 2500 ng/mL�,r2 > 0.997, 呈良好的線性關(guān)系。在準(zhǔn)確度和精密度分析批中�,每個(gè)QC樣品濃度水平的平均值準(zhǔn)確度在±15.0%以內(nèi)(LLOQ樣品平均準(zhǔn)確度偏差在±20.0%以內(nèi)),每個(gè)QC樣品濃度水平的精密度值(%CV)不超過15.0%(對(duì)于LLOQ不超過20.0%)�����。在大鼠血漿中加入穩(wěn)定劑后�����,能有效的保證在樣品處理過程中PDC的穩(wěn)定性���。經(jīng)分析方法確證和樣品分析,證明建立的分析方法穩(wěn)健且重現(xiàn)性良好�。
結(jié)語
與ADC藥物相比,PDC藥物具有強(qiáng)力的腫瘤穿透性�、免疫原性低以及生產(chǎn)成本較低等特點(diǎn),是繼ADC之后的下一代靶向治療藥物[6]�。目前全球已有兩款PDC藥物上市,數(shù)十款在研PDC進(jìn)入臨床階段�,并在腫瘤治療中表現(xiàn)出良好的療效,這預(yù)示了PDC藥物未來巨大的臨床應(yīng)用前景[3]�。
參考文獻(xiàn)
1. Peptide-Drug Conjugate: A Novel Drug Design Approach. Curr Med Chem. 2017;24(31):3373-3396.
2. Eirinaios I. Vrettos, Gábor Mez? and Andreas G. Tzakos. On the design principles of peptide–drug conjugates for targeted drug delivery to the malignant tumor site. Beilstein J. Org. Chem. 2018, 14:930–954. doi:10.3762/bjoc.14.80
3. Bethany M. Cooper, a Jessica Iegre, a Daniel H. O’ Donovan, et al. Peptides as a platform for targeted therapeutics for cancer: peptide–drug conjugates (PDCs) Chem. Soc. Rev., 2021,50, 1480-1494.
4.Liming Gong , Heming Zhao, Yanhong Liu ,. Research advances in peptide?drug conjugates. Acta Pharmaceutica Sinica B. Received 26 November 2022; received in revised form 5 February 2023; accepted 15 February 2023
5.Chen Fu, Lifeng Yu, Yuxi Miao, et al. Peptide-drug conjugates(PDCs): a novel trend of research and development on targeted therapy, hype or hope?. Acta Pharmaceutica Sinica B, 2023, 13(02):498-516.
6.Peptides as a platform for targeted therapeutics for cancer: peptide–drug conjugates (PDCs). Chem. Soc. Rev., 2021, 50, 1480-1494.