改良型新藥從有效性�����、安全性和依從性三方面進(jìn)行改良假設(shè)��,此改良假設(shè)也是立題依據(jù)����,最重要的是怎么獲得改良假設(shè)的證據(jù),證明臨床優(yōu)勢�����。本文的思路為通過分析在2016年-2022年期間受理的����,并最終獲得批準(zhǔn)的改良型品種的臨床開發(fā)路徑,以期為開發(fā)改良型新藥提供借鑒。
首先明確一點��,2.4類為新增適應(yīng)癥����,嚴(yán)格意義上不屬于改良型新藥,新增適應(yīng)癥主要有兩類����,一是原研本身新增適應(yīng)癥,這其實是原研企業(yè)開發(fā)新藥的一個基本路徑策略�����,另外是非原研企業(yè)新增適應(yīng)癥��。
所以本文統(tǒng)計未將2.4類列入����。
1�����、提高安全性
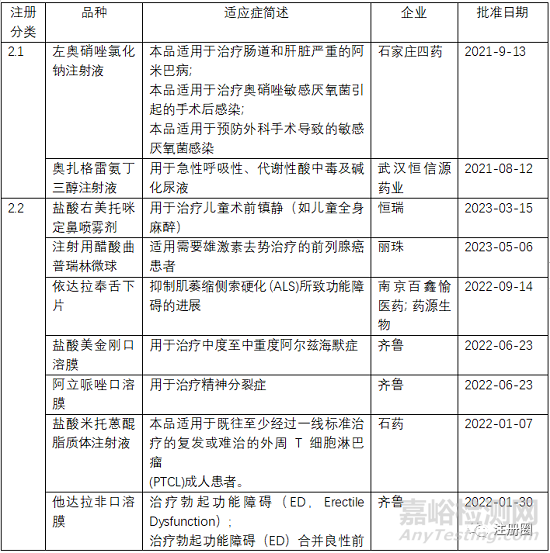
左奧硝唑氯化鈉注射液
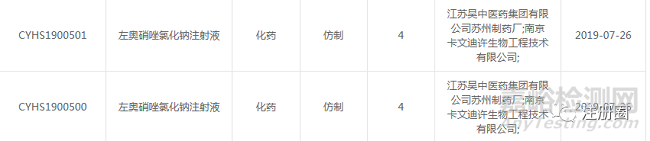
石家莊四藥的左奧硝唑氯化鈉注射液2018年7月獲得CDE的受理承辦�����,于2021年9月16日獲得批準(zhǔn)。
關(guān)于左奧硝唑氯化鈉注射液最先申報的是南京圣和藥業(yè)�����,2006年以1.3類申請臨床�����,2009年批準(zhǔn)100ml:左奧硝唑0.5g/氯化鈉0.83g規(guī)格�����,2019年批準(zhǔn)100ml:左奧硝唑0.25g/氯化鈉0.87g規(guī)格�����。但是南京圣和的左奧硝唑氯化鈉注射液的上市并沒有給石家莊四藥的注冊申報帶來任何影響����,2018年以2.1類申報。而且南京圣和獲批兩個規(guī)格再次進(jìn)行補(bǔ)充申請?zhí)峤?����,?019年獲得批準(zhǔn)。2019年之后國內(nèi)企業(yè)則以4類進(jìn)行申報����。所以推測南京圣和2009年獲批的技術(shù)審評要求不符合新的注冊分類改革下的要求。
左奧硝唑是第三代硝基咪唑抗厭氧菌�����、抗原蟲藥物奧硝唑的左旋體����。奧硝唑有左奧硝唑和右奧硝唑兩種異構(gòu)體,但是右奧硝唑會產(chǎn)生神經(jīng)毒性的安全性問題��,現(xiàn)已上市的的奧硝唑的安全性問題即是由于右奧硝唑的原因��,所以開發(fā)單一的左奧硝唑��,會提高安全性�����。
所以根據(jù)立題依據(jù)����,臨床試驗證明有效性非劣效的情況下,能夠提高安全性即可批準(zhǔn)上市�����。
2����、提高有效性,同時提高安全性
鹽酸米托蒽醌脂質(zhì)體注射液�����、注射用紫杉醇聚合物膠束
米托蒽醌和紫杉醇都是屬于毒性很大的細(xì)胞毒藥物�����,所以通過改變遞送系統(tǒng)�����,增強(qiáng)靶向性����,進(jìn)一步提高安全性和有效性。
鹽酸米托蒽醌脂質(zhì)體注射液做了臨床前的毒理試驗�����,共進(jìn)行了小鼠和犬單次給藥毒性試驗、大鼠靜脈注射4次間隔4周毒性試驗����、犬靜脈滴注4次間隔4周毒性試驗,犬重復(fù)靜脈輸注本品 36 周(每 4 周 1 次)毒性試驗�����。
PK藥代動力學(xué)試驗
關(guān)鍵II期臨床試驗(單臂多中心)有效性評價
13項安全性臨床研究��,共計307名患者
注射用紫杉醇聚合物膠束由于已有白蛋白��、脂質(zhì)體上市����,本品僅需要I期藥代動力學(xué)和耐受性研究和一項確證性臨床進(jìn)行安全性和有效性評價即可。
3�����、提高依從性
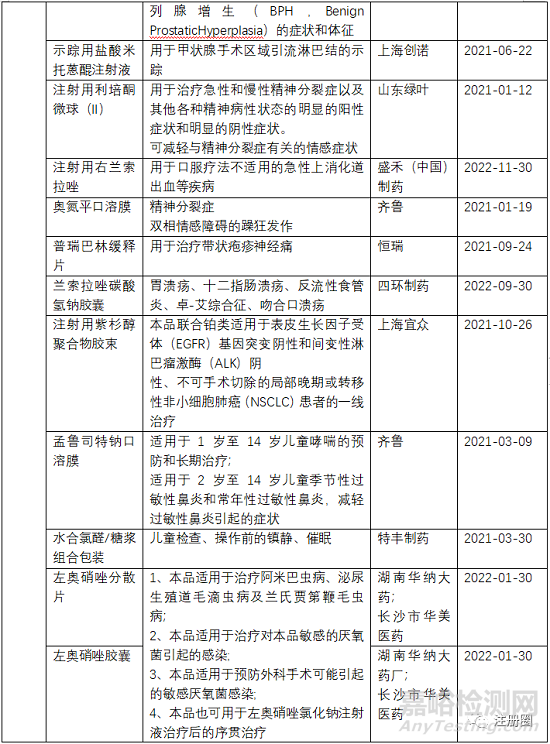
依達(dá)拉奉舌下片
依達(dá)拉奉注射液已被開發(fā)用于ALS����,原研日本三菱田邊的依達(dá)拉奉注射液2019年4月年申報進(jìn)口,2019年7月批準(zhǔn)進(jìn)口��。
ALS 需要長期治療����,本品是靜脈注射劑改為舌下給藥固體制劑,考慮到注射劑需長期住院輸液治療�����,舌下片劑能便捷�����、自主給藥����,可以極大提高用藥的便利性和病人的依從性,從而保障患者獲得充分的治療和更好的療效����。所以該改良為提高依從性。
注射用醋酸曲普瑞林微球
醋酸曲普瑞林國內(nèi)外已上市多年����,現(xiàn)國產(chǎn)有4家醋酸曲普瑞林注射液�����,均為水針����。法國Ipsen公司的曲普瑞林微球制劑于2003年進(jìn)入中國��,商品名達(dá)菲林�����。相比普通注射劑��,注射用醋酸曲普瑞林微球為一個月注射一次的長效劑型�����,顯著提高用藥依從性�����。但是在已有微球制劑上市的情況下��,麗珠是利用自己的技術(shù)平臺以2.2類進(jìn)行開發(fā),并未按照原研的工藝等進(jìn)行仿制��。
臨床開發(fā)路徑是����,開展PK試驗��,比較與達(dá)菲林的生物等效性����,開展確證性臨床證明有效性與安全性。
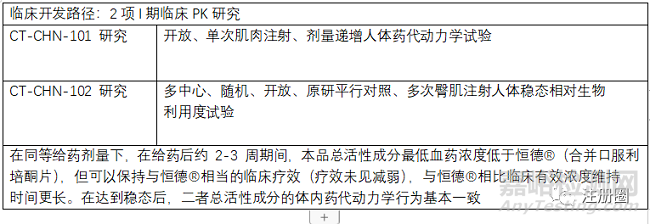
注射用利培酮微球
原研注射用利培酮微球(恒德)已經(jīng)上市��。但是原研在首次注射后有約 3 周的釋藥延遲期����,患者需在 3 周釋藥延遲期內(nèi)持續(xù)口服利培酮制劑,以保持臨床有效血藥濃度的穩(wěn)定��。本品注射用利培酮微球(II)通過釋藥方式的改良��,縮短釋藥延遲期����,不再需要首次注射后的口服制劑補(bǔ)充,提高臨床治療過程的便利性����。
鹽酸美金剛口溶膜����、阿立哌唑口溶膜����、他達(dá)拉非口溶膜、奧氮平口溶膜����、孟魯司特鈉口溶膜
鹽酸美金剛口溶膜和孟魯司特鈉口溶膜針對吞咽困難、不適宜吞咽藥片的人群�����,提高該類人群的用藥依從性�����。所以在已有鹽酸美金剛口服溶液和孟魯司特鈉咀嚼片上市的情況下�����,僅需與口服溶液和咀嚼片做生物等效性試驗,在生物等效的情況下��,即可證明依從性優(yōu)勢��。
阿立哌唑口溶膜和奧氮平口溶膜是為了解決精神分裂癥患者的藏藥行為����,所以臨床開發(fā)策略僅需與口崩片做生物等效性試驗即可。
他達(dá)拉非口溶膜用于男性勃起功能障礙��,相對于普通片劑��,他達(dá)拉非口溶膜服用更便利��,該口溶膜設(shè)計為薄薄的一片��,類似口香糖��,直接放入口腔��,無需用水吞服����,具有便利隱蔽性����,保護(hù)隱私��。證明與他達(dá)拉非片具有生物等效性即可����。
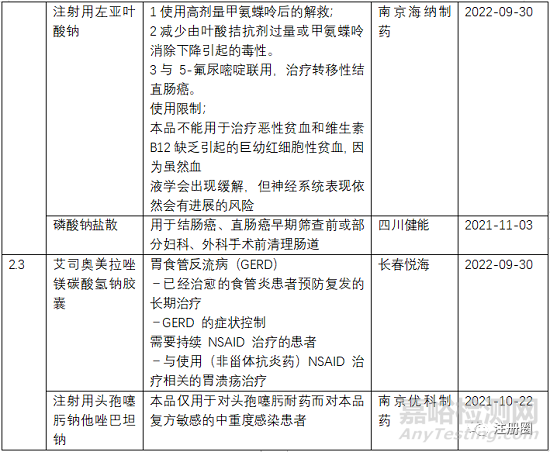
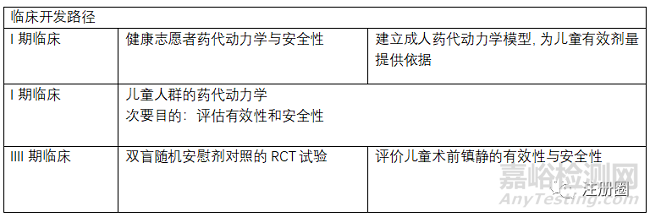
鹽酸右美托咪定鼻噴霧劑
鹽酸右美托咪定注射液于1999年首次獲得FDA的批準(zhǔn)��,用于(1)行全身麻醉的手術(shù)患者氣管插管和機(jī)械通氣時的鎮(zhèn)靜��;(2)重病監(jiān)護(hù)治療期間開始插管和使用呼吸機(jī)病人的鎮(zhèn)靜��。恒瑞于2009年獲得首仿批準(zhǔn)上市�����,目前國內(nèi)已有10+企業(yè)擁有該品種批文����,另外恒瑞的鹽酸右美托咪定氯化鈉注射液于2021年獲得批準(zhǔn),為國內(nèi)獨(dú)家��。恒瑞再進(jìn)一步�����,開發(fā)鹽酸右美托咪定鼻噴劑,用于治療兒童術(shù)前鎮(zhèn)靜(如兒童全身麻醉)�����。本品為開發(fā)用于專門人群的改良型劑量�����,相比注射劑�����,鼻噴霧劑對于兒童具有更好的用藥便利性����。
4�����、其他:減少耐藥
注射用頭孢噻肟鈉他唑巴坦鈉
注射用頭孢噻肟鈉他唑巴坦鈉用于下呼吸道和泌尿系統(tǒng)的抗感染治療����,但是在抗感染藥物的臨床使用和研發(fā)中,一個突出的問題就是抗菌藥濫用導(dǎo)致誘導(dǎo)耐藥和細(xì)菌選擇性壓力日益嚴(yán)重����,因此開發(fā)為固定劑量的聯(lián)用復(fù)方可以降低單藥的使用量����,減少耐藥問題��。
臨床開發(fā)路徑:
(1)進(jìn)行了單次和多次給藥的藥代動力學(xué)和耐受性研究��。
(2)進(jìn)行了兩種藥物的相互作用研究
(3)III期確證性臨床進(jìn)行有效性和安全性的評價
總結(jié)
創(chuàng)新藥和仿制藥的開發(fā)路徑相對比較固定����,而改良型新藥的臨床開發(fā)路徑是最具靈活多變的,改良型新藥基于風(fēng)險獲益等評估可以進(jìn)行原研或者文獻(xiàn)的數(shù)據(jù)借用�����。但是萬變不離其宗��,所有的變化都是基于風(fēng)險獲益評估����。
提高安全性方面的邏輯,比如左奧硝唑氯化鈉注射液����,這是一個新的化學(xué)成分����,新的化學(xué)成分一般要做非臨床研究的安全性研究�����,但是因為現(xiàn)在已上市的奧硝唑中含有左奧硝唑����,已經(jīng)應(yīng)用臨床多年,所以不需要進(jìn)行毒理研究�����。在證明提高安全性的情況下�����,僅需證明有效性非劣效�����,提高安全性����。所以需要做個PK、然后做一個確證性臨床�����。
提高有效性����,像細(xì)胞毒藥物,通過劑型改良�����,提高有效性��,提高有效性就需要開展確證性臨床��,在確證性臨床之前再開展PK研究��,但是像米托蒽醌脂質(zhì)體�����,因為脂質(zhì)體的工藝相對普通注射液有很大不同����,處方����、輔料等有很大區(qū)別��,風(fēng)險未知�����,在開展臨床之前��,需要進(jìn)行非臨床的安全性評價����。而像紫杉醇膠束,之前已經(jīng)有同屬高端注射劑的白蛋白和脂質(zhì)體上市��,已有臨床應(yīng)用數(shù)據(jù)�����,所以不需要開展非臨床的毒理研究��,僅需要PK和確證性臨床(與紫杉醇普通注射液對照)��。
提高依從性��,提高依從性一般需要從兩面證明一是證明與原型藥物相比具有生物等效(改良型新藥的生物等效與仿制藥的生物等效是有所區(qū)別的)�����;二是證明在改良后的更具依從性的給藥途徑與原型藥物非劣效�����,即可證明依從性優(yōu)勢����。但是關(guān)于非劣效下的依從性優(yōu)勢筆者多說一點,更好的改良應(yīng)該通過提高依從性����,進(jìn)而提高有效性和減少醫(yī)療支出(這更有利于改良型新藥的支付端定價),這是后話了�����。
總之�����,改良型新藥開發(fā)雖然變化多端,但本質(zhì)不變����。就像藥品注冊分類的劃分一樣,不要硬背幾類幾類��,劃分的本質(zhì)依據(jù)是基于風(fēng)險獲益評估的�����,這個方法論應(yīng)用于改良型新藥開發(fā)同樣適用����。