預充針逐漸成為復雜的生物制品的選擇�����,選擇使用預充針比使用小瓶包裝節(jié)省了產品的體積用量�����,降低了生產成本�����。有多種預充針來滿足不同的要求�����,這些要求使得在選擇預充針材質時面臨著挑戰(zhàn)��。Baxter生物制藥解決方案研究總監(jiān)對預充針的選擇給出了一些看法和建議���。
預充針(PFS)市場增長繼續(xù)保持強勁的態(tài)勢���,最近一份報告顯示預計到2019年PFS的全球銷售額可達49.8億美元(39億英鎊)。PFS產品銷售增長的推動因素包括藥企研發(fā)管線中注射用生物制劑的增加和生物制劑的全球化�����。
預充針對于高成本���、復雜的生物制品(如單克隆抗體和融合蛋白)的開發(fā)者有著特別的吸引力�����。與瓶裝制劑相比���,預充針需要最小的過量灌裝體積以確?�;颊咦⑸錅蚀_的劑量�����,每批節(jié)省的裝量就可以抵消PFS組件的成本��。
法規(guī)對生物制品的要求推動了預充針的創(chuàng)新�����。雖然I型玻璃仍然是注射器常用的材料��,但塑料注射器也越來越受歡迎���,包括環(huán)烯烴聚合物(COP)、環(huán)烯烴共聚物(COC)���、聚丙烯(PP)和聚碳酸酯(PC)�����。在日本�����,50%的注射器是塑料的�����。聚合物注射器無菌���、隨時可用、具有玻璃外觀(圖1)�����,并且耐磨損�����。
除了West Pharmaceutical Services Crystal Zenith公司的COP注射器外�����,大多數(shù)注射器針筒需要添加硅油使活塞在使用過程中平穩(wěn)滑動�����。一般需要硅膠的聚合物材質的注射器有BD公司的Sterifill™(使用較少的硅膠)或Schott公司的TopPac SD®(使用交聯(lián)硅膠)。
可以依據針筒形狀與結構��、硅膠水平和鎢含量選擇不同的預充針���,使得選擇預充針變得復雜�����。
對于生物制品而言���,理想的注射器針筒應該降低硅油的用量,因為硅油能引起多種蛋白質的聚集���。研究表明蛋白質的聚集水平與硅油含量成正比�����。
在大多數(shù)玻璃注射器針筒生產時�����,使用鎢探針在注射器尖端形成流體通道���,可能會殘留氧化鎢蒸汽和鎢顆粒���。已經確定可溶性鎢殘留是引起臨床批次的α重組人腎紅細胞生成素和α螺旋蛋白高水平異常聚集的根本原因。
注射器生產商已經專門為生物制品設計了PFS系統(tǒng)�����,這些產品鎢殘留量較低��,如BD公司的用于生物技術的Hypak™玻璃注射器和Sterifill™ COP注射器���。Schott syriQ®的玻璃固定針注射器和West Pharma Crystal Zenith COP固定針注射器均不含鎢。
隨著可以選擇注射器針筒結構�����、硅樹脂含量和鎢含量���,PFS系統(tǒng)的選擇變得復雜�����。使用較新的PFS系統(tǒng)會增加成本���,因此需要在最終確定處方之前通過實驗評估PFS對產品質量存在的潛在影響���,并平衡質量和成本。
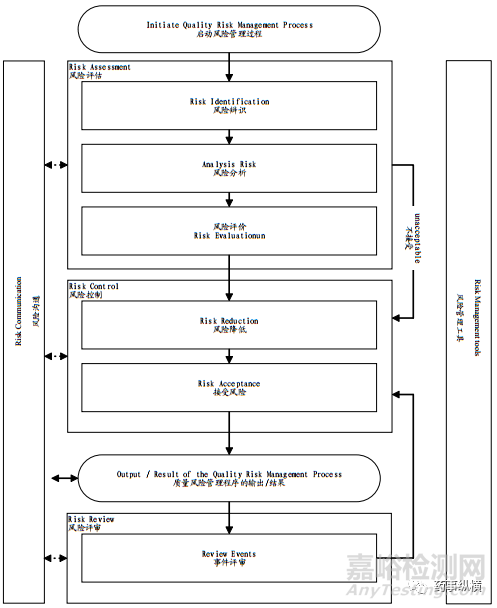
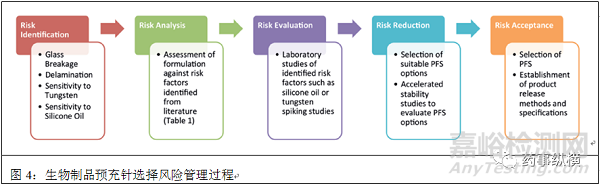
ICH Q9質量風險管理(圖2)中風險管理流程可用于評估藥物處方和PFS的相容性�����。第一步-風險識別�����,可以擴展到公司管線中的大多數(shù)肽類���、蛋白質和mAb產品�����。建議對不相容的風險進行評估��,包括1)玻璃分層�����,2)對鎢的敏感性和3)硅油引起的聚集�����;第二步-風險分析��,可以通過文獻調研完成��。
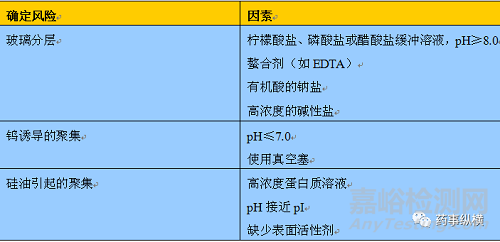
近年來���,已有玻璃分層或玻璃顆粒從容器內表面剝落導致產品召回的案例��。玻璃分層不是即刻顯現(xiàn)的,通常會在穩(wěn)定性樣品中發(fā)生��,特別是高溫條件下放置的樣品��。已知的處方風險因素包括pH≥8.0的藥品�����;醋酸鹽���、檸檬酸鹽和磷酸鹽緩沖溶液的存在���;EDTA等螯合劑的存在�����;有機酸的鈉鹽的存在以及高濃度的堿性鹽�����。終端滅菌也存在風險�����,但不適用于生物制品���。
玻璃的化學成分和生產工藝-特別是形成和退火也會影響玻璃分層。加熱速率���、最高溫度���、退火時間和溫度等因素都會引起玻璃耐用性的變化。
PFS的生產過程不同于小瓶注射劑�����,在生產期間降低了注射器針筒的接觸面積。在一項比較使用小瓶和PFS的處方研究中���,得出的結論是大多數(shù)測試條件下PFS優(yōu)于小瓶���,并且對于其他測試條件具有相同的性能。檸檬酸鹽或磷酸鹽緩沖液的存在可能導致釋放元素雜質�����。PFS沒有召回或分層報告���,表明使用PFS不存在重大風險�����。
已有多篇文獻報道了鎢誘導蛋白質聚集。用鎢沉淀mAb的研究表明在pH5.0的條件下鎢誘導其快速凝聚���,但在pH>6.0條件下處方中蛋白質聚集的風險較低���,因為較高pH條件會抑制鎢聚陰離子的形成。在pH7.0的重組人腎紅細胞生成素緩沖溶液中加入鎢針提取物�����,在25℃條件下儲存6個月后檢測到少量的聚集體。pH 4.0的α螺旋蛋白質制劑對鎢誘導的聚集敏感性研究��,確定了使用真空塞子增加了溶液中鎢的殘留量��。真空塞子除去了漏斗區(qū)域和產品之間的氣體�����,將溶液暴露于注射器中富含鎢的區(qū)域���,從而導致了蛋白質的聚集��。
在溶液中加入硅油以及通過比較硅化注射器中的溶液與非硅化注射器進行硅油-蛋白質相互作用的研究���。全面研究處方因素的影響,關于硅油引起蛋白質聚集的機制研究尚未完成���,但可以幫助研發(fā)人員確定一些風險因素���。
硅油引起的聚集最有可能發(fā)生在蛋白質的飽和溶液中。在針對多種抗SEB mAb研究中�����,僅在pH接近pI和振搖后才觀察到蛋白質聚集。在IgG1模型的研究中��,含0.01%的吐溫20的溶液在攪拌過程中能夠抑制硅油誘導的蛋白質聚集��。該研究的作者推測表面活性劑與蛋白質分子競爭吸附油-水���、空氣-水和油-空氣-水的相界面�����。同樣的研究表明蔗糖能夠部分抑制硅油誘導的蛋白質聚集��。
另一種理論是蔗糖增加了硅膠液滴的形成速度��,可能降低了油水界面面積���,但需要進一步研究來了解蔗糖是否有對硅油-蛋白質相互作用產生影響。
PFS選擇的風險分析匯總在表1中�����。在分析處方因素后���,該工藝轉向風險評估���。在具有多種玻璃分層風險因素的處方中,進行實驗對風險評估需要延長穩(wěn)定性研究的時間���。在這種情況下可能會面臨風險��,建議考慮使用共聚物注射器���。
蛋白質對鎢的敏感性可以通過簡單的摻加研究來評估。硅油誘導的蛋白質聚集風險評估可以通過硅油-水乳液摻加到處方中并使樣品聚集來進行研究�����。Badkar描述了詳細的試驗研究���。所引用的許多文獻都依賴之前發(fā)表的流動成像技術�����。流動成像技術既可以對顆粒進行計數(shù)��,也可以對顆粒形態(tài)的進行評估��。功能強大的軟件允許根據粒子的形狀對粒子進行分類��。硅油滴具有特征性的球形外觀��,具有光中心和朝向球體外部的增加的對比度(圖3)���,這允許流動成像軟件系統(tǒng)識別較小的硅油顆粒��。流動成像技術還可以識別與硅油滴結合的蛋白質聚集體��。
使用溶液摻加研究進行風險評估之后��,可以通過選擇注射器特性(如超低硅樹脂��、交聯(lián)硅樹脂或無硅樹脂產品)來降低風險�����。在進行最終選擇之前�����,建議使用手動注射器進行小型加速穩(wěn)定性研究���。樣品應在標準和加速條件下儲存。
對于生物制品���,至少應使用流動成像技術和產品穩(wěn)定性指示測試方法來評估亞可見聚集體的形成并評估產品穩(wěn)定性�����。此外��,加速穩(wěn)定性研究是確保注射器功能(特別是最大滑動力)不被產品改變并且滿足患者的需要��。
強烈建議評估多批PFS���。在內部未發(fā)表的研究中,使用流動成像技術發(fā)現(xiàn)不同批次的PFS中與硅油相關顆粒數(shù)量存在顯著差異�����。應在選擇容器密封蓋時啟動對可提取物/可浸出物的研究�����。風險管理流程(圖4)最后選擇了PFS��。通常定期對產品進行不同批次的檢測和供應商進行持續(xù)監(jiān)控,以便通知和評估任何注射器生產變化對于產品質量的重要性���。
生物制品的復雜要求推動了預充針技術的創(chuàng)新��,這為產品開發(fā)團隊提供了廣泛的選擇�����。雖然新的注射器選擇可能會增加產品的成本�����,但評估特定處方不穩(wěn)定性和組件的風險應該平衡質量�����、安全性���、成本。ICH Q9質量風險管理提供的框架可用于創(chuàng)建PFS容器選擇的有效流程�����。