歐洲醫(yī)學(xué)作家協(xié)會(EMMA)是于1989年成立的非營利性組織����,致力于支持及培訓(xùn)歐洲醫(yī)學(xué)傳播者的專業(yè)人員。EMMA會定期發(fā)布期刊�,分享藥品、獸藥����、醫(yī)療器械等最新生物醫(yī)藥相關(guān)的法規(guī)見解,今天就為大家分享今年6月期刊中醫(yī)療器械板塊的文章<聚焦醫(yī)療器械監(jiān)管下的類似器械>一文,共同拓展思路���,更好完成CE技術(shù)文檔的編制�。
本文章基于MDR法規(guī)和MDCG小組發(fā)布指南文件�,評估了類似器械在臨床文件中的潛力,如臨床評估計(jì)劃(CEP)����、臨床評估報(bào)告(CER)和上市后臨床跟蹤評估(PMCF)文件。從類似器械的概念開始����,文章介紹了如何識別類似器械,使用類似器械數(shù)據(jù)�,并將這些知識應(yīng)用于臨床文檔。
了解類似器械-similar devices
在MDR Article 2(7)中,類似器械(similar devices)屬于相同的通用器械組���,其定義為“一組器械具有相同或類似的預(yù)期目的或共性技術(shù)���,允許它們以不反映特定特征的通用方式進(jìn)行分類”。
簡而言之�,任何具有類似或相同預(yù)期目的或基于共同技術(shù)的器械都可以作為類似器械,而無需對技術(shù)����、生物學(xué)和臨床特征進(jìn)行詳盡的演示,這些都是聲稱等同的必要條件�。類似器械和等同器械之間的另一個關(guān)鍵區(qū)別是,對于類似器械����,制造商不需要“有足夠的權(quán)限訪問與設(shè)備有關(guān)的數(shù)據(jù)……”。因此����,聲明相似性比聲明等價性更直接�。
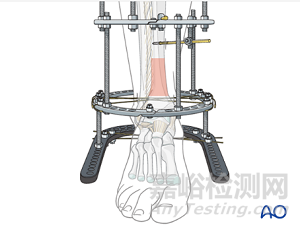
以Ilizarov lower extremity ring external fixator(下肢環(huán)形固定器)為例子,使用剛性棒���、銷釘和連接器通過皮膚插入骨頭以穩(wěn)定骨折���,上述定義可以翻譯為:
- "相同或類似預(yù)期用途":用于固定骨折的上肢或下肢的各種醫(yī)療器械
-"技術(shù)共性":任何外固定架
需要提及的一個重要細(xì)節(jié)是在MDR 定義的兩個元素之間使用OR(而不是AND)����,這使得它們在理論上是互斥的�。在臨床文件的準(zhǔn)備和審查過程中,如何將其用于實(shí)踐仍有待觀察�。
使用類似器械數(shù)據(jù)
1.基于成熟技術(shù)(WETs)的遺留器械的類似器械數(shù)據(jù)
根據(jù)MDCG 2020-6,“重要的是要從上市前和上市后階段確定所有可用的臨床數(shù)據(jù)來源�。這將包括所有由制造商生成和保存的臨床數(shù)據(jù),以及等同或類似器械的臨床數(shù)據(jù)�。
類似器械可以提供“soft”數(shù)據(jù),其證據(jù)水平與最新技術(shù)水平(SOTA)提供的臨床證據(jù)大致相似���,但低于來自自己和/或同等器械的臨床數(shù)據(jù)(見MDCG 2020-6 Annex III)����。盡管如此���,制造商可以使用類似的器械數(shù)據(jù)來設(shè)定基準(zhǔn)值�,以評估自己器械的臨床性能和安全性����。CEP或PMCF計(jì)劃將是這一目的的偉大文件���。根據(jù)MDCG2020-6:
·“來自類似器械的數(shù)據(jù)可用于證明設(shè)計(jì)的普遍性、缺乏新穎性���、已知的安全性和通用器械組的性能概況等���。
·對于成熟的技術(shù),臨床評估可以基于來自類似器械的數(shù)據(jù)�,在第6.5 (e)段詳細(xì)說明的條件下。
·來自類似器械的數(shù)據(jù)對于確定正在評估的器械和類似器械是否屬于被認(rèn)為是“成熟技術(shù)(WET)”的器械組也很重要���。
2.臨床評價的類似器械數(shù)據(jù)不基于等效性
當(dāng)臨床評價不能基于等效性時����,制造商可以通過幾種方式使用類似器械數(shù)據(jù)�。根據(jù)MDCG 2020-5,類似器械可能在以下方面有用:
1)通過識別相關(guān)危害和臨床風(fēng)險(xiǎn)����,確保風(fēng)險(xiǎn)管理系統(tǒng)全面���。
2)了解最新技術(shù)水平�,疾病的自然過程和可供選擇的治療方案。
3)通過識別類似器械中存在特殊性能或安全問題的任何設(shè)計(jì)特征�,幫助確定臨床評估的范圍
4)為臨床研究設(shè)計(jì)或上市后臨床跟蹤設(shè)計(jì)和上市后監(jiān)測系統(tǒng)提供輸入。
5)基于與類似器械相關(guān)的已公布臨床數(shù)據(jù)���,確定預(yù)期臨床獲益的相關(guān)和指定臨床結(jié)果參數(shù)����。
6)定義被認(rèn)為有臨床意義的量化臨床獲益的最低要求����,和/或確定風(fēng)險(xiǎn)和不良事件的可接受發(fā)生率。
總之�,類似器械數(shù)據(jù)對所有類型的臨床評估都是有益的,包括那些基于自己的�、等同的或沒有臨床數(shù)據(jù)的評估。此外�,類似器械數(shù)據(jù)可用于臨床評估的上市前和上市后階段。最后���,類似器械數(shù)據(jù)可以進(jìn)一步支持基于WET的遺留器械���。
在臨床文獻(xiàn)中提供類似器械數(shù)據(jù)
根據(jù)MDR AnnexII 1.2(b)�,技術(shù)文件應(yīng)包括“在歐盟或國際市場上現(xiàn)有的已識別的類似器械的概述���,如果此類器械存在”���。類似地,MDCG 2020-13(臨床評價評估報(bào)告模板����,Part J)中提供的模板堅(jiān)持要求NB檢查類似的器械數(shù)據(jù)。因此���,制造商應(yīng)查找類似器械�,并在存在此類器械的技術(shù)文檔中識別并包括它們���。如果不存在這樣的器械(在特殊情況下���,如獨(dú)特的預(yù)期用途和技術(shù)),制造商可以在CER中清楚地說明這一點(diǎn)���,以預(yù)先管理審查員的期望����。
如果存在類似器械,下面的逐步方法可能有助于識別和評估這些器械����,并將其呈現(xiàn)在臨床文件中�。這遵循了CER的MEDDEV 2.7/1 revision 4結(jié)構(gòu)。請注意����,這不是一個詳盡的清單;有幾種方法可以使用,但超出了本文的范圍����。
1. 類似器械的識別和選擇(階段0,范圍確定)
a. 識別:作為一個制造商����,第一步是識別類似器械。必須強(qiáng)調(diào)的是���,識別類似器械很容易成為這個過程中最具挑戰(zhàn)性的一步�。制造商必須證明他們的選擇是基于科學(xué)合理的理由�,如器械的市場份額、可用數(shù)據(jù)的質(zhì)量和數(shù)量����、器械的已知安全和性能概況等�。
b.證明:一旦選擇了類似器械�,制造商必須證明他們的選擇是正確的,并解決為什么選擇5個而不是20個器械的問題�。這將包括嚴(yán)格遵守MDR 定義,即相同或類似的預(yù)期目的或技術(shù)共性以及MDCG 2020-7節(jié)E中提到的標(biāo)準(zhǔn)(產(chǎn)品名稱�、預(yù)期目的、預(yù)期用戶����、預(yù)期患者群體、醫(yī)療狀況和適應(yīng)癥)����。這必須在PMCF計(jì)劃層面完成,理想情況下也應(yīng)該在CEP或CER層面完成�。
2. 類似器械數(shù)據(jù)識別(階段1,相關(guān)數(shù)據(jù)識別)
一旦選擇了類似的器械����,這些器械上可用和/或已知的所有數(shù)據(jù)必須在臨床文獻(xiàn)中搜索和討論生產(chǎn)廠家。類似的器械數(shù)據(jù)源可能包括:
a.科學(xué)文獻(xiàn)���,包括同行評議的科學(xué)文章����、Cochrane系統(tǒng)綜述等。
b.上市后臨床隨訪研究
c.上市后監(jiān)測數(shù)據(jù)
d.登記和其他真實(shí)世界的證據(jù)
3.類似器械數(shù)據(jù)評估(第二階段���,相關(guān)數(shù)據(jù)評估)
這可以是可選的���。對于臨床數(shù)據(jù)�,類似的器械數(shù)據(jù)也可以評估其適用性和貢獻(xiàn)標(biāo)準(zhǔn)。
4. 類似器械數(shù)據(jù)分析(第三階段�,臨床數(shù)據(jù)分析)
a.類似器械數(shù)據(jù)必須在PMCF評估報(bào)告(PMCFER)層面進(jìn)行分析,最好也在CER層面進(jìn)行分析�。在PMCFER中,鼓勵制造商遵循MDCG 2020-8第d .5節(jié)����。在CER中,類似的器械數(shù)據(jù)可以與SOTA分開討論�,也可以作為SOTA的一部分討論?��;蛘?,類似的器械數(shù)據(jù)可以在一組獨(dú)立的文檔中討論���,這些文檔具有與臨床文檔的適當(dāng)接口�。
b.從類似器械數(shù)據(jù)中得出的結(jié)論應(yīng)用于更新風(fēng)險(xiǎn)管理和上市后監(jiān)督活動,包括PMCF���。
結(jié)論
根據(jù)MDR ����,制造商應(yīng)在其臨床文件中識別類似的器械并討論類似器械數(shù)據(jù)���,特別是CERs和PMCFER�。然而�,識別和選擇類似器械的過程并沒有很好地定義,因此給制造商提供了幾種可能的方法����。類似的器械數(shù)據(jù)預(yù)計(jì)將用于提供閾值/基準(zhǔn)值,可用于評估被評估器械的臨床安全性和性能概況���。這些數(shù)據(jù)不僅會加強(qiáng)臨床結(jié)論但也允許制造商做出重要決定前和后市場階段的臨床評估�。此外���,所有類型的臨床評估(基于自己的���、同等的或沒有臨床數(shù)據(jù))都可以從類似的器械中受益����。與整個臨床評價過程一樣�,類似器械數(shù)據(jù)也應(yīng)持續(xù)、系統(tǒng)地更新�。