1.前言
本文針對(duì)2023年上半年在中國境內(nèi)公示的注冊(cè)類藥物臨床試驗(yàn)數(shù)據(jù)進(jìn)行匯總與分析。數(shù)據(jù)參考“國家藥品審批中心藥物臨床試驗(yàn)登記與信息公示平臺(tái)”��,并結(jié)合藥研社TDC數(shù)據(jù)庫進(jìn)行了標(biāo)準(zhǔn)化�、結(jié)構(gòu)化的梳理和表達(dá)��。
回首是為了更好地前進(jìn)����。在進(jìn)行數(shù)據(jù)匯總與呈現(xiàn)時(shí),我們本著嚴(yán)謹(jǐn)?shù)膽B(tài)度����,希望給行業(yè)相關(guān)方呈現(xiàn)信息薈萃。通過年中盤點(diǎn)����,我們期望業(yè)界同仁從數(shù)據(jù)中獲益��,更好地助力我國新藥研發(fā)����。
2.試驗(yàn)相關(guān)情況
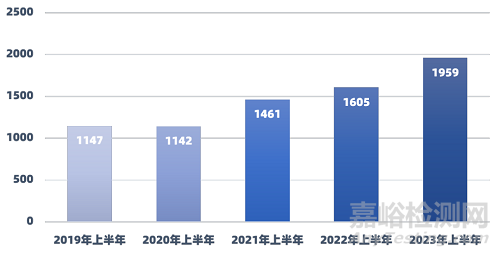
2.1 藥物臨床試驗(yàn)登記概況
2023年上半年,在CDE公示登記的藥物臨床試驗(yàn)共計(jì)1959個(gè)��,較2022年上半年同比增長22.06%�。
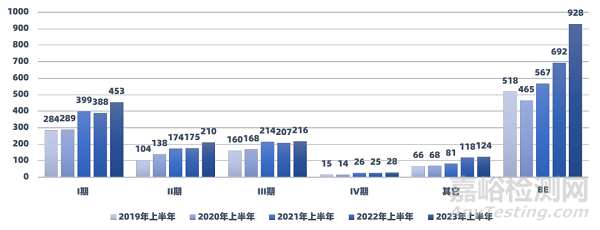
2.2 歷年試驗(yàn)分期對(duì)比
按照試驗(yàn)階段來看�,2023年上半年所有分期臨床試驗(yàn)的數(shù)量均出現(xiàn)同比上升,Ⅰ期 Ⅱ期 BE分期臨床試驗(yàn)數(shù)量同比上升較大����,BE試驗(yàn)同比增長最快,增長約34.1%��。
.
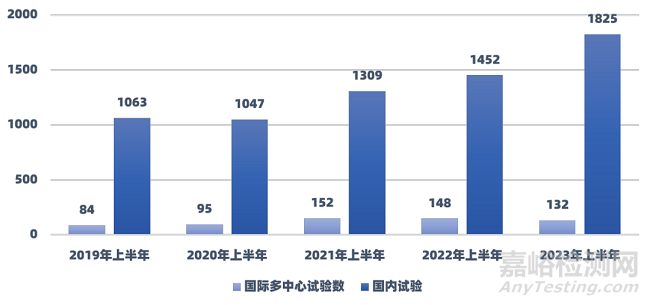
2.3 試驗(yàn)范圍分布情況
2021年上半年至2023年上半年國際多中心臨床試驗(yàn)數(shù)量同比均出現(xiàn)下降�,國內(nèi)試驗(yàn)同比保持上升�,2023年上半年,公示信息中的國內(nèi)試驗(yàn)數(shù)量達(dá)到1825個(gè)�。
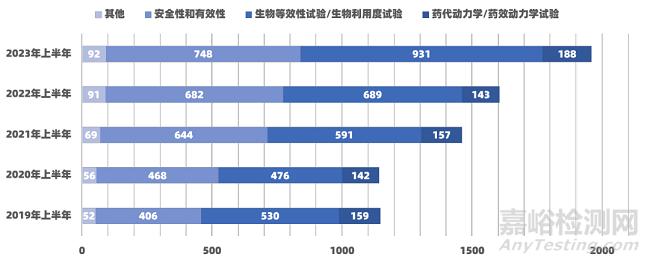
2.4 試驗(yàn)分類情況
從數(shù)量上看����,2023年上半年生物等效性試驗(yàn)/生物利用度試驗(yàn)931個(gè)、安全性和有效性試驗(yàn)748個(gè)�、藥代動(dòng)力學(xué)/藥效動(dòng)力學(xué)試驗(yàn)188個(gè),均同比上升��。
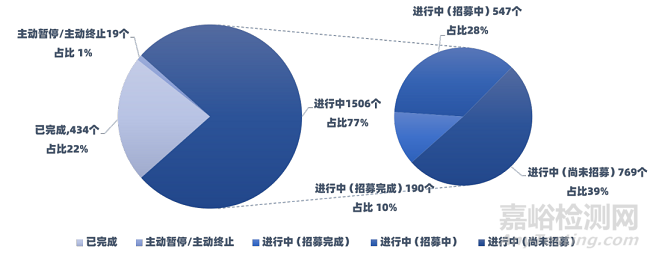
2.5 試驗(yàn)狀態(tài)
2023年上半年��,在CDE公示登記的1959個(gè)藥物臨床試驗(yàn)中��,截止2023年7月1日,有1506個(gè)試驗(yàn)正在進(jìn)行��,占比77%��;另有19個(gè)試驗(yàn)主動(dòng)暫停/主動(dòng)終止�,占比1%。
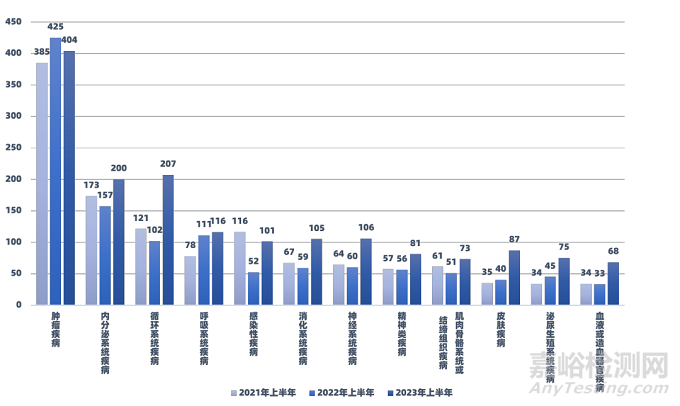
2.6 治療領(lǐng)域
從治療領(lǐng)域上來看�,2023年上半年在CDE公示的1959項(xiàng)藥物臨床試驗(yàn)中��,腫瘤疾病依舊是臨床研究的主要適應(yīng)癥��,共有404項(xiàng)�;緊隨其后的是內(nèi)分泌系統(tǒng)疾病、循環(huán)系統(tǒng)疾病和呼吸系統(tǒng)疾病��。其中循環(huán)系統(tǒng)疾病同比增長102.94%�。
3.試驗(yàn)研究藥物情況
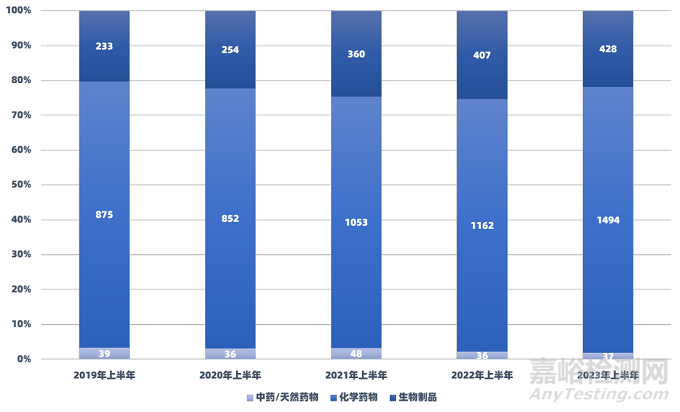
3.1 藥物類型
2023年上半年,在CDE公示登記的藥物臨床試驗(yàn)中����,化學(xué)藥物1494個(gè)��,占比76.26%����;生物制品428個(gè),占比21.84%��,較2022年有所下降����;中藥/天然藥物37個(gè),占比1.89%��,總數(shù)基本與去年持平�,在近5年注冊(cè)臨床試驗(yàn)中占比較低����。
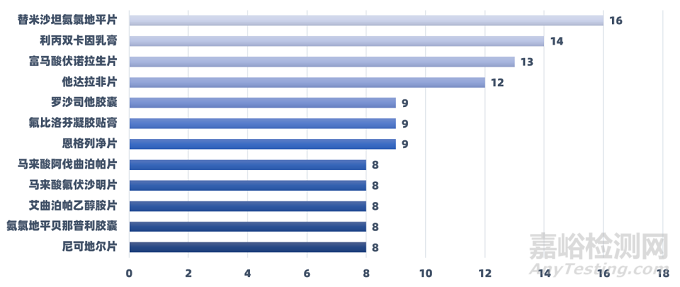
3.2 藥物品種
2023年上半年在CDE公示的藥物臨床登記品種中,共有12個(gè)藥物開展達(dá)到8項(xiàng)及以上臨床試驗(yàn)����。其中,替米沙坦氨氯地平片在2023年上半年共有16項(xiàng)臨床試驗(yàn)登記����,位列第一����。
(注:因?yàn)椴糠峙R床試驗(yàn)對(duì)藥物名稱備案沒有嚴(yán)格標(biāo)準(zhǔn),或者對(duì)新藥有保密保護(hù)行為����,故部分藥物名稱的數(shù)量可能存在些許誤差����,本數(shù)據(jù)僅統(tǒng)計(jì)同一藥物名稱的試驗(yàn)數(shù)量。)
4.結(jié)語
本文整理了2023年上半年在中國境內(nèi)公示的注冊(cè)類藥物臨床試驗(yàn)數(shù)據(jù)����,并對(duì)數(shù)據(jù)進(jìn)行了匯總與分析。源數(shù)據(jù)參考“國家藥品審批中心藥物臨床試驗(yàn)登記與信息公示平臺(tái)”(以下簡稱“CDE試驗(yàn)平臺(tái)”)��,臨床試驗(yàn)公示年份參考在CDE試驗(yàn)平臺(tái)中登記字段“首次公示日期”來判斷��。同時(shí)�,結(jié)合藥研社TDC數(shù)據(jù)庫對(duì)以上數(shù)據(jù)進(jìn)行了標(biāo)準(zhǔn)化和結(jié)構(gòu)化的梳理和表達(dá),以期呈現(xiàn)更為精確��、更具參考價(jià)值的內(nèi)容����。

 .
.