編者按:近年來,新分子療法成為醫(yī)藥產(chǎn)業(yè)的關(guān)注焦點���,為這個行業(yè)帶來了革命性的創(chuàng)新及無限的可能性���。這些前沿療法不僅在治療罕見疾病方面表現(xiàn)出驚人的潛力,同時也為一些常見疾病開啟了嶄新的治療路徑��。為了讓讀者更深入地了解這個創(chuàng)新領(lǐng)域�����,本文研究了近期研發(fā)投入最為活躍的十大藥企的產(chǎn)品管線�����,深度探討它們的新分子研發(fā)管線布局及其最新進展��,以期為大家展示新分子療法如何塑造醫(yī)療行業(yè)的未來格局�����。
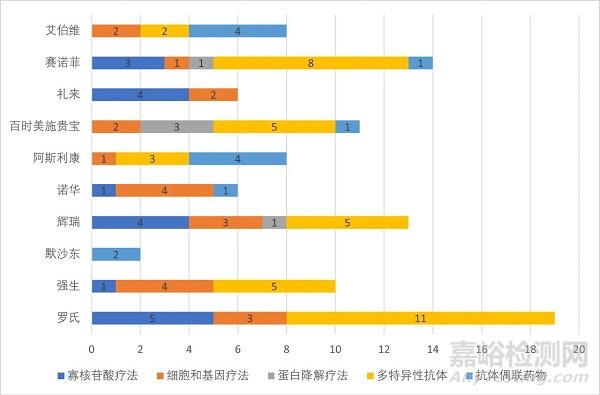
▲2022年研發(fā)投入最多的十家藥企新分子療法管線布局(藥明康德內(nèi)容團隊制圖)
1986年��,美國FDA批準了首個單克隆抗體。現(xiàn)如今�����,已有100多種抗體類藥物獲批上市���。隨著抗體發(fā)現(xiàn)的障礙不斷減少��,生物技術(shù)人員和科學(xué)家們都已意識到���,這類生物制品肯定會變得越來越多樣化。
傳統(tǒng)的單克隆抗體具有精確結(jié)合目標抗原并中和或促進其活性的能力���,但它們都是單特異性的�����,即兩個抗原結(jié)合點都結(jié)合到同一個抗原表位���。然而,大多數(shù)病理生理條件都具有多方面的復(fù)雜性�����,因此比起僅針對一個表位/抗原,同時靶向��、阻斷或抑制多個表位/抗原的多特異性抗體能夠同時與多個抗原相結(jié)合�����,從而探索單特異性抗體無法觸及的治療機會���。近年來,多特異性抗體治療模式已成為了抗體領(lǐng)域的后起之秀�����,這一新趨勢也推動了多特異性抗體的工程化設(shè)計和開發(fā)�����,為治療各種疾病提供了更多可能性���。
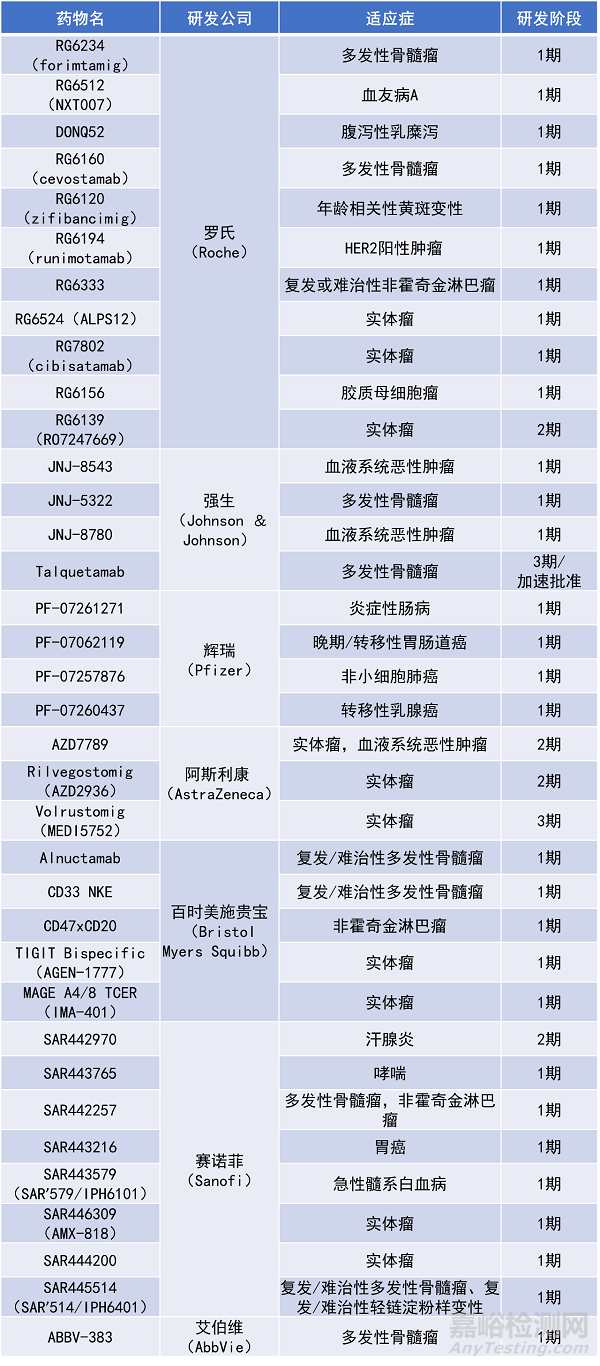
▲2022年研發(fā)投入最多的十家藥企旗下的多特異性抗體療法(藥明康德內(nèi)容團隊制圖)
2022年在研發(fā)上投入最多的十家藥企中�����,共有36款多特異性抗體處于臨床開發(fā)階段�����,其中30款針對的是血液腫瘤或?qū)嶓w瘤�����,針對非癌癥適應(yīng)癥的多特異性抗體為6款��。根據(jù)這些多特異性抗體所處的臨床階段進行劃分���,絕大多數(shù)尚處于早期臨床階段,共有30款處于1期臨床階段���,4款處于2期臨床階段��,還有2款已處于3期臨床階段,其中1項已獲得FDA的加速批準��。在這篇文章中�����,我們將根據(jù)這些在研療法的適應(yīng)癥和所處臨床階段為大家進行介紹�����。
血液腫瘤
藥物:talquetamab
強生旗下楊森(Janssen)公司與Genmab開發(fā)的talquetamab是一款皮下注射的“first-in-class”的雙特異性抗體���,同時靶向GPRC5D與CD3分子��,其中GPRC5D是表達在多發(fā)性骨髓瘤(MM)細胞上的靶標�����,其表達不會隨著時間而減少,而CD3則是T細胞受體�����,與活化T細胞有關(guān)�����。
2022年年底��,楊森基于talquetamab治療復(fù)發(fā)或難治性MM的1/2期臨床試驗的數(shù)據(jù)��,完成了上市申請的遞交���,并在今年8月獲得美國FDA的加速批準。此療法已于2021年在中國啟動臨床1/2期試驗���。
藥物:AZD7789
AZD7789是阿斯利康管線中一款抗PD-1/TIM3雙特異性抗體,擬開發(fā)治療實體瘤和血液系統(tǒng)惡性腫瘤�����。PD-1是程序性細胞死亡受體���,PD-1/PD-L1信號通路在腫瘤免疫的逃逸中扮演著重要角色。TIM-3是一種負調(diào)控的免疫檢查點���,存在于不同類型的免疫細胞中。TIM-3受體多在免疫細胞和髓系白血病細胞表面表達�����,其水平與急性髓系白血病和骨髓增生異常綜合癥的嚴重程度相關(guān)�����。
根據(jù)ClinicalTrials.gov網(wǎng)站��,AZD7789目前正在開展1/2期開放標簽�����、劑量遞增和擴展研究,評估該藥治療非小細胞肺癌和經(jīng)典霍奇金淋巴瘤的安全性��、藥代動力學(xué)和療效���。2022年12月,AZD7789在中國獲批開展針對非小細胞肺癌的臨床試驗���。
除了以上兩款臨床進展較快的多特異性抗體,針對血液腫瘤的在研多特異性抗體有13款處于1期臨床階段�����,其中有8款針對MM這一適應(yīng)癥�����。
藥物:RG6234(forimtamig)
RG6234是羅氏管線中一款潛在“best-in-class”的靶向新興靶點GPRC5D的T細胞銜接雙特異性抗體��。它攜帶兩個靶向GPRC5D的蛋白域和一個靶向CD3的蛋白域��。GPRC5D是G蛋白偶聯(lián)受體家族C組5成員D,在MM細胞中特異性高表達��,并且與不良預(yù)后因子相關(guān)�����,不過它幾乎不在正常組織上表達��,因此GPRC5D靶向療法有望為MM患者帶來新的臨床獲益。該候選療法能夠?qū)細胞募集到腫瘤周圍���,進而引發(fā)抗腫瘤免疫反應(yīng)�����。
此前�����,RG6234已在針對接受過多種前期治療的的復(fù)發(fā)/難治性MM患者的1期臨床試驗中���,取得良好的療效和可控的安全性��。該療法單藥治療的總緩解率(ORR)達到71.4%���,其中52.4%的患者達到非常好的部分緩解。近期���,羅氏在中國遞交了RG6234的臨床試驗申請,并獲得受理��。
藥物:RG6160(cevostamab)
羅氏在該公司2022年的醫(yī)藥日(Pharma Day 2022)活動中表示�����,RG6160是首個針對FcRH5的靶向療法��。FcRH5受體在所有骨髓瘤細胞中表達�����,而且在骨髓瘤細胞和正常漿細胞中的表達水平高于正常B細胞。RG6160通過與T細胞表面的CD3受體結(jié)合���,將T細胞募集到MM細胞周圍���,激活它們殺死骨髓瘤細胞。在治療復(fù)發(fā)/難治性MM的1期臨床試驗中��,RG6160的ORR為57%���,33%的患者達到非常好的部分緩解�����。
藥物:Alnuctamab
Alnuctamab是百時美施貴寶管線中一款靶向BCMA和CD3雙特異性抗體���。在2022年美國血液學(xué)會(ASH)年會上,該公司公布了alnuctamab治療復(fù)發(fā)/難治性MM患者的最新臨床1期數(shù)據(jù)���。Alnuctamab的皮下注射劑與靜脈注射劑相較���,其安全性有顯著改善,所造成的細胞因子釋放綜合征(CRS)多屬于低級別,使得在劑量遞增試驗中可使用較高劑量的抗體�����。靜脈與皮下注射的alnuctamab皆展現(xiàn)出色療效��,接受皮下注射alnuctamab患者的ORR為53%(36/68)��。
藥物:SAR442257
SAR442257是賽諾菲基于其三特異性T細胞激活平臺開發(fā)的靶向CD38的三特異性抗體��。該候選療法除了與CD3受體結(jié)合�����,還攜帶了與共刺激受體CD28結(jié)合的蛋白域��,同時激活CD28信號通路可以促進激活后T細胞的生存以及產(chǎn)生“T細胞記憶”��。同時���,CD28還在多種骨髓瘤細胞和血液癌癥細胞表面表達,這種三特異性抗體有可能通過靶向腫瘤細胞表面表達的兩種不同靶點來改善對腫瘤細胞的靶向作用��。
在體外試驗中���,SAR442257表現(xiàn)出比CD38單克隆抗體高1000至1萬倍的骨髓瘤細胞殺傷活性���。這款三特異性抗體已經(jīng)進入臨床試驗階段�����,治療復(fù)發(fā)/難治性MM和非霍奇金淋巴瘤(NHL)患者�����。
藥物:SAR445514(SAR’514/IPH6401)
SAR445514是賽諾菲與Innate Pharma合作開發(fā)的靶向BCMA���、NKp46、CD16三功能NK細胞接合器��。SAR445514能夠通過激活受體NKp46和CD16吸引NK細胞殺死腫瘤細胞�����。該候選療法目前正處于針對復(fù)發(fā)/難治性MM和復(fù)發(fā)/難治性輕鏈淀粉樣變性的首次人體臨床試驗中�����,并于今年7月完成了首例患者給藥�����。
藥物:ABBV-383
ABBV-383是艾伯維臨床管線中的一款靶向BCMA和CD3的雙特異性抗體,目前正處于針對復(fù)發(fā)/難治性MM的1期臨床研究中��。此前公布的臨床結(jié)果顯示�����,ABBV-383在復(fù)發(fā)/難治性MM患者中的耐受性良好���,劑量≥40 mg時的ORR為68%�����,表明這種新型療法在先前接受過多線治療的患者中具有良好的初步抗腫瘤活性��,值得進一步進行臨床評估�����。
藥物:JNJ-5322�����、CD33 NKE
JNJ-5322是強生臨床管線中的一款三特異性抗體,CD33 NKE是百時美施貴寶開發(fā)的一款靶向CD33的多特異性抗體,這兩款候選療法均針對MM���,處于1期臨床階段��。目前關(guān)于這兩款療法的公開信息并不多。
除MM外���,針對血液腫瘤開發(fā)的多特異性抗體的另一大適應(yīng)癥為NHL�����,除了上文中已提到的賽諾菲公司的SAR442257���,還有羅氏的RG6333���、百時美施貴寶的一款CD47xCD20雙特異性抗體以及強生的雙特異性抗體JNJ-8780正針對這一適應(yīng)癥開展1期臨床試驗���。
藥物:RG6333、CD47xCD20
RG6333是一種具有不同作用機制的T細胞共刺激受體激動劑���,能夠?qū)邢駽D19的蛋白域和激活共刺激受體CD28的蛋白域連接在一起。在小鼠模型中�����,RG6333與靶向CD20和CD3的T細胞銜接雙特異性抗體聯(lián)用��,已經(jīng)表現(xiàn)出更強的T細胞活性。目前���,RG6333在1期臨床試驗中與glofitamab聯(lián)用���,治療復(fù)發(fā)/難治性NHL患者。
目前���,關(guān)于百時美施貴寶CD47xCD20雙特異性抗體的公開信息并不多�����。
藥物:JNJ-8780��、JNJ-8543
JNJ-8780和JNJ-8543是強生臨床管線中兩款針對血液系統(tǒng)惡性腫瘤開發(fā)的多特異性抗體��。JNJ-8780是楊森與Teneobio共同開發(fā)的CD3/CD22雙特異性抗體���,用于治療B細胞淋巴惡性腫瘤,包括NHL和慢性淋巴細胞白血?�。–LL)���。JNJ-8543是一種皮下給藥的T細胞重定向三特異性抗體��,能識別T淋巴細胞上的CD3�����、成熟健康和惡性B淋巴細胞上的CD20表面抗原���,以及CD79b,用于治療包括CLL��、淋巴瘤在內(nèi)的多種血液系統(tǒng)惡性腫瘤���。這兩款候選療法目前正處于1期臨床階段���,關(guān)于它們的其他公開信息并不多�����。
藥物:SAR443579(SAR'579/IPH6101)
SAR443579是賽諾菲與Innate Pharma合作開發(fā)的基于ANKET平臺設(shè)計的靶向CD123的三功能NKp46×CD16 NK細胞銜接蛋白���,用于治療急性髓系白血?����。ˋML)�����。臨床前研究表明��,AML的原始細胞(blasts)上CD64的表達使其對抗CD123抗體產(chǎn)生耐藥性,而SAR443579通過與CD16a和NKp46的結(jié)合將NK細胞重定向到癌癥靶點���,可以規(guī)避這種耐藥性���。此外�����,SAR443579僅在AML細胞存在時誘導(dǎo)NK細胞活化和細胞因子分泌。
近期���,賽諾菲公布了SAR443579的1/2期臨床試驗結(jié)果。初步數(shù)據(jù)顯示��,該候選療法的耐受性良好,并在1 mg/kg的最高劑量下使8名復(fù)發(fā)/難治性AML患者中的3名患者達到了完全緩解��。2023年5月底��,SAR443579在中國獲批開展臨床試驗,擬開發(fā)用于治療12歲及以上復(fù)發(fā)/難治性惡性血液病��。
實體瘤
圖片來源:123RF
藥物:RG6194(runimotamab)
Runimotamab是由羅氏旗下基因泰克公司開發(fā)的一種T細胞接合器���,可同時靶向癌細胞上的HER2和T細胞上的CD3�����。這種雙重靶向的作用機制旨在讓T細胞攻擊表達HER2的癌細胞���。
當前�����,runimotamab正在臨床1期試驗中測試其對于局部晚期或轉(zhuǎn)移性HER2陽性的癌癥患者的安全性���、耐受性和藥代動力學(xué)特征�����,尚未有試驗數(shù)據(jù)公布���。
藥物:RG6524(ALPS12),RG7802(cibisatamab)��,RG6156���,RG6139(RO7247669)
上述4款療法均為羅氏旗下針對實體瘤研發(fā)的多特異性抗體療法。
RG6524是一種由羅氏旗下的Chugai Pharmaceutical開發(fā)的三特異性抗體,可同時靶向DLL3��、CD3和CD137。目前�����,該藥物已進入1期臨床開發(fā)階段��。
RG7802旨在同時靶向腫瘤細胞上表達的癌胚抗原(CEA)和T細胞上的CD3受體���,從而觸發(fā)T細胞激活�����、遷移和腫瘤殺傷���。RG7802正在1期臨床試驗中接受測試���,以評估其作為單一藥物或者與阿替利珠單抗聯(lián)合使用治療CEA陽性的實體瘤的效果��。
RG6156是一款雙特異性抗體,可結(jié)合腫瘤細胞上的表皮生長因子受體III型突變體(EGFRvIII)和T細胞上的CD3��。EGFRvIII是一種致癌突變�����,約在30%的膠質(zhì)母細胞瘤中表達���。該藥物針對膠質(zhì)母細胞瘤的適應(yīng)癥正在1期臨床開發(fā)階段�����。
RG6139是一款靶向PD-1和LAG-3的雙特異性抗體�����,通過同時阻斷PD-1和LAG-3介導(dǎo)的檢查點信號通路���,激活T細胞的抗癌反應(yīng)。它能夠優(yōu)先靶向?qū)δ[瘤產(chǎn)生反應(yīng)的腫瘤浸潤淋巴細胞(TIL)��,減少與調(diào)節(jié)性T細胞的結(jié)合�����,從而避免免疫抑制效果�����。這款療法已經(jīng)完成了在實體瘤患者中進行的1期臨床試驗,目前正在進行2期研究���,旨在評估其治療乳腺癌��、非小細胞肺癌等多種實體瘤的效果���。
藥物:PF-07062119,PF-07257876���,PF-07260437
輝瑞旗下共有3款在研雙特異性抗體療法進入臨床開發(fā)階段�����。
PF-07062119可同時靶向GUCY2c和CD3兩個靶點。在臨床前實驗中��,PF-07062119在多種人源結(jié)直腸癌異種移植腫瘤模型中顯示出強大的T細胞活性和體內(nèi)療效���。這款藥物的活性在與PD-1/PD-L1抑制劑聯(lián)合或與抗血管生成療法聯(lián)合時進一步增強���。該療法目前正在1期臨床開發(fā)階段�����,用于治療晚期/轉(zhuǎn)移性胃腸道癌���。
PF-07257876是一款針對CD47和PD-L1的雙特異性抗體,適用于實體腫瘤的治療��。當前,該療法針對非小細胞肺癌的適應(yīng)癥正在1期臨床試驗中進行測試。根據(jù)最新發(fā)布的結(jié)果��,PF-07257876在非小細胞肺癌患者中的耐受性良好,毒性可控��。其中,外周血中CD47和PD-L1的靶點參與度很高�����。
PF-07260437可針對B7-H4和CD3兩個靶點發(fā)揮作用�����。當前�����,該藥物正在1期臨床研究中進行測試�����,以評估其對于18歲以上晚期或轉(zhuǎn)移性乳腺癌���、卵巢癌或子宮內(nèi)膜癌患者的安全性���、耐受性���、藥代動力學(xué)�����、藥效學(xué)和抗腫瘤活性�����。
藥物:rilvegostomig(AZD2936)��,volrustomig(MEDI5752)
阿斯利康旗下兩款雙特異性抗體rilvegostomig和volrustomig均已進入2期臨床開發(fā)階段。
Rilvegostomig可同時靶向PD-1和TIGIT��,其治療Ⅲ期不可切除或Ⅳ期非小細胞肺癌患者的2期臨床試驗在2022年11月正式啟動��。阿斯利康在其2022年第4季度和全年財報中表示�����,rilvegostomig預(yù)計將在今年進入3期臨床試驗。
Volrustomig是一款靶向免疫檢查點PD-1和CTLA-4的雙特異性抗體���,目前正在臨床試驗中評估其對多種實體腫瘤的療效。其中�����,volrustomig針對非小細胞肺癌和局部晚期宮頸癌的適應(yīng)癥已進入3期臨床階段�����。
在針對非小細胞肺癌的一項1b/2期臨床試驗中��,患者在接受化療后,隨機接受volrustomig/化療組合���,或者獲批PD-1抗體/化療組合的治療�����。試驗結(jié)果顯示�����,在接受劑量為1500 mg(每3周一次)volrustomig治療的患者組中���,患者的中位緩解持續(xù)時間為20.5個月��,活性對照組為9.9個月。Volrustomig組的中位無進展生存期為15.1個月�����,活性對照組為8.9個月���。此外��,volrustomig組在總生存期方面也表現(xiàn)出優(yōu)勢。
藥物:TIGIT Bispecific(AGEN-1777)�����,MAGE A4/8 TCER (IMA-401)
AGEN-1777和IMA-401都是百時美施貴寶公司旗下的雙特異性抗體��,適用于實體瘤的治療��。
AGEN-1777可以特異性靶向TIGIT�����,同時還具有增強的Fc區(qū)域��,旨在通過靶向T細胞和NK細胞上表達的主要抑制性受體���,以提高抗腫瘤活性��。2021年5月�����,百時美施貴寶與Agenus達成協(xié)議���,百時美施貴寶獲得了AGEN-1777的全球獨家許可��。目前這款療法處于1期臨床開發(fā)階段��。
IMA-401是一款T細胞接合器���,其中一個結(jié)合區(qū)域靶向MAGEA4/8——這是一種在多種實體腫瘤中普遍存在的抗原;另一個區(qū)域可與T細胞結(jié)合并激活其活性�����。在臨床前概念驗證研究中��,IMA401顯示出了抗腫瘤活性�����,在包括患者來源的異種移植模型在內(nèi)的各種體內(nèi)腫瘤模型中實現(xiàn)了完全緩解���。2021年12月��,百時美施貴寶和Immatics公司簽訂了許可��、開發(fā)和商業(yè)化協(xié)議�����,共同推進IMA-401的開發(fā)�����。目前這款療法處于1期臨床開發(fā)階段���。
藥物:SAR443216�����,SAR446309(AMX-818),SAR444200
在實體瘤領(lǐng)域�����,賽諾菲共有3款多特異性抗體進入臨床開發(fā)階段�����。
SAR443216是一款三特異性抗體���,具有HER2���、CD3���、CD28三個結(jié)合位點。其中��,CD3的結(jié)合有助于將CD3陽性T細胞募集到表達HER2的腫瘤細胞附近�����;CD28的結(jié)合有助于T細胞的活化���,包括激活I(lǐng)L-2和NFκB通路���,后者可激活CD8陽性T細胞、自然殺傷細胞并且促進它們增殖的能力�����。公開資料顯示���,賽諾菲正在開展SAR443216針對HER2陽性實體瘤的1期劑量遞增和擴展臨床研究��,評估該藥皮下注射和靜脈注射兩種劑型針對不同類型腫瘤的初步療效和安全性�����,針對的適應(yīng)癥包括乳腺癌���、肺癌���、胃癌等等。
SAR446309(曾用名AMX-818)最初由Amunix公司研發(fā)���,是一款T細胞接合器�����,可靶向腫瘤細胞上的HER2并實現(xiàn)T細胞激活��。2021年,賽諾菲收購了Amunix公司的免疫腫瘤學(xué)管線��,將SAR446309納入自身產(chǎn)品管線���。目前該療法仍處于1期臨床開發(fā)階段��。
SAR444200是賽諾菲研發(fā)的一款抗GPC3/TCR納米抗體��,基于Nanobody技術(shù)開發(fā)而成��。其中���,GPC3(Glypican-3)是細胞膜表面的硫酸乙酰肝素糖蛋白��,在肝癌組織中高度表達�����,但在正常組織中幾乎很少或不表達��,屬于肝癌組織的高特異性靶點�����。GPC3通過結(jié)合Wnt���、成纖維細胞生長因子和胰島素樣生長因子等生長因子來調(diào)節(jié)細胞增殖信號,并在胚胎細胞的增殖和分化中發(fā)揮重要作用���。T細胞受體(TCR)是存在于T細胞表面的一種能夠識別和結(jié)合蛋白質(zhì)抗原的特異性受體���,為所有T細胞的特征性標志��。目前���,賽諾菲正在開展一項1/2期劑量遞增和擴展、開放標簽���、首次人體研究��,以評估SAR444200作為單一療法或與其他抗癌藥物聯(lián)合在至少18歲��、既往治療過轉(zhuǎn)移性惡性腫瘤的受試者中的安全性和有效性���。
非腫瘤相關(guān)
藥物:RG6512
RG6512是羅氏開發(fā)用于治療血友病A的新一代雙特異性抗體,靶向凝血因子X和凝血因子IXa�����。該候選療法可以將激活天然凝血級聯(lián)所需的凝血因子IXa和凝血因子X聚集在一起��,幫助血友病A患者恢復(fù)凝血功能��。根據(jù)羅氏財報�����,RG6512與FIX和FX形成三元復(fù)合物的能力顯著優(yōu)于該公司此前獲批的同靶點重磅雙特異性抗體Hemlibr��。目前該候選療法正處于1期臨床階段��,關(guān)于它的其他公開信息并不多��。
藥物:DONQ52
DONQ52是羅氏開發(fā)的一款雙特異性抗體�����,可針對HLADQ2.5/谷蛋白肽復(fù)合物發(fā)揮作用�����。該藥物通過中和T細胞受體和HLADQ2.5/谷蛋白肽復(fù)合物的相互作用直接抑制谷蛋白依賴性T細胞激活���。根據(jù)羅氏公司官網(wǎng)介紹��,DONQ52的靶標涵蓋了超過25種谷蛋白衍生肽���,包括所有介導(dǎo)了乳糜瀉的免疫顯性谷蛋白肽。
目前���,DONQ52正在1期臨床試驗中進行測試�����,以測試其在乳糜瀉患者中的安全性���、耐受性和藥代動力學(xué)特征�����。
藥物:RG6120(zifibancimig)
RG6120是羅氏開發(fā)的一種基于Fab分子結(jié)構(gòu)��、可同時靶向血管內(nèi)皮生長因子(VEGF)和血管生成素-2(Angiopoietin-2)的雙特異性抗體���。這款療法的開發(fā)是基于羅氏的DutaFab技術(shù)平臺,并且可以與其端口遞送系統(tǒng)(Port Delivery System)相兼容�����。
RG6120正處于1期臨床開發(fā)階段���,其主要適應(yīng)癥為年齡相關(guān)性黃斑變性���,相關(guān)試驗數(shù)據(jù)尚未披露��。
藥物:PF-07261271
PF-07261271是輝瑞研發(fā)的一款針對炎癥性腸病的雙特異性抗體,可同時靶向TNFSF15和IL12的p40亞基兩個靶點��。這款療法正在1期臨床試驗中進行測試��,以了解其治療炎癥性腸病的安全性和效果���,目前尚無相關(guān)數(shù)據(jù)披露��。
藥物:SAR442970
SAR442970是一款靶向TNFα和OX40L的雙特異性抗體�����。目前�����,賽諾菲正在開展一項2期臨床試驗��,評估SAR442970與安慰劑相比���,治療化膿性汗腺炎的有效性和安全性。
藥物:SAR443765
SAR443765是賽諾菲臨床管線中的一款靶點為IL-13和TSLP的在研療法��,該療法目前正在針對哮喘的1期臨床試驗中進行測試,以評估其安全性���、耐受性和藥代動力學(xué)��。
小結(jié)
多特異性抗體療法的研發(fā)不僅映射出科學(xué)界對復(fù)雜疾病機制更為深刻的理解���,也體現(xiàn)了當前藥物研發(fā)正走向更為個體化和精準的趨勢。這些具有多重作用靶標的抗體預(yù)示著一種創(chuàng)新治療模式的誕生�����,它們能夠綜合干預(yù)多個病理途徑�����,為我們提供了一種更為全面和高效的治療方案��。
展望未來�����,我們期待著多特異性抗體能夠給醫(yī)療行業(yè)帶來革命性的變革�����,尤其是在治療一些目前尚無有效治療方法的疾病方面。同時���,我們也期待它們能夠為常見疾病提供更為全面和有效的治療方案��,從而使患者得到更為個體化和精準的治療。