摘 要 早期抗體藥物是鼠源單克隆抗體�,存在免疫原性強(qiáng)、半衰期短等問題�����。歷經(jīng)數(shù)十年的發(fā)展��,抗體藥物從最初的鼠源單抗�����,逐步發(fā)展為人鼠嵌合抗體��、人源化抗體及全人源化抗體�����。通過片段重組、位點(diǎn)修飾��、藥物偶聯(lián)等方法��,科研人員研發(fā)了包括抗體融合蛋白���、抗體偶聯(lián)藥物、雙特異性抗體�����、小分子抗體片段等形式多樣的抗體藥物�?�?贵w藥物在惡性腫瘤�、自身免疫病��、感染性疾病的治療上發(fā)揮重要作用��。通過對(duì)抗體藥物人源化歷程�����,不同類型的抗體結(jié)構(gòu)和特點(diǎn)����,以及抗體藥物在新型冠狀病毒肺炎治療中的應(yīng)用進(jìn)行綜述��,并對(duì)抗體藥物的發(fā)展前景進(jìn)行展望�����,以期為我國(guó)抗體藥物的研發(fā)提供參考��。
關(guān)鍵詞 抗體藥物;人源化���;抗體融合蛋白����;抗體偶聯(lián)藥物;雙特異性抗體���;小分子抗體片段;新型冠狀病毒肺炎
抗體藥國(guó)內(nèi)及全球研發(fā)概況
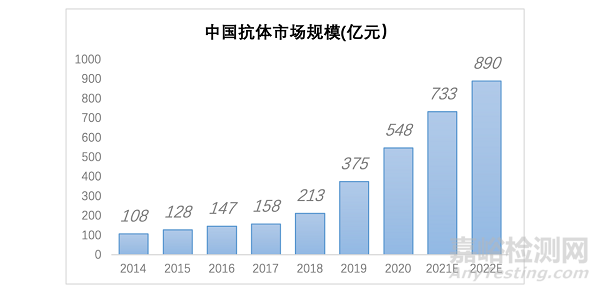
國(guó)內(nèi)抗體藥物雖然起步較晚���,但近些年國(guó)內(nèi)對(duì)抗體藥物的需求放量增長(zhǎng)�,市場(chǎng)迎來飛速發(fā)展。據(jù)統(tǒng)計(jì)����,中國(guó)2014年抗體藥物市場(chǎng)規(guī)模為108億元,2019年增至375億元(圖1)��。鑒于抗體藥物應(yīng)用廣泛�����,適用腫瘤���、自身免疫性疾病、神經(jīng)病學(xué)及骨質(zhì)疏松癥等不同的治療領(lǐng)域�����,預(yù)計(jì)2022年市場(chǎng)規(guī)模將擴(kuò)大至890億元。
圖1.中國(guó)抗體市場(chǎng)規(guī)模(億元)參考來源:中商情報(bào)網(wǎng)
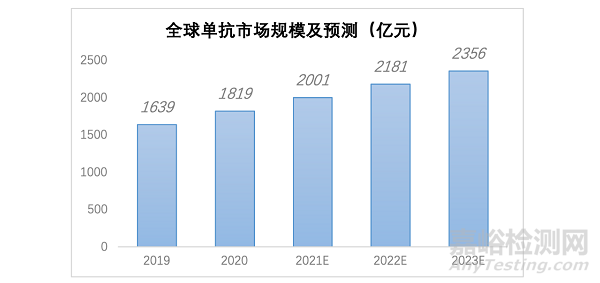
目前抗體藥物主要包括單克隆抗體(亦稱為裸單克隆抗體)��、雙特異性抗體及抗體藥物偶聯(lián)物(ADC��,亦稱為偶聯(lián)的單克隆抗體)��。其中��,單克隆抗體是研發(fā)最早、研究最為深入的抗體藥�����,具有較高的安全性與有效性�����。根據(jù)弗若斯特沙利文報(bào)告����,2018年全球單克隆抗體規(guī)模占全球生物藥和整體醫(yī)藥市場(chǎng)規(guī)模分別為 55.3%����、11.4%���。相較于全球單克隆抗體市場(chǎng),中國(guó)單克隆抗體市場(chǎng)尚處于起步階段�,2018年中國(guó)單克隆抗體市場(chǎng)在中國(guó)整體醫(yī)藥市場(chǎng)的比重僅約1.0%�����,遠(yuǎn)低于全球11.4%的水平(圖2)�����。
圖2.全球單抗市場(chǎng)規(guī)模及預(yù)測(cè)(億元)參考來源:中商情報(bào)網(wǎng)
從2017年開始,國(guó)家醫(yī)療保險(xiǎn)制度在單抗藥物覆蓋面顯著擴(kuò)大,這有利于提高國(guó)內(nèi)未來單抗處方的滲透率��。同時(shí),免疫治療產(chǎn)品如Opdivo����、Keytruda等PD-1抑制劑在中國(guó)相繼獲批,也將進(jìn)一步促進(jìn)中國(guó)單抗市場(chǎng)的擴(kuò)容��。數(shù)據(jù)顯示�����,預(yù)計(jì)到2024年,單抗市場(chǎng)將增長(zhǎng)到1,580億元人民幣��,2019年到2024年的年復(fù)合增長(zhǎng)率為40.6%����。
抗體藥物熱門靶點(diǎn)
目前抗體藥物研發(fā)熱點(diǎn)是免疫檢查點(diǎn)�����,這也是近年來廣為熟知的靶點(diǎn)。腫瘤細(xì)胞的免疫逃逸機(jī)制主要可歸結(jié)為三個(gè)方面:一是通過改變腫瘤相關(guān)抗原的表達(dá)水平或者降低MHC I類分子的表達(dá)來規(guī)避免疫細(xì)胞的識(shí)別����;二是通過釋放TGF-β、IL-10等免疫抑制因子形成抑制性的腫瘤微環(huán)境�����;三是通過調(diào)節(jié)腫瘤細(xì)胞表面的共刺激分子水平降低腫瘤致免疫能力�,從而有效避免對(duì)T細(xì)胞的激活�����。腫瘤免疫治療(Cancer Immunotherapy)的目的是克服腫瘤細(xì)胞的免疫逃逸機(jī)制�����,重建免疫系統(tǒng)對(duì)腫瘤細(xì)胞的識(shí)別和清除��。所謂免疫檢查點(diǎn)(Immune Checkpoint)���,即是控制T細(xì)胞免疫響應(yīng)的分子開關(guān),2011年全球首個(gè)免疫檢查點(diǎn)抗體伊匹單抗(Ipilimumab��,anti-CTLA-4)獲批上市���,正式開啟了腫瘤免疫治療的全新時(shí)代���。
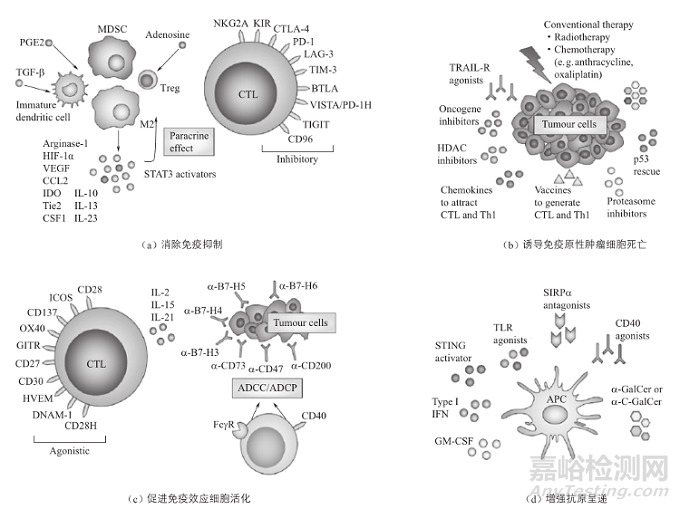
從作用機(jī)制來看�����,腫瘤免疫治療涉及四大策略(圖3):(a)消除免疫抑制�,代表性的靶點(diǎn)有CTLA-4、PD-1�����、LAG-3�、TIM-3���、TIGIT�����、CD96等免疫檢查點(diǎn)以及VEGF、CSF1��、TGF-β�����、IL-10�����、IL-34���、IL-35�、CCL2��、FGF等免疫抑制因子及受體��,靶向這類分子的抗體均為拮抗型。(b)誘導(dǎo)免疫原性腫瘤細(xì)胞死亡(Immunogenic Cancer-Cell Death)��,一些常規(guī)靶向治療制劑可劃歸此類����。(c)是促進(jìn)T細(xì)胞����、巨噬細(xì)胞和NK細(xì)胞等效應(yīng)細(xì)胞的活化,代表靶點(diǎn)有OX40�����、GITR、CD28��、CD47�����、CD137��、CD200����、B7-H3、B7-H4��、B7-H5��、B7-H6��、IL-15R�����、SIRPα/CD47和KIR等�。(d)增強(qiáng)APC細(xì)胞的抗原呈遞和輔助性����,進(jìn)而激活效應(yīng)細(xì)胞的功能,代表靶點(diǎn)有SIRPα����、CD40、STING�����、TLR等�。后兩類靶點(diǎn)因功能和作用機(jī)制不同����,可區(qū)分為拮抗劑或激動(dòng)劑。
圖3. 腫瘤免疫治療的四大策略
參考來源:www.biobusiness.com.cn 生物產(chǎn)業(yè)技術(shù)
雖然腫瘤免疫治療在腫瘤治療中已發(fā)展成獨(dú)立分支����,取得巨大成就���,但仍有部分技術(shù)問題亟待解決。比如需要提高用藥標(biāo)志物的有效率����、克服腫瘤微環(huán)境的免疫抑制問題��。針對(duì)該問題的策略是聯(lián)合應(yīng)用不同作用機(jī)制的免疫治療靶點(diǎn)抗體或聯(lián)用其他療法����,通過合理選擇靶點(diǎn)能達(dá)到協(xié)同治療的效果�。另外,能抑制免疫抑制性細(xì)胞進(jìn)入腫瘤內(nèi)部的創(chuàng)新靶點(diǎn)���,CD25、Gr-1���、CXCL12/CXCR4���、CSF1/CSF1R���、TGF-β、IL-10��、IL-35 和 EphA3等也是當(dāng)前研發(fā)熱點(diǎn)。
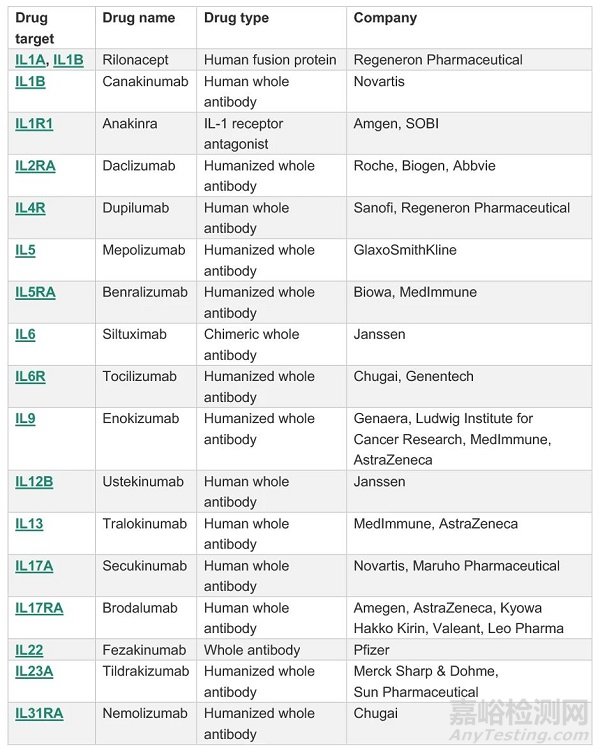
白介素類細(xì)胞因子是抗體藥另外的重要研發(fā)靶點(diǎn)����。白介素與多種疾病呈現(xiàn)廣泛的復(fù)雜關(guān)系,表現(xiàn)出“一種疾病與多種白介素分子相關(guān)��,一種白介素分子與多種疾病相關(guān)”的特點(diǎn)�����,這為以白介素及受體為靶點(diǎn)的藥物研發(fā)帶來巨大挑戰(zhàn)�����。以銀屑病為例�,已報(bào)道的相關(guān)白介素成員就有IL-1、IL-8��、IL-17����、IL-18、IL-19�、IL-20、IL-22��、IL-23、IL-24等��。在白介素抗體研發(fā)領(lǐng)域�,目前呈現(xiàn)兩種趨勢(shì)���,一是進(jìn)一步加深相關(guān)基礎(chǔ)領(lǐng)域的研究��,開發(fā)更多有效靶點(diǎn)��,二是研究聯(lián)合用藥及雙特異抗體聯(lián)用的治療方法����,為臨床用藥提供更多選擇��。下表為目前已上市或處于研發(fā)后期階段的主要白介素抗體藥(表1)。
表1.全球已上市或處于研發(fā)后期的白介素抗體藥
參考來源:www.sinobiological.com
除了上述熱門靶點(diǎn)外���,近年來針對(duì)PCSK9、CGRP/CGRP受體����、β淀粉樣蛋白等靶點(diǎn)開展的抗體藥研究也如火如荼,多個(gè)趨化因子受體(如CCR2���、CCR5、CXCR4)的相關(guān)抗體初露端倪���。同時(shí),針對(duì)如TNF-α�����、VEGF/VEGFR���、Her2、CD20等明星靶點(diǎn)的藥物研發(fā)持續(xù)升溫����,針對(duì)病原微生物及其毒素的抗體藥物研發(fā)也取得巨大進(jìn)步。
抗體藥物熱門技術(shù)
在熱門技術(shù)領(lǐng)域�����,近年來雙特異性抗體藥物的研發(fā)備受矚目��。此外����,兩種或兩種以上單克隆抗體的聯(lián)合療法、基于單抗治療與小分子靶向藥物和化療及ADC組合的療法也表現(xiàn)亮眼�����。
雙特異性抗體(bispecific antibodies����,bsAbs)是采用抗體工程和基因工程技術(shù)(或體外偶聯(lián))構(gòu)建的能夠特異性結(jié)合兩種抗原或兩個(gè)表位的重組抗體/抗體片段�����。目前應(yīng)用雙特異性抗體技術(shù)��,能為蛋白復(fù)合物連接�����、分子阻斷協(xié)同、免疫細(xì)胞募集�、分子遞送工作提供有力的技術(shù)支持。雙抗藥涉及的治療領(lǐng)域也在不斷拓展�����,包括腫瘤學(xué)��、自身免疫/炎癥性疾病����、傳染病和心血管疾病等。
從廣義來講����,bsAbs可分為三個(gè)主要的結(jié)構(gòu)類別:(1)缺乏Fc域的抗體片段(例如雙抗體和串聯(lián)單鏈可變片段);(2)抗體片段或替代支架蛋白融合到一個(gè)抗體����、抗體Fc區(qū)或人血清白蛋白,以增強(qiáng)其藥代動(dòng)力學(xué)(PK)特性和/或效價(jià)�����;(3)完全的IgG雙抗結(jié)構(gòu),有助于避免非天然抗體產(chǎn)生的免疫原性問題(圖4)����。
圖4.雙特異性抗體結(jié)構(gòu)示意
參考來源:Bispecific antibodies in IBD Review
雙特異性抗體可設(shè)計(jì)為能同時(shí)作用于兩種細(xì)胞類型的膜受體,能選擇性修改致病性免疫細(xì)胞的信號(hào)傳導(dǎo)路徑����。以炎癥性腸病(IBD)疾病為例,針對(duì)IL-23R + /IL-1R + T細(xì)胞和與IBD相關(guān)的先天淋巴細(xì)胞�����,通過優(yōu)先結(jié)合能表達(dá)兩種靶蛋白的細(xì)胞��,能實(shí)現(xiàn)目標(biāo)細(xì)胞或活性的高效選擇�����,這種方法也被用于開發(fā)MGF010�����,一種抑制B細(xì)胞的雙親和重定向bsAb,能激活自身免疫細(xì)胞活性�,治療炎癥性疾病��。
雙特異性抗體的技術(shù)瓶頸在于結(jié)構(gòu)調(diào)整成藥性�,包括免疫原性、藥代動(dòng)力學(xué)以及分子穩(wěn)定性��,未來技術(shù)發(fā)展也會(huì)從兼顧雙抗可制備性、成藥性和通用性等三方面入手��,解決上述問題的抗體藥將具有巨大市場(chǎng)價(jià)值和應(yīng)用價(jià)值����。
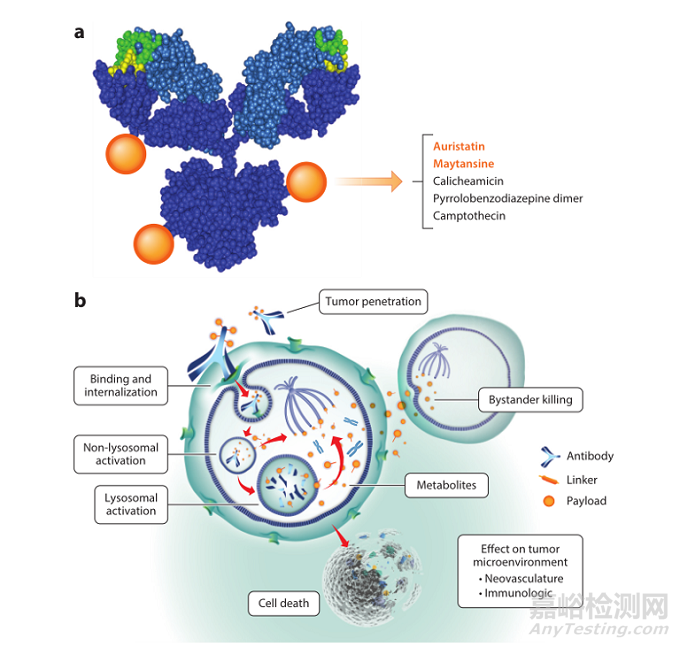
抗體偶聯(lián)藥物(ADC)是當(dāng)下抗體藥研發(fā)的又一熱點(diǎn)領(lǐng)域�����。ADC由三部分——抗體、細(xì)胞毒性有效載荷和連接的接頭組成�。其中有效載荷部分必須有皮摩爾范圍濃度的細(xì)胞毒性效力,以便能殺死腫瘤細(xì)胞及組織�。目前臨床開發(fā)中大多數(shù)ADC會(huì)使用的細(xì)胞毒性化合物有耳他汀類或美登素的衍生物����,它們是抗有絲分裂微管破壞劑���,其他高細(xì)胞毒性的化合物有加利車霉素��、雙霉素���、PBD 二聚體、吲哚并苯二氮卓假二聚體等�����。ADC藥物化學(xué)結(jié)構(gòu)和作用機(jī)制如圖5所示��。
圖5.ADC化學(xué)結(jié)構(gòu)(a)及作用機(jī)制(b)示意
(說明:a圖中IgG1分子與三個(gè)細(xì)胞毒性載荷(橙色球體)結(jié)合�����,重鏈和輕鏈分別為深藍(lán)色和淺藍(lán)色球體����?;パa(bǔ)決定區(qū)域顯示黃色為重鏈��,綠色為輕鏈)
參考來源: Antibody–Drug Conjugates for Cancer Treatment
近年來��,ADC藥物相關(guān)技術(shù)的研發(fā)工作取得了長(zhǎng)足的進(jìn)步�,如非天然氨基酸介導(dǎo)和酶切介導(dǎo)的定點(diǎn)偶聯(lián)技術(shù)���、親水性高且細(xì)胞穿透能力低的偶聯(lián)物、以及多種新形式的可裂解連接物����。不僅如此,基于bsAbs抗體以及 PD-L1 抗體的ADC藥物也在開發(fā)中���。
抗體藥物發(fā)展至今,已成為生物藥領(lǐng)域最火熱的研究分支之一���。相信隨著人類對(duì)疾病機(jī)制研究的不斷深入�,新的靶點(diǎn)將會(huì)不斷涌現(xiàn)����,也將擴(kuò)展更多適應(yīng)癥,為更多患者帶來福音�����。
1、單克隆抗體藥物的人源化歷程
傳統(tǒng)的單克隆抗體藥物具有完整的抗體結(jié)構(gòu),包括決定抗體特異性和親和力的抗原結(jié)合片段(fragment of antigen binding��, Fab)和誘導(dǎo)抗體依賴的細(xì)胞介導(dǎo)的細(xì)胞毒性作用(antibody-dependent cell-mediated cytotoxicity,ADCC)����、補(bǔ)體依賴的細(xì)胞毒性作用(complement dependent cytotoxicity,CDC)的可結(jié)晶片段(fragment crystallizable�����, Fc)���。
早期單克隆抗體藥物是以莫羅莫那單抗為代表的全鼠源單抗,用于治療器官移植后的急性排異反應(yīng)��,但由于具有較短的半衰期和較強(qiáng)的免疫原性�����,易誘發(fā)人抗鼠抗體(human anti-mouse antibody, HAMA)反應(yīng)而被迫退出市場(chǎng)�����。為了使抗體藥物更好地應(yīng)用于臨床,抗體人源化改造的步伐從未停止����,經(jīng)歷了鼠源性����、人鼠嵌合性��、人源化和全人源化4個(gè)階段。
人鼠嵌合抗體通過基因重組技術(shù)���,保留了鼠源的可變區(qū)以保證抗體特異性和親和力����,而恒定區(qū)為人源成分以減低免疫原性����。目前市場(chǎng)份額較大的人鼠嵌合抗體藥物是1997年上市的利妥昔單抗(rituximab-CD20)�,該抗體藥物通過ADCC和CDC殺死腫瘤細(xì)胞�����,適用于非霍奇金淋巴瘤和慢性淋巴細(xì)胞白血病���。
基于CDR移植技術(shù),人源化抗體將人源化部分提高到95%�,僅保留動(dòng)物來源的部分可變區(qū)(即骨架區(qū)),進(jìn)一步降低了免疫原性����。代表性藥物是1998年批準(zhǔn)上市的曲妥珠單抗(trastuzumab-HER2)����,用于治療乳腺癌�����,通過阻斷HER2信號(hào)通路�����,抑制腫瘤生長(zhǎng)。2008年���,我國(guó)首個(gè)自主研發(fā)的人源化抗體藥物尼妥珠單抗(nimotuzumab-EGFR)上市,用于鼻咽癌的治療,打破了國(guó)外對(duì)抗體藥物壟斷的局面�����。
全人源化抗體完全由人類基因編碼,顯著減低了免疫原性����,主要依賴于抗體展示技術(shù)和轉(zhuǎn)基因小鼠技術(shù)��。2002年����,經(jīng)噬菌體展示文庫(kù)篩選得到的阿達(dá)木單抗(adalimumab-TNFα)成為首個(gè)經(jīng)FDA獲批上市的全人源化抗體����,因其廣泛的適應(yīng)證和連續(xù)多年排名第一的銷量而有“藥王”之稱,至今仍具有巨大的發(fā)展?jié)摿Α?/span>
2����、 新型抗體藥物的類型及特點(diǎn)
隨著現(xiàn)代生物技術(shù)的發(fā)展及對(duì)抗體結(jié)構(gòu)和功能認(rèn)識(shí)的不斷深入,研究人員通過不同抗體片段的組合����、對(duì)抗體表面的位點(diǎn)進(jìn)行修飾��、偶聯(lián)小分子藥物或其他化學(xué)物質(zhì)等策略��,發(fā)展了數(shù)量龐大的抗體結(jié)構(gòu)形式��,并各有優(yōu)勢(shì)��。包括抗體融合蛋白(antibody fusion protein)����、抗體偶聯(lián)藥物(antibody-drug conjugate��, ADC)����、雙特異性抗體(bispecific antibody, BsAb)����、小分子抗體片段等。
2.1 抗體融合蛋白
抗體融合蛋白是指通過DNA重組技術(shù)��,將目的蛋白基因與抗體片段基因相連并表達(dá)的重組蛋白����,具有抗體的特性及融合功能蛋白的活性�����。由于直接由基因編碼表達(dá)為完整的融合蛋白�����,其優(yōu)勢(shì)在于蛋白與抗體連接穩(wěn)定����,結(jié)合均一�����。根據(jù)抗體結(jié)構(gòu)的不同�����,可以將抗體融合蛋白分為完整抗體融合蛋白和抗體片段融合蛋白��,且以Fc融合蛋白最多見��。
Fc融合蛋白的抗體Fc段可以通過增大融合蛋白的分子量及FcRn介導(dǎo)的再循環(huán)機(jī)制延長(zhǎng)藥物半衰期����,提高融合蛋白的穩(wěn)定性,還可以發(fā)揮Fc段特有的細(xì)胞毒性作用殺傷腫瘤細(xì)胞����。另外,F(xiàn)c段也有助于融合蛋白生產(chǎn)過程中的表達(dá)和檢測(cè)��。
研究發(fā)現(xiàn)��,細(xì)胞因子及其受體有治療疾病的潛能�����,但受限于治療窗口較窄�����,而細(xì)胞因子受體與抗體融合組成的重組抗體細(xì)胞因子受體融合蛋白能有效解決該問題,目前相關(guān)研究多處在臨床前或早期臨床研究階段?����,F(xiàn)已上市且應(yīng)用廣泛的重組抗體細(xì)胞因子受體融合蛋白是重組人Ⅱ型腫瘤壞死因子受體-抗體融合蛋白——依那西普(etanercept-TNF)����,屬于Fc融合蛋白��,適應(yīng)證為類風(fēng)濕性關(guān)節(jié)炎�����、銀屑病��、強(qiáng)直性脊柱炎�����。另外,各種來源于細(xì)菌��、病毒的毒素也可以與抗體融合組成抗體融合蛋白����,通過干擾細(xì)胞的蛋白合成發(fā)揮功能�����。重組免疫毒素也是一類重要的抗體融合蛋白��,它是全抗體或抗體片段與蓖麻毒素等生物毒素蛋白的融合蛋白�����。目前已獲批上市的重組免疫毒素有remitoro��、lumoxiti��、vicineum,主要用于血液系統(tǒng)腫瘤����。
2.2 抗體偶聯(lián)藥物
抗體偶聯(lián)藥物是一類由高特異性和親和力的單克隆抗體��、穩(wěn)定的連接頭(linker)、高效的細(xì)胞毒性化學(xué)藥物(cytotoxic chemical agent)三部分組成的靶向生物藥劑�����。通過單克隆抗體的靶向作用特異結(jié)合腫瘤細(xì)胞��,釋放細(xì)胞毒性藥物��,殺死腫瘤細(xì)胞��,從而實(shí)現(xiàn)藥物的高速靶向運(yùn)輸、精準(zhǔn)殺傷腫瘤細(xì)胞、減少全身不良反應(yīng)的目的��。
人源IgG1型抗體憑借其較弱的免疫原性、較好的親和力和特異性��、較長(zhǎng)的半衰期�����,能誘發(fā)ADCC和CDC的特點(diǎn)而常被應(yīng)用于ADC。連接頭的選擇對(duì)ADC的效能和安全性有重要影響����,需要保證其在循環(huán)中的穩(wěn)定性和到達(dá)靶點(diǎn)后有效釋放藥物����,以腙鍵、肽鍵或二硫鍵較常見�����。常見的細(xì)胞毒性藥物類型主要有微管蛋白抑制劑和DNA損傷試劑。
但ADC仍存在一些問題有待改進(jìn)�����,包括化學(xué)偶聯(lián)的方法導(dǎo)致細(xì)胞毒性藥物與抗體偶聯(lián)比例(drug-to-antibody ratio, DAR)不穩(wěn)定�����,連接頭不穩(wěn)定導(dǎo)致的脫靶毒性����,以及藥物釋放后擴(kuò)散殺傷周圍正常細(xì)胞的旁觀者效應(yīng)����。
在臨床應(yīng)用上����,F(xiàn)DA已批準(zhǔn)的ADC共10個(gè),主要針對(duì)血液系統(tǒng)腫瘤和實(shí)體瘤����,包括白血病��、淋巴瘤��、乳腺癌、泌尿系統(tǒng)腫瘤等�����。目前我國(guó)已經(jīng)獲批進(jìn)口的ADC有恩美曲妥珠單抗(trastuzumab emtansine-HER2)和維布妥昔單抗(brentuximab vedotin-CD30),分別針對(duì)乳腺癌和淋巴瘤發(fā)揮功能����。2021年�����,我國(guó)首個(gè)自主研發(fā)ADC維迪西妥單抗(disitamab vedotin-HER2)上市��,用于局部晚期或轉(zhuǎn)移性胃癌��。
2.3 雙特異性抗體
雙特異性抗體是一類可以同時(shí)識(shí)別和結(jié)合兩種不同抗原的新型抗體。相比于傳統(tǒng)單克隆抗體��,雙特異性抗體通過誘導(dǎo)細(xì)胞相互靠近����,增強(qiáng)殺傷作用��,還可以結(jié)合同一細(xì)胞表面不同抗原,減少脫靶效應(yīng)�����。
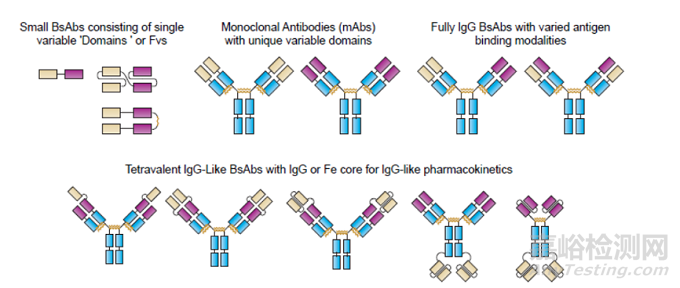
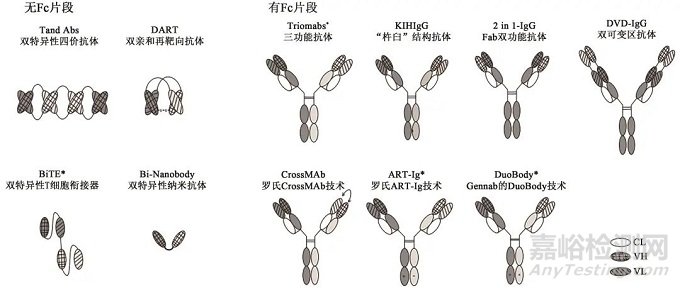
已經(jīng)上市或在研發(fā)的雙特異性抗體種類繁多,形式多樣(圖1)�����。根據(jù)是否含F(xiàn)c段將雙特異性抗體分為兩類����。一類是含F(xiàn)c段的雙特異性抗體�����,其與傳統(tǒng)抗體結(jié)構(gòu)類似,但兩個(gè)Fab區(qū)可以結(jié)合不同抗原��,穩(wěn)定性好�����、親和力強(qiáng)、半衰期較長(zhǎng)��,包括Triomabs、KIHIgG��、DVD-IgG�����、2 in 1-IgG��、CrossMAb、DuoBody和ART-IG等����。另一類是不含F(xiàn)c段的雙特異性抗體��,由Fab或更小的片段構(gòu)成��,具有分子量小、穿透力強(qiáng)�����、半衰期短等特點(diǎn),如TandAbs����、DART�����、BiTE、Bi-Nanobody等��。
圖1 不同形式的雙特異性抗體
Fig.1 Different types of bispecific antibodies
注:CL—輕鏈恒定區(qū)(constant light chain)�����,VH—重鏈可變區(qū)(variable heavy chain)����,VL—輕鏈可變區(qū)(variable light chain)����,顏色深淺代表抗體來源不同�����。已經(jīng)有成功上市產(chǎn)品的雙特異性抗體形式用*標(biāo)注。
已經(jīng)獲批上市的雙特異性抗體藥物主要通過介導(dǎo)免疫細(xì)胞殺傷����,促進(jìn)蛋白形成功能性復(fù)合體��,干擾信號(hào)通路發(fā)揮作用。通過雙特異性的結(jié)合位點(diǎn)使靶細(xì)胞(如腫瘤細(xì)胞)和免疫細(xì)胞(如T細(xì)胞)結(jié)合����,準(zhǔn)確定位�����,激活免疫細(xì)胞發(fā)揮殺傷作用����。2009年上市的卡妥索單抗(catumaxomab-EpCam*CD3)和2014年上市的博納吐單抗(blinatumomab-CD3*CD19)均通過該機(jī)制發(fā)揮功能����,分別適用于惡性腹水和急性淋巴細(xì)胞白血病��。2017年上市的艾美賽珠單抗(emicizumab-FIXa*FX)通過促進(jìn)蛋白形成功能性復(fù)合體發(fā)揮功能����。該抗體可以橋接凝血因子IXa和凝血因子X��,促進(jìn)凝血酶生成,用于A型血友病的常規(guī)預(yù)防��。2021年獲批上市的埃萬妥單抗(amivantamab-EGFR*c-MET)則通過阻斷信號(hào)通路和介導(dǎo)免疫細(xì)胞殺傷雙重抗癌����,適用于EGFR突變的非小細(xì)胞肺癌�����。
2.4 小分子抗體片段
小分子抗體片段包括以下幾種:抗原結(jié)合片段�����、單鏈可變區(qū)(single-chain fragment variable��,scFv)和單域抗體,具有體積小����、穿透能力強(qiáng)��、特異性強(qiáng)�����、免疫原性弱�����、易于基因工程改造和表達(dá)生產(chǎn)等特點(diǎn)。其半衰期短��、易清除的缺點(diǎn)可以通過結(jié)合不同的小分子和肽段適當(dāng)增加分子大小來彌補(bǔ)��,在延長(zhǎng)其半衰期的同時(shí),也能夠拓寬其功能����,增強(qiáng)效能����?���?贵w片段的制備方法包括體外酶消化法����、多種表達(dá)系統(tǒng)表達(dá)以及噬菌體展示技術(shù)��。其中,大腸桿菌表達(dá)系統(tǒng)具有生產(chǎn)成本低��、產(chǎn)量高、生產(chǎn)效率高的特點(diǎn)�����。
1994年����,第2個(gè)獲批上市的抗體藥物阿昔單抗(abciximab-GPⅡb/Ⅲa)是由哺乳動(dòng)物細(xì)胞表達(dá)重組人鼠嵌合IgG抗體,經(jīng)木瓜蛋白酶消化獲得顯著降低其免疫原性的Fab片段����,用于治療克羅恩病及類風(fēng)濕性關(guān)節(jié)炎的培塞利珠單抗(certolizumab pegol-TNFα)是來源于大腸桿菌表達(dá)系統(tǒng)的人源化F(ab′)2。我國(guó)自主研發(fā)的美妥昔單抗(metuximab-HAb18G)是鼠源F(ab′)2����,偶聯(lián)碘[131I]用于治療晚期肝癌。
scFv抗體片段是由抗體重鏈的可變區(qū)(VH)與輕鏈的可變區(qū)(VL)在一段肽鏈的連接下構(gòu)成的小分子抗體�����。如雙特異性T細(xì)胞銜接器(bispecific T cell engager)類型的雙特異性抗體——博納吐單抗也屬于小分子抗體范疇��。
單域抗體(single-domain antibody��,SdAb)是只包含單一可變區(qū)(VH/VL)的抗體。第一個(gè)單域抗體是從駱駝科動(dòng)物體內(nèi)發(fā)現(xiàn)的����,又稱納米抗體(nanobody)。單域抗體體積小��、穿透能力強(qiáng)����、能夠結(jié)合傳統(tǒng)抗體所不能觸及的位點(diǎn),如結(jié)合酶的活性中心�����,進(jìn)入實(shí)體腫瘤內(nèi)部��,穿過血腦屏障�����,為免疫治療提供了新的思路����。單域抗體穩(wěn)定性強(qiáng)�����,可以耐受極端pH、高離子強(qiáng)度��、蛋白酶存在��、高溫等極端情況����。2019年,首個(gè)單域抗體藥物卡拉西單抗(caplacizumab-vWF)獲批上市����,用于獲得性血栓性血小板減少性紫癜的治療。
3����、 抗體藥物在新型冠狀病毒肺炎治療中的應(yīng)用
抗體藥物在腫瘤殺傷、自身免疫病治療��、移植后免疫抑制均發(fā)揮重要作用��,其在感染性疾病�����,尤其是病毒感染相關(guān)疾病的預(yù)防和治療中,也有不可替代的作用����。
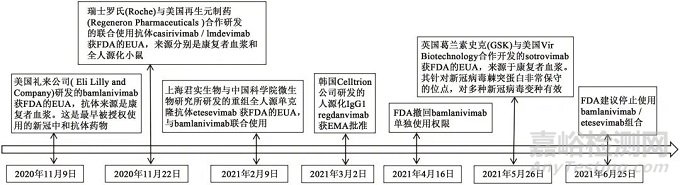
新型冠狀病毒肺炎(coronavirus disease 2019, COVID-19����,以下簡(jiǎn)稱新冠肺炎)疫情蔓延全球,嚴(yán)重威脅人們的身體健康和生命安全����。而新型冠狀病毒(SARS-CoV-2,以下簡(jiǎn)稱新冠病毒)中和抗體是人類對(duì)抗病毒的有力武器��,在疾病的預(yù)防和治療中都發(fā)揮了重要作用�����。目前已經(jīng)獲批使用的新冠病毒中和抗體藥物(以下簡(jiǎn)稱新冠抗體藥物)共6個(gè)(圖2)�����,適應(yīng)證為具有進(jìn)展至重度或住院高風(fēng)險(xiǎn)的輕��、中度COVID-19成年患者����。
圖2 新冠抗體藥物發(fā)展時(shí)間軸
Fig. 2 Timeline of antibody drug development of COVID-19
注:FDA為美國(guó)食品與藥品監(jiān)督管理局(US Food and Drug Administration);EUA為緊急使用授權(quán)(emergency use authorization)��;EMA為歐洲藥品管理局(European Medicines Agency)��。
新冠抗體藥物來源包括:恢復(fù)期患者血漿�����、基因工程重組抗體以及轉(zhuǎn)基因人源化小鼠�����。由于恢復(fù)期患者來源的中和抗體有活性及濃度的差異�����,難以標(biāo)準(zhǔn)化��,來源珍貴�����,推廣困難�����。利用基因工程技術(shù)及轉(zhuǎn)基因人源化小鼠生產(chǎn)抗體則是更好的選擇。如利用噬菌體展示技術(shù)可以高效�����、低成本��、大批量地生產(chǎn)抗體藥物�����。
不同機(jī)構(gòu)研發(fā)的新冠抗體藥物靶點(diǎn)為新冠病毒表面刺突蛋白的不同位點(diǎn)��。使用單一的抗體藥物容易誘導(dǎo)病毒變異和進(jìn)化�����,從而對(duì)現(xiàn)有的中和抗體產(chǎn)生逃逸[38]�����。如bamlanivimab單獨(dú)使用導(dǎo)致的新冠逃逸突變率達(dá)10%����。為此�����,科學(xué)家們提出了兩種解決方案�����。一是研發(fā)針對(duì)病毒刺突保守位點(diǎn)的抗體藥物,如sotrovimab��,其針對(duì)的保守位點(diǎn)若突變會(huì)影響病毒的功能��,但通常保守位點(diǎn)難以接觸及開發(fā)��。另一解決方案為“雞尾酒療法”��,通過聯(lián)用針對(duì)不同位點(diǎn)的多種抗體來避免逃逸�����。如抗體藥物組合bamlanivimab/etesevimab和casirivimab/imdevimab�����。但由于病毒變異性較強(qiáng)�����,bamlanivimab/etesevimab組合在獲批近5個(gè)月后被FDA建議停止使用。