近年來���,中國醫(yī)療器械行業(yè)在政策的推動下呈現(xiàn)出強勁的發(fā)展勢頭。許多國產(chǎn)廠家已經(jīng)開始在技術(shù)創(chuàng)新��、產(chǎn)品質(zhì)量等多方面展現(xiàn)出與國際頭部醫(yī)療器械企業(yè)長期匹敵�����,甚至超越的競爭優(yōu)勢����。國產(chǎn)廠家的崛起,使中國醫(yī)療器械走向全球市場水到渠成���。
近日���,健世科技宣布,其自主研發(fā)的經(jīng)導管三尖瓣置換系統(tǒng)�����,獲選加入美國食品藥品監(jiān)督管理局(FDA)的產(chǎn)品全生命周期咨詢計劃(TAP)����,將有效加速其在美國的臨床試驗和商業(yè)化拓展進度。
公告發(fā)出后�,健世科技開盤一度上漲超14%,直觀地反映出市場對于健世科技的經(jīng)導管三尖瓣置換系統(tǒng)LuX-Valve系列產(chǎn)品的認可以及公司未來發(fā)展的信心�����。
1����、創(chuàng)新性、臨床價值獲認可���,出海進程再提速
對于健世科技而言���,經(jīng)導管三尖瓣置換系統(tǒng)進入TAP是其獲得FDA授予突破性器械認定后的又一大里程碑事件���,將進一步加速其在美國的臨床和商業(yè)化進展。
簡單來說�,TAP旨在通過促進FDA與醫(yī)療器械廠商之間早期、頻繁和戰(zhàn)略性的溝通�����,以確保美國患者能夠于未來幾年內(nèi)在全球范圍率先獲得高質(zhì)量����、安全、有效和創(chuàng)新的醫(yī)療器械����。截止至2023年9月8日,F(xiàn)DA在TAP試點中僅納入了9款器械��。
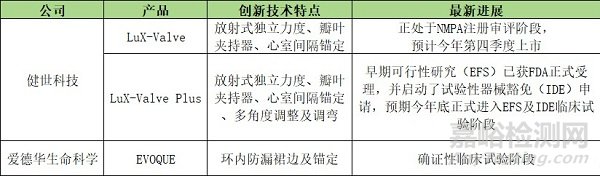
不難判斷��,健世科技的經(jīng)導管三尖瓣置換系統(tǒng)能夠獲納入TAP��,一方面意味著產(chǎn)品的創(chuàng)新性���,以及在治療方面的安全性和適用性已經(jīng)獲得權(quán)威標準的認可�����,擁有值得期待的競爭優(yōu)勢�。另一方面�,F(xiàn)DA也將從戰(zhàn)略和執(zhí)行兩個層面提供持續(xù)的支持,推動該產(chǎn)品后續(xù)在美國的臨床和商業(yè)化進程��。
資料來源:公司資料
更深層次地來看���,作為一款為治療重度三尖瓣反流及高手術(shù)風險患者設(shè)計的產(chǎn)品�����,LuX-Valve系列產(chǎn)品成功獲得FDA授予的突破性醫(yī)療器械認定和獲選納入TAP�,且臨床資料已被歐洲心臟病學會(ESC)和歐洲心胸外科協(xié)會(EACTS)瓣膜性心臟病管理指南所引用�����,標志著中國國產(chǎn)醫(yī)療器械在國際標準引領(lǐng)方面取得了重大進展���。健世科技的經(jīng)導管三尖瓣置換系統(tǒng)的成功經(jīng)驗亦是為其他中國醫(yī)療器械企業(yè)提供了借鑒�,將有力推動中國醫(yī)療器械產(chǎn)業(yè)的發(fā)展和國際競爭力的提升。
此外�,一代產(chǎn)品LuX-Valve及二代產(chǎn)品LuX-Valve Plus均已進入NMPA創(chuàng)新醫(yī)療器械特別審查程序,多項國內(nèi)外認可的資質(zhì)更是直接彰顯出健世科技在介入醫(yī)療器械方面強勁的技術(shù)實力����。
目前,LuX-Valve已進入NMPA注冊審評階段且注冊發(fā)補資料已遞交國家藥監(jiān)局��,有望成為全球首批上市的三尖瓣置換介入治療產(chǎn)品�����。若LuX-Valve順利于今年第四季度在中國如期上市銷售�����,后續(xù)其也將為該產(chǎn)品在美國及其他海外地區(qū)的商業(yè)化提供更多數(shù)據(jù)支撐����,加速在美國的臨床試驗和商業(yè)化進程。
2����、走出去到全球化�,清晰的全球化戰(zhàn)略
透過健世科技這一動態(tài)回到行業(yè)視角上����,不由得引發(fā)出一個問題��,國產(chǎn)醫(yī)療器械為什么要出海�����?
投資領(lǐng)域有一句話�,"不做中國市場做不大,不做全球市場做不強����。"歸結(jié)為一句話,那就是國產(chǎn)醫(yī)療器械廠家出海是發(fā)展壯大的必經(jīng)之路�����,并將為國內(nèi)醫(yī)療器械公司在多變的環(huán)境下提高抗風險能力����。我們不妨從以下三個方面來看:
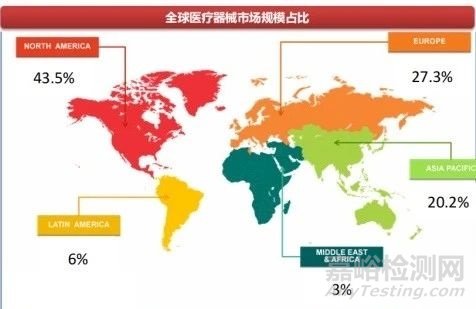
其一,海外醫(yī)療器械市場空間廣闊����。西南證券指出�����,目前全球器械市場主要由美國和歐洲貢獻�,預(yù)計后續(xù)以中國為主的亞太市場���、以及拉美���、中東、非洲等發(fā)展中國家市場增速將快于發(fā)達市場����,國內(nèi)器械出海進可攻發(fā)達市場,退可守發(fā)展中國家市場�����。
以全球結(jié)構(gòu)性心臟病介入醫(yī)療器械市場為例�,弗若斯特沙利文預(yù)計,全球結(jié)構(gòu)性心臟病介入醫(yī)療器械市場規(guī)模將由2021年的93億美元增至2025年的198億美元��,年復(fù)合增長率為20.8%,并于2030年增至481億美元����。
資料來源:西南證券
其二,海外市場具有多元化的購買方結(jié)構(gòu)�����,以商業(yè)保險為主��,這與國內(nèi)單一的支付方模式形成鮮明對比��。這種支付結(jié)構(gòu)使整個產(chǎn)品價格體系更為穩(wěn)定�����,并且隨著產(chǎn)品的不斷創(chuàng)新和迭代�,部分產(chǎn)品的價格逐漸趨于穩(wěn)定甚至略有提升�����。以TAVR為例��,愛德華的Sapien系列自2011年在美國上市以來����,單價基本維持穩(wěn)定��。
其三����,海外市場受經(jīng)濟發(fā)展水平���、醫(yī)療保健政策�、健康意識以及醫(yī)療器械技術(shù)等多方面因素作用影響����,如北美、歐洲等發(fā)達地區(qū)有著較強的商業(yè)保險支付能力以及患者支付意愿�。
順應(yīng)這一必然趨勢,健世科技作為一家深耕結(jié)構(gòu)性心臟病介入治療領(lǐng)域的醫(yī)療器械企業(yè)�����,已形成了一套清晰的全球化戰(zhàn)略��。目前��,公司同時推進自研產(chǎn)品在歐洲��、北美、亞太等地區(qū)的國際化布局�����,旗下產(chǎn)品已在全球超過10個國家或地區(qū)擁有164項已授權(quán)專利及196項專利申請���。
以三尖瓣置換產(chǎn)品為例�����,除前文提及的LuX-Valve以外��,公司的二代三尖瓣置換產(chǎn)品LuX-Valve Plus也同樣在海外市場取得了積極進展。
在北美市場�����,已在美國及加拿大地區(qū)完成數(shù)十例臨床植入����,持續(xù)推進經(jīng)導管三尖瓣置換系統(tǒng)產(chǎn)品在北美地區(qū)的臨床及商業(yè)化進程。預(yù)計在今年內(nèi)正式進入EFS和IDE臨床試驗階段�����。
在歐洲方面,持續(xù)在歐洲進行以獲取CE認證為目標的臨床應(yīng)用��。已經(jīng)在法國�����、德國�����、西班牙�����、意大利��、丹麥等歐洲主要國家及地區(qū)開展數(shù)十例臨床植入��,取得多國專家的一致好評����。
在亞太區(qū)域,已成功開展多例收費同情救治使用�����,進一步提升公司在亞太地區(qū)的學術(shù)地位和商業(yè)化影響力。
可以預(yù)想��,未來公司的收入將呈現(xiàn)多產(chǎn)品��、多國家��、多區(qū)域均衡分布的局面�,以適應(yīng)細分市場和多樣化的消費者需求,獲取更多收益����。同時積極拓展國際市場和不同地區(qū)業(yè)務(wù),也將提高公司的市場占有率和競爭力����,從而實現(xiàn)持續(xù)、穩(wěn)定的發(fā)展�。
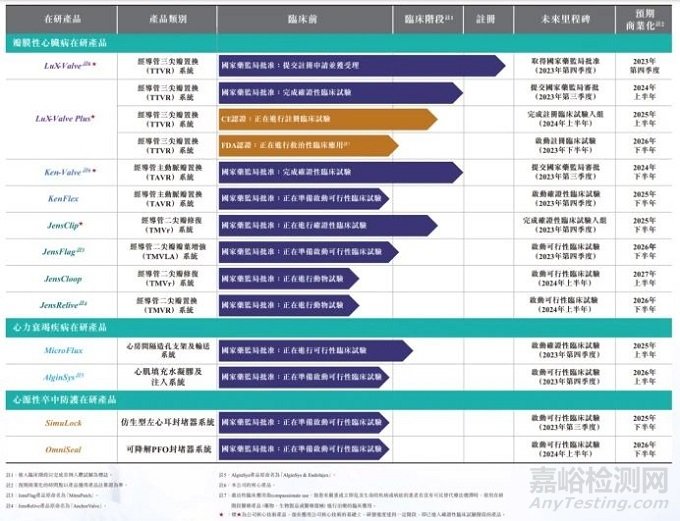
從競爭格局來看�����,目前全球還未有一款三尖瓣介入置換治療產(chǎn)品獲批上市���,相較于全球已經(jīng)進入確證性臨床試驗階段的三尖瓣介入置換產(chǎn)品�����,健世科技的LuX-Valve系列無論是在技術(shù)理念�����、臨床進度和臨床效果上�����,均有著領(lǐng)先優(yōu)勢����。
值得一提的是,LuX-Valve系列產(chǎn)品作為一款中國自主創(chuàng)新研發(fā)的第三類醫(yī)療器械���,其研發(fā)過程相當漫長����,從立項����、臨床試驗到預(yù)期拿證,歷經(jīng)10年����。而健世科技憑借著前瞻性的布局���,力克三尖瓣介入置換的高技術(shù)門檻,推動LuX-Valve邁入商業(yè)化的最后階段�,即將獲批上市搶跑市場。
資料來源:公開資料
此外�,健世科技的其他管線臨床也在穩(wěn)步推進中。例如�����,經(jīng)導管主動脈瓣置換系統(tǒng)Ken-Valve已于今年上半年完成確證性臨床試驗的一年隨訪工作��,即將向NMPA提交注冊����,預(yù)計2024年下半年獲批上市,有望成為中國第二款�����、全球第三款能夠治療主動脈瓣重度關(guān)閉不全(或合并狹窄)的主動脈瓣介入治療產(chǎn)品��。經(jīng)導管二尖瓣修復(fù)系統(tǒng)JensClip確證性臨床試驗入組已將近過半�。經(jīng)導管二尖瓣瓣葉增強系統(tǒng)JensFlag已成功完成數(shù)例人體應(yīng)用,驗證了二尖瓣瓣葉增強技術(shù)的可行性�。其全資子公司迪創(chuàng)醫(yī)療孵化的房間隔造孔支架系統(tǒng)MicroFlux和左心耳封堵器系統(tǒng)SimuLock亦均進入到正式FIM臨床試驗入組階段,當前入組均順利成功�����。
資料來源:公司資料
3�����、小結(jié)
"出海"作為企業(yè)能否在行業(yè)中走得更遠的關(guān)鍵�����,已成為國產(chǎn)醫(yī)療器械廠家的追求目標�����。但海外市場存在空白的臨床需要��,自身產(chǎn)品力的強大����,公司過硬的綜合能力(持續(xù)的創(chuàng)新研發(fā)能力、穩(wěn)定的質(zhì)量體系�、前瞻性的全球布局眼光)仍是擺在許多國產(chǎn)醫(yī)療器械尋求出海目標所必須面對和解決的�����。
健世科技持續(xù)不斷的創(chuàng)新研發(fā)升級出三尖瓣置換系統(tǒng)LuX-Valve����、LuX-Valve Plus���,以及主動脈瓣置換系統(tǒng)Ken-Valve等多個極具競爭力的醫(yī)療器械���,展現(xiàn)出公司在行業(yè)中的先發(fā)優(yōu)勢和獨特競爭力,為其瞄準全球市場的國際化布局奠定堅實的基礎(chǔ)�����。
反映到估值層面�����,筆者認為�,隨著市場情緒逐漸回歸理性,LuX-Valve及更多產(chǎn)品上市兌現(xiàn)業(yè)績�����,可以靜待健世科技的價值升維��。