新藥研發(fā)���,是指從發(fā)現(xiàn)藥物靶點到上市銷售的一系列科學研究和技術(shù)開發(fā)活動���,是醫(yī)藥產(chǎn)業(yè)的核心和動力。新藥研發(fā)具有高投入����、高風險、高回報的特點�,對人類健康和社會進步有著重要的意義。但是����,眾所周知���,新藥研發(fā)是面臨著諸多困難和挑戰(zhàn)的,如技術(shù)難度大���、周期長�、成本高���、成功率低���、法規(guī)嚴格、競爭激烈等�。按照公認的概述,平均每開發(fā)一種新藥需要花費10-15年時間����,耗資10-20億美元,但只有不到10%的候選藥物能夠最終上市����。
因此,為了應對這些困難和挑戰(zhàn)����,提高新藥研發(fā)的效率和質(zhì)量,降低新藥研發(fā)的風險和成本����,增強新藥研發(fā)的競爭力和創(chuàng)新力,建立新藥研發(fā)項目管理體系是非常必要的�。
本文將從新藥研發(fā)人員的角度出發(fā),闡述建立新藥研發(fā)項目管理體系的重要性�,以及新藥研發(fā)項目管理通常應該涉及哪些方面的內(nèi)容。
一�、已經(jīng)有GMP-like體系了,還需要項目管理嗎����?
在正式談到新藥研發(fā)項目管理之前,我們先確定一個概念����,那就是——合規(guī)性和項目管理是一件事嗎?比如���,某公司的研發(fā)質(zhì)量體系���,是從GMP like過來的,這樣能夠?qū)ρ邪l(fā)項目有效管理嗎?
其實���,有過新藥研發(fā)經(jīng)驗的同學們���,馬上就發(fā)現(xiàn)問題了:
我們借鑒GMP的質(zhì)量體系經(jīng)驗、把人機料法環(huán)規(guī)定的很嚴格了——但是——研發(fā)效率也受影響了����;
我們把數(shù)據(jù)可靠性規(guī)定的很詳細,保證了我們的申報資料是真實有效的���,但是——研發(fā)人員還是不知道如何開展研發(fā)�;
我們的研發(fā)現(xiàn)場QA每天跟蹤進展����,但是申報還是延期了;
所以����,我們的“研發(fā)質(zhì)量體系”同我們想要的那種效果,是否�,有可能,是不同的東西����?
從下圖可以看出���,我們新藥研發(fā)因為周期很長要求很多���,很多企業(yè)單位可能搞混了研發(fā)質(zhì)量體系���、GMP-like質(zhì)量體系以及商業(yè)化GMP質(zhì)量體系的概述���。
我們可以看到���,對于新藥研發(fā)來說,最基本的�、也是現(xiàn)在注冊申報最為關(guān)注的問題,就是數(shù)據(jù)真實性的要求(《藥品記錄與數(shù)據(jù)管理要求(試行)》(2020年第74號))���。所以���,進行新藥研發(fā),基礎(chǔ)的基礎(chǔ)�,是需要將研發(fā)過程中����,人機料法環(huán)管理的真實性做好�。
其次,新藥研究是一個證明新藥安全�、有效和質(zhì)量可控的過程,如何證明以上這些�,我們需要按照國內(nèi)外的注冊申報法規(guī),以及不同產(chǎn)品的指南來開展藥學�、臨床前及臨床試驗。
以上兩個環(huán)節(jié)是新藥研發(fā)的關(guān)鍵要點����,也是基礎(chǔ)。
但是����,這樣就足夠了嗎���?在現(xiàn)在競爭越發(fā)激烈的情況下���,我們的友商研究一個藥花了5年時間�,而我們要用7年���?是不是別人已經(jīng)吃完肉了�,而我們還沒有湯喝���?
也就是一個研發(fā)效率的問題了——新藥研發(fā)是一個復雜而漫長的過程,涉及多個階段����、多個部門、多個專業(yè)�、多個利益相關(guān)方。在這個過程中���,如何有效地協(xié)調(diào)各方資源�、控制各項風險����、保證各項質(zhì)量、實現(xiàn)各項目標���,是新藥研發(fā)人員面臨的重大挑戰(zhàn)���。如何在有限的資源下�,合理地利用及管理各部門�、各學科的人員和資源,使整體研發(fā)按照預期開展�,最后成功申報上市。
在這個時候���,我們的主角可以上場了——新藥研發(fā)項目管理����。
二�、研發(fā)項目管理體系,能帶給我們什么
新藥研發(fā)項目管理體系����,是指在新藥研發(fā)過程中,運用項目管理的理念和方法���,對新藥研發(fā)項目進行規(guī)劃�、組織���、實施���、監(jiān)控和總結(jié)的一套系統(tǒng)化的管理機制���。
新藥研發(fā)項目管理體系的作用主要有以下幾個方面:
1�、提高新藥研發(fā)效率
新藥研發(fā)項目管理體系可以幫助新藥研發(fā)人員明確項目目標、范圍���、進度���、成本�、質(zhì)量等關(guān)鍵要素,制定合理的項目計劃�,并根據(jù)計劃分配資源和任務。這樣可以避免資源浪費�、任務重復、進度延誤等問題����,提高新藥研發(fā)效率。
2�、降低新藥研發(fā)風險
新藥研發(fā)項目管理體系可以幫助新藥研發(fā)人員識別和分析項目中存在的各種風險,如技術(shù)風險���、市場風險�、法律風險等,并制定相應的風險應對策略���。這樣可以減少風險對項目造成的負面影響�,降低新藥研發(fā)失敗率����。
3、保證新藥研發(fā)質(zhì)量
新藥研發(fā)項目管理體系可以幫助新藥研發(fā)人員建立和執(zhí)行一套完善的質(zhì)量管理體系�,包括質(zhì)量規(guī)劃、質(zhì)量保證����、質(zhì)量控制和質(zhì)量改進等環(huán)節(jié)。這樣可以確保新藥研發(fā)過程符合相關(guān)法規(guī)和標準����,保證新藥安全性和有效性�。
4、增強新藥研發(fā)競爭力
新藥研發(fā)項目管理體系可以幫助新藥研發(fā)人員及時收集和分析項目相關(guān)的內(nèi)外部信息����,如市場需求���、競爭對手、政策變化等����,并根據(jù)信息變化調(diào)整項目策略和方向。這樣可以使新藥研發(fā)更加符合市場和社會的需求���,增強新藥的競爭力和商業(yè)價值����。
三���、新藥研發(fā)全生命周期概述
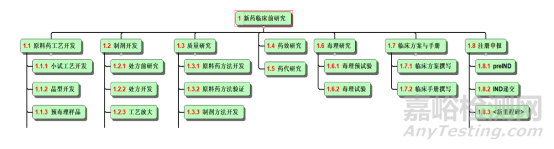
新藥研究是一項綜合性的探索工作,是一項創(chuàng)造性的科學研究�,必須多學科相互配合。發(fā)現(xiàn)有效化合物是研究新藥的基礎(chǔ)����,開發(fā)新藥的物質(zhì)來源可以是天然資源或生物合成或化學合成的化合物。
通常�,先導化合物的發(fā)現(xiàn)是研究新藥的起始。在研究其結(jié)構(gòu)和性質(zhì)后,通過生物系統(tǒng)的各項試驗����,了解化合物的藥效、毒性����、藥代以及與機體的相互作用,再進一步進行構(gòu)效關(guān)系研究和結(jié)構(gòu)的化���、改造���、修飾或優(yōu)化,從而發(fā)現(xiàn)并創(chuàng)造具有新型結(jié)構(gòu)與特殊藥理作用的新藥����。
新藥研究開發(fā)過程一般有以下三個階段。
1����、制訂研究計劃和制備新化合物階段
這一階段是調(diào)查研究,收集資料���,整理文獻�,制定計劃進行實驗和制備供篩選化合物(生物藥物供篩選的化合物包括從天然資源獲得的化合物和以生物技術(shù)手段獲得的化合物)。此階段研究主要是為篩選和進行實驗室研究提供物質(zhì)基礎(chǔ)���。
2���、篩選和臨床前研究階段
首先進行藥效學的藥理篩選,通常用實驗動物模型進行篩選���,也可以通過藥效學靶標進行分子水平或細胞水平篩選�,然后再用動物模型進行體內(nèi)篩選�,篩選時應盡量縮短動物模型和臨床病理作用之間的差距。生物新藥的臨床前研究主要包括實驗研究�,小量試制和中間試制三個階段。
1)實驗研究階段
實驗研究是基礎(chǔ)性研究�,比如對于生物制品來說,研究內(nèi)容主要有生產(chǎn)用菌�、毒種和細胞株的構(gòu)建、培養(yǎng)�、遺傳穩(wěn)定性和生物組織選擇,有效成分的提取����,純化及其理化特性����、結(jié)構(gòu)與生物特征的分析等研究����,取得制造和質(zhì)量檢定的基本條件和方法����。
2)小量試驗階段
根據(jù)實驗研究結(jié)果,確定配方及給藥方式����,建立制備工藝和檢定方法,實驗小批量樣品進行臨床前初步安全性和有效性的實驗(包括藥效作用及其特點���、毒理及初步藥代試驗)���,并制定制造與檢定基本要求。確定目的化合物具有新藥的可能性�。
3)中間試制階段
(1)生產(chǎn)工藝基本定型,產(chǎn)品質(zhì)量和產(chǎn)率相對穩(wěn)定���,并能放大生產(chǎn)�。
(2)有產(chǎn)品質(zhì)量標準����、檢定方法和保存穩(wěn)定性資料���,并有測定效價的參考品或?qū)φ掌贰?/span>
(3)全面、系統(tǒng)地完成臨床前研究工作���。包括藥的藥物化學研究����,藥理學研究(主要藥效學研究����,一般藥理學研究,藥物代謝動力學研究)���,毒理學研究�,以及生物等效性����、生物利用度研究和耐受性、依賴性試驗等���。
(4)制定較完善的制造檢定試行規(guī)程和產(chǎn)品使用說明書(草案)���。在新藥臨床前研究項目中,最重要的是新藥的安全性及其有效性是否優(yōu)于已知藥物�,因此取得臨床試驗批件的最重要資料是滿意的藥理學學和毒理學研究結(jié)果。
3���、臨床試驗研究階段
新藥臨床試驗是指對其臨床療效和安全性作出評價�,通過各期臨床試驗�,對新藥作出能否上市的結(jié)論����。所以臨床試驗是新藥評價的關(guān)鍵階段,是對新藥實際應用價值的最終驗證���。
藥物的臨床試驗(包括生物等效性試驗)�,必須執(zhí)行《藥物臨床試驗質(zhì)量管理規(guī)范》(GCP)����。申請新藥注冊,應當進行臨床試驗�。臨床試驗分為Ⅰ、Ⅱ���、 Ⅲ���、Ⅵ期�。新藥在批準上市前����,應當進行Ⅰ、Ⅱ�、Ⅲ期臨床試驗。經(jīng)批準后�,個別情況下可僅進行Ⅱ期和Ⅲ期臨床試驗或者僅進行Ⅲ期臨床試驗。
1)Ⅰ期臨床試驗
初步的臨床藥理學及人體安全性評價試驗�。觀察人體對于新藥的耐受程度和藥代動力學,為制定給藥方案提供依據(jù)���。
2)Ⅱ期臨床試驗
治療作用初步評價階段���。其目的是初步評價藥物對目標適應證患者的治療作用和安全性,也包括為設計Ⅲ期臨床試驗研究和確定給藥劑量的方案提供依據(jù)�。此階段的研究設計可以根據(jù)具體的研究目的,采用多種形式���,包括隨機雙盲法對照臨床試驗�。
3)Ⅲ期臨床試驗
治療作用確證階段。其目的是進一步驗證藥物對目標適應證患者的治療作用和安全性���,評價其利益與風險關(guān)系,最終為藥物注冊申請的市在提供充分的依據(jù)���。試驗一般應采用具有足夠樣本量的隨機雙盲法對照試驗����。
4)Ⅵ期臨床試驗
新藥上市后由申請人進行的應用研究階段����。其目的是考察在廣泛使用條件下藥物的療效和不良反應、評價在普通或者特殊人群中使用的利益與風險關(guān)系以及改進給藥劑量等���。
新生物藥物的種類繁多�,如天然生物藥物�、 反義藥物、新型疫苗���、治療性抗體�、基因工程藥物�、基因治療藥物等���。藥物種類不同,新藥申報和審批程序大同小異����、但這些藥物的研究過程是不同的。
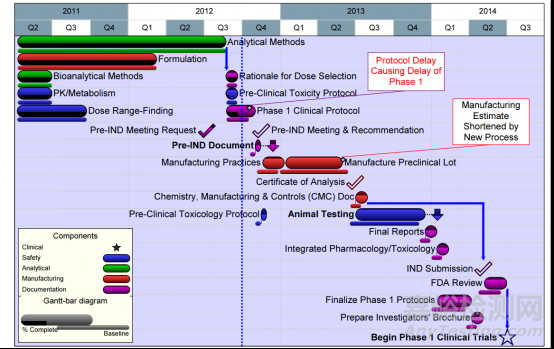
以下是某個藥品全項目時間管理的案例���。
四����、新藥項目管理能做些什么
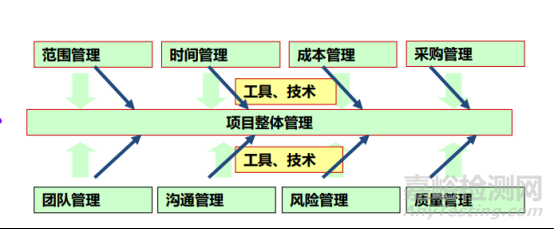
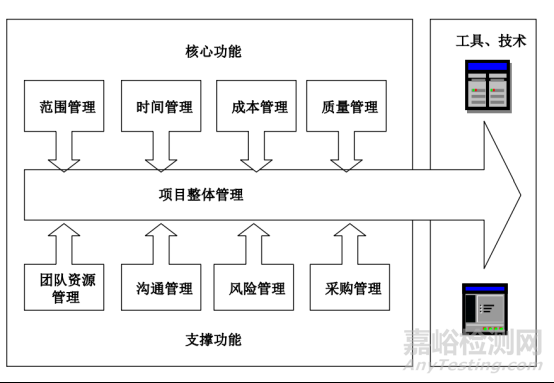
在新藥研發(fā)項目啟動之后����,根據(jù)項目SOP和干系人登記冊,對項目進行詳細的規(guī)劃����,包括項目進度規(guī)劃、項目成本規(guī)劃�、項目質(zhì)量規(guī)劃、項目資源規(guī)劃�、項目風險規(guī)劃、項目采購規(guī)劃等,以制定一個完整的項目管理計劃�。
制定一個具體的時間表
時間是新藥研發(fā)項目的重要因素之一,影響著新藥的上市速度和市場占有率���。如果時間安排不合理�,可能導致項目延期�、超支、質(zhì)量下降等問題�。因此����,制定一個具體的時間表,確定項目的開始時間和結(jié)束時間���,以及各個活動和輸出物的持續(xù)時間和先后順序�,是非常重要的�。
制定時間表的方法有多種,如甘特圖�、關(guān)鍵路徑法、PERT圖等���。這些方法可以幫助新藥研發(fā)人員清晰地展示項目的整體進度和各個階段的關(guān)鍵節(jié)點����,以及各個活動和輸出物之間的依賴關(guān)系和時間緩沖。這樣可以幫助新藥研發(fā)人員合理地安排資源和任務�,優(yōu)化工作流程和效率。
制定一個合理的預算
成本是新藥研發(fā)項目的重要因素之一����,影響著新藥的投資回報率和盈利能力。如果成本控制不好�,可能導致項目超支、虧損�、取消等問題。因此�,制定一個合理的預算,估算項目的總成本和各個活動和輸出物的成本����,以及控制成本的方法和標準,是必不可少的����。
制定預算的方法有多種,如自上而下法�、自下而上法、類比法����、參數(shù)法等����。這些方法可以幫助新藥研發(fā)人員準確地估算項目所需的人力成本���、物料成本�、設備成本����、外包成本等,并考慮可能出現(xiàn)的成本變化和風險���。這樣可以幫助新藥研發(fā)人員合理地分配資金和資源,優(yōu)化成本結(jié)構(gòu)和效益����。
制定一個完善的質(zhì)量體系
質(zhì)量是新藥研發(fā)項目的重要因素之一,影響著新藥的安全性和有效性�。如果質(zhì)量管理不好,可能導致項目失敗���、召回����、訴訟等問題。制定質(zhì)量體系的方法有多種����,如質(zhì)量計劃、質(zhì)量保證����、質(zhì)量控制、質(zhì)量改進等�。這些方法可以幫助新藥研發(fā)人員明確地定義各個活動和輸出物需要滿足的質(zhì)量要求和指標,并建立相應的質(zhì)量檢查���、審核����、檢驗����、偏差處理等流程和機制。這樣可以幫助新藥研發(fā)人員有效地保證并提高項目質(zhì)量����。
制定一個有效的資源計劃
資源是新藥研發(fā)項目的重要因素之一���,影響著項目的可行性和可持續(xù)性。如果資源管理不好�,可能導致項目缺乏資源、浪費資源�、沖突資源等問題。
制定資源計劃的方法有多種���,如需求分析法����、供給分析法���、平衡分析法等�。這些方法可以幫助新藥研發(fā)人員準確地評估項目所需的各種資源的數(shù)量和質(zhì)量���,并考慮可能出現(xiàn)的資源變化和限制。這樣可以幫助新藥研發(fā)人員合理地配置和調(diào)整資源���,優(yōu)化資源利用和效果���。
制定一個全面的風險計劃
風險是新藥研發(fā)項目的重要因素之一����,影響著項目的成功率和收益率����。如果風險管理不好,可能導致項目失敗���、損失�、危機等問題����。因此,制定一個全面的風險計劃�,識別和分析項目可能遇到的各種風險,并制定相應的風險應對策略和措施���。
制定風險計劃的方法有多種�,如風險識別法����、風險分析法、風險評估法����、風險應對法等����。這些方法可以幫助新藥研發(fā)人員系統(tǒng)地識別和分析項目中存在的各種技術(shù)風險�、市場風險、法律風險等�,并評估它們對項目目標和范圍的影響程度和可能性。這樣可以幫助新藥研發(fā)人員有效地規(guī)避或減輕風險�,或者轉(zhuǎn)化或利用風險。
制定一個適當?shù)牟少徲媱?/span>
采購是新藥研發(fā)項目的重要因素之一����,影響著項目的成本和質(zhì)量。如果采購管理不好����,可能導致項目采購錯誤、延誤�、爭議等問題。因此�,制定一個適當?shù)牟少徲媱?��,確定項目需要采購或外包的服務或產(chǎn)品�,并選擇合適的供應商或合作伙伴,是非常重要的���。
制定采購計劃的方法有多種�,如需求分析法�、市場調(diào)研法、評標法����、談判法等。這些方法可以幫助新藥研發(fā)人員準確地確定項目所需的各種服務或產(chǎn)品的內(nèi)容����、數(shù)量和質(zhì)量,并選擇具有良好信譽和能力的供應商或合作伙伴�,并簽訂合理的合同條款和條件。這樣可以幫助新藥研發(fā)人員有效地控制采購成本和質(zhì)量����,維護良好的采購關(guān)系,預防和解決可能出現(xiàn)的采購問題����。
五、最后
新藥研發(fā)項目管理涉及到多個方面�,如項目啟動�、項目規(guī)劃���、項目執(zhí)行���、項目監(jiān)控和項目收尾等。每個方面都有其重要的作用和輸出物���,需要新藥研發(fā)人員根據(jù)具體的項目情況和要求進行合理的設計和實施����。